视网膜静脉阻塞(RVO)

高血压和血脂异常的眼科风险
一目了然的要点
Section titled “一目了然的要点”1. 高血压/血脂异常与眼病的关系
Section titled “1. 高血压/血脂异常与眼病的关系”高血压和血脂异常促进全身动脉硬化,并反映在眼底表现中。眼底血管是全身唯一肉眼直接观察的血管床,被视为反映全身血管状态的“窗口” 1)。
高血压性眼底改变是心血管风险的独立指标,通过视网膜小动脉的变化可以评估高血压的严重程度和动脉硬化的程度 1)。高血压是视网膜静脉阻塞(RVO)最重要的危险因素,报告的优势比为3.0~5.0 2)。此外,在视网膜动脉阻塞(RAO)中,高血压和血脂异常也是主要危险因素 3)。
在血脂异常中,除了促进动脉硬化外,还会出现特征性的眼底表现,如Hollenhorst斑块(胆固醇栓子)。眼睑黄色瘤和角膜弓(arcus senilis)也是血脂异常的重要眼部表现 6)。
- 眼底是全身唯一可以直接观察血管的部位,是心血管风险评估的窗口 1)
- 高血压是视网膜静脉阻塞的最重要危险因素,OR为3.0~5.0 2)
- 视网膜动脉阻塞被视为“视网膜卒中”,需要像脑卒中一样进行紧急评估 3)
- 发现Hollenhorst斑块是颈动脉病变和卒中风险的指标
- 血脂异常的眼部表现包括眼睑黄色瘤、角膜环和视网膜脂血症6)
高血压反映在眼底血管变化上,增加视网膜静脉阻塞、视网膜动脉阻塞和缺血性视神经病变的风险。高血压性眼底变化采用Keith-Wagener-Barker(KWB)分级评估,Ⅱ级及以上时心血管事件风险显著升高。眼底是唯一可直接观察全身血管状态的部位,眼底检查有助于心血管风险评估。
2. 高血压性眼底变化
Section titled “2. 高血压性眼底变化”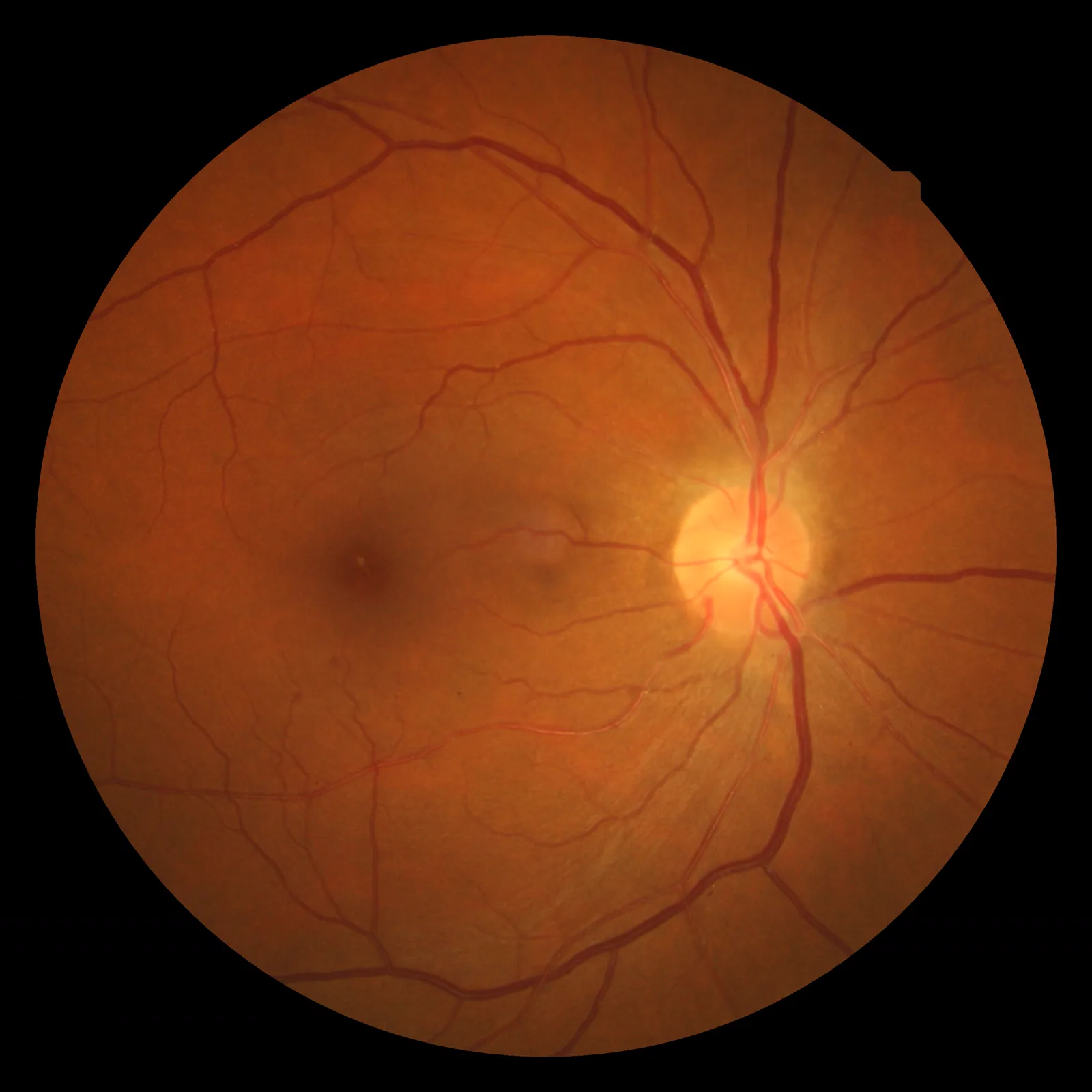
高血压导致视网膜小动脉出现特征性变化。目前仍在体检等中使用的Keith-Wagener-Barker(KWB)分级等多种分类方法。
Keith-Wagener-Barker(KWB)分级:
| 分级 | 眼底所见 |
|---|---|
| Ⅰ级 | 小动脉口径不均、轻度光反射增强 |
| Ⅱ级 | 动静脉交叉现象(Gunn征:静脉受压狭窄,Salus征:静脉走行偏移) |
| Ⅲ级 | 火焰状出血、棉絮状白斑、硬性渗出1) |
| Ⅳ级 | 视乳头水肿(恶性高血压、高血压脑病)1) |
KWB分级Ⅱ级及以上表示视网膜小动脉出现器质性改变,脑卒中和冠状动脉疾病风险显著升高5)。Ⅳ级(恶性高血压)是眼科急症,需要迅速降压治疗。
Scheie分级:
- 独立评估高血压性改变(H分级)和动脉硬化性改变(S分级)4)
- 采用H0~H4 / S0~S4的双轴分类,可分别评估高血压改变和动脉硬化改变
Wong-Mitchell简化分类:
- 轻度(mild)、中度(moderate)、恶性(malignant)三级5)
- 中度及以上时,脑卒中和心血管事件风险显著升高5)
- 大型队列研究(ARIC研究)显示,中度及以上的视网膜小动脉狭窄是冠状动脉疾病的独立预测因子5)
动静脉比(AVR):
- 正常视网膜动静脉比(AVR)约为0.675)
- AVR降低(动脉直径变窄)是高血压和动脉硬化的定量指标,与心血管风险相关5)
动脉硬化性眼底改变:
- 铜线动脉:动脉壁玻璃样变性导致反光带增宽
- 银线动脉:动脉壁纤维性增厚导致血柱反射消失(提示严重动脉硬化)
- Hollenhorst斑:来自颈动脉或主动脉粥样斑块的胆固醇栓子嵌顿于视网膜动脉分支
3. 血脂异常与眼病
Section titled “3. 血脂异常与眼病”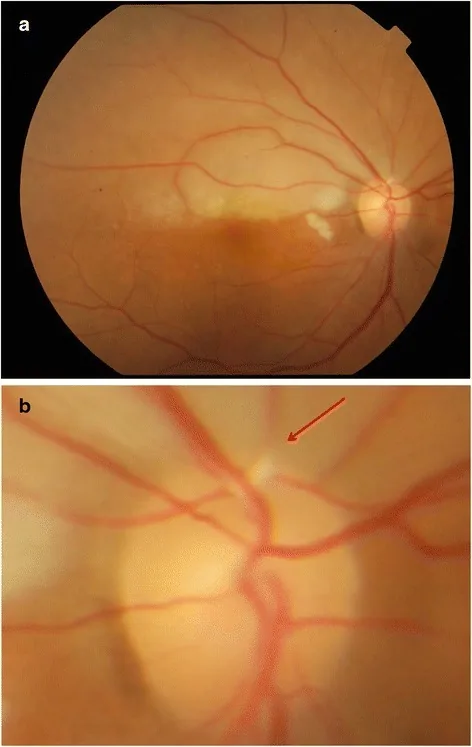
血脂异常通过促进动脉硬化增加多种眼病风险,并引起特征性眼部表现。
动脉硬化性眼底改变(脂质相关):
- Hollenhorst斑:来自颈动脉或主动脉粥样斑块的胆固醇栓子嵌顿于视网膜动脉。发现时需行颈动脉超声和超声心动图检查,为预防脑卒中需与神经内科和心血管科协作。
- 胆固醇斑的存在通常无症状,但提示脑栓塞风险。
血脂异常的特征性眼部表现:
- 角膜弓(老年环):角膜周边脂质沉积。50岁前出现被认为是血脂异常的征象6)
- 眼睑黄色瘤:眼睑皮肤脂质沉积(黄色斑块状病变)。与LDL胆固醇升高相关6)
- 视网膜脂血症:高甘油三酯血症(TG > 2,000 mg/dL)导致视网膜血管呈乳白色的罕见表现7)
血脂异常与视网膜静脉阻塞:
4. 相关眼病
Section titled “4. 相关眼病”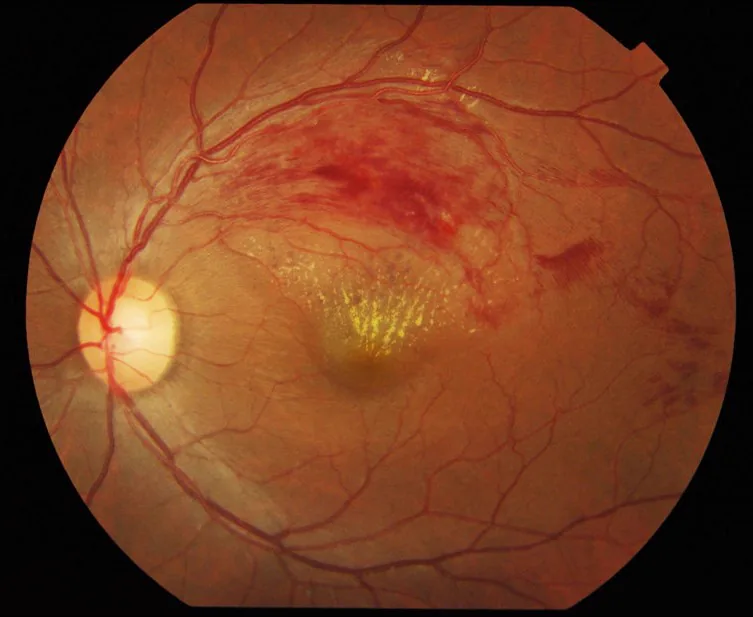
高血压和血脂异常与多种重要眼病直接相关。
视网膜动脉阻塞(RAO)
视网膜卒中:需要类似脑卒中的紧急评估3)
脑梗死合并:约30%的CRAO患者和约25%的BRAO患者在一周内合并脑梗死
必要的全身检查:颈动脉超声、心脏超声、MRI、心电图(评估房颤)3)
急性期治疗:t-PA溶栓治疗(发病4.5小时内)有效,但尚未获得医保批准
非动脉炎性前部缺血性视神经病变(NAION)
危险因素:高血压、糖尿病、血脂异常是主要危险因素8)
夜间血压下降的作用:夜间血压过度下降(nocturnal dipping)导致的视神经血流障碍参与发病机制8)
管理:考虑调整降压药的服用时间(如避免睡前服用)
高血压性脉络膜病变
恶性高血压中的脉络膜缺血:由脉络膜血管的纤维素样坏死引起9)
妊娠期高血压综合征也可引起类似病变
特征性表现:Elschnig斑(RPE损伤导致的脱色素斑)和Siegrist条纹(线状色素沉着)9)
紧急性:与KWB分级IV度一样,需要迅速降压管理
眼底是全身唯一可以直接观察血管的部位。动脉硬化的程度可以通过铜丝动脉、银丝动脉、动静脉交叉征(Gunn征、Salus征)以及动静脉比(AVR)等表现进行评估,这些是心血管风险的指标。如果在眼底发现Hollenhorst斑块(胆固醇栓子),可能提示存在颈动脉粥样硬化,从脑卒中风险的角度需要内科进一步检查。
5. 诊断与管理
Section titled “5. 诊断与管理”与高血压、血脂异常相关的眼病管理,基本原则是眼科治疗与全身疾病的内科管理相结合。
眼科检查:
- 散瞳眼底检查(眼底镜、眼底相机):根据KWB分类和Scheie分类进行评估
- 荧光眼底血管造影(FA):评估视网膜循环,确认血管闭塞部位
- OCT:评估黄斑水肿和视网膜内层损伤
- 眼底照相:记录和随访
全身评估(与内科协作):
- 血压测量(诊室、家庭、24小时动态血压)
- 血脂谱:总胆固醇(TC)、LDL-C、HDL-C、甘油三酯(TG)、HbA1c
- 颈动脉超声:发现RAO、一过性黑矇或Hollenhorst斑块时必须检查3)
- 心电图和超声心动图:评估房颤和瓣膜病(CRAO患者必须检查)3)
按眼病分类的治疗策略:
- RVO(合并黄斑水肿):抗VEGF治疗(雷珠单抗、阿柏西普等)10)
- 急性CRAO:t-PA溶栓治疗(发病4.5小时内)被认为有效,但未获医保批准,需根据各机构情况处理
- NAION:若怀疑夜间低血压,需与内科协商调整降压药服用时间
内科管理:
- 降压药:ARB(血管紧张素II受体拮抗剂)和ACE抑制剂具有血管保护作用 11)
- 他汀类药物:降低LDL-C可抑制动脉硬化进展。荟萃分析显示其对AMD发病风险有微弱的保护作用 12)
- 目标血压:<130/80 mmHg(高危病例)
6. 病理生理学及详细发病机制
Section titled “6. 病理生理学及详细发病机制”高血压和血脂异常损害眼组织的机制大致分为三类:血管壁结构改变、血流障碍和栓塞机制。
高血压引起的视网膜小动脉变化的阶段性进展:
- 第1相(血管收缩相):小动脉收缩作为对高血压的功能性反应。出现口径不均和光反射增强(KWB I级)1)
- 第2相(动脉硬化相):持续性高血压导致血管壁器质性增厚。在动静脉交叉处,动脉壁和静脉壁共享外膜,静脉被压迫变窄(KWB II级)2)
- 第3期(渗出期):血管壁通透性增高和破裂导致火焰状出血、棉絮状白斑和硬性白斑(KWB III级)1)
- 第4期(恶性高血压期):脉络膜血管纤维素样坏死和视乳头水肿(KWB IV级)9)
动静脉交叉征的机制(KWB II级):
- 视网膜动静脉在交叉处共享同一外膜2)
- 高血压导致动脉壁增厚,通过共同外膜压迫静脉,使其变窄(Gunn征)
- 严重压迫时静脉走行发生移位(Salus征)
- 动静脉交叉处的狭窄增加了静脉内血栓形成的风险,直接导致BRVO的发生
胆固醇栓子(Hollenhorst斑块)的机制:
- 颈动脉或主动脉弓的动脉粥样硬化斑块脱落微小胆固醇结晶3)
- 随血流进入眼动脉、视网膜中央动脉及分支动脉,嵌顿于分叉处
- 在眼底表现为有光泽的黄色至橙色斑块
- 通常不完全阻塞动脉,但提示存在栓子来源(颈动脉),表明卒中风险
血脂异常与血管内皮损伤:
- 氧化低密度脂蛋白胆固醇损伤血管内皮细胞11)
- 内皮源性一氧化氮(NO)生成减少,血管扩张反应受损
- 泡沫细胞形成→动脉粥样硬化斑块形成→斑块不稳定→栓塞是主要机制。
- 脉络膜血管的类似变化导致高血压性脉络膜病变和RPE损伤9)。
夜间低血压在NAION中的作用:
- 视神经乳头的血流取决于眼灌注压(平均血压−眼压)。
- 夜间血压过度下降(夜间血压下降)会减少视神经乳头的血流,导致视神经缺血8)。
- 睡前服用降压药可能导致夜间血压过度降低,作为NAION的风险因素需要注意。
7. 最新研究与未来展望
Section titled “7. 最新研究与未来展望”基于AI的眼底照片心血管风险预测:
- 已有报道使用深度学习模型从眼底照片估计心血管风险因素(年龄、性别、吸烟史、收缩压等)13)。
- 谷歌的研究表明,可以从眼底照片预测主要心血管事件风险13)。
- 有望应用于远程眼科,将眼底作为心血管筛查工具。
眼底血管参数与心血管风险的前瞻性研究:
- AVR(动静脉比)、视网膜小动脉直径和小静脉直径的定量评估与心血管事件的关联正在大型前瞻性队列中进行研究5)。
- ARIC研究(社区动脉粥样硬化风险研究)表明,视网膜小动脉狭窄是冠心病的独立预测因子5)
OCTA定量评估视网膜微循环:
- 研究正在探讨使用光学相干断层扫描血管成像(OCTA)定量评估视网膜毛细血管密度和无血管区是否有助于早期检测高血压性眼底改变
- 据报道,高血压患者浅层和深层毛细血管密度降低
他汀类药物与视网膜保护作用:
- 荟萃分析研究了他汀类药物使用与AMD发病风险之间的关联,提示存在微弱的保护作用12)
- 关于他汀类药物对RVO风险影响的前瞻性研究也在进行中
- 基础研究显示他汀类药物具有直接的视网膜血管保护作用(多效性),但尚未确立其临床意义
8. 参考文献
Section titled “8. 参考文献”- Wong TY, Mitchell P. Hypertensive retinopathy. N Engl J Med. 2004;351(22):2310-2317.
- Hayreh SS, Zimmerman MB, Podhajsky P. Incidence of various types of retinal vein occlusion and their recurrence and demographic characteristics. Am J Ophthalmol. 1994;117(4):429-441.
- Mac Grory B, Schrag M, Biousse V, et al. Management of central retinal artery occlusion: a scientific statement from the American Heart Association. Stroke. 2021;52(6):e282-e294.
- Scheie HG. Evaluation of ophthalmoscopic changes of hypertension and arteriolar sclerosis. AMA Arch Ophthalmol. 1953;49(2):117-138.
- Wong TY, Klein R, Sharrett AR, et al. Retinal arteriolar narrowing and risk of coronary heart disease in men and women. The Atherosclerosis Risk in Communities Study. JAMA. 2002;287(9):1153-1159.
- Zech LA Jr, Hoeg JM. Correlating corneal arcus with atherosclerosis in familial hypercholesterolemia. Lipids Health Dis. 2008;7:7.
- Vinger PF, Sachs BA. Ocular manifestations of hyperlipoproteinemia. Am J Ophthalmol. 1970;70(4):563-573.
- Hayreh SS. Management of ischemic optic neuropathies. Indian J Ophthalmol. 2011;59(2):123-136. PMID: 21350282. PMCID: PMC3116541. doi:10.4103/0301-4738.77024.
- Tso MO, Jampol LM. Pathophysiology of hypertensive retinopathy. Ophthalmology. 1982;89(10):1132-1145.
- Campochiaro PA, Heier JS, Feiner L, Gray S, Saroj N, Rundle AC, et al. Ranibizumab for macular edema following branch retinal vein occlusion: six-month primary end point results of a phase III study. Ophthalmology. 2010;117(6):1102-1112.e1. doi:10.1016/j.ophtha.2010.02.021.
- O’Brien T, Nguyen TT, Zimmermann MB. Hyperlipidemia and diabetes mellitus. Mayo Clin Proc. 1998;73(10):969-976.
- Ma L, Wang Y, Du J, et al. The association between statin use and risk of age-related macular degeneration. Sci Rep. 2015;5:18280.
- Poplin R, Varadarajan AV, Blumer K, et al. Prediction of cardiovascular risk factors from retinal fundus photographs via deep learning. Nat Biomed Eng. 2018;2(3):158-164.
