網膜静脈閉塞症(RVO)

高血圧と脂質異常症の眼科的リスク(Hypertension and Dyslipidemia Ocular Risks)
ひとめでわかるポイント
Section titled “ひとめでわかるポイント”1. 高血圧・脂質異常症と眼疾患の関連とは
Section titled “1. 高血圧・脂質異常症と眼疾患の関連とは”高血圧・脂質異常症は全身の動脈硬化を促進し、眼底所見として反映される。眼底血管は全身で唯一肉眼的に直接観察できる血管床であり、全身の血管状態を反映する「窓」として位置づけられる1)。
高血圧性眼底変化は心血管リスクの独立した指標とされ、網膜細動脈の変化から高血圧の重症度や動脈硬化の程度を評価できる1)。高血圧は網膜静脈閉塞症(RVO)の最も重要なリスク因子であり、オッズ比3.0〜5.0が報告されている2)。また網膜動脈閉塞症(RAO)においても高血圧・脂質異常症が主要なリスク因子となっている3)。
脂質異常症では動脈硬化の促進に加え、Hollenhorstプラーク(コレステロール塞栓)という特徴的な眼底所見をきたす。眼瞼黄色腫・角膜輪(arcus senilis)なども脂質異常症の眼所見として重要である6)。
- 眼底は全身で唯一直接血管を観察できる部位であり、心血管リスク評価の窓となる1)
- 高血圧は網膜静脈閉塞症のOR 3.0〜5.0の最重要リスク因子である2)
- 網膜動脈閉塞症は「網膜の脳卒中(retinal stroke)」として脳卒中に準じた緊急評価が必要である3)
- Hollenhorstプラークの発見は頚動脈病変・脳卒中リスクの指標となる
- 脂質異常症の眼所見として眼瞼黄色腫・角膜輪・網膜脂血症がある6)
2. 高血圧性眼底変化
Section titled “2. 高血圧性眼底変化”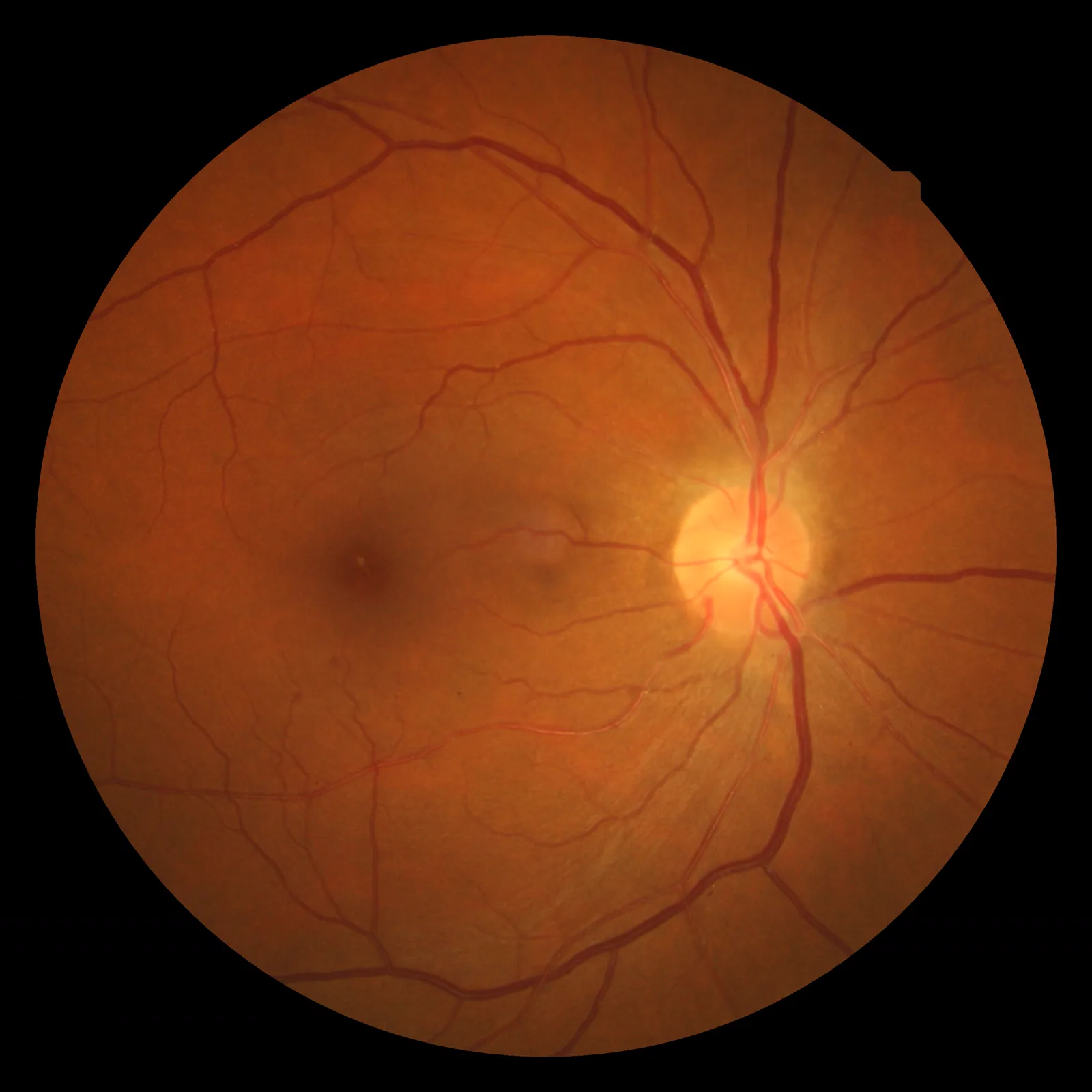
高血圧は眼底の細動脈に特徴的な変化をもたらす。現在も健診などで用いられるKeith-Wagener-Barker(KWB)分類をはじめ、複数の分類法がある。
Keith-Wagener-Barker(KWB)分類:
| 分類 | 眼底所見 |
|---|---|
| Ⅰ度 | 細動脈の口径不均等・軽度の光反射亢進 |
| Ⅱ度 | 動静脈交叉現象(Gunn徴候: 静脈の圧排狭小化、Salus徴候: 静脈の走行変位) |
| Ⅲ度 | 火炎状出血・綿花状白斑・硬性白斑1) |
| Ⅳ度 | 乳頭浮腫(悪性高血圧・高血圧性脳症)1) |
KWB分類のⅡ度以上では網膜細動脈の器質的変化が生じており、脳卒中・冠動脈疾患リスクが有意に上昇する5)。Ⅳ度(悪性高血圧)は眼科的緊急症であり、速やかな降圧管理が必要である。
Scheie分類:
- 高血圧性変化(H分類)と動脈硬化性変化(S分類)を独立に評価する4)
- H0〜H4 / S0〜S4 の二軸分類で、高血圧変化と動脈硬化変化を別々に評価できる
Wong-Mitchell簡略分類:
- 軽度(mild)・中等度(moderate)・悪性(malignant)の3段階5)
- 中等度以上では脳卒中・心血管イベントリスクが有意に上昇する5)
- 大規模コホート研究(ARIC Study)で中等度以上の網膜細動脈狭窄が冠動脈疾患の独立予測因子であることが示された5)
動静脈比(AVR):
- 正常の網膜動静脈比(AVR)は0.67前後とされる5)
- AVRの低下(動脈径の狭小化)は高血圧・動脈硬化の定量的指標であり、心血管リスクと相関する5)
動脈硬化性眼底変化:
- 銅線動脈:動脈壁の硝子様変性による反射帯の拡大
- 銀線動脈:動脈壁の線維性肥厚による血柱反射の消失(重篤な動脈硬化を示す)
- Hollenhorstプラーク:頚動脈または大動脈のアテロームから遊離したコレステロール塞栓が網膜動脈分枝に嵌頓した所見
3. 脂質異常症と眼疾患
Section titled “3. 脂質異常症と眼疾患”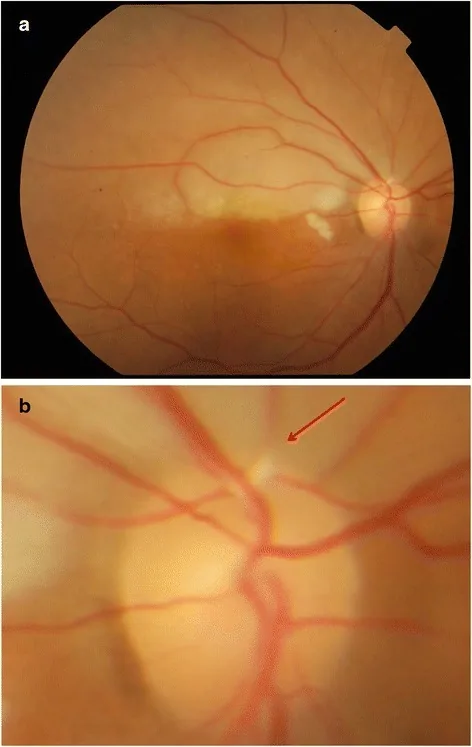
脂質異常症は動脈硬化を促進することで多くの眼疾患リスクを高めるほか、特徴的な眼所見をきたす。
動脈硬化性眼底変化(脂質関連):
- Hollenhorstプラーク:頚動脈・大動脈のアテロームから遊離したコレステロール塞栓が網膜動脈に嵌頓。発見時は頚動脈エコー・心エコーによる精査が必須であり、脳卒中予防の観点から神経内科・循環器科との連携が必要となる
- コレステロールプラークの存在は無症候であることが多いが、脳塞栓の危険性を示す
脂質異常症の特徴的眼所見:
- 角膜輪(arcus senilis):角膜周辺部への脂質沈着。50歳未満での出現は脂質異常症のサインとされる6)
- 眼瞼黄色腫(xanthelasma):眼瞼皮膚への脂質沈着(黄色板状病変)。LDLコレステロール上昇と関連する6)
- 網膜脂血症(lipemia retinalis):高トリグリセリド血症(TG > 2,000 mg/dL以上)で網膜血管が乳白色化する希少な所見7)
脂質異常症と網膜静脈閉塞症:
4. 関連する眼疾患
Section titled “4. 関連する眼疾患”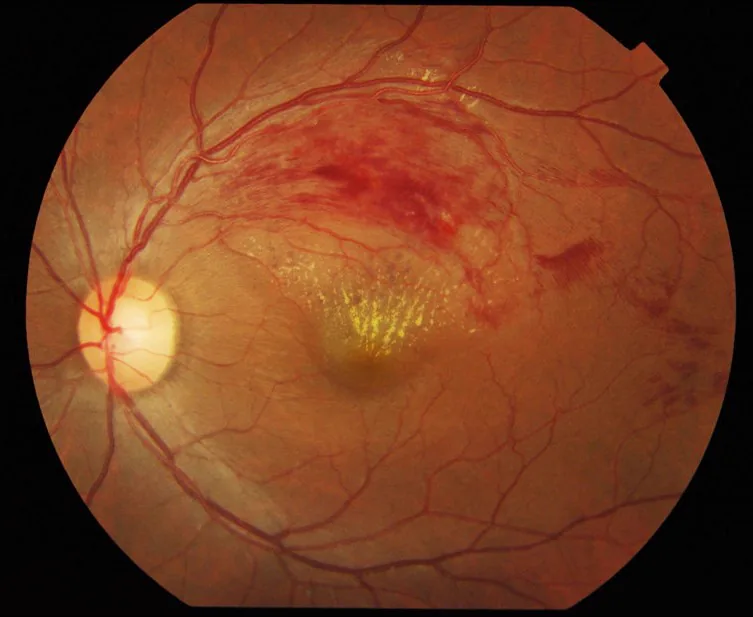
高血圧・脂質異常症は複数の重要眼疾患と直接的に関連する。
網膜動脈閉塞症(RAO)
非動脈炎性前部虚血性視神経症(NAION)
リスク因子:高血圧・糖尿病・脂質異常症が主要リスク因子8)
夜間血圧低下の関与:nocturnal dipping(夜間血圧過剰低下)による視神経血流障害が病態に関与する8)
管理:降圧薬の服用タイミングの調整(就寝前服用を避ける等)を検討
高血圧性脈絡膜症
悪性高血圧での脈絡膜虚血:脈絡膜血管のフィブリノイド壊死に起因する9)
妊娠高血圧症候群でも同様の病態が生じる
特徴的所見:Elschnig斑(RPE障害による脱色素斑)・Siegrist条線(線状色素沈着)9)
緊急性:KWB分類Ⅳ度と同様に速やかな降圧管理が必要
眼底は全身で唯一直接血管を観察できる部位である。動脈硬化の程度は銅線動脈・銀線動脈・動静脈交叉現象(Gunn徴候・Salus徴候)・動静脈比(AVR)などの所見で評価でき、これらは心血管リスクの指標となる。Hollenhorstプラーク(コレステロール塞栓)を眼底に認めた場合は、頚動脈アテロームの存在を示す可能性があり、脳卒中リスクの観点から内科的精査が必要となる。
5. 診断・管理
Section titled “5. 診断・管理”高血圧・脂質異常症に関連する眼疾患の管理は、眼科的治療と全身疾患の内科的管理を組み合わせることが基本である。
眼科的検査:
- 散瞳眼底検査(眼底鏡・眼底カメラ):KWB分類・Scheie分類による評価
- 蛍光眼底造影(FA):網膜循環の評価・血管閉塞部位の確認
- OCT:黄斑浮腫・網膜内層障害の評価
- 眼底写真:記録・フォローアップ
全身評価(内科と連携):
- 血圧測定(診察室・家庭・24時間血圧計)
- 脂質プロフィール:総コレステロール(TC)・LDL-C・HDL-C・トリグリセリド(TG)・HbA1c
- 頚動脈エコー:RAO・一過性黒内障・Hollenhorstプラーク発見時は必須3)
- 心電図・心エコー:心房細動・弁膜症の評価(CRAO患者では必須)3)
眼疾患別治療方針:
- RVO(黄斑浮腫合併):抗VEGF療法(ラニビズマブ、アフリベルセプト等)10)
- CRAO急性期:t-PA血栓溶解療法(発症4.5時間以内)が有効とされるが保険未承認のため施設ごとの対応が必要
- NAION:夜間低血圧の関与が疑われる場合は降圧薬の服用タイミング調整を内科と協議する
内科的管理:
- 降圧薬:ARB(アンジオテンシンII受容体拮抗薬)・ACE阻害薬が血管保護作用を有する11)
- スタチン:LDL-C低下による動脈硬化進展抑制。AMD発症リスクへの弱い保護効果がメタ解析で示されている12)
- 目標血圧:130/80 mmHg未満(高リスク例)
高血圧性眼底変化は心血管リスクの指標である。KWB分類Ⅱ度以上・Scheie分類H2以上の所見は、動脈硬化性変化が器質的段階に達していることを示す。眼科での精密検査(散瞳眼底・OCT)に加え、内科での血圧・脂質・血糖の評価が推奨される。Hollenhorstプラーク(光輝性黄色プラーク)を指摘された場合は頚動脈病変の精査が特に重要であり、速やかに内科・神経内科を受診すべきである。
6. 病態生理学・詳細な発症機序
Section titled “6. 病態生理学・詳細な発症機序”高血圧・脂質異常症が眼組織を障害するメカニズムは、血管壁の構造変化・血流障害・塞栓性機序の3つに大別される。
高血圧による網膜細動脈変化の段階的進行:
- 第1相(血管収縮相):高血圧に対する機能的反応として細動脈が収縮。口径不均等・光反射亢進(KWB Ⅰ度)が生じる1)
- 第2相(動脈硬化相):持続的高血圧により血管壁が器質的に肥厚。動脈壁と静脈壁が共通外膜を共有する交叉部で静脈を圧排・狭小化させる(KWB Ⅱ度)2)
- 第3相(滲出相):血管壁の透過性亢進・破綻による火炎状出血・綿花状白斑・硬性白斑(KWB Ⅲ度)1)
- 第4相(悪性高血圧期):脈絡膜血管のフィブリノイド壊死・乳頭浮腫(KWB Ⅳ度)9)
動静脈交叉現象の機序(KWB Ⅱ度):
- 網膜動静脈は交叉部で共通の外膜を共有している2)
- 高血圧による動脈壁肥厚が共通外膜を介して静脈を圧排し、狭小化させる(Gunn徴候)
- 圧排が強い場合は静脈の走行そのものが変位する(Salus徴候)
- この動静脈交叉部での狭小化が静脈内血栓形成のリスクを高め、BRVO発症に直結する
コレステロール塞栓(Hollenhorstプラーク)の機序:
- 頚動脈・大動脈弓のアテロームプラークから微小コレステロール結晶が遊離する3)
- 血流に乗って眼動脈→網膜中心動脈→分枝動脈へ流入し、分枝部に嵌頓する
- 光沢のある黄色〜橙色のプラークとして眼底に観察される
- 動脈を完全閉塞しないことも多いが、塞栓源(頚動脈)の存在を意味し脳卒中リスクを示す
脂質異常症と血管内皮障害:
- 酸化LDLコレステロールが血管内皮細胞を障害する11)
- 内皮由来一酸化窒素(NO)産生が低下し、血管拡張反応が障害される
- 泡沫細胞形成→アテロームプラーク形成→プラーク不安定化→塞栓症という経路が主要メカニズムである
- 脈絡膜血管での同様の変化が高血圧性脈絡膜症・RPE障害につながる9)
NAIONにおける夜間低血圧の関与:
- 視神経乳頭の血流は眼灌流圧(平均血圧 − 眼圧)に依存する
- 夜間の過剰な血圧低下(nocturnal dipping)により視神経乳頭の血流が低下し、視神経の阻血が生じる8)
- 降圧薬の就寝前服用が夜間血圧を過剰に低下させる可能性があり、NAIONリスクとして注意が必要である
7. 最新の研究と今後の展望
Section titled “7. 最新の研究と今後の展望”AIによる眼底写真からの心血管リスク予測:
- 深層学習モデルを用いた眼底写真からの心血管リスク因子(年齢・性別・喫煙歴・収縮期血圧等)の推定が報告されている13)
- Googleの研究では眼底写真から主要心血管イベントリスクを予測できることが示された13)
- 眼底を心血管スクリーニングツールとして活用するテレオフサルモロジーへの応用が期待されている
眼底血管パラメータと心血管リスクの前向き研究:
- AVR(動静脈比)・網膜細動脈径・静脈径の定量的評価と心血管イベントの関連が大規模前向きコホートで研究されている5)
- ARIC Study(Atherosclerosis Risk in Communities Study)では網膜細動脈狭窄が冠動脈疾患の独立予測因子であることが示された5)
OCTAによる網膜微小循環の定量評価:
- 光干渉断層血管造影(OCTA)を用いた網膜毛細血管密度・無血管域の定量的評価が高血圧性眼底変化の早期検出に有用である可能性が研究されている
- 高血圧患者では浅層・深層の毛細血管密度が低下することが報告されている
スタチンと網膜保護効果:
- スタチン使用とAMD発症リスクの関連がメタ解析で検討されており、弱い保護効果が示唆されている12)
- RVOリスクへのスタチンの影響についても前向き研究が進行中である
- スタチンの直接的な網膜血管保護効果(多面的効果)が基礎研究で示されているが、臨床的意義の確立には至っていない
8. 参考文献
Section titled “8. 参考文献”- Wong TY, Mitchell P. Hypertensive retinopathy. N Engl J Med. 2004;351(22):2310-2317.
- Hayreh SS, Zimmerman MB, Podhajsky P. Incidence of various types of retinal vein occlusion and their recurrence and demographic characteristics. Am J Ophthalmol. 1994;117(4):429-441.
- Mac Grory B, Schrag M, Biousse V, et al. Management of central retinal artery occlusion: a scientific statement from the American Heart Association. Stroke. 2021;52(6):e282-e294.
- Scheie HG. Evaluation of ophthalmoscopic changes of hypertension and arteriolar sclerosis. AMA Arch Ophthalmol. 1953;49(2):117-138.
- Wong TY, Klein R, Sharrett AR, et al. Retinal arteriolar narrowing and risk of coronary heart disease in men and women. The Atherosclerosis Risk in Communities Study. JAMA. 2002;287(9):1153-1159.
- Zech LA Jr, Hoeg JM. Correlating corneal arcus with atherosclerosis in familial hypercholesterolemia. Lipids Health Dis. 2008;7:7.
- Vinger PF, Sachs BA. Ocular manifestations of hyperlipoproteinemia. Am J Ophthalmol. 1970;70(4):563-573.
- Hayreh SS. Management of ischemic optic neuropathies. Indian J Ophthalmol. 2011;59(2):123-136. PMID: 21350282. PMCID: PMC3116541. doi:10.4103/0301-4738.77024.
- Tso MO, Jampol LM. Pathophysiology of hypertensive retinopathy. Ophthalmology. 1982;89(10):1132-1145.
- Campochiaro PA, Heier JS, Feiner L, Gray S, Saroj N, Rundle AC, et al. Ranibizumab for macular edema following branch retinal vein occlusion: six-month primary end point results of a phase III study. Ophthalmology. 2010;117(6):1102-1112.e1. doi:10.1016/j.ophtha.2010.02.021.
- O’Brien T, Nguyen TT, Zimmermann MB. Hyperlipidemia and diabetes mellitus. Mayo Clin Proc. 1998;73(10):969-976.
- Ma L, Wang Y, Du J, et al. The association between statin use and risk of age-related macular degeneration. Sci Rep. 2015;5:18280.
- Poplin R, Varadarajan AV, Blumer K, et al. Prediction of cardiovascular risk factors from retinal fundus photographs via deep learning. Nat Biomed Eng. 2018;2(3):158-164.
