OCTA は造影剤不要で網膜 ・脈絡膜 血管を三次元的に描出できる非侵襲的検査である。2014年に初めて臨床応用され、光干渉断層計 (OCT )と同一装置でモーションコントラスト原理により血流を検出する。
網膜 を4層(表層毛細血管叢・深層毛細血管叢・外網膜 ・脈絡膜 毛細血管叢)に分けて描出できる。従来のフルオレセイン蛍光眼底造影 (FA )と比べ、漏出の描出はできないが三次元定量が可能である。
糖尿病網膜症 ・加齢黄斑変性 ・網膜静脈閉塞症 ・網膜動脈閉塞症 ・緑内障 など幅広い疾患に応用される。アーチファクトが多く、セグメンテーション確認が画質管理の要である。
血管密度などの定量値は機種間で異なるため、同一機種での経時比較が原則である。
光干渉断層血管撮影 (Optical Coherence Tomography Angiography; OCTA )は、近赤外光を用いたOCT 装置に血流検出機能を追加した非侵襲的眼底血管撮影技術である。2014年に初めて臨床応用され、造影剤を使用しない血管可視化技術として急速に普及した。
OCTA は網脈絡膜 血流から血管構造を非侵襲的に可視化し、加齢黄斑変性 や糖尿病網膜症 などの診断や治療の判断に寄与している。
OCTA の基本原理はモーションコントラスト(分割フロー:OCTA 信号)である。同一部位を繰り返しスキャンし、時間的に変動する信号成分(=血球の移動)と静止した組織信号を分離することで血流情報を抽出する。具体的には、同一部位を短時間で繰り返しOCT スキャンし、A-scan間の振幅・位相変化(decorrelation)を計算する。静止組織は変化なし、血流がある部位は変化あり。この差分から血管構造が可視化される。
使用する光源によってSD-OCT (スペクトラルドメイン)とSS-OCT (スウェプトソース)の2種類が存在する。SS-OCT は波長が長いため脈絡膜 深部の描出に優れる。
SSADA(Split Spectrum Amplitude Decorrelation Angiography) :Optovue社(AngioVue®)に搭載OMAG(Optical Microangiography) :Zeiss社(Angioplex®)に搭載OCTA RAOCTA に搭載その他 :AngioScan®(NIDEK®)、SPECTR ALIS®(Heidelberg®)の各方式
Q
OCTAとフルオレセイン蛍光造影(FA)はどう違うのか?
A
FA は造影剤を静脈注射し、漏出を含む蛍光パターンを二次元的に記録する。OCTA は造影剤不要で血管の流れのみを三次元的に描出し、層別解析や定量が可能である。ただし漏出・染色・poolingの評価はできないため、FA と相補的に用いられる。造影剤アレルギー患者・腎機能障害患者で特に有用である。詳細は「主な特徴とFAとの比較」の項 を参照。
非侵襲・迅速
造影剤不要 :アナフィラキシーなど造影剤副作用のリスクがない。
短時間検査 :1回の撮影は数秒〜数十秒で完了する。
繰り返し施行可能 :経過観察目的での頻回な撮影が患者負担なく実施できる。
三次元・定量
層別解析 :網膜 を4層に分け、各層の血管網を個別に描出できる。
定量評価 :血管密度(VD)・毛細血管灌流密度(MPD)などを数値化できる。
形態と血流の同時評価 :OCT 構造画像と血管画像を重ね合わせて確認できる。
FAにない利点
フローボイド描出 :無灌流領域 ・毛細血管脱落を精細に可視化できる。
毛細血管叢の分離 :表層と深層の毛細血管叢を個別に評価できる。
NPA描出の優位性 :無灌流領域 (NPA)はFA よりも境界明瞭に描出される。
FAにない制限
漏出の描出不可 :血管透過性亢進・新生血管 からの漏出は検出できない。
画角が狭い :標準は3×3〜12×12mm程度で、広角FA に及ばない。
定量値の機種差 :血管密度などの数値は機種間で直接比較できない。
FA とOCTA の主な相違点を以下に示す。
特性 FA OCTA 造影剤 必要 不要 漏出評価 可 不可 層別解析 不可 可 画角 広角可 通常3〜12mm 定量評価 困難 VD・MPD等で可能 副作用リスク あり(アレルギー等) なし
OCTA を正確に行うためには適切な準備と撮影手順が必要である。
散瞳 散瞳 下撮影が推奨される。小瞳孔 (4mm未満)では画質が著しく低下する。固視確認 :固視不良は眼球運動アーチファクトの主因となる。固視灯を注視させ、安定した固視を確認してから撮影する。白内障 ・硝子体混濁 の評価
OCT と同一機器で連続撮影(追加の準備不要)固視灯を固視させ、安定したB-scanスキャンを確保
撮影範囲設定(黄斑部 : 3×3mm、6×6mm;乳頭部: 4.5×4.5mm)
自動セグメンテーションを確認し、必要に応じて手動修正
en face画像(層別)とB-scan(血流シグナル確認)を組み合わせて読影
OCTA ではOCT 断層像に基づいて各層の境界(セグメンテーション)を自動設定するが、病的眼では自動セグメンテーションが失敗することが多い。撮影後は必ずセグメンテーションラインを確認し、ずれがあれば手動修正する。
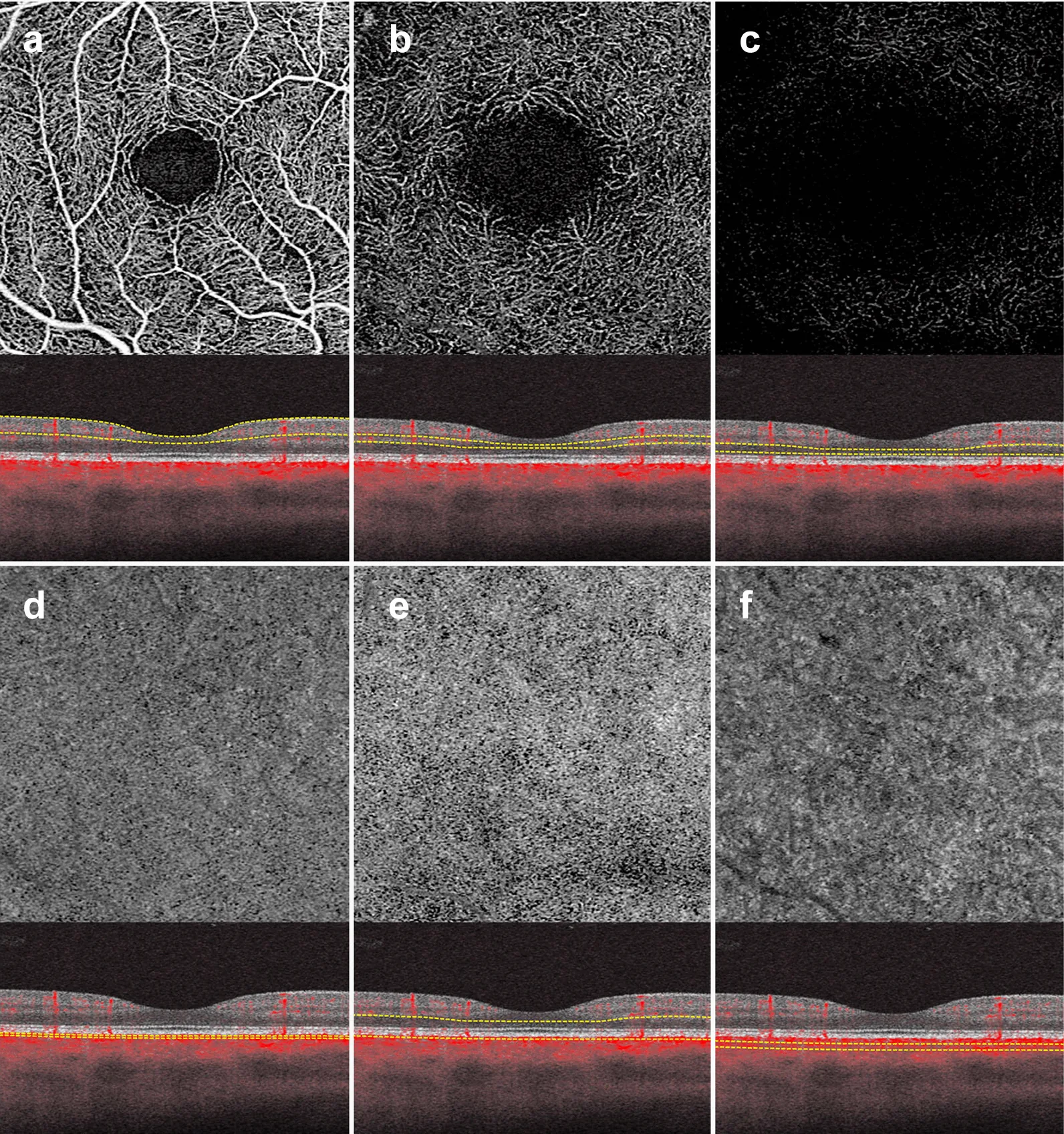
OCTAで描出される網膜6層スラブ(表層・深層・無血管層・脈絡膜毛細血管叢・ORCC・脈絡膜)のen face像 Greig EC, Duker JS, Waheed
NK . A practical guide to optical coherence tomography angiography interpretation. Int J Retina Vitreous. 2020;6:55. Figure 3. PM
CI D: PMC7666474. License: CC BY 4.0.
OCTA の6つの
網膜 スラブを示す。(a)表層(SCP)、(b)深層(DCP)、(c)無血管層、(d)
脈絡膜 毛細血管叢(CC)、(e)外
網膜 -
脈絡膜 毛細血管叢(ORCC)、(f)
脈絡膜 の各en face像とセグメンテーションラインを表示する。本文「4. 正常所見と各層の血管叢」の項で扱う
網膜 血管叢の層別構造に対応する。
OCTA では網膜 血管叢を以下の4層に分けて描出する。
層名 略称 主な位置 表層毛細血管叢 SCP 神経線維層〜神経節細胞層 深層毛細血管叢 DCP 内顆粒層内側〜外側 外網膜 — 無血管層(正常では血流なし) 脈絡膜 毛細血管叢CC ブルッフ膜 直下
さらに神経線維層毛細血管叢(RPC P)を加えた分類を採用する装置もある。
SCP(表層毛細血管叢) :太い動静脈と毛細血管網が密に分布。中心窩 周囲の毛細血管脱落帯(FA Z: foveal avascular zone)は明瞭に描出される。DCP(深層毛細血管叢) :より緻密な蜂巣状の毛細血管網。SCPよりFA Zが小さく見えることが多い。外網膜 :正常では血流信号なし。ここに血流信号が検出された場合は1型・2型・3型新生血管 (MNV)を疑う。CC(脈絡膜 毛細血管叢) :顆粒状(granular)の血流パターン。フロースポイント(flow spots)として描出される。
OCTA には特有のアーチファクトが存在し、臨床判断に影響するため理解が不可欠である。造影検査と同等に評価できるものもあれば、評価が難しいものも存在し、読影には注意が必要である。
アーチファクト 原因 影響 信号低下 メディア混濁・色素 偽フローボイド プロジェクション 表層血管の影 深層への偽血流 セグメンテーションエラー 病的形態変化 層間信号混入 眼球運動 固視不良 線状白帯・重複
信号低下アーチファクト :白内障 ・硝子体出血 ・色素沈着により深部の信号が減弱し、実際には灌流している血管がフローボイドとして誤認される。プロジェクションアーチファクト :表層血管からの信号が深層スラブに投影されて偽血流として描出される。プロジェクション除去アルゴリズム(PR)が実装された機種では軽減されるが完全には除去できない。セグメンテーションエラー :網膜 浮腫・萎縮・epiretinal membraneなどで自動セグメンテーションが失敗し、目的層以外の血管情報が混入する。手動修正が必要。眼球運動アーチファクト :固視不良による白線状・ジッパー状のノイズ。再撮影が原則だが、一部の装置ではアイトラッカーによる補正が可能。
Q
アーチファクトを最小化するにはどうすればよいか?
A
散瞳 ・固視確認・メディア評価を撮影前に行い、画質スコアを確認することが基本である。セグメンテーションは撮影後に必ず目視確認する。プロジェクション除去機能が搭載された機種ではこれを有効にする。動きによるアーチファクト、血管セグメンテーションの誤り、中間透光体の混濁がある画像は評価から除外する。
OCTA は多様な網膜 ・視神経 疾患の診断と管理に活用される。
OCTA はDRの毛細血管異常を精細に描出できる。FA Z拡大・不整、毛細血管脱落(フローボイド)、新生血管 の検出が可能である。無灌流領域 (NPA)はFA よりも境界明瞭に描出される。en face画像のみではNVとIRMAの形状が紛らわしいため、OCT B-scanで血流シグナルの有無を確認する必要がある。AAO 糖尿病網膜症 診療ガイドライン(2024)では、OCTA はFA の補完的検査として、特に黄斑部 毛細血管網の評価に有用であると位置づけられている4) 。
血管密度(VD)はDRの病期と相関し、網膜 虚血の客観的指標として研究が進んでいる。Srinivasanら(2023)はDR患者を対象とした縦断研究で、ベースライン時のSCP-VDが低いほど1年間でのDR重症度進行リスクが高いことを報告した2) 。DR進行群のSCP-VD中央値は12.90%、非進行群は14.90%で有意差があり(p=0.032)、ハザード比は0.825(AUC=0.643)であった。
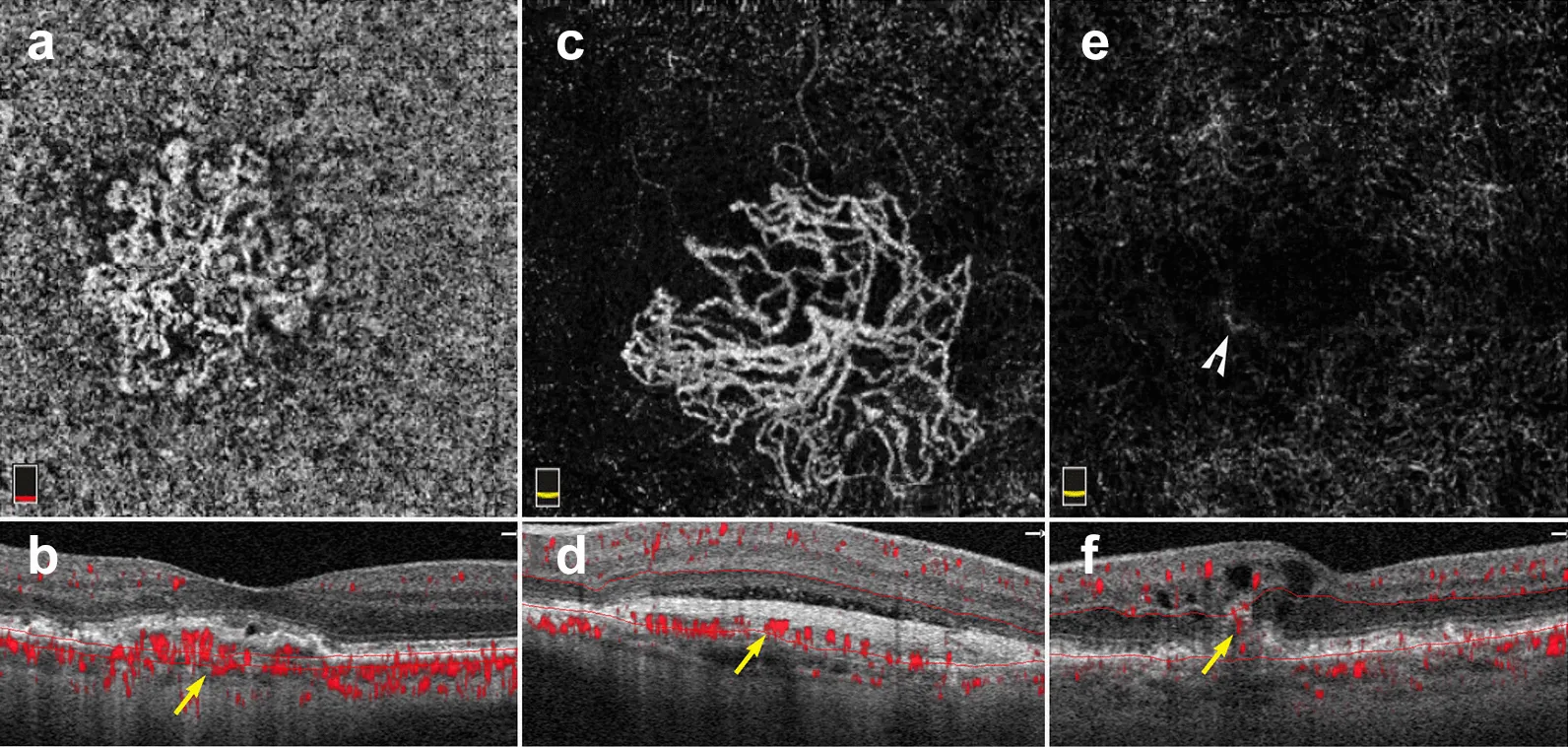
滲出型AMDにおける3種類の黄斑新生血管(MNV)のOCTA en face像とBスキャン Greig EC, Duker JS, Waheed
NK . A practical guide to optical coherence tomography angiography interpretation. Int J Retina Vitreous. 2020;6:55. Figure 9. PM
CI D: PMC7666474. License: CC BY 4.0.
滲出型
AMD の3型
黄斑 新生血管 を3×3mm en face像とBスキャンで示す。(a-b)1型MNV(
RPE 下血流)、(c-d)2型MNV(
RPE と
網膜 の間の血管)、(e-f)3型MNV(
網膜 内輝点)を表示する。本文「6. 臨床応用(
網膜 疾患)」の項で扱う
脈絡膜新生血管 (MNV)の検出に対応する。
脈絡膜新生血管 (MNV)の検出はOCTA の主要な適応の一つである。黄斑部 のOCTA の評価には3×3mmや6×6mmの細かい画角が望ましい。AAO AMD 診療ガイドライン(2024)では、OCTA による黄斑 新生血管 検出感度は0.87、特異度は0.97と報告されており、FA に匹敵する診断精度を有する5) 。
また、FA では検出できない無症候性のsubclinical 黄斑 新生血管 (1型MNV・drusen下MNV)をOCTA で検出できる可能性があり、早期介入の観点から注目されている5) 。
RVO では閉塞部位の毛細血管脱落・フローボイドがOCTA で明確に描出される。網膜 の層別に血管構造を評価することが可能で、表層あるいは深層の毛細血管層に生じた毛細血管瘤 (MA)も確認できる。AAO RVO 診療ガイドライン(2024)では、黄斑部 毛細血管網の虚血範囲の評価にOCTA が有用であると記載されている6) 。
RAO では閉塞血管の支配領域に一致した表層毛細血管のフローボイドが急性期から認められる。AAO RAO 診療ガイドライン(2024)では、OCTA による早期の血流評価が管理上有用であるとされている7) 。
Torpedo黄斑 症 :OCTA により外網膜 ・脈絡膜 毛細血管叢の無血管領域が確認される。Knaniら(2023)は1型・2型のtorpedo黄斑 症に対してOCTA を実施し、病変に一致した脈絡膜 毛細血管叢の信号欠損を報告した1) 。鎌状赤血球症 (SCD)結膜 ・網膜 の血管障害を複数の部位で評価する意義がある。Mgbojiら(2022)は結膜 OCTA を用いてSCD患者の結膜 微小血管形態の特徴を記録し、本法がSCDの血管合併症モニタリングに応用可能であることを示した3) 。
緑内障 は不可逆的失明の主要原因であり、OCTA は緑内障 眼における血管密度低下を検出可能であり、診断と進行評価への応用が期待されている。緑内障 診療ガイドライン(第5版)では、OCTA による網膜 表層・深層血流の評価が可能であるとし、進行した緑内障 ほど網膜 表層血流が低下することが知られる8) 。
緑内障 眼では乳頭周囲および黄斑部 の血管密度(VD)が低下し、疾患重症度と相関する。浅層(表層)でVD低下がより顕著である。構造的OCT のfloor effectを受けにくく、進行した緑内障 眼における進行判定で有利となる可能性がある8) 。陥凹拡大の進行に伴い乳頭内毛細血管が消失し、網膜神経線維層 欠損と一致して放射状乳頭周囲毛細血管が脱落する。
微小血管脱落(Microvascular dropout: MvD)は乳頭周囲萎縮領域における脈絡膜 毛細血管の消失である。多くはβゾーン内の耳下側に認められる。MvDはRNFL 菲薄化・篩状板 欠損・視野欠損 と関連し、RNFL 菲薄化と視野欠損 のより速い進行速度を予測する指標である。
ベースラインの乳頭周囲・黄斑 VDが低いことは、初期〜中期緑内障 におけるRNFL 進行の速い速度と関連する。この関連はベースラインRNFL 厚とは独立しており、OCTA が進行リスク評価に追加的な寄与を提供する可能性を示唆する。
緑内障 手術後に微細血管VDの有意な増加が複数の研究で報告されており、手術による眼圧 下降の影響で眼血流が増加すると考えられる。
機械説
眼圧 上昇と篩状板 変形眼圧 上昇により篩状板 が変形・菲薄化し、網膜神経節細胞 (RGC )の軸索輸送が途絶してアポトーシス が生じる。
眼圧 下降治療の根拠眼圧 を緑内障 発症・進行の最大の危険因子と位置づけている。
限界 :正常眼圧緑内障 や眼圧 下降でも進行する症例を十分に説明できない。
血管説
眼血流低下と虚血 :眼灌流圧の低下や血管自動調節能の喪失により視神経 が虚血・酸化ストレス に曝される。
動脈硬化の関与 :動脈硬化が高い拍動性を生み、眼の微小血管に障害をもたらす可能性が示唆されている9) 。
OCTA の意義OCTA が有力なツールとなる。
近年では「機械説」と「血管説」は互いに独立したものではなく、視神経乳頭 の生体力学理論として統合的に捉える考え方が主流となっている。眼圧 依存性因子と眼圧 非依存性因子(循環障害・自己免疫・酸化ストレス など)が複雑に関連し合い、緑内障 性視神経症 を構成すると考えられる10) 。
Q
緑内障の早期発見にOCTAは役立つか?
A
緑内障 眼では視野異常に先行して神経線維層菲薄化と乳頭周囲血管密度の低下が生じる可能性があり、OCTA による早期検出の研究が進んでいる。OCTA の診断能はOCT (RNFL 厚・GCC厚)と概ね同等とされるが、初期緑内障 ではOCT によるRNFL 厚の方が感度が良いとする報告もある。進行した緑内障 ではfloor effectを受けにくいOCTA が有利となる可能性がある8) 。現時点では診断・管理の主役はOCT 構造画像と視野検査 であり、OCTA は補完的役割にとどまる。
OCTA はSD-OCT またはSS-OCT を基盤とする。同一網膜 位置で繰り返しBスキャンを取得し、連続画像間のdecorelation(信号変化)を検出する。血管内を流れる赤血球は反射信号を変化させるが、周囲の静止組織は変化しない。この差が血流マップとして可視化される。
主要アルゴリズム
SSADA :スペクトラム分割振幅デコリレーション法。AngioVue®(Optovue®)に搭載。
OMAG :OCT ベースの微細血管撮影法。Angioplex®(Zeiss®)に搭載。
OCTA RAOCTA 比分析法。Triton®(TopCon®)のSS-OCTA に搭載。
その他 :AngioScan®(NIDEK®)の強度・位相デコリレーション結合法など。
装置選択の注意点
装置間非互換性 :アルゴリズムやデフォルトのスラブ深度が異なるため、同一患者でも装置間の直接比較は不可能である。
SS-OCTA :TopCon®、Canon®、Zeiss®が波長掃引型OCTA を提供しており、脈絡膜 層の評価で速度・解像度が向上する。
画質基準 :信号強度指数(SSI)40未満(Zeissでは6未満)の低画質画像は除外する。
用語 定義 血管密度(VD) 血管が占める面積の割合(%) 乳頭周囲VD 乳頭境界から外側750µm環状領域のVD 傍中心窩 VD 中心窩 中心の直径1〜3mm間のVDフローボイド 毛細血管脱落・無灌流領域 FA Z中心窩 無血管帯(foveal avascular zone)
OCTA の定量指標をDR進行予測バイオマーカー として活用する研究が進んでいる。Srinivasanら(2023)は、ベースラインのSCP-VD(血管密度)がDR進行リスクと有意に関連することを縦断的に示した2) 。VD 12.90%(進行群)vs 14.90%(非進行群)でp=0.032、ハザード比0.825、AUC=0.643であった。
12×12mmを超える超広角OCTA の開発・普及により、周辺部網膜 の血管病変や増殖前網膜 症における新生血管 の検出感度が向上することが期待される3) 。
OCTA で検出されたsubclinical 黄斑 新生血管 に対して抗VEGF治療を行うことで、滲出性AMD への移行を抑制できるかどうかを検討する臨床研究が進行中である5) 。
Berosら(2024)は大規模コホートにおいて、動脈脈波伝播速度(aPWV)が原発開放隅角緑内障 リスクの上昇と関連することを示した9) 。高い動脈硬化が眼の微小血管障害を介して緑内障 発症に寄与する可能性があり、OCTA による血管密度評価が将来的にバイオマーカー としての役割を担う可能性が示唆されている10) 。
AIによるOCTA 画像の自動解析、機種間定量値の標準化、進行予測モデルの開発が主要な研究課題である。定量値の標準化が達成されれば、多施設間での縦断的な比較研究が可能となる。
Q
OCTAは今後どのような方向に進化するか?
A
広角化・高速化・AIによる自動解析・定量バイオマーカー の標準化が主な方向性である。機種間の定量値差を解消する標準化基準の確立も重要な研究課題である。結膜 OCTA による全身疾患のモニタリングへの応用も期待されている3) 。
Knani L, Ghribi O, Trigui A, et al. Optical coherence tomography angiography features of torpedo maculopathy. Saudi J Ophthalmol. 2023;37:63-65.
Srinivasan S, Bhambra N, Jaiswal N, et al. Optical coherence tomography angiography as a predictor of diabetic retinopathy progression. Eye. 2023;37:3781-3786.
Mgboji GE, Cain D, Scott AW. Conjunctival optical coherence tomography angiography imaging in sickle cell maculopathy. Am J Ophthalmol Case Rep. 2022;26:101428. doi:10.1016/j.ajoc.2022.101428. PMID:35243165; PMCI D:PMC8861406.
American Academy of Ophthalmology. Diabetic Retinopathy Preferred Practice Pattern. AAO ; 2024.
American Academy of Ophthalmology. Age-Related Macular Degeneration Preferred Practice Pattern. AAO ; 2024.
American Academy of Ophthalmology. Retinal Vein Occlusions Preferred Practice Pattern. AAO ; 2024.
American Academy of Ophthalmology. Retinal Artery Occlusions Preferred Practice Pattern. AAO ; 2024.
日本緑内障 学会. 緑内障 診療ガイドライン(第5版). 日眼会誌. 2022.
Beros AL, Sluyter JD, Hughes AD, et al. Arterial Stiffness and Incident Glaucoma: A Large Population-Based Cohort Study. Am J Ophthalmol. 2024;266:68-76. doi:10.1016/j.ajo.2024.05.015. PMID:38754800.
Stangos A, et al. Ocular and Systemic Risk Factors and Biomarkers for Glaucoma: An Umbrella Review of Systematic Reviews and Meta-Analyses. Invest Ophthalmol Vis Sci. 2025;66(12):35.
記事の全文をコピーして、お好みのAIに貼り付けて質問できます
下のAIを開いて、チャット欄に貼り付け(ペースト)してください