ไม่รุกรานและรวดเร็ว
ไม่ต้องใช้สารทึบรังสี: ไม่มีความเสี่ยงจากผลข้างเคียงของสารทึบรังสี เช่น ภาวะแพ้รุนแรง
ตรวจใช้เวลาสั้น: การถ่ายภาพแต่ละครั้งใช้เวลาไม่กี่วินาทีถึงหลายสิบวินาที
ทำซ้ำได้: สามารถถ่ายภาพซ้ำเพื่อติดตามผลได้โดยไม่เป็นภาระต่อผู้ป่วย

การถ่ายภาพหลอดเลือดด้วยแสงคลื่นสั้น (Optical Coherence Tomography Angiography; OCTA) เป็นเทคนิคการถ่ายภาพหลอดเลือดจอตาแบบไม่รุกรานที่เพิ่มฟังก์ชันตรวจจับการไหลเวียนเลือดให้กับเครื่อง OCT ที่ใช้แสงอินฟราเรดใกล้ เริ่มใช้ทางคลินิกครั้งแรกในปี 2014 และแพร่กระจายอย่างรวดเร็วในฐานะเทคนิคการสร้างภาพหลอดเลือดโดยไม่ต้องใช้สารทึบแสง
OCTA สร้างภาพโครงสร้างหลอดเลือดจากการไหลเวียนเลือดจอตาและคอรอยด์แบบไม่รุกราน และมีส่วนช่วยในการวินิจฉัยและการตัดสินใจรักษาสำหรับจุดภาพชัดเสื่อมตามอายุและจอประสาทตาเสื่อมจากเบาหวาน
หลักการพื้นฐานของ OCTA คือคอนทราสต์การเคลื่อนไหว (การไหลแบบแบ่งส่วน: สัญญาณ OCTA) บริเวณเดียวกันถูกสแกนซ้ำๆ และส่วนประกอบสัญญาณที่แปรผันตามเวลา (การเคลื่อนที่ของเม็ดเลือด) จะถูกแยกออกจากสัญญาณเนื้อเยื่อที่อยู่นิ่งเพื่อดึงข้อมูลการไหลเวียนเลือด โดยเฉพาะอย่างยิ่ง บริเวณเดียวกันถูกสแกนซ้ำด้วย OCT ในช่วงเวลาสั้นๆ และคำนวณการเปลี่ยนแปลงแอมพลิจูด/เฟส (decorrelation) ระหว่างการสแกน A เนื้อเยื่อที่อยู่นิ่งไม่เปลี่ยนแปลง บริเวณที่มีการไหลเวียนเลือดเปลี่ยนแปลง จากความแตกต่างนี้ โครงสร้างหลอดเลือดจึงถูกสร้างภาพขึ้นมา
OCT แบ่งออกเป็น 2 ประเภทตามแหล่งกำเนิดแสงที่ใช้: SD-OCT (Spectral Domain) และ SS-OCT (Swept Source) SS-OCT มีความยาวคลื่นที่ยาวกว่าจึงดีกว่าในการแสดงภาพชั้นลึกของคอรอยด์
FA ต้องฉีดสารทึบรังสีทางหลอดเลือดดำเพื่อบันทึกรูปแบบการเรืองแสงสองมิติรวมถึงการรั่วซึม OCTA ไม่ต้องใช้สารทึบรังสีและแสดงเฉพาะการไหลเวียนของหลอดเลือดในสามมิติ ช่วยให้วิเคราะห์แยกชั้นและวัดปริมาณได้ อย่างไรก็ตาม ไม่สามารถประเมินการรั่วซึม การย้อมสี หรือการสะสมของสารได้ จึงใช้เสริมกับ FA มีประโยชน์โดยเฉพาะในผู้ป่วยที่แพ้สารทึบรังสีหรือมีภาวะไตเสื่อม ดูรายละเอียดในหัวข้อ “ลักษณะสำคัญและการเปรียบเทียบกับ FA”
ไม่รุกรานและรวดเร็ว
ไม่ต้องใช้สารทึบรังสี: ไม่มีความเสี่ยงจากผลข้างเคียงของสารทึบรังสี เช่น ภาวะแพ้รุนแรง
ตรวจใช้เวลาสั้น: การถ่ายภาพแต่ละครั้งใช้เวลาไม่กี่วินาทีถึงหลายสิบวินาที
ทำซ้ำได้: สามารถถ่ายภาพซ้ำเพื่อติดตามผลได้โดยไม่เป็นภาระต่อผู้ป่วย
สามมิติและเชิงปริมาณ
การวิเคราะห์แบบชั้น: จอประสาทตาสามารถแบ่งออกเป็น 4 ชั้น และสามารถแสดงภาพหลอดเลือดในแต่ละชั้นแยกกันได้
การประเมินเชิงปริมาณ: ความหนาแน่นของหลอดเลือด (VD) และความหนาแน่นของการไหลเวียนเลือดในเส้นเลือดฝอย (MPD) สามารถวัดเป็นตัวเลขได้
การประเมินรูปร่างและการไหลเวียนเลือดพร้อมกัน: สามารถซ้อนทับภาพโครงสร้าง OCT และภาพหลอดเลือดเพื่อตรวจสอบได้
ข้อดีที่ไม่มีใน FA
การแสดง Flow Void: สามารถมองเห็นบริเวณที่ไม่มีการไหลเวียนเลือดและการสูญเสียเส้นเลือดฝอยได้อย่างละเอียด
การแยกช่องท้องเส้นเลือดฝอย: สามารถประเมินช่องท้องเส้นเลือดฝอยชั้นผิวและชั้นลึกแยกกันได้
ความเหนือกว่าในการแสดง NPA: บริเวณที่ไม่มีการไหลเวียนเลือด (NPA) จะถูกแสดงขอบเขตชัดเจนกว่า FA
ข้อจำกัดที่ไม่มีใน FA
ไม่สามารถแสดงการรั่วซึม: ไม่สามารถตรวจพบการเพิ่มขึ้นของการซึมผ่านของหลอดเลือดหรือการรั่วซึมจากหลอดเลือดใหม่ได้
มุมมองแคบ: ช่วงมาตรฐานประมาณ 3×3 ถึง 12×12 มม. ซึ่งน้อยกว่า FA มุมกว้าง
ความแตกต่างของค่าปริมาณระหว่างเครื่อง: ค่าต่างๆ เช่น ความหนาแน่นของหลอดเลือด ไม่สามารถเปรียบเทียบโดยตรงระหว่างเครื่องมือต่างๆ ได้
ด้านล่างนี้คือความแตกต่างหลักระหว่าง FA และ OCTA
| คุณลักษณะ | FA | OCTA |
|---|---|---|
| สารทึบรังสี | จำเป็น | ไม่จำเป็น |
| การประเมินการรั่วซึม | สามารถทำได้ | ไม่สามารถทำได้ |
| การวิเคราะห์แยกชั้น | ไม่สามารถทำได้ | สามารถทำได้ |
| มุมมองภาพ | สามารถมุมกว้างได้ | ปกติ 3-12 มม. |
| การประเมินเชิงปริมาณ | ยาก | สามารถทำได้ผ่าน VD, MPD ฯลฯ |
| ความเสี่ยงของผลข้างเคียง | มี (เช่น อาการแพ้) | ไม่มี |
เพื่อทำ OCTA อย่างแม่นยำ จำเป็นต้องมีการเตรียมตัวที่เหมาะสมและขั้นตอนการถ่ายภาพที่ถูกต้อง
ใน OCTA ขอบเขตของแต่ละชั้น (การแบ่งส่วน) จะถูกตั้งค่าโดยอัตโนมัติตามภาพ OCT แบบตัดขวาง แต่ในตาที่เป็นโรค การแบ่งส่วนอัตโนมัติมักจะล้มเหลว หลังจากถ่ายภาพ ให้ตรวจสอบเส้นแบ่งส่วนเสมอ และแก้ไขด้วยตนเองหากมีการเบี่ยงเบน
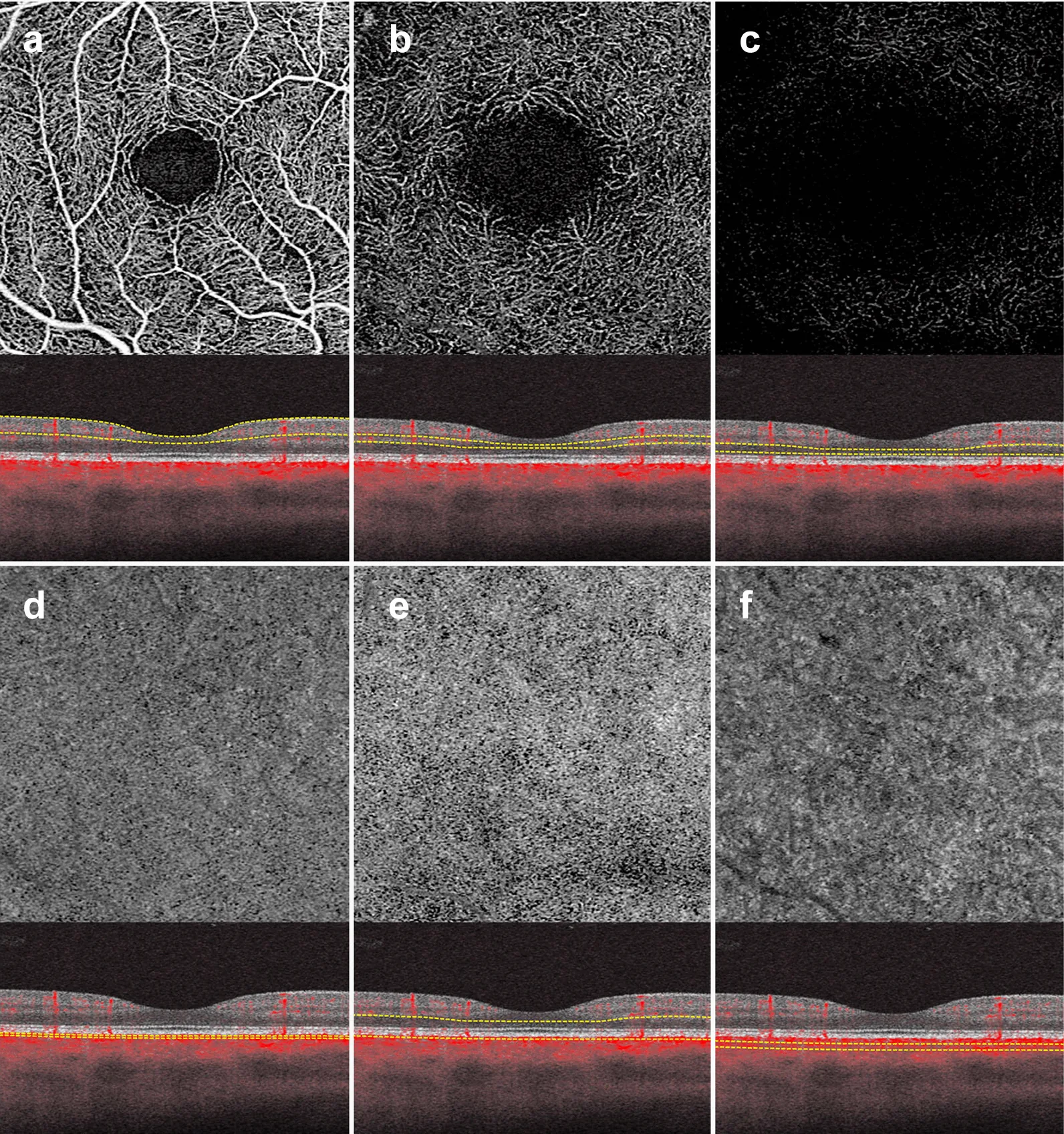
ใน OCTA ข่ายหลอดเลือดเรตินาจะถูกแสดงโดยแบ่งออกเป็นสี่ชั้นดังต่อไปนี้
| ชื่อชั้น | ชื่อย่อ | ตำแหน่งหลัก |
|---|---|---|
| ข่ายหลอดเลือดฝอยชั้นผิว | SCP | ชั้นเส้นใยประสาทถึงชั้นเซลล์ปมประสาท |
| ข่ายเส้นเลือดฝอยชั้นลึก | DCP | จากด้านในถึงด้านนอกของชั้นนิวเคลียสชั้นใน |
| จอประสาทตาชั้นนอก | — | ชั้นไร้หลอดเลือด (ไม่มีเลือดไหลปกติ) |
| ข่ายเส้นเลือดฝอยคอรอยด์ | CC | ใต้เยื่อบรูชโดยตรง |
อุปกรณ์บางรุ่นใช้การจำแนกที่รวมข่ายเส้นเลือดฝอยชั้นเส้นใยประสาท (RPCP) ด้วย
OCTA มีสิ่งรบกวนเฉพาะที่ส่งผลต่อการตัดสินใจทางคลินิก ดังนั้นจึงจำเป็นต้องเข้าใจ บางอย่างสามารถประเมินได้เทียบเท่ากับการตรวจหลอดเลือดด้วยสารทึบรังสี ในขณะที่บางอย่างประเมินได้ยาก จึงต้องใช้ความระมัดระวังในการแปลผล
| สิ่งรบกวน | สาเหตุ | ผลกระทบ |
|---|---|---|
| สัญญาณต่ำ | ความขุ่นของสื่อหรือเม็ดสี | ช่องว่างการไหลเทียม |
| การฉายภาพ | เงาของหลอดเลือดผิว | การไหลเทียมสู่ชั้นลึก |
| ข้อผิดพลาดในการแบ่งส่วน | การเปลี่ยนแปลงรูปร่างทางพยาธิวิทยา | การปนกันของสัญญาณระหว่างชั้น |
| การเคลื่อนไหวของลูกตา | การจ้องไม่ดี | แถบสีขาวเชิงเส้น / การซ้ำกัน |
พื้นฐานคือการขยายม่านตา, ตรวจสอบการจ้อง, และประเมินสื่อกลางก่อนถ่ายภาพ และตรวจสอบคะแนนคุณภาพภาพ ควรตรวจสอบการแบ่งส่วนด้วยสายตาหลังถ่ายภาพเสมอ เปิดใช้งานฟังก์ชันกำจัดการฉายภาพในเครื่องที่มี ตัดภาพที่มีสิ่งรบกวนจากการเคลื่อนไหว, ข้อผิดพลาดในการแบ่งส่วนหลอดเลือด, หรือความขุ่นของสื่อกลางหักเหแสงออก.
OCTA ใช้ในการวินิจฉัยและจัดการโรคจอประสาทตาและเส้นประสาทตาหลายชนิด.
OCTA สามารถแสดงความผิดปกติของเส้นเลือดฝอยใน DR ได้อย่างละเอียด สามารถตรวจพบการขยายและความไม่สม่ำเสมอของ FAZ, การสูญเสียเส้นเลือดฝอย (flow void), และเส้นเลือดใหม่ พื้นที่ที่ไม่มีการไหลเวียน (NPA) แสดงขอบเขตชัดเจนกว่า FA เนื่องจากรูปร่างของ NV และ IRMA อาจคล้ายกันในภาพ en face จึงจำเป็นต้องตรวจสอบสัญญาณการไหลเวียนใน OCT B-scan ในแนวทางปฏิบัติทางคลินิกของ AAO สำหรับจอประสาทตาเสื่อมจากเบาหวาน (2024) OCTA ถูกจัดให้เป็นการตรวจเสริมของ FA โดยเฉพาะอย่างยิ่งมีประโยชน์ในการประเมินเครือข่ายเส้นเลือดฝอยจุดรับภาพ 4).
ความหนาแน่นของหลอดเลือด (VD) สัมพันธ์กับระยะของ DR และกำลังถูกวิจัยในฐานะตัวบ่งชี้ภาวะขาดเลือดของจอประสาทตาอย่างเป็นกลาง Srinivasan และคณะ (2023) ในการศึกษาระยะยาวในผู้ป่วย DR รายงานว่า SCP-VD ที่ต่ำกว่าเมื่อเริ่มต้นมีความสัมพันธ์กับความเสี่ยงที่สูงขึ้นของการดำเนินโรค DR ที่รุนแรงขึ้นภายใน 1 ปี 2) ค่ามัธยฐานของ SCP-VD ในกลุ่มที่ DR ดำเนินโรคคือ 12.90% ในกลุ่มที่ไม่ดำเนินโรคคือ 14.90% โดยมีความแตกต่างอย่างมีนัยสำคัญ (p=0.032) อัตราส่วนอันตรายคือ 0.825 (AUC=0.643)
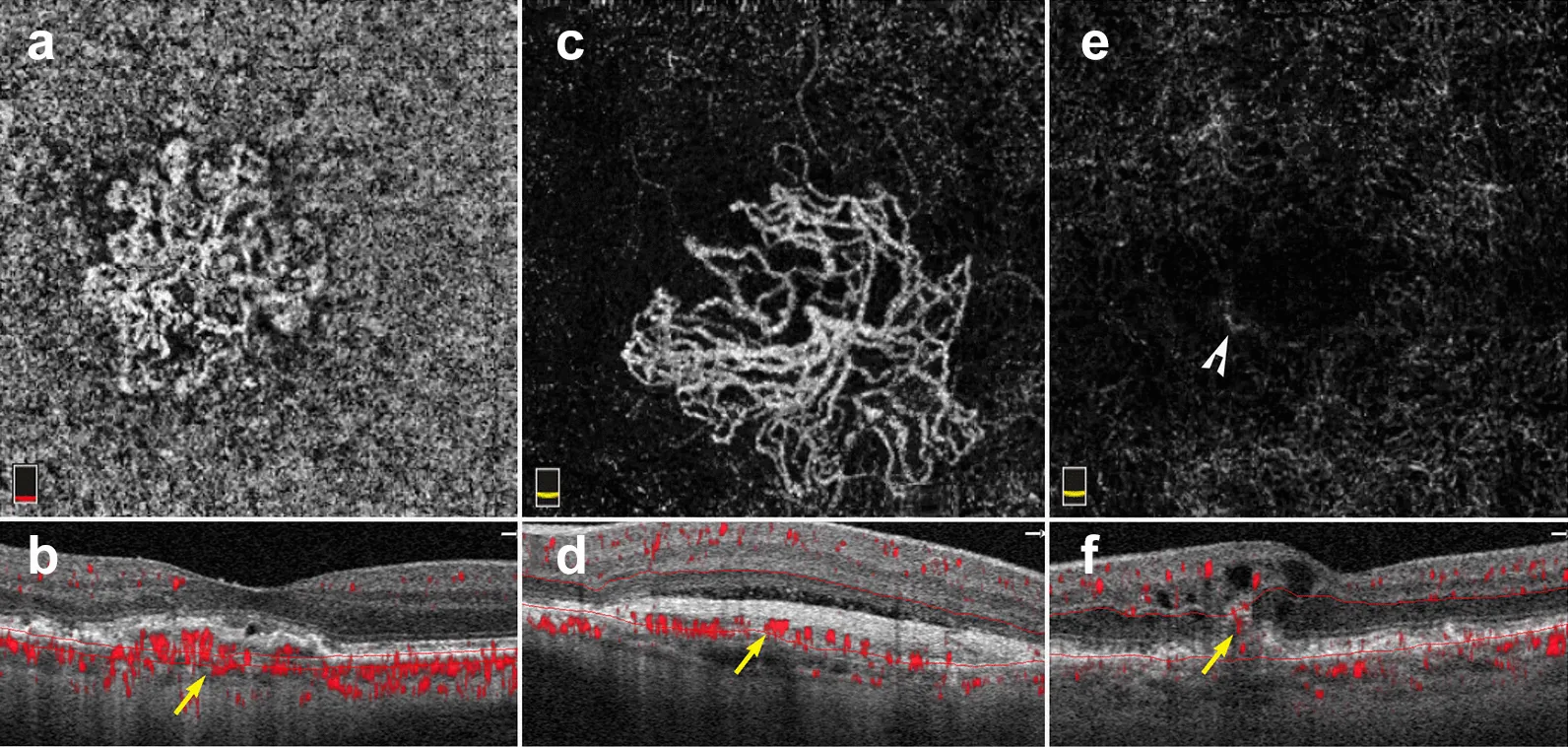
การตรวจหาเส้นเลือดใหม่คอรอยด์ (MNV) เป็นหนึ่งในข้อบ่งชี้หลักของ OCTA สำหรับการประเมิน OCTA บริเวณจอประสาทตา ควรใช้มุมมองแคบ 3×3 มม. หรือ 6×6 มม. ในแนวทางปฏิบัติทางคลินิกของ AAO สำหรับ AMD (2024) รายงานความไวของ OCTA ในการตรวจหาเส้นเลือดใหม่จอประสาทตาเท่ากับ 0.87 และความจำเพาะเท่ากับ 0.97 โดยมีความแม่นยำในการวินิจฉัยเทียบเท่ากับ FA 5)
นอกจากนี้ OCTA อาจตรวจพบเส้นเลือดใหม่จอประสาทตาแบบไม่แสดงอาการ (subclinical MNV) (MNV ชนิดที่ 1 / MNV ใต้ drusen) ซึ่ง FA ไม่สามารถตรวจพบได้ ซึ่งเป็นที่น่าสนใจจากมุมมองของการแทรกแซงตั้งแต่เนิ่นๆ 5)
ใน RVO การสูญเสียเส้นเลือดฝอยและบริเวณที่ไม่มีการไหลเวียนเลือดบริเวณที่อุดตันจะถูกแสดงอย่างชัดเจนด้วย OCTA สามารถประเมินโครงสร้างหลอดเลือดทีละชั้นของจอประสาทตา และสามารถยืนยันหลอดเลือดโป่งพองขนาดเล็ก (MA) ในชั้นเส้นเลือดฝอยตื้นหรือลึกได้ ในแนวทางปฏิบัติทางคลินิกของ AAO สำหรับ RVO (2024) ระบุว่า OCTA มีประโยชน์ในการประเมินขอบเขตของภาวะขาดเลือดในเครือข่ายเส้นเลือดฝอยจอประสาทตา 6)
ใน RAO จะสังเกตเห็นบริเวณที่ไม่มีการไหลเวียนเลือดในเส้นเลือดฝอยตื้นซึ่งสอดคล้องกับบริเวณที่หลอดเลือดแดงที่อุดตันไปเลี้ยงตั้งแต่ระยะเฉียบพลัน ในแนวทางปฏิบัติทางคลินิกของ AAO สำหรับ RAO (2024) การประเมินการไหลเวียนเลือดตั้งแต่เนิ่นๆ ด้วย OCTA ถือว่ามีประโยชน์ในการจัดการ 7)
โรคต้อหินเป็นสาเหตุหลักของการตาบอดที่ไม่สามารถกลับคืนได้ และ OCTA สามารถตรวจพบความหนาแน่นของหลอดเลือดที่ลดลงในดวงตาที่เป็นต้อหิน และคาดว่าจะนำไปใช้ในการวินิจฉัยและประเมินการดำเนินโรค ในแนวทางปฏิบัติทางคลินิกสำหรับโรคต้อหิน (ฉบับที่ 5) กล่าวว่า OCTA สามารถประเมินการไหลเวียนเลือดของจอประสาทตาชั้นผิวและชั้นลึก และเป็นที่ทราบกันว่ายิ่งต้อหินรุนแรงมากเท่าใด การไหลเวียนเลือดของจอประสาทตาชั้นผิวยิ่งลดลง 8)
ในดวงตาที่เป็นต้อหิน ความหนาแน่นของหลอดเลือด (VD) รอบขั้วประสาทตาและบริเวณจุดรับภาพลดลง และสัมพันธ์กับความรุนแรงของโรค การลดลงของ VD จะเด่นชัดกว่าในชั้นผิว มีความไวต่อพื้นล่างของ OCT เชิงโครงสร้างน้อยกว่า และอาจเป็นประโยชน์ในการระบุการดำเนินโรคในต้อหินระยะลุกลาม 8) เมื่อการขยายของหลุมดำเนินไป เส้นเลือดฝอยภายในขั้วประสาทตาจะหายไป และเส้นเลือดฝอยรอบขั้วประสาทตาแบบรัศมีจะหลุดหายไปสอดคล้องกับข้อบกพร่องของชั้นเส้นใยประสาทจอประสาทตา
การหลุดหายของหลอดเลือดขนาดเล็ก (Microvascular dropout: MvD) คือการหายไปของเส้นเลือดฝอยคอรอยด์ในบริเวณฝ่อรอบขั้วประสาทตา มักพบในบริเวณขมับด้านล่างภายในโซนเบตา MvD สัมพันธ์กับการบางลงของ RNFL ข้อบกพร่องของแผ่น cribrosa และข้อบกพร่องของลานสายตา และเป็นตัวบ่งชี้ที่ทำนายอัตราการดำเนินโรคที่เร็วขึ้นของการบางลงของ RNFL และข้อบกพร่องของลานสายตา
VD รอบขั้วประสาทตาและจุดรับภาพที่ต่ำที่จุดเริ่มต้นสัมพันธ์กับอัตราการดำเนินโรคของ RNFL ที่รวดเร็วในต้อหินระยะต้นถึงปานกลาง ความสัมพันธ์นี้เป็นอิสระจากความหนาของ RNFL ที่จุดเริ่มต้น ซึ่งบ่งชี้ว่า OCTA อาจให้การมีส่วนร่วมเพิ่มเติมในการประเมินความเสี่ยงของการดำเนินโรค
การเพิ่มขึ้นอย่างมีนัยสำคัญของ VD ของหลอดเลือดขนาดเล็กหลังการผ่าตัดต้อหินได้รับการรายงานในการศึกษาหลายชิ้น และเชื่อว่าการไหลเวียนเลือดในลูกตาเพิ่มขึ้นเนื่องจากผลของการลดความดันลูกตาจากการผ่าตัด
ทฤษฎีเชิงกล
ความดันลูกตาสูงและการเสียรูปของแผ่น cribrosa: ความดันลูกตาที่สูงขึ้นสัมพัทธ์ทำให้แผ่น cribrosa ผิดรูปและบางลง ขัดขวางการขนส่งแอกซอนของเซลล์ปมประสาทจอประสาทตา และนำไปสู่การตายของเซลล์แบบอะพอพโทซิส
พื้นฐานของการรักษาลดความดันลูกตา: การศึกษาขนาดใหญ่หลายชิ้นถือว่าความดันลูกตาเป็นปัจจัยเสี่ยงที่ใหญ่ที่สุดสำหรับการเกิดและการดำเนินโรคของต้อหิน
ข้อจำกัด: ไม่สามารถอธิบายต้อหินความดันปกติหรือกรณีที่ดำเนินโรคแม้จะลดความดันลูกตาได้อย่างเพียงพอ
ทฤษฎีหลอดเลือด
การลดลงของการไหลเวียนเลือดในตาและภาวะขาดเลือด: ความดันเลือดไปเลี้ยงตาที่ลดลงหรือการสูญเสียการควบคุมตนเองของหลอดเลือดทำให้เส้นประสาทตาสัมผัสกับภาวะขาดเลือดและความเครียดออกซิเดชัน
บทบาทของหลอดเลือดแดงแข็ง: หลอดเลือดแดงแข็งถูกสงสัยว่าสร้างการเต้นเป็นจังหวะสูง ซึ่งอาจทำให้เกิดความเสียหายต่อหลอดเลือดขนาดเล็กของตา9)
ความสำคัญของ OCTA: ในการตรวจสอบทฤษฎีหลอดเลือด OCTA ซึ่งสามารถประเมินความหนาแน่นของหลอดเลือดในเชิงปริมาณได้กลายเป็นเครื่องมือที่มีประสิทธิภาพ
ในช่วงไม่กี่ปีที่ผ่านมา “ทฤษฎีเชิงกล” และ “ทฤษฎีหลอดเลือด” ไม่ได้ถูกมองว่าเป็นอิสระจากกันอีกต่อไป และแนวทางที่โดดเด่นคือการมองทั้งสองอย่างบูรณาการเป็นทฤษฎีชีวกลศาสตร์ของจานประสาทตา ปัจจัยที่ขึ้นกับความดันลูกตาและปัจจัยที่ไม่ขึ้นกับความดันลูกตา (เช่น ความผิดปกติของการไหลเวียน ภูมิต้านทานตนเอง ความเครียดออกซิเดชัน) เชื่อว่ามีปฏิสัมพันธ์ที่ซับซ้อนในการก่อให้เกิดโรคเส้นประสาทตาจากต้อหิน10)
ในตาที่เป็นต้อหิน การบางลงของชั้นใยประสาทและการลดลงของความหนาแน่นของหลอดเลือดรอบจานประสาทตาอาจเกิดขึ้นก่อนความบกพร่องของลานสายตา และการวิจัยเกี่ยวกับการตรวจพบระยะเริ่มต้นโดยใช้ OCTA กำลังดำเนินอยู่ ความสามารถในการวินิจฉัยของ OCTA โดยทั่วไปเทียบเท่ากับ OCT (ความหนา RNFL, ความหนา GCC) แต่มีรายงานว่าความหนา RNFL โดย OCT มีความไวที่ดีกว่าในต้อหินระยะเริ่มต้น ในต้อหินระยะลุกลาม OCTA อาจได้เปรียบเนื่องจากได้รับผลกระทบจาก floor effect น้อยกว่า8) ในปัจจุบัน บทบาทหลักในการวินิจฉัยและการจัดการยังคงเป็นภาพโครงสร้าง OCT และการตรวจลานสายตา โดย OCTA มีบทบาทเสริม
OCTA ใช้พื้นฐานจาก SD-OCT หรือ SS-OCT โดยทำการสแกน B-scan ซ้ำๆ ที่ตำแหน่งจอประสาทตาเดียวกัน และตรวจจับการสูญเสียความสัมพันธ์ (การเปลี่ยนแปลงสัญญาณ) ระหว่างภาพที่ต่อเนื่องกัน เซลล์เม็ดเลือดแดงที่ไหลภายในหลอดเลือดจะเปลี่ยนสัญญาณสะท้อน ในขณะที่เนื้อเยื่อที่อยู่นิ่งรอบข้างไม่เปลี่ยนแปลง ความแตกต่างนี้จะถูกแสดงเป็นแผนที่การไหลเวียนเลือด
อัลกอริทึมหลัก
SSADA: วิธีการสูญเสียความสัมพันธ์ของแอมพลิจูดแบบแบ่งสเปกตรัม ติดตั้งใน AngioVue® (Optovue®)
OMAG: การถ่ายภาพหลอดเลือดขนาดเล็กโดยใช้ OCT ติดตั้งใน Angioplex® (Zeiss®)
OCTARA: วิธีการวิเคราะห์อัตราส่วน OCTA ติดตั้งใน SS-OCTA ของ Triton® (TopCon®)
อื่นๆ: วิธีการรวมการแยกความสัมพันธ์ของความเข้มและเฟสของ AngioScan® (NIDEK®) เป็นต้น
ข้อควรระวังในการเลือกอุปกรณ์
ความไม่เข้ากันระหว่างอุปกรณ์: เนื่องจากอัลกอริทึมและความลึกของชั้นเริ่มต้นที่แตกต่างกัน จึงไม่สามารถเปรียบเทียบโดยตรงระหว่างอุปกรณ์ได้ แม้ในผู้ป่วยรายเดียวกัน
SS-OCTA: TopCon®, Canon® และ Zeiss® มี OCTA แบบกวาดความยาวคลื่น ซึ่งช่วยเพิ่มความเร็วและความละเอียดในการประเมินชั้นคอรอยด์
มาตรฐานคุณภาพภาพ: ภาพที่มีดัชนีความแรงสัญญาณ (SSI) ต่ำกว่า 40 (ต่ำกว่า 6 ใน Zeiss) จะถูกแยกออก
| คำศัพท์ | คำจำกัดความ |
|---|---|
| ความหนาแน่นของหลอดเลือด (VD) | ร้อยละของพื้นที่ที่หลอดเลือดครอบครอง (%) |
| VD รอบหัวประสาทตา | VD ในบริเวณวงแหวนกว้าง 750 ไมโครเมตรนอกขอบจานประสาทตา |
| VD รอบรอยบุ๋มจอตา | VD ในบริเวณเส้นผ่านศูนย์กลาง 1-3 มม. จากศูนย์กลางรอยบุ๋มจอตา |
| ฟลอว์วอยด์ | บริเวณที่เส้นเลือดฝอยหายไป / ไม่มีการไหลเวียนเลือด |
| FAZ | บริเวณไร้หลอดเลือดที่โฟเวีย (foveal avascular zone) |
การวิจัยกำลังดำเนินไปในการใช้ตัวชี้วัดเชิงปริมาณของ OCTA เป็นตัวบ่งชี้ทางชีวภาพในการทำนายการดำเนินของ DR. Srinivasan และคณะ (2023) แสดงให้เห็นในระยะยาวว่าความหนาแน่นของหลอดเลือดในชั้นเส้นเลือดฝอยผิว (SCP-VD) ที่จุดเริ่มต้นมีความสัมพันธ์อย่างมีนัยสำคัญกับความเสี่ยงของการดำเนินของ DR 2) VD 12.90% (กลุ่มที่ดำเนินโรค) เทียบกับ 14.90% (กลุ่มที่ไม่ดำเนินโรค) โดย p=0.032, อัตราส่วนอันตราย 0.825, AUC=0.643
การพัฒนาและการแพร่หลายของ OCTA แบบมุมกว้างพิเศษที่เกิน 12×12 มม. คาดว่าจะช่วยเพิ่มความไวในการตรวจหารอยโรคหลอดเลือดที่จอประสาทตาส่วนปลายและเส้นเลือดใหม่ในจอประสาทตาก่อนระยะงอก 3)
กำลังมีการศึกษาทางคลินิกเพื่อตรวจสอบว่าการรักษาด้วย anti-VEGF สำหรับเส้นเลือดใหม่ใต้จอประสาทตาระดับต่ำกว่าทางคลินิกที่ตรวจพบโดย OCTA สามารถยับยั้งการเปลี่ยนเป็น AMD ชนิดมีน้ำใต้จอประสาทตาได้หรือไม่ 5)
Beros และคณะ (2024) แสดงให้เห็นในกลุ่มตัวอย่างขนาดใหญ่ว่าความเร็วคลื่นชีพจรหลอดเลือดแดง (aPWV) สัมพันธ์กับความเสี่ยงที่เพิ่มขึ้นของโรคต้อหินมุมเปิดปฐมภูมิ 9) ภาวะหลอดเลือดแดงแข็งสูงอาจมีส่วนทำให้เกิดโรคต้อหินผ่านความผิดปกติของหลอดเลือดเล็กในตา ซึ่งชี้ให้เห็นว่าการประเมินความหนาแน่นของหลอดเลือดด้วย OCTA อาจมีบทบาทเป็นตัวบ่งชี้ทางชีวภาพในอนาคต 10)
หัวข้อการวิจัยหลักคือการวิเคราะห์ภาพ OCTA โดยอัตโนมัติด้วย AI การกำหนดมาตรฐานของค่าปริมาณระหว่างเครื่องมือ และการพัฒนาแบบจำลองทำนายการดำเนินโรค หากการกำหนดมาตรฐานของค่าปริมาณสำเร็จ จะทำให้สามารถศึกษาเปรียบเทียบระยะยาวระหว่างหลายศูนย์ได้
ทิศทางหลักคือการขยายมุมมอง เพิ่มความเร็ว การวิเคราะห์อัตโนมัติด้วย AI และการกำหนดมาตรฐานของตัวบ่งชี้ทางชีวภาพเชิงปริมาณ การกำหนดมาตรฐานเพื่อแก้ไขความแตกต่างของค่าปริมาณระหว่างเครื่องมือก็เป็นหัวข้อวิจัยที่สำคัญเช่นกัน การประยุกต์ใช้ในการติดตามโรคทางระบบผ่าน OCTA เยื่อบุตาก็เป็นที่คาดหวัง 3)