TD-OCT(第一代)
波长:810 nm
速度:400 A扫描/秒
轴向分辨率:约10 μm
第一代技术通过可移动参考镜改变光路长度来获取断层图像。目前基本已被SD-OCT取代。

光学相干断层扫描(Optical Coherence Tomography; OCT)是一种利用近红外光干涉现象非侵入性获取眼底和眼前段断层图像的诊断成像设备。其分辨率约为2–5 μm,是眼科超声的约100倍。它能够高分辨率评估视网膜和视神经的细微结构,有助于多种眼病的早期发现和监测。
1991年由Huang等人引入后,OCT在眼科领域迅速普及。如今,它已成为视网膜疾病、青光眼、眼前段疾病和神经眼科等广泛领域的标准检查。保险点数为187点(眼底三维图像分析)。
OCT主要有三代技术。各代特性如下所示。
TD-OCT(第一代)
波长:810 nm
速度:400 A扫描/秒
轴向分辨率:约10 μm
第一代技术通过可移动参考镜改变光路长度来获取断层图像。目前基本已被SD-OCT取代。
SD-OCT(第二代)
波长:840 nm
速度:40,000–100,000 A扫描/秒
轴向分辨率:3–7 μm
第二代技术使用光谱仪和傅里叶变换一次性获取深度信息,是目前临床标准。可精确评估黄斑和视盘。代表机型:Cirrus(蔡司)、Spectralis(海德堡)、RS-3000(尼德克)、3D-OCT(拓普康)。
SS-OCT(第三代)
波长:1050 nm
速度:100,000~400,000 A扫描/秒
轴向分辨率:约5 μm
采用扫频激光和双平衡探测器的第三代技术。由于波长较长,能更好地显示脉络膜等深层结构。优点是不需要EDI-OCT。
OCT是一种无创、非接触的检查,完全没有疼痛。可能需要使用散瞳眼药水,但只需照射光线,不会接触角膜或视网膜。检查时间通常只需几分钟。
| 成像模式 | 特点/用途 |
|---|---|
| 交叉扫描 | 通过中心凹的基本扫描。首先进行。 |
| 5线 | 薄层扫描确认细微结构(如黄斑裂孔) |
| 放射状扫描 | PCV息肉确认、中心外病灶评估 |
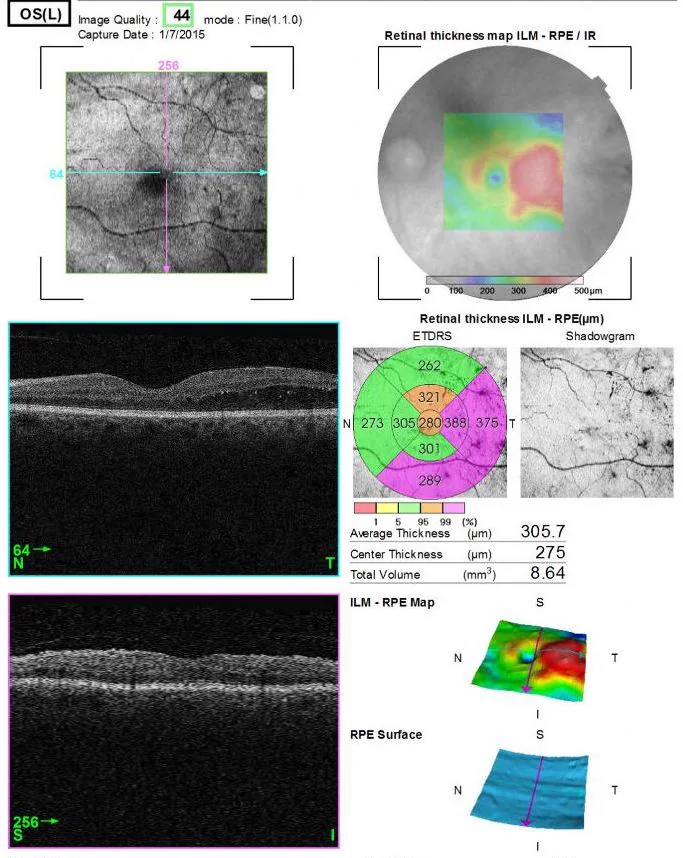
| 黄斑地图 | 视网膜厚度图。糖尿病黄斑水肿、RVO疗效评估 |
| 青光眼分析(cpRNFL/GCA) | RNFL厚度、GCL+IPL厚度。青光眼诊断及进展判定 |
观察部位分为后节OCT(黄斑部、视乳头周围、周边部)和前节OCT(AS-OCT;角膜、前房、房角)。
基本拍摄步骤如下。
在中心凹扫描中,重要的是显示中心凹凹陷且无视网膜内层的切片。黄斑疾病中,由于固视不良可能导致中心偏移,理解视网膜正常结构有助于提高检查技能和诊断技能。
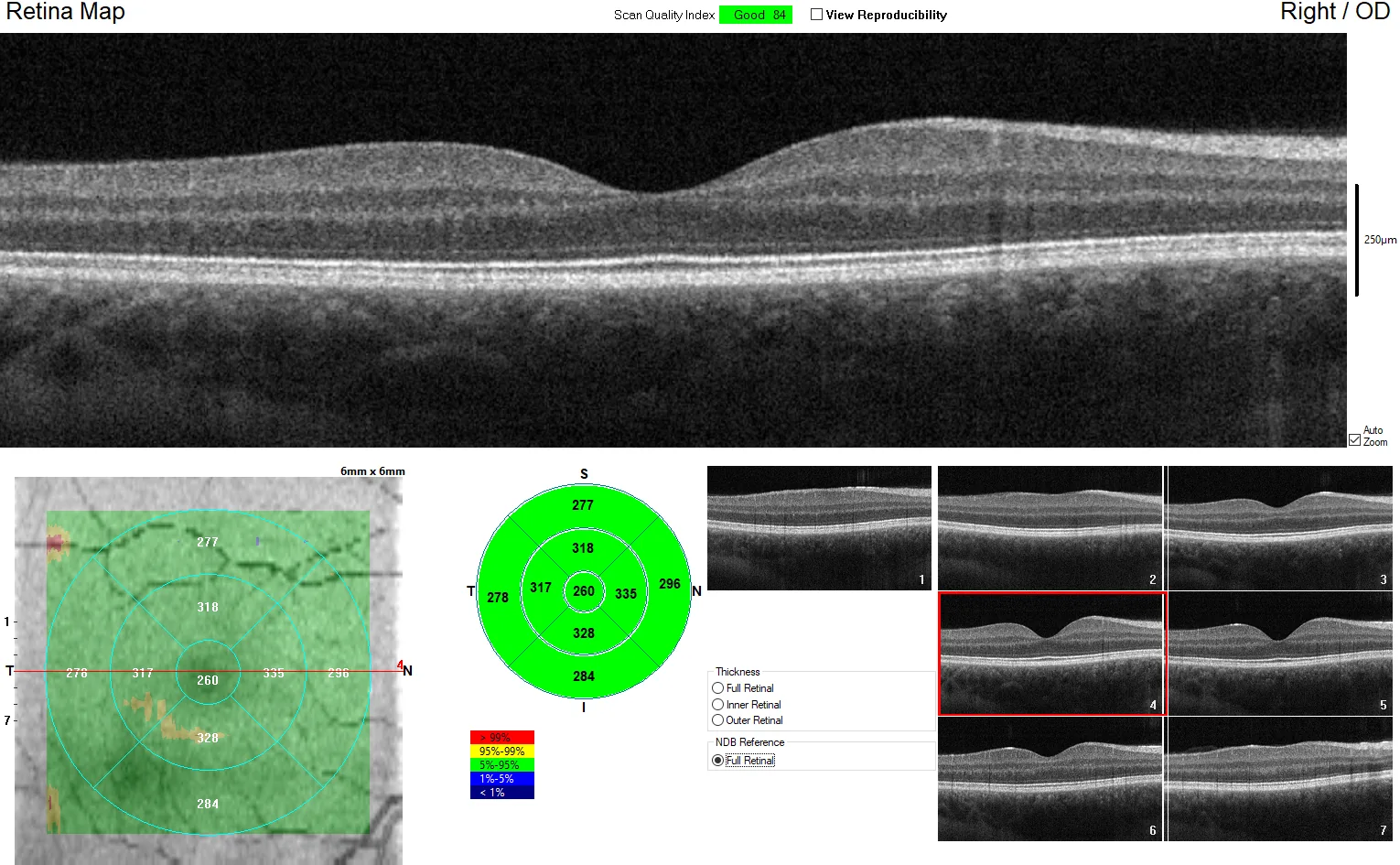
中心凹扫描的正常层结构(从内到外)由以下13层组成:
玻璃体 → 内界膜(ILM)→ 神经纤维层(RNFL)→ 神经节细胞层(GCL)→ 内丛状层(IPL)→ 内核层(INL)→ 外丛状层(OPL)→ 外核层(ONL)→ 外界膜(ELM)→ 椭圆体带(EZ)→ 嵌合体带(IZ)→ 视网膜色素上皮(RPE)→ 脉络膜
各层的反射特性反映病理状态,因此准确的层识别是阅片的基础。
| 疾病 | 代表性OCT所见 |
|---|---|
| 黄斑裂孔 | 视网膜全层缺损±VMT |
| 黄斑前膜(ERM) | 内界膜上的高反射层 |
| 玻璃体黄斑牵拉(VMT) | 后部玻璃体部分脱离伴黄斑牵拉 |
| 糖尿病黄斑水肿 | 视网膜增厚、CME、DRIL、SRF |
| 视网膜静脉阻塞(RVO) | 囊样黄斑水肿、视网膜下液 |
| 年龄相关性黄斑变性(AMD) | CNV(1型/2型/3型)、色素上皮脱离 |
| 中心性浆液性脉络膜视网膜病变(CSC) | 神经感觉视网膜脱离、EDI-OCT显示脉络膜增厚 |
| RPE撕裂 | RPE及外层结构突然消失 |
黄斑裂孔表现为视网膜全层缺损。SD-OCT是诊断黄斑裂孔最敏感和特异的检查方法1)。
黄斑前膜(ERM) 在内界膜上表现为高反射层2)。关于术后视力,据报道80%的病例在玻璃体手术后获得两行或以上的视力改善2)。
糖尿病黄斑水肿:OCT定量测量视网膜厚度是抗VEGF治疗启动和再治疗决策的指标3)。DRIL(视网膜内层紊乱)是视力预后不良的重要标志。
RVO:OCT可定量评估黄斑水肿并检测玻璃体视网膜界面变化4)。
AMD:RPE脱离分为浆液性、纤维血管性和玻璃膜疣样色素上皮脱离,CNVM可分为1型(RPE下)、2型(RPE上)和3型(视网膜内新生血管)5)。
成像条件所致
镜像伪影:由于成像范围设置错误,实际图像反转并重叠显示。
渐晕:周边信号衰减,取决于照明光的入射角。
范围外错误:超出设定深度范围的结构被折叠显示。
患者因素
软件因素
分割错误:自动分层算法错误识别视网膜层。在病变、严重白内障或高度近视眼中频繁发生。
可通过手动校正或重新扫描来处理。如果信号强度指数(SS)低于6,考虑重新检查。
SD-OCT是一种非接触、非侵入性的影像诊断技术,可客观评估青光眼的结构损伤,在青光眼诊断中具有高度实用性6)。在前视野青光眼的诊断中尤其有用,能够在视野缺损出现前捕捉到结构变化6)7)。
RNFL厚度
测量原理:量化内界膜(ILM)与RNFL边界之间的厚度。
TSNIT图:以视神经中心3.4mm直径圆上的RNFL厚度,按T(颞侧)→S(上方)→N(鼻侧)→I(下方)→T(颞侧)顺序显示。
正常模式:上下方向呈双峰(反映弓状神经纤维束的解剖分布)6)。
青光眼检测能力:平均RNFL厚度的敏感性83%,特异性88%(5%水平)。在1%水平,特异性100%,敏感性65%。
ONH参数
视神经乳头分析:自动描绘视盘、杯凹和盘缘。
布鲁赫膜参考:以布鲁赫膜开口定义盘缘,并计算到ILM的最短距离。
诊断能力高的指标:垂直盘缘厚度、盘缘面积和垂直杯盘比具有最高的诊断性能7)。
BMO-MRW:基于布鲁赫膜开口的盘沿宽度评估,重复性优异6)
神经节细胞分析(GCA)
测量对象:黄斑周围神经节细胞层(GCL)和内丛状层(IPL)的复合厚度
不同设备名称:Cirrus称为GCIPL(GCL+IPL),Optovue称为GCC(RNFL+GCL+IPL)
有用参数:最小值、颞下象限、平均值在诊断中最有用6)7)
与地板效应的关系:黄斑参数的地板效应出现晚于RNFL厚度,对晚期评估有用6)
与正常数据库比较有用,但需注意以下因素导致的假阳性和假阴性。
青光眼进展判定有两种方法:事件分析和趋势分析。
Cirrus的GPA整合了这两种方法7)。平均RNFL厚度的检查间可重复性界限为3.89 μm,可重复性减少4 μm以上提示有统计学意义的显著变化。
在进展期青光眼中,RNFL厚度趋于平稳,由于胶质组织和血管等非神经组织残留,很少低于50 μm6)7)。这种“地板效应”降低了SD-OCT在终末期的临床实用性,此时主要依靠视野检查来判定进展。黄斑参数(GCIPL)的地板效应出现比RNFL厚度晚,因此在进展期仍保持一定的实用性6)。
在高度近视眼中,与正常数据库的比较存在局限性。由于RNFL束向颞侧移位,即使在正常眼中也可能被判定为“变薄”。对于此类病例,以患者自身基线进行纵向比较是有效的。通过一系列SD-OCT扫描评估进行性变薄。注意,即使在健康人群中,RNFL厚度也会因年龄增长每年减少约0.52 μm,因此需要考虑这种自然减少。
OCT在神经眼科领域的应用正在迅速扩展9)。视盘周围RNFL(cpRNFL)厚度和黄斑部GCIPL(神经节细胞层+内丛状层)是主要评估参数,有时可在明显的临床体征或视功能障碍出现之前检测到变化9)。
| 疾病 | 急性期表现 | 慢性期表现 |
|---|---|---|
| 视神经炎 | RNFL增厚(轴突水肿)或正常 | RNFL和GCIPL变薄(发病后至6个月) |
| 多发性硬化症(MS) | 无症状时也有cpRNFL减少 | 进展型RNFL和GCIPL萎缩速度增加 |
| NMOSD | 视乳头水肿 | 严重RNFL变薄(<30μm),微囊样黄斑水肿(AQP4阳性者40%)9) |
| 压迫性视神经病变(如垂体腺瘤) | GCIPL鼻侧双重变薄 | 蝶形RNFL萎缩(对应双颞侧偏盲) |
| NAION | 视乳头水肿导致RNFL评估困难,GCIPL变薄先出现 | 水平下鼻侧变薄 |
| 视乳头玻璃膜疣(ODD) | EDI-OCT是检测的金标准 | ODD体积大与RNFL变薄和视野缺损相关 |
| 视乳头水肿 | cpRNFL增厚 | GCIPL变薄>10μm→1年后视功能不良9) |
视神经炎和多发性硬化(MS):RNFL和GCIPL变薄是已确立的生物标志物9)。即使没有眼部症状的MS患者也出现cpRNFL减少,尸检研究证实99%的MS患者存在视神经脱髓鞘病灶。cpRNFL厚度与最佳矫正视力、对比敏感度、色觉和脑萎缩相关。
NMOSD以严重的视神经萎缩为特征,微囊样黄斑水肿的发生率(AQP4阳性约40%)显著高于MS(5%)9)。在MOG-IgG相关视神经炎中,GCIPL相对保留,而在AQP4-IgG相关视神经炎中,GCIPL显著丧失9)。
**视乳头玻璃膜疣(ODD)**的检测:EDI-OCT是金标准9)。ODD表现为位于筛板上方的低反射结构,具有高反射边缘,在埋藏型玻璃膜疣的检测能力上优于B超、自发荧光和CT。PHOMS(视乳头周围高反射卵圆形团块样结构)应作为与ODD不同的现象加以区分9)。
压迫性视神经病变:术前RNFL厚度≥70μm是术后视力和视野改善的显著预测因子9),术前OCT评估可用于预后预测。
由于不同设备的分割算法和正常数据库不同,不同设备之间的数值无法直接比较。建议纵向评估使用同一设备9)。
OCT基于迈克尔逊干涉仪的原理。近红外光(波长840-1050nm)被分为测量光和参考光,分别照射到样本(眼底)和参考镜。两者反射光重新结合时产生的干涉条纹(干涉图)用于计算每个深度的反射强度。沿深度方向的反射强度剖面称为A扫描,A扫描横向排列形成B扫描(断层图像)。
在青光眼和视神经疾病中,优先评估以下三层9)。
随着RGC损伤,RNFL会脱落。所有RGC中约50%集中在黄斑中心20°区域,即使在早期青光眼中,也可能有约50%的RGC已经消失6)。SD-OCT通过RNFL厚度评估RGC轴突的脱落,GCA评估包含细胞体的内层变薄。
最大的区别在于使用的波长和深层结构的可视化能力。SD-OCT使用840 nm波段,SS-OCT使用1050 nm波段。1050 nm受黑色素散射较少,更容易穿透RPE,因此SS-OCT在观察脉络膜和巩膜方面更优。此外,SS-OCT的成像速度超过SD-OCT,便于进行广角扫描。另一方面,两者的轴向分辨率都在5-7 μm左右,没有显著差异。
SS-OCT在1050 nm波长下的高速、广角扫描能力推进了对厚脉络膜疾病谱的评估。包括脉络膜增厚(pachydysm)在内的中心性浆液性脉络膜视网膜病变、息肉状脉络膜血管病变(PCV)和中心凹旁毛细血管扩张症的评估精度得到提高,有助于阐明病理机制。此外,正在尝试在与黄斑部相同的扫描中评估包括周边视网膜在内的广泛区域的断层图像。
针对青光眼、AMD和DME的自动诊断AI已经开发出来,诊断准确性的提高已有报道。基于深度学习的OCT图像分析正在实现分割精度的提高和报告自动生成,并逐步投入实际应用6)7)。
需要纵向研究来确立OCT作为阿尔茨海默病、帕金森病等神经退行性疾病筛查和监测工具的有效性9)。REM睡眠行为障碍(RBD)患者的RNFL和GCIPL变薄作为前驱期帕金森病的替代标志物受到关注9)。
American Academy of Ophthalmology Retina/Vitreous Panel. Idiopathic Macular Hole Preferred Practice Pattern. Ophthalmology. 2019.
American Academy of Ophthalmology Retina/Vitreous Panel. Idiopathic Epiretinal Membrane and Vitreomacular Traction Preferred Practice Pattern. Ophthalmology. 2019.
American Academy of Ophthalmology Retina/Vitreous Panel. Diabetic Retinopathy Preferred Practice Pattern. Ophthalmology. 2024.
American Academy of Ophthalmology Retina/Vitreous Panel. Retinal Vein Occlusions Preferred Practice Pattern. Ophthalmology. 2024.
American Academy of Ophthalmology Retina/Vitreous Panel. Age-Related Macular Degeneration Preferred Practice Pattern. Ophthalmology. 2024.
日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126:85-177.
American Academy of Ophthalmology. Primary Open-Angle Glaucoma Preferred Practice Pattern®. 2020.
American Academy of Ophthalmology. Primary Open-Angle Glaucoma Suspect Preferred Practice Pattern®. 2020.
Lo C, Vuong LN, Micieli JA. Recent advances and future directions on the use of optical coherence tomography in neuro-ophthalmology. Taiwan J Ophthalmol. 2021;11(2):107-131.