中心性浆液性脉络膜视网膜病变(CSC)是一种在黄斑部 引起浆液性视网膜脱离 (SRF)的疾病,荧光素眼底血管造影 (FA )可见RPE 水平的荧光渗漏。
好发于30~40岁男性,男女比例约为8:1。
类固醇 是最大的危险因素(OR 37.1),所有给药途径均有发病风险。大多数典型病例在3-4个月内自行缓解,但如果SRF持续超过6个月,则作为慢性型需要积极治疗。
慢性型的一线治疗是半剂量PDT (光动力疗法 )。PLACE试验显示其显著优于微脉冲激光 ,SPECTR A试验显示12周时SRF完全消退率为78%,而依普利酮为17%9) 。
它是厚脉络膜 疾病谱的一部分,厚脉络膜 组的自然消退率低于非厚脉络膜 组(28.8% vs 48%)3) 。
FA 和OCT 的结合是诊断的基础,IA有助于评估脉络膜 异常和鉴别诊断。 中心性浆液性脉络膜视网膜病变(Central Serous Chorioretinopathy; CSC)是一种在黄斑部 发生浆液性视网膜脱离 (SRF)的疾病。荧光素眼底血管造影 (FA )显示视网膜色素上皮 (RPE )水平的荧光渗漏。它被认为是继年龄相关性黄斑变性 、糖尿病视网膜病变 和视网膜静脉阻塞 之后第四常见的视网膜 疾病。1866年von Graefe将其描述为“中心性复发性视网膜 炎”,1967年Gass等人命名了现在的病名。在日本,以前通常仅指黄斑部 局限性视网膜脱离 的典型病例(所谓中心性视网膜 炎),但现在分为三种亚型。许多病例可自行愈合,但SRF持续存在的病例视力 预后可能恶化。
流行病学上,男性发病率为每10万人9.9例,女性为1.7例,男女比例约为8:14) 。一项250只眼的研究显示平均年龄46.6岁,男性占88.4%3) 。
本病有以下三种亚型。
典型型
患者人群 :以30-40岁男性为主。通常单眼发病。
病理 :黄斑部 局限性浆液性视网膜脱离 。
病程 :大多数在3-4个月内自行吸收。视力 预后通常良好。
慢性型
患者人群 :多见于老年人。常为双眼发病。近期有增加趋势。
病理生理 :广泛的RPE 损伤。常反复发作。
病程 :SRF持续6个月以上。需要积极治疗5) 。
泡状视网膜脱离
患者群体 :多见于大剂量使用类固醇 的病例。相当于日本以前称为多发性后极部视网膜色素上皮 病变的疾病。
病理生理 :伴有泡状视网膜脱离 的重症型。伴有大型RPE 脱离(PED )和多发性白色斑纹。
病程 :SRF的范围常波及眼底下方,视力 预后可能较差。
复发率很高,一年内高达50%。本病被认为是厚脉络膜 疾病谱(以脉络膜 增厚为特征的疾病群)的一部分3) 9) 。
Q
能自然痊愈吗?
A
典型病例常在3~4个月内自然缓解,视力 预后一般良好。但一年内复发率高达50%。若SRF持续6个月以上,则视为慢性型,需要PDT 等治疗。在厚脉络膜 组中,自然消退率低于非厚脉络膜 组(28.8% vs 48%),复发率也更高(31.2% vs 10.4%),需注意3) 。
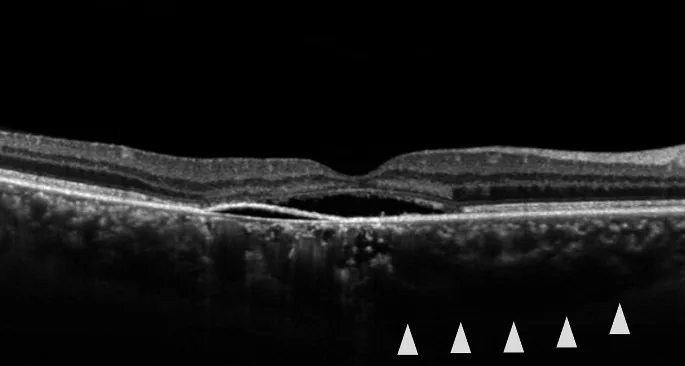
中心性浆液性脉络膜视网膜病变的OCT。黄斑部可见浆液性视网膜脱离和轻度PED。 Koizumi H, et al. Central serous chorioretinopathy and the sclera: what we have learned so far. Jpn J Ophthalmol. 2024. Figure 4. PM
CI D: PMC11420308. License: CC BY.
黄斑部 OCT 显示中心凹 下伴有视网膜下液 的浅层浆液性视网膜脱离 。还可见RPE 小隆起和提示脉络膜 增厚的表现,显示了中心性浆液性脉络膜视网膜病变的临床图像。
视力 下降远视 化(hyperopic shift)。视物变形 中心暗点 一样,是患者不适的症状,可能影响驾驶和工作。小视症 :物体看起来比实际小。中心暗点 对比敏感度 下降色觉异常 (获得性蓝黄色觉异常 )。
当视网膜下液 被吸收后,中心暗点 和视物变形 症会相对较早改善。另一方面,小视症和对比敏感度 下降可能持续存在。慢性型容易复发,视力 不良的病例较多。典型病例多为单眼性,而慢性型和泡状视网膜脱离 多为双眼性。
通过裂隙灯 显微镜和各种影像检查可观察到以下所见。
浆液性视网膜脱离 (SRF)黄斑部 无出血的圆形或椭圆形隆起。视网膜色素上皮脱离 (PED )OCT 上最多63%可见。沉着物 :脱离视网膜 后面的白色点状沉积物。多见于色素上皮脱离和浆液性视网膜脱离 的好发部位。视网膜 下纤维蛋白沉积(白色斑纹)脉络膜 增厚OCT (增强深度成像OCT )评估。正常为250~300μm,而本病为350~450μm以上。厚脉络膜 组的中心凹 下脉络膜 厚度(SFCT)据报道为406.6±80.8μm 3) 。部分病例可达500μm。Haller层血管扩张和Sattler层变薄 :EDI-OCT 可确认的脉络膜 结构特征性变化 3) 。
慢性型中,色素上皮损伤广泛,有时可见伴有色素上皮萎缩索并向下延伸的视网膜脱离 。泡状视网膜脱离 中,视网膜脱离 严重,常波及眼底下方,伴有大型色素上皮脱离和多发性白色斑纹。
本病的根本原因尚未明确,但脉络膜 血管通透性亢进被认为是本质。已知压力和类固醇 与本病的发病和恶化有关。以下风险因素已被报道。
风险因素 关联强度 备注 类固醇 OR 37.11) 所有给药途径 A型性格 中等 与压力相关 妊娠 0.008%/年7) 产后自然缓解多见 OSA 61%的患者9) 交感神经亢进 PDE5抑制剂 病例报告8) 停药后消退
类固醇 系统性红斑狼疮 (SLE )患者使用类固醇 后发病的报道,OR值为37.1(95% CI 6.2–221.8),极高1) 。类固醇 与本病的发生和加重有关,因此对于正在使用的患者,考虑停药或减量非常重要。需与其他科室协作,根据具体病例处理。精神科药物 :有服用喹硫平(非典型抗精神病药)后发病的报道。停药2周后最佳矫正视力 改善,2个月后完全消退2) 。PDE5抑制剂 :有服用他达拉非5mg后发病,停药3个月后消退的病例报道8) 。妊娠 :妊娠期发病率为每年0.008%7) 。OSA(阻塞性睡眠呼吸暂停) :61%的患者存在OSA9) 。COVID-19疫苗 :有接种后复发的报道,认为与HPA轴激活有关6) 。幽门螺杆菌感染 :53–69%的患者存在幽门螺杆菌感染,OR值为4.6。
发病机制用多因素假说(multi-hit theory)解释9) 。认为分为三个阶段:①解剖学易感因素(短眼轴 、巩膜 增厚、涡静脉引流不对称等),②诱发事件(类固醇 、压力、OSA等),③代偿失调。
避免压力,保持规律生活。
正在使用类固醇 药物的患者,请勿自行停药,如出现眼部症状请咨询医生。
如有睡眠呼吸暂停,接受适当治疗(如CPAP)非常重要。
吸烟可能会增加风险,因此建议戒烟。
Q
类固醇与中心性浆液性脉络膜视网膜病变有什么关系?
A
类固醇 是本病的最大危险因素,无论滴眼、吸入、注射还是口服,所有给药途径都会增加风险。据报道,比值比高达37.11) 。如果确诊本病且正在使用类固醇 ,请与主治医生商量,尽可能考虑减量或停药。如果因全身性疾病而使用类固醇 ,则需要每例患者与其他科室协作处理。
本病的诊断以FA 和OCT 的组合为基础。主要检查的特点如下所示。
检查 特征性所见 主要作用 FA 点状荧光素 渗漏 确定渗漏点和治疗计划 IA(ICG) 脉络膜 高荧光评估脉络膜 异常和鉴别诊断 OCT 显示SRF和色素上皮脱离 随访和定量
各项检查的详细内容如下。
荧光素眼底血管造影 (FA )RPE 的点状荧光素 渗漏,造影早期出现点状强荧光,随时间扩大并积聚在视网膜 下。渗漏形态有喷出型 和圆形增大 两种。典型的渗漏模式为墨渍样(31%)和烟囱样(12%)。典型病例渗漏点常为单个,而大泡性视网膜脱离 常可见多个渗漏点。慢性型可见颗粒状强荧光和晚期弥漫性弱荧光渗漏,常难以识别单个渗漏点。吲哚青绿血管造影(IA/ICG) :造影中期可见脉络膜 强荧光(异常脉络膜 组织染色)。此征象见于所有类型,但与典型病例相比,慢性型和大泡性视网膜脱离 范围更广、程度更强,且为双眼性。有助于评估厚脉络膜 变化及鉴别诊断(CNV /PCV )。OCT 视网膜脱离 尤为有效。还可观察到光感受器外节线性延长(冰柱样改变)。EDI-OCT (频域OCT 的脉络膜 观察模式)可准确评估脉络膜 厚度。正常中心凹 下脉络膜 厚度为250300μm,而本病为350450μm(部分病例超过500μm),形态学上也证实了脉络膜 异常。OCTA (OCT血管成像 )脉络膜 毛细血管的血流障碍(阴影效应)6) 。眼底自发荧光 (FAF )RPE 损伤范围。慢性CSC中可见边缘强荧光的带状弱荧光(萎缩带),有助于推测病程和确认视网膜下液 向下移动。
渗出型年龄相关性黄斑变性 (尤其是息肉状脉络膜血管病变 ;PCV ) :通过ICG造影 确认息肉状病变。50岁以上患者是特别重要的鉴别诊断。特发性脉络膜新生血管 :发生于年轻患者时需鉴别。IA有助于鉴别。Vogt-小柳-原田病 (VKH)全葡萄膜炎 症状、多发性浆液性视网膜脱离 。视盘小凹 黄斑 病变视盘小凹 相关的SRF。狼疮性脉络膜 视网膜 病变 :女性、活动性SLE 、双眼性SRF需与本病鉴别1) 。视网膜 血管病视网膜静脉阻塞 、糖尿病黄斑 病变等引起黄斑部 视网膜脱离 的疾病鉴别。脉络膜 肿瘤高血压及妊娠高血压综合征 :可继发性引起黄斑部 SRF。孔源性视网膜脱离 视网膜脱离 病例中需要鉴别。
目前尚无针对本病的既定药物治疗。对荧光素眼底血管造影 (FA )上的荧光渗漏点进行激光光凝是目前唯一普遍接受的治疗方法,治疗方案根据类型、分期和渗漏点位置决定。
典型的急性型有自然缓解趋势,初发急性期可等待4-6个月让视网膜下液 自然吸收。典型病例常在3-4个月内完全吸收,视力 预后良好。非厚脉络膜 组的自然消退率为48%,而厚脉络膜 组仅为28.8%3) 。
如果自觉症状严重且患者希望早期改善,即使是急性典型病例也可考虑光凝治疗。若正在使用类固醇 ,应尽可能减量或停用。若因全身疾病使用类固醇 ,需与相关科室协作个体化处理。
对于发病后4-6个月以上仍持续脱离的病例、复发病例、重症病例,或对侧眼因本病残留视力 障碍的病例(慢性型、大疱性视网膜脱离 ),需要通过治疗促进视网膜下液 早期吸收,因为黄斑 损伤会导致视力 预后不良。
适用于渗漏点距中心凹 500μm以上且至少位于中心凹 无血管区之外的情况。直接光凝FA 上确定的渗漏点(200μm光斑、0.2秒、70-120mW)。光凝强度应为弱光凝,在视网膜 深层产生淡灰白色光凝斑 。即使渗漏位于视盘黄斑 之间,弱光凝也无问题。若渗漏位于色素上皮脱离内,仅需光凝渗漏点。
光凝有效时,视网膜脱离 在数周内消退。但自觉症状的改善通常需要更长时间。并发症包括中心凹 误照、术后脉络膜新生血管 (CNV )形成(长波长、短时间、小光斑光凝更易发生)等。
使用577nm黄色激光。设置参数为240mW、200μm光斑、200ms、5%占空比进行照射4) 。由于能量选择性作用于RPE ,不形成瘢痕。可直接照射中心凹 下方。
Bodea F等人(2024)报告,接受MPLT治疗的中心性浆液性脉络膜视网膜病变患者,治疗后2周SRF减少,6周消退4) 。
对于妊娠期本病,微脉冲激光 被认为是唯一安全的治疗选择7) 。
观察随访
适应症 :急性典型病例的一线治疗。
持续时间 :4-6个月。等待自然吸收。
注意 :使用类固醇 期间,应与其他科室协调考虑减量或停药。
PDT(光动力疗法)
适应症 :慢性中心性浆液性脉络膜视网膜病变的一线治疗。
方法 :推荐半剂量(半光通量)PDT 。
依据 :PLACE试验和SPECTR A试验(12周SRF消退率78% vs 依普利酮17%)证明了其有效性9) 。
微脉冲激光
特点 :无瘢痕,可直接照射中心凹 下方。
优势 :是唯一可在妊娠期使用的治疗方法7) 。
效果 :2周时SRF减少,6周时消退4) 。
用于渗漏点位于中心凹 无血管区或慢性型等无法进行激光光凝的病例。使用维替泊芬(Visudyne)的半剂量PDT (常规剂量的一半)或半光通量PDT (一半激光输出)被推荐为慢性中心性浆液性脉络膜视网膜病变的一线治疗9) 。
主要临床试验结果如下9) 。
PLACE试验 :半剂量PDT 在SRF消退率、BCVA改善、视网膜 敏感度和RPE 脱离高度等所有指标上均显著优于微脉冲激光 (HS ML)。SPECTR A试验 :半剂量PDT 相比依普利酮,SRF完全消退率显著更高(12周时:78% vs 17%)。12个月时,初始PDT 组的BCVA优于依普利酮→延迟PDT 组。REPLACE试验 :HS ML无效的患者交叉至半剂量PDT 后改善。交叉1年后,PDT 组SRF完全消退率为78%(32眼中),HS ML组为67%(10眼中)。仅PDT 组视网膜 敏感度改善。SPECS试验 :依普利酮无效的患者交叉至半剂量PDT 后改善。交叉3个月后,PDT 组SRF完全消退率为87.5%(37眼中),HS ML组为22.2%(9眼中)。PDT 实施时机的重要性视力 改善的可能性越低。据报道,每延迟1周,可能性降低4%,因此适时干预很重要9) 。对57只半剂量PDT 眼的分析未发现中心凹 萎缩病例9) 。
盐皮质激素受体拮抗剂。每日50mg使用。在VICI 试验 (多中心随机双盲安慰剂对照试验)中,治疗12个月后,依普利酮在BCVA改善方面与安慰剂相比无显著差异9) 。其效果被认为不如PDT ,有病例报告显示即使治疗10个月仍无效5) 。
一种新疗法,使用590nm黄色LED和625nm红色LED各照射6分钟5) 。有病例报告显示,对于依普利酮无效的慢性中心性浆液性脉络膜视网膜病变伴浆液性色素上皮脱离,最佳矫正视力 从20/80改善至20/25,中心视网膜 厚度从752μm减少至296μm(1个月时)5) 。
类固醇 滴眼液或全身给药可能加重或延长病程,原则上应避免使用。使用维替泊芬的PDT 可能出现药物供应问题。PBM作为替代方案正在研究中5) 。
依普利酮需注意高钾血症等副作用。
慢性型视功能障碍持续时,建议尽早考虑在专业机构治疗。
Q
怀孕期间患上中心性浆液性脉络膜视网膜病变该怎么办?
A
据报道,妊娠期本病的发病率为0.008%/年7) 。多数病例在产后3个月内自然缓解。如果需要治疗,微脉冲激光 (MPLT)被认为是妊娠期唯一安全的选择,并且可以直接照射到中心凹 下方而不留瘢痕7) 。
Q
选择哪种治疗方法?
A
对于急性典型病例,基本是观察4-6个月。对于SRF持续超过6个月的慢性型,半剂量PDT 是一线选择9) 。SPECTR A试验显示,12周时SRF完全消退率在PDT 组为78%,依普利酮组为17%,差异显著。如果渗漏点在中心凹 无血管区外侧,选择激光光凝(弱凝固);在中心凹 正下方或妊娠期,选择微脉冲激光 。依普利酮在VICI 试验中与安慰剂相比,BCVA改善无显著差异9) 。
本病的发病机制以“脉络膜 血管通透性增高”为中心,由复合机制解释。根据IA研究,原发病灶位于脉络膜 ,继发性引起RPE 损伤。为什么脉络膜 会发生病变,目前仍有很多不明之处。已知压力和类固醇 与本病的发生和加重有关。
脉络膜 血管(主要是Haller层扩张血管)通透性增高脉络膜 间质压升高、脉络膜 增厚RPE 外侧血-视网膜屏障 破坏RPE 泵功能下降SRF在视网膜 下腔积聚
在FA 上表现为色素上皮的荧光渗漏和视网膜 下染料积存。OCT 研究显示,本病患者脉络膜 较正常眼增厚,形态学上也证明了脉络膜 异常。
Cheung CMG等人(2025)用多重打击理论解释本病的发病机制9) 。
解剖学易感性 :短眼轴 、巩膜 增厚、涡静脉引流分布不对称等。本病在近视 眼中罕见,眼球形态参与发病机制。诱发事件 :类固醇 、压力、OSA、药物使用等。无明显诱因的病例也不少见。代偿机制的激活 :Haller层血管扩张、涡静脉吻合形成(约90%的厚脉络膜 疾病谱中存在10) )。代偿失调 :脉络膜 毛细血管缺血→RPE 损伤→外层视网膜 萎缩→恶性循环9) 。
CSC眼的前部和后部巩膜 显著厚于正常眼9) 。由于涡静脉斜行穿过巩膜 (巩膜 内走行约4mm),巩膜 增厚可能增加静脉流出阻力,导致脉络膜 充血 9) 。62%的CSC眼可见脉络膜 上腔液体积聚(loculation of fluid),19%可见睫状体 脉络膜 渗出(ciliochoroidal effusion)9) 。在类固醇 诱发的CSC中,巩膜 比特发性CSC更薄,提示巩膜 在发病机制中的作用可能不同9) 。
PDE5抑制剂(如他达拉非) :通过增加cGMP/NO扩张和增厚脉络膜 血管,诱发本病8) 。喹硫平 :推测通过D1受体介导的血管扩张机制2) 。
基于多模态成像的新分类已被提出9) 。
简单型 :RPE 异常总面积≤2 DA(视盘面积)复杂型 :RPE 异常总面积>2DA或多灶性非典型型 :大泡型、RPE 撕裂、合并其他视网膜 疾病
每个类别内又分为初发、复发和消退亚类。复杂型CSC发生脉络膜新生血管 (MNV)的风险高于简单型CSC。10名视网膜 专家之间的一致性κ=0.57(中等),分类仍在持续改进中9) 。
超过40%的CSC患者存在厚玻璃膜疣 9) 。伴有厚玻璃膜疣 的CSC眼RPE 异常更广泛,其形态和分布与传统软性玻璃膜疣 不同。已显示Haller层增厚与脉络膜 毛细血管变薄相关9) 。
PBM作为一种不使用维替泊芬的新疗法备受关注。它采用590nm黄色LED和625nm红色LED组合照射5) 。在维替泊芬供应不足的情况下,它被期待作为替代治疗。
厚脉络膜 表现的有无作为本病的预后预测因子日益重要。与非厚脉络膜 组相比,厚脉络膜 组的复发率更高(31.2% vs 10.4%),自然消退率更低(28.8% vs 48%)3) 。厚脉络膜 表现的有无是决定治疗方案的重要指标。
COVID-19疫苗接种后本病发病和复发的报告不断积累6) 。提示疫苗可能通过激活HPA轴和类固醇 激素样作用参与其中。
Rao Q, Wang R, Liu C, et al. Systemic lupus erythematosus combined with central serous chorioretinopathy treated with glucocorticoids. J Int Med Res. 2023;51(3):03000605231163716.
Durmaz Engin C, Güngör SG, Yıldız Şeker DY. Central serous chorioretinopathy following oral quetiapine. GMS Ophthalmol Cases. 2023;13:Doc13.
Bhattacharyya S, Ghorpade A, Mandal S, et al. Presentation and outcome of central serous chorioretinopathy with and without pachychoroid. Eye (Lond). 2024;38:127-131.
Bodea F, Munteanu M, Balica NC, et al. Micropulse Laser Therapy in Central Serous Chorioretinopathy. Clin Pract. 2024;14:2484-2490.
Iovino C, Coppola M, Gioia AD, et al. Photobiomodulation therapy for serous pigment epithelial detachment in chronic central serous chorioretinopathy. Retinal Cases Brief Rep. 2025;19:766-770.
Sanjay S, Leo SW, Au Eong KG. Recurrent central serous chorioretinopathy following COVID-19 vaccination. Am J Ophthalmol Case Rep. 2022;27:101644.
Ochinciuc R, Roșca C, Zaharia IM, et al. Central serous chorioretinopathy in pregnancy. Rom J Ophthalmol. 2022;66(4):382-385.
Alsarhani A, Alsulaiman R, Aljehani M, et al. Central serous chorioretinopathy associated with Tadalafil. Case Rep Ophthalmol. 2022;13:1008-1011.
Cheung CMG, Lai TYY, Gomi F, et al. Pathogenesis and management of pachychoroid disease spectrum. Eye (Lond). 2025;39:819-834.
Ochinciuc U, Pop RM, Mălāescu GD, et al. Vortex vein anastomosis in pachychoroid spectrum disease. Clin Ophthalmol. 2023;17:53-62.
复制全文后,可以粘贴到你常用的 AI 助手中提问。
打开下面的 AI 助手,并把复制的内容粘贴到聊天框。