النوع النمطي
الفئة العمرية: الذكور في الثلاثينيات والأربعينيات من العمر. عادة ما يكون أحادي العين.
الحالة المرضية: انفصال مصلي محدود في البقعة.
المسار: يختفي تلقائيًا في معظم الحالات خلال 3-4 أشهر. التشخيص البصري جيد بشكل عام.

اعتلال المشيمية والشبكية المصلي المركزي (Central Serous Chorioretinopathy; CSC) هو مرض يحدث فيه انفصال مصلي للشبكية (SRF) في منطقة البقعة. يُلاحظ تسرب فلوريسئيني على مستوى ظهارة الشبكية الصبغية (RPE) في تصوير الأوعية بالفلوريسئين (FA). يُعتبر رابع أكثر أمراض الشبكية شيوعًا بعد التنكس البقعي المرتبط بالعمر واعتلال الشبكية السكري وانسداد الوريد الشبكي. وصفه فون غريفه في عام 1866 باسم “التهاب الشبكية المركزي المتكرر”، وسماه غاس وزملاؤه بالاسم الحالي في عام 1967. في السابق، كان يشير في اليابان غالبًا إلى الحالات النمطية التي تسبب انفصالًا شبكيًا محدودًا في البقعة (ما يسمى بالتهاب الشبكية المركزي)، ولكنه الآن يُصنف إلى ثلاثة أنواع. تتعافى معظم الحالات تلقائيًا، ولكن في الحالات التي يستمر فيها انفصال السائل تحت الشبكية، قد يسوء التشخيص البصري.
وبائيًا، معدل الإصابة هو 9.9 لكل 100,000 رجل و1.7 لكل 100,000 امرأة، ونسبة الجنس حوالي 8:1 (ذكور:إناث)4). في دراسة شملت 250 عينًا، كان متوسط العمر 46.6 سنة، و88.4% من الذكور3).
لهذا المرض ثلاثة أنواع:
النوع النمطي
الفئة العمرية: الذكور في الثلاثينيات والأربعينيات من العمر. عادة ما يكون أحادي العين.
الحالة المرضية: انفصال مصلي محدود في البقعة.
المسار: يختفي تلقائيًا في معظم الحالات خلال 3-4 أشهر. التشخيص البصري جيد بشكل عام.
النوع المزمن
الفئة العمرية: أكثر شيوعًا لدى كبار السن. غالبًا ما يكون ثنائي العين. في ازدياد مؤخرًا.
الإمراضية: اضطراب واسع النطاق في ظهارة الشبكية الصبغية. غالبًا ما يتكرر.
المسار: استمرار السائل تحت الشبكية لأكثر من 6 أشهر. يتطلب علاجًا فعالًا 5).
انفصال الشبكية الفقاعي
مجموعة المرضى: شائع في حالات الاستخدام المكثف للستيرويدات. يتوافق مع ما كان يُسمى سابقًا باعتلال ظهارة الشبكية الصبغية المتعدد في القطب الخلفي في اليابان.
الإمراضية: شكل حاد مصحوب بانفصال الشبكية الفقاعي. يرافقه انفصال كبير في ظهارة الشبكية الصبغية وبقع بيضاء متعددة.
المسار: غالبًا ما يمتد السائل تحت الشبكية إلى أسفل قاع العين، وقد يكون تشخيص الرؤية سيئًا.
معدل التكرار مرتفع يصل إلى 50% خلال عام واحد. يُعتبر هذا المرض جزءًا من طيف أمراض المشيمية السميكة (مجموعة أمراض تتميز بسماكة المشيمية) 3)9).
في الحالات النمطية، غالبًا ما يحدث شفاء تلقائي خلال 3-4 أشهر، ويكون تشخيص الرؤية جيدًا بشكل عام. ومع ذلك، يصل معدل التكرار إلى 50% خلال عام واحد. إذا استمر السائل تحت الشبكية لأكثر من 6 أشهر، يُعتبر مزمنًا ويتطلب علاجًا مثل العلاج الضوئي الديناميكي. في مجموعة المشيمية السميكة، يكون معدل الشفاء التلقائي أقل (28.8%) مقارنة بالمجموعة غير السميكة (48%)، ومعدل التكرار أعلى (31.2% مقابل 10.4%)، لذا يجب الحذر 3).
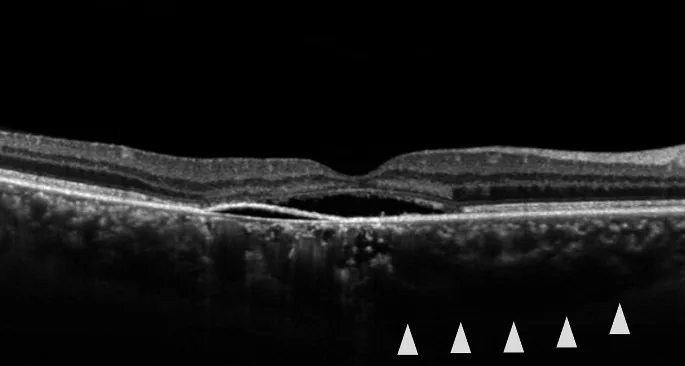
عند امتصاص السائل تحت الشبكية، تتحسن العتمة المركزية وتشوه الرؤية (Metamorphopsia) في وقت مبكر نسبيًا. من ناحية أخرى، قد يبقى صغر البصر وانخفاض حساسية التباين. في النوع المزمن، تتكرر الانتكاسات وتكون حالات ضعف البصر شائعة. في الحالات النموذجية، تكون إصابة عين واحدة أكثر شيوعًا، بينما في النوع المزمن والانفصال الشبكي الفقاعي، تكون إصابة كلتا العينين أكثر شيوعًا.
يكشف الفحص بالمصباح الشقي (Slit lamp) وفحوصات التصوير المختلفة عن النتائج التالية.
في النوع المزمن، يكون تلف الظهارة الصباغية واسع النطاق، وقد يُرى انفصال شبكي يمتد إلى الأسفل مصحوبًا بحبال ضامرة للظهارة الصباغية. في الانفصال الشبكي الفقاعي، غالبًا ما يكون الانفصال الشبكي شديدًا ويمتد إلى الجزء السفلي من قاع العين، مصحوبًا بانفصال كبير للظهارة الصباغية وبقع بيضاء متعددة.
السبب الأساسي لهذا المرض غير معروف، لكن يُعتقد أن زيادة نفاذية الأوعية المشيمية هي الآلية الأساسية. من المعروف أن الإجهاد والستيرويدات مرتبطان بظهور المرض وتفاقمه. تم الإبلاغ عن عوامل الخطر التالية.
| عوامل الخطر | قوة الارتباط | ملاحظات خاصة |
|---|---|---|
| الستيرويدات | نسبة الأرجحية 37.11) | جميع طرق الإعطاء |
| الشخصية من النوع A | متوسط | مرتبط بالإجهاد |
| الحمل | 0.008% سنويًا7) | شفاء تلقائي شائع بعد الولادة |
| انقطاع النفس النومي | 61% من المرضى9) | فرط نشاط الجهاز العصبي الودي |
| مثبطات PDE5 | تقارير حالات8) | تختفي عند التوقف |
يُفسر ظهور المرض بنظرية الضربات المتعددة (multi-hit theory)9). يُعتقد أن المرض يحدث في ثلاث مراحل: ① الاستعداد التشريحي (قصر طول المحور، سماكة الصلبة، عدم تناسق تصريف الأوردة الدوارة، إلخ)، ② الحدث المحفز (الستيرويدات، الإجهاد، انقطاع النفس النومي، إلخ)، ③ فشل التعويض.
الستيرويدات هي أكبر عامل خطر لهذا المرض، وتزيد المخاطر عبر جميع طرق الإعطاء بما في ذلك القطرات العينية والاستنشاق والحقن والأقراص الفموية. تم الإبلاغ عن نسبة الأرجحية (Odds Ratio) البالغة 37.1 وهي مرتفعة للغاية 1). عند تشخيص هذا المرض، إذا كان المريض يستخدم الستيرويدات، فيجب استشارة الطبيب المعني والنظر في تقليل الجرعة أو إيقافها قدر الإمكان. إذا كانت الستيرويدات تُعطى بسبب مرض جهازي، فمن الضروري التعاون مع أقسام أخرى لمعالجة كل حالة على حدة.
لتشخيص هذا المرض، يعتبر الجمع بين تصوير الأوعية بالفلوريسين (FA) والتصوير المقطعي التوافقي البصري (OCT) أساسياً. فيما يلي خصائص الفحوصات الرئيسية.
| الفحص | النتائج المميزة | الدور الرئيسي |
|---|---|---|
| تصوير الأوعية بالفلوريسين (FA) | تسرب فلوري نقطي | تحديد نقطة التسرب والتخطيط العلاجي |
| تصوير الأوعية بالخضاب الأخضر (IA/ICG) | فرط تألق المشيمية | تقييم شذوذ المشيمية والتشخيص التفريقي |
| التصوير المقطعي التوافقي البصري (OCT) | تصوير السائل تحت الشبكية (SRF) وانفصال الظهارة الصباغية | المتابعة والقياس الكمي |
تفاصيل كل فحص هي كما يلي.
لا يوجد علاج دوائي مثبت لهذا المرض. التخثير الضوئي بالليزر لنقاط تسرب الفلوريسئين هو العلاج الوحيد المقبول بشكل عام حاليًا، وتعتمد خطة العلاج على النوع والمرحلة وموقع نقطة التسرب.
في النوع الحاد النموذجي، هناك ميل للشفاء التلقائي، وفي الحالات الأولية الحادة، يُنتظر 4-6 أشهر لامتصاص السائل تحت الشبكية تلقائيًا. في الحالات النموذجية، يحدث الامتصاص الكامل غالبًا خلال 3-4 أشهر، ويكون تشخيص الرؤية جيدًا. معدل التراجع التلقائي في مجموعة غير المصابة بتثخن المشيمية هو 48%، بينما في مجموعة المصابة بتثخن المشيمية هو 28.8% 3).
إذا كانت الأعراض الذاتية شديدة ورغب المريض في التحسن المبكر، فإن التخثير الضوئي يكون مناسبًا حتى في الحالات الحادة النموذجية. إذا كان المريض يستخدم الستيرويدات، فيجب تقليل الجرعة أو إيقافها قدر الإمكان. إذا تم إعطاء الستيرويدات بسبب مرض جهازي، فيجب التعامل مع كل حالة بالتعاون مع الأقسام الأخرى.
في الحالات التي يستمر فيها الانفصال لأكثر من 4-6 أشهر من البداية، أو الحالات المتكررة، أو الحالات الشديدة، أو الحالات التي تعاني فيها العين الأخرى من ضعف الرؤية بسبب هذا المرض (مثل النوع المزمن أو انفصال الشبكية الفقاعي)، يجب تحقيق امتصاص مبكر للسائل تحت الشبكية بالعلاج. وذلك لأن تشخيص الرؤية يكون سيئًا بسبب تلف البقعة.
يكون مناسبًا عندما تكون نقطة التسرب على بعد 500 ميكرومتر أو أكثر من النقرة، وعلى الأقل خارج المنطقة اللاوعائية للنقرة. يتم تخثير نقطة التسرب المحددة بالتصوير الفلوري مباشرة (قطر 200 ميكرومتر، 0.2 ثانية، 70-120 ملي واط). درجة التخثير تكون تخثيرًا خفيفًا يعطي بقعة تخثير رمادية فاتحة في الطبقات العميقة للشبكية. حتى التسرب بين الحليمة والبقعة لا يمثل مشكلة مع التخثير الخفيف. إذا كان هناك تسرب داخل انفصال الظهارة الصبغية، فيكفي تخثير نقطة التسرب فقط.
عندما يكون التخثير الضوئي فعالاً، يتراجع انفصال الشبكية في غضون أسابيع قليلة. ومع ذلك، غالبًا ما يستغرق تحسن الأعراض الذاتية وقتًا أطول. تشمل المضاعفات: التعرض الخاطئ للنقرة، وحدوث أوعية دموية مشيمية جديدة بعد العملية (والتي تحدث بسهولة مع التخثير بطول موجة طويل ووقت قصير وبقعة صغيرة).
يستخدم ليزر أصفر بطول موجة 577 نانومتر. يتم التشعيع بإعدادات 240 ملي واط، قطر بقعة 200 ميكرومتر، 200 مللي ثانية، دورة عمل 5% 4). يتم إعطاء الطاقة بشكل انتقائي للظهارة الصبغية فقط، لذلك لا يتشكل ندب. يمكن التشعيع مباشرة تحت النقرة.
أفاد Bodea F وآخرون (2024) أن مرضى اعتلال المشيمية والشبكية المصلي المركزي الذين عولجوا بـ MPLT أظهروا انخفاضًا في السائل تحت الشبكية بعد أسبوعين من العلاج، واختفاءً بعد 6 أسابيع 4).
بالنسبة لهذا المرض أثناء الحمل، يعتبر الليزر النبضي الدقيق الخيار العلاجي الآمن الوحيد 7).
المراقبة
التطبيق: الخيار الأول للحالات الحادة النموذجية.
المدة: 4-6 أشهر. انتظار الامتصاص الطبيعي.
ملاحظة: أثناء استخدام الستيرويدات، يجب النظر في تقليل الجرعة أو إيقافها بالتنسيق مع الأقسام الأخرى.
PDT (العلاج الضوئي الديناميكي)
التطبيق: الخيار الأول لاعتلال المشيمية والشبكية المصلي المركزي المزمن.
الطريقة: يُوصى باستخدام نصف الجرعة (نصف التدفق) PDT.
الأساس: أثبتت تجارب PLACE و SPECTRA الفعالية (معدل تراجع السائل تحت الشبكية في 12 أسبوعًا 78% مقابل 17% للإبليرينون)9).
الليزر النبضي الدقيق
الميزات: لا يترك ندبات، ويمكن تطبيقه مباشرة تحت النقرة.
الميزة: العلاج الوحيد الذي يمكن استخدامه أثناء الحمل7).
التأثير: انخفاض السائل تحت الشبكية في أسبوعين، واختفاء في 6 أسابيع4).
يُستخدم في الحالات التي لا يمكن فيها التخثير الضوئي بالليزر، مثل وجود نقطة التسرب في المنطقة اللاوعائية النقريّة أو النوع المزمن. يُوصى باستخدام نصف جرعة فيرتبورفين (visudyne) PDT (نصف الجرعة المعتادة) أو نصف التدفق PDT (نصف طاقة الليزر) كخيار أول لاعتلال المشيمية والشبكية المصلي المركزي المزمن9).
نتائج التجارب السريرية الرئيسية هي كما يلي9).
مضاد مستقبلات القشرانيات المعدنية. يُستخدم بجرعة 50 ملغ/يوم. في تجربة VICI (تجربة عشوائية مزدوجة التعمية مضبوطة بالغفل)، لم يُظهر الإبليرينون فرقًا ذا دلالة إحصائية في تحسين BCVA مقارنة بالغفل بعد 12 شهرًا9). يُعتبر أقل فعالية من PDT، وقد وُجدت تقارير عن عدم استجابته حتى بعد 10 أشهر من العلاج5).
علاج جديد يتضمن التعرض لضوء LED أصفر بطول 590 نانومتر وأحمر بطول 625 نانومتر لمدة 6 دقائق لكل منهما5). تم الإبلاغ عن حالة تحسنت فيها حدة البصر المصححة من 20/80 إلى 20/25، وانخفض سمك الشبكية المركزي من 752 ميكرومتر إلى 296 ميكرومتر (عند شهر واحد) في مريض يعاني من انفصال ظهارة صبغية مصلي مزمن مرتبط بـ CSC غير المستجيب للإبليرينون5).
تم الإبلاغ عن معدل حدوث هذا المرض أثناء الحمل بنسبة 0.008% سنويًا 7). في معظم الحالات، يحدث الشفاء التلقائي في غضون 3 أشهر بعد الولادة. إذا كان العلاج ضروريًا، يُعتبر الليزر النبضي الدقيق (MPLT) الخيار الآمن الوحيد أثناء الحمل، ويمكن تطبيقه دون ترك ندبات حتى تحت النقرة 7).
في الحالات الحادة النموذجية، تكون المتابعة لمدة 4-6 أشهر هي الأساس. في النوع المزمن الذي يستمر فيه السائل تحت الشبكية لأكثر من 6 أشهر، يُعد العلاج الضوئي الديناميكي بنصف الجرعة (half-dose PDT) الخيار الأول 9). أظهرت تجربة SPECTRA أن معدل الاختفاء الكامل للسائل تحت الشبكية عند 12 أسبوعًا كان 78% في مجموعة PDT مقابل 17% في مجموعة إبليرينون، بفارق ذي دلالة إحصائية. إذا كانت نقطة التسرب خارج المنطقة اللاوعائية للنقرة، يُستخدم التخثير الضوئي بالليزر (تخثير ضعيف)، أما إذا كانت تحت النقرة مباشرة أو أثناء الحمل، فيُختار الليزر النبضي الدقيق. لم يُظهر الإبليرينون تحسنًا ذا دلالة إحصائية في حدة البصر المصححة مقارنة بالعلاج الوهمي في تجربة VICI 9).
تُفسر آلية حدوث هذا المرض من خلال آليات معقدة تركز على “زيادة نفاذية الأوعية الدموية المشيمية”. من خلال دراسات تصوير الأوعية بالخضاب الأخضر (IA)، يُعتقد أن الآفة الأولية تقع في المشيمية، ويحدث تلف في الظهارة الصبغية للشبكية بشكل ثانوي. لا يزال هناك الكثير من الغموض حول سبب حدوث الآفة في المشيمية. من المعروف أن الإجهاد والستيرويدات مرتبطان بظهور المرض وتفاقمه.
في تصوير الأوعية بالفلوريسين (FA)، يظهر تسرب الفلوريسين من الظهارة الصبغية وتراكم الصبغة تحت الشبكية. أظهرت دراسات التصوير المقطعي البصري (OCT) أن المشيمية تكون أكثر سمكًا في هذا المرض مقارنة بالعين الطبيعية، مما يثبت وجود شذوذ مشيمي شكليًا.
يشرح Cheung CMG وآخرون (2025) حدوث هذا المرض من خلال نظرية الضربات المتعددة 9).
الصلبة الأمامية والخلفية في عيون CSC أكثر سمكًا بشكل ملحوظ مقارنة بالعيون الطبيعية 9). نظرًا لأن الأوردة الدوارة تخترق الصلبة بشكل مائل (مسافة داخل الصلبة حوالي 4 مم)، فإن سماكة الصلبة قد تزيد من مقاومة التدفق الوريدي وتسبب احتقان المشيمية 9). في 62% من عيون CSC، يوجد تراكم للسوائل في الفضاء فوق المشيمي (loculation of fluid)، وفي 19% يوجد انصباب هدبي مشيمي (ciliochoroidal effusion) 9). في CSC المستحث بالستيرويدات، تكون الصلبة أرق من CSC مجهول السبب، مما يشير إلى دور مختلف للصلبة في المرض 9).
تم اقتراح تصنيف جديد يعتمد على التصوير متعدد الوسائط 9).
داخل كل فئة توجد تصنيفات فرعية: أولي / متكرر / منحل. CSC المعقد له خطر أعلى للإصابة بالأوعية الدموية المشيمية الجديدة (MNV) مقارنة بـ CSC البسيط. معامل الاتفاق بين 10 خبراء شبكية هو κ=0.57 (متوسط)، ويستمر تحسين التصنيف 9).
يوجد باكيدروزن في أكثر من 40% من مرضى CSC 9). عيون CSC المصحوبة بباكيدروزن لديها شذوذات RPE أكثر انتشارًا، وتختلف شكليًا وتوزيعيًا عن الدرنات اللينة التقليدية. تم إظهار ارتباط بين سماكة طبقة هالر وترقق الشعيرات الدموية المشيمية 9).
PBM هو علاج جديد لا يستخدم فيرتبورفين، ويتم تسليط الضوء بمزيج من LED أصفر 590 نانومتر وLED أحمر 625 نانومتر 5). يُتوقع كعلاج بديل في حالات نقص إمدادات فيرتبورفين.
وجود علامات المشيمية السميكة يزداد أهمية كعامل تنبؤي للتشخيص في هذا المرض. في مجموعة المشيمية السميكة، معدل التكرار أعلى (31.2% مقابل 10.4%) ومعدل الانحدار التلقائي أقل (28.8% مقابل 48%) مقارنة بالمجموعة غير السميكة 3). وجود علامات المشيمية السميكة هو مؤشر مهم في تحديد خطة العلاج.
تتراكم تقارير عن ظهور أو تكرار هذا المرض بعد تلقي لقاح COVID-19 6). يُقترح أن تنشيط محور HPA بواسطة اللقاح وتأثير مشابه للهرمونات الستيرويدية قد يكون له دور.