نوع معمولی
گروه سنی بیماران: عمدتاً مردان ۳۰ تا ۴۰ ساله. معمولاً یکطرفه.
پاتوفیزیولوژی: جداشدگی سروز شبکیه محدود به ماکولا.
سیر: بیشتر موارد در عرض ۳ تا ۴ ماه جذب خودبهخودی پیدا میکنند. پیشآگهی بینایی معمولاً خوب است.

کوریورتینوپاتی سروز مرکزی (CSC) بیماری است که در آن جداشدگی سروز شبکیه (SRF) در ناحیه ماکولا رخ میدهد. در آنژیوگرافی فلورسئین (FA)، نشت فلورسئین در سطح اپیتلیوم رنگدانه شبکیه (RPE) مشاهده میشود. این بیماری چهارمین بیماری شایع شبکیه پس از دژنراسیون ماکولا وابسته به سن، رتینوپاتی دیابتی و انسداد ورید شبکیه محسوب میشود. فون گریف در سال ۱۸۶۶ آن را به عنوان «رتینیت سروز مرکزی عودکننده» توصیف کرد و در سال ۱۹۶۷ گاس و همکاران نام فعلی را به آن دادند. پیش از این، در کشور ما اغلب فقط موارد معمولی که جداشدگی شبکیه محدود به ماکولا ایجاد میکردند (به اصطلاح رتینیت سروز مرکزی) به این نام خوانده میشدند، اما اکنون به سه نوع طبقهبندی میشود. در بسیاری از موارد، بیماری به طور خودبهخودی بهبود مییابد، اما در مواردی که SRF طولانی شود، پیشآگهی بینایی ممکن است بدتر شود.
از نظر اپیدمیولوژی، بروز سالانه ۹.۹ نفر در هر ۱۰۰٬۰۰۰ مرد و ۱.۷ نفر در هر ۱۰۰٬۰۰۰ زن است و نسبت مرد به زن حدود ۸:۱ است4). در مطالعهای روی ۲۵۰ چشم، میانگین سنی ۴۶.۶ سال و ۸۸.۴٪ مرد بودند3).
این بیماری دارای سه نوع زیر است:
نوع معمولی
گروه سنی بیماران: عمدتاً مردان ۳۰ تا ۴۰ ساله. معمولاً یکطرفه.
پاتوفیزیولوژی: جداشدگی سروز شبکیه محدود به ماکولا.
سیر: بیشتر موارد در عرض ۳ تا ۴ ماه جذب خودبهخودی پیدا میکنند. پیشآگهی بینایی معمولاً خوب است.
نوع مزمن
گروه سنی بیماران: بیشتر در افراد مسن دیده میشود. اغلب دوطرفه است. اخیراً روند افزایشی دارد.
پاتوفیزیولوژی: آسیب گسترده RPE. اغلب عود میکند.
سیر: SRF بیش از 6 ماه ادامه دارد. نیاز به درمان فعال دارد 5).
جداشدگی تاولی شبکیه
گروه بیماران: در موارد مصرف زیاد استروئید شایع است. معادل چیزی است که در ژاپن “اپیتلیوپاتی رنگدانهای شبکیه قطب خلفی متعدد” نامیده میشد.
پاتوفیزیولوژی: نوع شدید همراه با جداشدگی تاولی شبکیه. همراه با جداشدگی بزرگ RPE (PED) و لکههای سفید متعدد.
سیر: محدوده SRF اغلب تا پایین فوندوس گسترش مییابد و ممکن است پیشآگهی بینایی بد باشد.
نرخ عود تا 50% در یک سال بالاست. این بیماری بخشی از طیف بیماریهای پاکیکوروئید (گروهی از بیماریها با مشخصه ضخیم شدن مشیمیه) در نظر گرفته میشود 3)9).
در موارد معمول، اغلب در عرض 3-4 ماه بهبود خودبهخودی رخ میدهد و پیشآگهی بینایی معمولاً خوب است. با این حال، نرخ عود در یک سال تا 50% میرسد. اگر SRF بیش از 6 ماه ادامه یابد، به عنوان نوع مزمن در نظر گرفته شده و نیاز به درمان مانند PDT دارد. در گروه پاکیکوروئید، نرخ بهبود خودبهخودی کمتر از گروه غیرپاکیکوروئید (48%) است (28.8%) و نرخ عود نیز بالاتر است (31.2% در مقابل 10.4%)، بنابراین احتیاط لازم است 3).
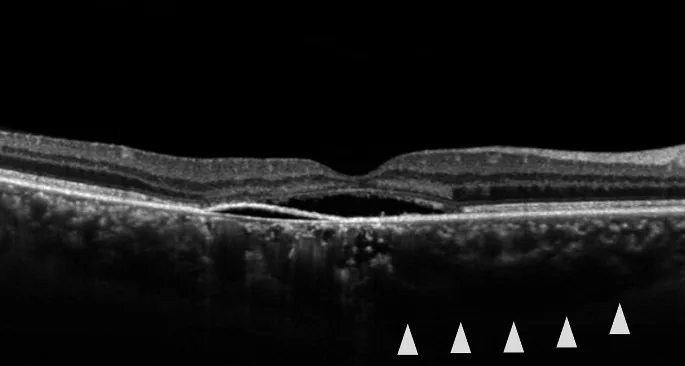
پس از جذب مایع زیرشبکیه، اسکوتوم مرکزی و دگرگونبینی نسبتاً زود بهبود مییابند. با این حال، میکروپسی و کاهش حساسیت کنتراست ممکن است باقی بمانند. در نوع مزمن، عودهای مکرر رخ میدهد و موارد با دید ضعیف شایع هستند. در موارد معمول، بیماری اغلب یکطرفه است، در حالی که در نوع مزمن و جداشدگی تاولی شبکیه، دوطرفه شایع است.
در معاینه با لامپ شکافی و تصویربرداریهای مختلف، یافتههای زیر مشاهده میشوند:
در نوع مزمن، آسیب گسترده اپیتلیوم رنگدانهای همراه با نوارهای آتروفیک اپیتلیوم رنگدانهای و جداشدگی شبکیه که به سمت پایین گسترش مییابد، ممکن است دیده شود. در جداشدگی تاولی شبکیه، جداشدگی شدید است و اغلب تا قسمت تحتانی فوندوس گسترش مییابد و با PED بزرگ و لکههای سفید متعدد همراه است.
علت اصلی این بیماری ناشناخته است، اما افزایش نفوذپذیری عروق مشیمیه به عنوان عامل اصلی در نظر گرفته میشود. استرس و استروئیدها در شروع و تشدید بیماری نقش دارند. عوامل خطر زیر گزارش شدهاند:
| عوامل خطر | شدت ارتباط | نکات ویژه |
|---|---|---|
| استروئیدها | OR 37.11) | همه راههای تجویز |
| شخصیت نوع A | متوسط | مرتبط با استرس |
| بارداری | 0.008%/سال7) | بهبود خودبهخودی پس از زایمان شایع است |
| آپنه انسدادی خواب (OSA) | 61% از بیماران9) | افزایش فعالیت سمپاتیک |
| مهارکنندههای PDE5 | گزارش موردی8) | با قطع دارو برطرف میشود |
بروز بیماری با فرضیه چندعاملی (multi-hit theory) توضیح داده میشود9). شامل سه مرحله: ① استعداد آناتومیک (طول محوری کوتاه، ضخامت صلبیه، عدم تقارن تخلیه وریدهای گردابی و غیره)، ② رویداد محرک (استروئید، استرس، OSA و غیره)، ③ جبرانناپذیری.
استروئیدها بزرگترین عامل خطر برای این بیماری هستند و تمام راههای مصرف (قطره چشمی، استنشاقی، تزریقی، خوراکی) خطر را افزایش میدهند. نسبت شانس 37.1 گزارش شده است که بسیار بالا است 1). در صورت تشخیص این بیماری و مصرف استروئید، باید با پزشک معالج مشورت کرده و در صورت امکان کاهش دوز یا قطع مصرف را بررسی کرد. اگر استروئید به دلیل بیماری سیستمیک تجویز شده است، باید در هر مورد جداگانه با همکاری سایر بخشها اقدام شود.
برای تشخیص این بیماری، ترکیب FA و OCT اساسی است. ویژگیهای اصلی آزمایشها در زیر آورده شده است.
| آزمایش | یافتههای مشخصه | نقش اصلی |
|---|---|---|
| FA | نشت فلورسین نقطهای | شناسایی نقطه نشت و برنامهریزی درمان |
| IA (ICG) | هایپرفلورسانس مشیمیه | ارزیابی ناهنجاری مشیمیه و تشخیص افتراقی |
| OCT | نمایش SRF و جداشدگی اپیتلیوم رنگدانه | پیگیری و اندازهگیری کمی |
جزئیات هر آزمایش به شرح زیر است.
برای این بیماری درمان دارویی اثبات شدهای وجود ندارد. لیزر فوتوکوآگولاسیون روی نقاط نشت فلورسئین آنژیوگرافی (FA) در حال حاضر تنها درمان پذیرفته شده عمومی است و استراتژی درمان بر اساس نوع، مرحله و محل نقاط نشت تعیین میشود.
در نوع حاد معمولی تمایل به بهبود خودبهخودی وجود دارد و در مرحله حاد اولین حمله، ۴ تا ۶ ماه برای جذب خودبهخودی مایع زیرشبکیه صبر میشود. در موارد معمولی، مایع اغلب در ۳ تا ۴ ماه به طور کامل جذب میشود و پیشآگهی بینایی نیز خوب است. میزان بهبود خودبهخودی در گروه غیر پاکیکوروئید ۴۸٪ است، در حالی که در گروه پاکیکوروئید ۲۸.۸٪ و کمتر است 3).
اگر علائم ذهنی شدید باشد و بیمار خواهان بهبود زودهنگام باشد، حتی در موارد حاد معمولی نیز فوتوکوآگولاسیون اندیکاسیون دارد. در صورت مصرف استروئید، تا حد امکان دوز کاهش داده یا قطع شود. اگر استروئید به دلیل بیماری سیستمیک تجویز شده است، در هر مورد با همکاری سایر بخشها اقدام شود.
در مواردی که جداشدگی بیش از ۴ تا ۶ ماه از شروع ادامه یابد، موارد عود، موارد شدید، یا مواردی که چشم دیگر نیز به دلیل این بیماری دچار کاهش بینایی شده است (نوع مزمن و جداشدگی تاولی شبکیه)، نیاز به درمان برای جذب زودهنگام مایع زیرشبکیه وجود دارد. زیرا آسیب ماکولا منجر به پیشآگهی بد بینایی میشود.
اندیکاسیون زمانی است که نقطه نشت حداقل ۵۰۰ میکرومتر از فووئا فاصله داشته باشد و حداقل خارج از ناحیه بدون عروق فووئا قرار گیرد. نقطه نشت شناسایی شده در FA مستقیماً کوآگوله میشود (قطر ۲۰۰ میکرومتر، ۰.۲ ثانیه، ۷۰-۱۲۰ میلیوات). شدت کوآگولاسیون باید ضعیف باشد به طوری که یک لخته سفید مایل به خاکستری کم رنگ در لایههای عمقی شبکیه ایجاد شود. حتی نشت بین پاپیل و ماکولا با کوآگولاسیون ضعیف مشکلی ندارد. اگر نشت در داخل جداشدگی اپیتلیوم پیگمانته وجود داشته باشد، فقط نقطه نشت کوآگوله شود.
اگر فوتوکوآگولاسیون مؤثر باشد، جداشدگی شبکیه در عرض چند هفته برطرف میشود. با این حال، بهبود علائم ذهنی اغلب زمان بیشتری میبرد. عوارض شامل تابش اشتباه به فووئا و ایجاد غشای نئوواسکولار کوروئید (CNV) پس از عمل (که با کوآگولاسیون با طول موج بلند، زمان کوتاه و اسپات کوچک بیشتر رخ میدهد) است.
از لیزر زرد ۵۷۷ نانومتر استفاده میشود. تابش با تنظیمات ۲۴۰ میلیوات، قطر اسپات ۲۰۰ میکرومتر، ۲۰۰ میلیثانیه و چرخه وظیفه ۵٪ انجام میشود 4). از آنجایی که انرژی به طور انتخابی فقط به RPE داده میشود، اسکار ایجاد نمیکند. حتی میتوان مستقیماً زیر فووئا تابش کرد.
Bodea F و همکاران (2024) گزارش کردند که در بیماران مبتلا به کوریورتینوپاتی سروز مرکزی تحت MPLT، کاهش مایع زیرشبکیه (SRF) در ۲ هفته و برطرف شدن آن در ۶ هفته پس از درمان مشاهده شد 4).
برای این بیماری در دوران بارداری، لیزر میکروپالس تنها گزینه درمانی ایمن در نظر گرفته میشود 7).
پیگیری
موارد مصرف: درمان خط اول برای موارد حاد معمولی.
مدت زمان: ۴ تا ۶ ماه. منتظر جذب طبیعی میمانیم.
توجه: در صورت استفاده از استروئید، با هماهنگی سایر بخشها کاهش دوز یا قطع آن را بررسی کنید.
PDT (درمان فتودینامیک)
موارد مصرف: درمان خط اول برای کوریورتینوپاتی سروز مرکزی مزمن.
روش: PDT با دوز نصف (نصف شار نوری) توصیه میشود.
شواهد: کارآزماییهای PLACE و SPECTRA (نرخ جذب مایع زیر شبکیه در ۱۲ هفته ۷۸٪ در مقابل ۱۷٪ برای اپلرنون) اثربخشی را نشان دادهاند9).
لیزر میکروپالس
ویژگی: بدون ایجاد اسکار، قابل استفاده حتی در زیر حفره مرکزی.
مزیت: تنها درمان قابل استفاده در دوران بارداری7).
اثر: کاهش مایع زیر شبکیه در ۲ هفته و جذب در ۶ هفته4).
در مواردی که نقطه نشت در ناحیه بدون عروق حفره مرکزی قرار دارد یا در نوع مزمن که لیزر فتوکوآگولاسیون امکانپذیر نیست، استفاده میشود. PDT با دوز نصف (نصف دوز معمول) یا نصف شار نوری (نصف توان لیزر) با استفاده از ورتپورفین (visudyne) به عنوان درمان خط اول برای کوریورتینوپاتی سروز مرکزی مزمن توصیه میشود9).
نتایج کارآزماییهای بالینی اصلی به شرح زیر است9).
آنتاگونیست گیرنده مینرالوکورتیکوئید. با دوز ۵۰ میلیگرم در روز استفاده میشود. در مطالعه VICI (کارآزمایی چندمرکزی تصادفی دوسوکور کنترل شده با دارونما)، پس از ۱۲ ماه مصرف، اپلرنون در مقایسه با دارونما تفاوت معنیداری در بهبود BCVA نشان نداد9). گفته میشود که اثربخشی آن کمتر از PDT است و گزارش مواردی از عدم پاسخ پس از ۱۰ ماه مصرف وجود دارد5).
یک روش درمانی جدید که شامل تابش LED زرد ۵۹۰ نانومتر و LED قرمز ۶۲۵ نانومتر هر کدام به مدت ۶ دقیقه است5). برای جداشدگی اپیتلیوم رنگدانه سروز همراه با کوریورتینوپاتی سروز مرکزی مزمن مقاوم به اپلرنون، موردی گزارش شده که بهترین دید اصلاح شده از ۲۰/۸۰ به ۲۰/۲۵ بهبود یافت و ضخامت مرکزی شبکیه از ۷۵۲ میکرومتر به ۲۹۶ میکرومتر کاهش یافت (در یک ماهگی)5).
بروز این بیماری در دوران بارداری ۰/۰۰۸٪ در سال گزارش شده است7). در بسیاری از موارد، طی سه ماه پس از زایمان خودبهخود بهبود مییابد. در صورت نیاز به درمان، لیزر میکروپالس (MPLT) تنها گزینه ایمن در دوران بارداری محسوب میشود و میتواند بدون ایجاد اسکار حتی در زیر حفره مرکزی شبکیه اعمال شود7).
در موارد حاد معمولی، پیگیری به مدت ۴ تا ۶ ماه اساس کار است. در نوع مزمن که مایع زیر شبکیه بیش از ۶ ماه ادامه دارد، PDT با دوز نیمی از دوز استاندارد، درمان خط اول است9). در مطالعه SPECTRA، نرخ رفع کامل مایع زیر شبکیه در هفته ۱۲ در گروه PDT ۷۸٪ و در گروه اپلرنون ۱۷٪ بود که تفاوت معنیداری را نشان داد. اگر نقطه نشت در خارج از ناحیه بدون عروق حفره مرکزی باشد، از لیزر فتوکوآگولاسیون (با شدت کم) و در موارد زیر حفره مرکزی یا در دوران بارداری، از لیزر میکروپالس استفاده میشود. اپلرنون در مطالعه VICI بهبود معنیداری در بهترین دید اصلاحشده نسبت به دارونما نشان نداد9).
مکانیسم بروز این بیماری با یک مکانیسم پیچیده با محوریت «افزایش نفوذپذیری عروق مشیمیه» توضیح داده میشود. مطالعات آنژیوگرافی با ایندوسیانین سبز نشان دادهاند که ضایعه اولیه در مشیمیه است و به دنبال آن آسیب به اپیتلیوم رنگدانهای شبکیه رخ میدهد. این که چرا ضایعه در مشیمیه ایجاد میشود، هنوز تا حد زیادی ناشناخته است. استرس و استروئیدها با شروع و تشدید این بیماری مرتبط شناخته شدهاند.
در آنژیوگرافی فلورسئین، نشت فلورسئین از اپیتلیوم رنگدانهای و تجمع رنگ در زیر شبکیه دیده میشود. مطالعات OCT نشان دادهاند که در این بیماری، مشیمیه در مقایسه با چشم سالم ضخیمتر است و از نظر مورفولوژیکی نیز ناهنجاری مشیمیه اثبات شده است.
Cheung CMG و همکاران (۲۰۲۵) بروز این بیماری را با نظریه ضربات متعدد توضیح میدهند9).
در چشمهای مبتلا به CSC، صلبیه قدامی و خلفی به طور معنیداری ضخیمتر از چشمهای طبیعی است9). از آنجایی که وریدهای گردابی به صورت مورب از صلبیه عبور میکنند (حدود 4 میلیمتر مسیر داخل صلبیه)، ضخیم شدن صلبیه ممکن است مقاومت در برابر خروج وریدی را افزایش داده و باعث احتقان کوروئید شود9). در 62% از چشمهای CSC، تجمع مایع در فضای فوقکوروئیدی (loculation of fluid) و در 19% افیوژن سیلیوکوروئیدال (ciliochoroidal effusion) دیده میشود9). در CSC ناشی از استروئید، صلبیه نازکتر از CSC ایدیوپاتیک است که نشان میدهد نقش صلبیه در پاتوژنز ممکن است متفاوت باشد9).
یک طبقهبندی جدید بر اساس تصویربرداری چندوجهی پیشنهاد شده است9).
در هر دسته، زیرگروههای primary (اولیه) / recurrent (عودکننده) / resolved (برطرفشده) وجود دارد. CSC Complex در مقایسه با CSC Simple خطر بروز عروق جدید مشیمیهای (MNV) بالاتری دارد. میزان توافق بین 10 متخصص شبکیه κ=0.57 (متوسط) بود و بهبود طبقهبندی ادامه دارد9).
بیش از 40% از بیماران CSC پاکیدروزن دارند9). چشمهای CSC همراه با پاکیدروزن ناهنجاریهای RPE گستردهتری دارند و از نظر شکل و توزیع با دروزن نرم معمولی متفاوت هستند. ارتباط بین ضخامت لایه Haller و نازکشدن مویرگهای مشیمیه نشان داده شده است9).
PBM به عنوان یک روش درمانی جدید بدون استفاده از ورتپورفین مورد توجه قرار گرفته است. این روش ترکیبی از LED زرد 590 نانومتر و LED قرمز 625 نانومتر است5). در شرایط کمبود عرضه ورتپورفین به عنوان درمان جایگزین امیدوارکننده است.
وجود یافتههای پاکیکروئید به عنوان عامل پیشبینیکننده پیشآگهی این بیماری اهمیت فزایندهای یافته است. در گروه پاکیکروئید، نرخ عود بالاتر (31.2% در مقابل 10.4%) و نرخ بهبود خودبهخودی پایینتر (28.8% در مقابل 48%) نسبت به گروه غیرپاکیکروئید گزارش شده است3). وجود یافتههای پاکیکروئید شاخص مهمی در تعیین استراتژی درمانی است.
گزارشهایی از بروز و عود این بیماری پس از واکسیناسیون COVID-19 انباشته شده است6). فعالسازی محور HPA توسط واکسن و اثرات شبهاستروئیدی ممکن است در این امر نقش داشته باشد.