Tipo Típico
Grupo de pacientes: Homens na faixa dos 30-40 anos. Geralmente unilateral.
Patologia: Descolamento seroso limitado à mácula.
Evolução: A maioria absorve espontaneamente em 3-4 meses. Prognóstico visual geralmente bom.

A Coriorretinopatia Serosa Central (Central Serous Chorioretinopathy; CSC) é uma doença na qual ocorre descolamento seroso da retina (SRF) na área macular. Na angiografia fluoresceínica (FA), observa-se vazamento de fluoresceína ao nível do epitélio pigmentar da retina (EPR). É considerada a quarta doença retiniana mais comum após degeneração macular relacionada à idade, retinopatia diabética e oclusão venosa retiniana. Von Graefe a descreveu como “retinite central recorrente” em 1866, e Gass et al. a nomearam com o nome atual em 1967. Anteriormente no Japão, referia-se frequentemente apenas aos casos típicos que causavam descolamento retiniano limitado à mácula (chamado retinite central), mas agora é classificada em três tipos. A maioria dos casos cura espontaneamente, mas em casos com SRF persistente, o prognóstico visual pode piorar.
Epidemiologicamente, a incidência é de 9,9 por 100.000 homens e 1,7 por 100.000 mulheres, com uma proporção homem:mulher de aproximadamente 8:14). Em um estudo com 250 olhos, a idade média foi de 46,6 anos e 88,4% eram homens3).
Esta doença tem os seguintes três tipos:
Tipo Típico
Grupo de pacientes: Homens na faixa dos 30-40 anos. Geralmente unilateral.
Patologia: Descolamento seroso limitado à mácula.
Evolução: A maioria absorve espontaneamente em 3-4 meses. Prognóstico visual geralmente bom.
Tipo Crônico
Grupo de pacientes: Mais comum em idosos. Frequentemente bilateral. Tendência crescente recentemente.
Patologia: Distúrbio extenso do EPR. Frequentemente recidivante.
Evolução: Líquido subrretiniano persistente por ≥6 meses. Requer tratamento ativo 5).
Descolamento bolhoso da retina
Perfil do paciente: Comum em usuários de altas doses de esteroides. Corresponde ao que era chamado de epiteliopatia pigmentar retiniana multifocal do polo posterior no Japão.
Patologia: Forma grave com descolamento bolhoso da retina. Acompanhado de grande descolamento do EPR e manchas brancas múltiplas.
Evolução: O líquido subrretiniano frequentemente se estende até a parte inferior do fundo, podendo ter mau prognóstico visual.
A taxa de recorrência é alta, chegando a 50% em 1 ano. Esta doença é considerada parte do espectro das doenças paquicoroides (grupo de doenças caracterizadas por espessamento coroidal) 3)9).
Nos casos típicos, ocorre remissão espontânea em 3-4 meses, e o prognóstico visual geralmente é bom. No entanto, a taxa de recorrência chega a 50% em 1 ano. Se o líquido subrretiniano persistir por >6 meses, é considerado crônico e requer tratamento como terapia fotodinâmica. No grupo paquicoroide, a taxa de remissão espontânea é menor (28,8%) do que no grupo não paquicoroide (48%), e a taxa de recorrência é maior (31,2% vs 10,4%), exigindo atenção 3).
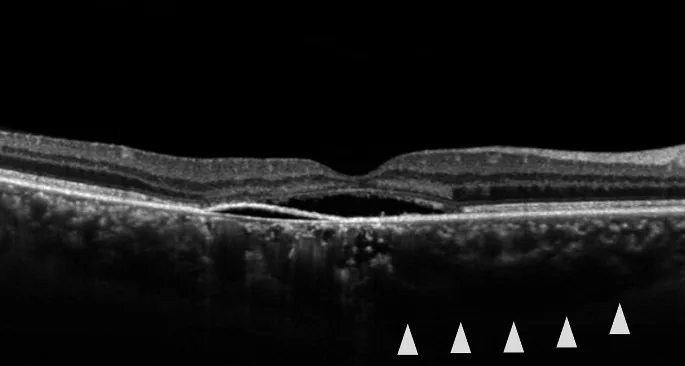
Quando o fluido sub-retiniano é absorvido, o escotoma central e a metamorfopsia melhoram relativamente cedo. Por outro lado, a micropsia e a redução da sensibilidade ao contraste podem persistir. No tipo crônico, as recidivas são frequentes e muitos casos apresentam baixa visão. Nos casos típicos, é mais frequentemente unilateral, enquanto no tipo crônico e no descolamento bolhoso da retina é mais frequentemente bilateral.
O exame com lâmpada de fenda e vários exames de imagem revelam os seguintes achados.
No tipo crônico, o dano ao epitélio pigmentar é extenso, e pode-se observar descolamento da retina estendendo-se inferiormente com faixas de atrofia do epitélio pigmentar. No descolamento bolhoso da retina, o descolamento é frequentemente grave e se estende até a parte inferior do fundo, acompanhado por grandes descolamentos do epitélio pigmentar e múltiplas manchas brancas.
A causa fundamental desta doença é desconhecida, mas acredita-se que o aumento da permeabilidade dos vasos coroidais seja a essência. Sabe-se que estresse e esteroides estão relacionados ao início e exacerbação da doença. Os seguintes fatores de risco foram relatados.
| Fatores de risco | Força da associação | Observações especiais |
|---|---|---|
| Esteroides | OR 37,11) | Todas as vias de administração |
| Personalidade tipo A | Moderada | Relacionada ao estresse |
| Gravidez | 0,008% ao ano7) | Remissão espontânea comum após o parto |
| AOS | 61% dos pacientes9) | Hiperatividade simpática |
| Inibidores da PDE5 | Relatos de caso8) | Regride com a suspensão |
O início da doença é explicado pela teoria do múltiplos eventos (multi-hit theory)9). Acredita-se que ocorra em três estágios: ① predisposição anatômica (eixo curto, espessamento escleral, assimetria da drenagem das veias vorticosas, etc.), ② evento desencadeante (esteroides, estresse, SAOS, etc.), ③ descompensação.
Os esteroides são o maior fator de risco para esta doença, e o risco aumenta em todas as vias de administração, incluindo colírios, inalação, injeção e uso oral. A razão de chances (odds ratio) foi relatada como extremamente alta, 37,1 1). Se diagnosticado com esta doença e estiver usando esteroides, consulte o médico responsável e considere reduzir ou interromper a dose sempre que possível. Se os esteroides forem administrados devido a uma doença sistêmica, é necessário colaborar com outros departamentos para lidar com cada caso individualmente.
O diagnóstico desta doença baseia-se na combinação de FA e OCT. As características dos principais exames são mostradas abaixo.
| Exame | Achados Característicos | Papel Principal |
|---|---|---|
| FA | Vazamento fluorescente puntiforme | Identificação do ponto de vazamento e planejamento terapêutico |
| IA (ICG) | Hiperfluorescência coroidal | Avaliação de anormalidades coroidais e diagnóstico diferencial |
| OCT | Visualização de SRF e descolamento do epitélio pigmentar | Acompanhamento e quantificação |
Os detalhes de cada exame são os seguintes.
Não há tratamento medicamentoso estabelecido para esta doença. A fotocoagulação a laser dos pontos de vazamento na angiografia fluoresceínica é atualmente o único tratamento geralmente aceito, e a estratégia terapêutica é determinada pelo tipo, estágio e localização do ponto de vazamento.
No tipo agudo típico, há tendência à remissão espontânea. Na fase aguda dos casos iniciais, aguarda-se a absorção espontânea do líquido sub-retiniano por 4 a 6 meses. Em casos típicos, a absorção completa ocorre frequentemente em 3 a 4 meses, e o prognóstico visual é bom. A taxa de regressão espontânea no grupo não paquicoroide é de 48%, enquanto no grupo paquicoroide é menor, 28,8% 3).
Se os sintomas subjetivos forem intensos e o paciente desejar melhora precoce, a fotocoagulação é indicada mesmo em casos agudos típicos. Se estiver em uso de esteroides, reduza ou suspenda ao máximo. Se os esteroides forem administrados devido a doença sistêmica, cada caso deve ser tratado em colaboração com outros departamentos.
Em casos com descolamento persistente por mais de 4 a 6 meses desde o início, casos recorrentes, casos graves ou casos em que o outro olho também apresenta comprometimento visual devido a esta doença (tipo crônico ou descolamento bolhoso), é necessária a absorção precoce do líquido sub-retiniano com tratamento. Isso porque o prognóstico visual é ruim devido ao dano macular.
É indicada quando o ponto de vazamento está a 500 μm ou mais da fóvea e pelo menos fora da zona avascular foveal. Coagula-se diretamente o ponto de vazamento identificado pela angiografia fluoresceínica (diâmetro 200 μm, 0,2 s, 70-120 mW). O grau de coagulação é coagulação leve que produz um ponto de coagulação branco-acinzentado nas camadas profundas da retina. Vazamentos entre a papila e a mácula não são problema com coagulação leve. Se houver vazamento dentro de descolamento do epitélio pigmentar, coagule apenas o ponto de vazamento.
Quando a fotocoagulação é eficaz, o descolamento da retina regride em algumas semanas. No entanto, a melhora dos sintomas subjetivos geralmente leva mais tempo. As complicações incluem: irradiação acidental da fóvea, ocorrência de neovascularização coroidal pós-operatória (mais fácil com coagulação de comprimento de onda longo, tempo curto e spot pequeno).
Utiliza laser amarelo de 577 nm. Irradiação com configurações de 240 mW, diâmetro do spot 200 μm, 200 ms, ciclo de trabalho 5% 4). A energia é administrada seletivamente apenas ao EPR, portanto não forma cicatriz. Pode irradiar diretamente abaixo da fóvea.
Bodea F et al. (2024) relataram que em pacientes com coriorretinopatia serosa central submetidos a MPLT, houve redução do líquido sub-retiniano em 2 semanas e resolução em 6 semanas 4).
Para esta doença durante a gravidez, o laser de micropulso é considerado a única opção de tratamento segura 7).
Observação
Indicação: Primeira escolha para casos agudos típicos.
Duração: 4 a 6 meses. Aguardar absorção natural.
Atenção: Durante o uso de esteroides, considerar redução ou descontinuação em coordenação com outros departamentos.
PDT (Terapia Fotodinâmica)
Indicação: Primeira escolha para coriorretinopatia serosa central crônica.
Método: PDT com meia dose (meia fluência) é recomendado.
Evidência: Os estudos PLACE e SPECTRA demonstraram eficácia (taxa de resolução de LSR em 12 semanas: 78% vs. 17% com eplerenona)9).
Laser de Micropulso
Características: Sem cicatriz, pode ser aplicado diretamente abaixo da fóvea.
Vantagem: Único tratamento que pode ser usado durante a gravidez7).
Efeito: Redução do LSR em 2 semanas, resolução em 6 semanas4).
Usado em casos onde a fotocoagulação a laser não é possível, como ponto de vazamento na zona avascular da fóvea ou tipo crônico. PDT com meia dose de verteporfina (Visudyne) (meia dose usual) ou meia fluência (metade da energia do laser) é recomendado como primeira escolha para coriorretinopatia serosa central crônica9).
Os resultados dos principais ensaios clínicos são os seguintes9).
Antagonista do receptor mineralocorticoide. Usado na dose de 50 mg/dia. No estudo VICI (ensaio randomizado duplo-cego controlado por placebo), a eplerenona não mostrou diferença significativa na melhora da BCVA em relação ao placebo após 12 meses de administração9). É considerada menos eficaz que a PDT, e há relatos de casos sem resposta mesmo após 10 meses de tratamento5).
Nova terapia que envolve irradiação com LED amarelo de 590 nm e LED vermelho de 625 nm por 6 minutos cada5). Foi relatado um caso em que a BCVA melhorou de 20/80 para 20/25, e a espessura retiniana central diminuiu de 752 μm para 296 μm (em 1 mês) em um paciente com descolamento seroso do epitélio pigmentar crônico associado a CSC refratário à eplerenona5).
A incidência desta doença durante a gravidez é relatada como 0,008% ao ano 7). Na maioria dos casos, ocorre remissão espontânea dentro de 3 meses após o parto. Se o tratamento for necessário, o laser de micropulso (MPLT) é considerado a única opção segura durante a gravidez, podendo ser aplicado sem cicatrizes mesmo abaixo da fóvea 7).
Em casos agudos típicos, a observação por 4-6 meses é a base. Para o tipo crônico com SRF persistente por mais de 6 meses, a PDT com meia dose (half-dose PDT) é a primeira escolha 9). O estudo SPECTRA mostrou taxa de resolução completa da SRF em 12 semanas de 78% no grupo PDT vs. 17% no grupo eplerenona, com diferença significativa. Se o ponto de vazamento estiver fora da zona avascular da fóvea, utiliza-se fotocoagulação a laser (coagulação fraca); se estiver diretamente abaixo da fóvea ou durante a gravidez, opta-se pelo laser de micropulso. A eplerenona não mostrou melhora significativa na BCVA em relação ao placebo no estudo VICI 9).
O mecanismo desta doença é explicado por mecanismos complexos centrados no “aumento da permeabilidade dos vasos coroidais”. A partir de estudos de IA, acredita-se que a lesão primária está na coroide, e o dano ao EPR ocorre secundariamente. Ainda há muito desconhecido sobre por que a lesão ocorre na coroide. Sabe-se que estresse e esteroides estão relacionados ao início e agravamento da doença.
Na FA, observa-se vazamento de fluoresceína do epitélio pigmentar e acúmulo de pigmento subrretiniano. Estudos de OCT mostram que a coroide é mais espessa nesta doença em comparação com olhos normais, comprovando morfologicamente a anormalidade coroidal.
Cheung CMG et al. (2025) explicam a ocorrência desta doença pela teoria do multi-hit 9).
Olhos com CSC têm esclera anterior e posterior significativamente mais espessas em comparação com olhos normais 9). As veias vorticosas perfuram a esclera obliquamente (trajeto intraescleral de cerca de 4 mm), portanto, o espessamento escleral pode aumentar a resistência ao fluxo venoso e causar congestão coroidal 9). Em 62% dos olhos com CSC, há acúmulo de fluido no espaço supracoroidal (loculação de fluido), e em 19%, há efusão ciliocoroidal 9). Na CSC induzida por esteroides, a esclera é mais fina do que na CSC idiopática, sugerindo um papel diferente da esclera na patogênese 9).
Uma nova classificação baseada em imagem multimodal foi proposta 9).
Dentro de cada categoria, há subclasses: primário / recorrente / resolvido. A CSC complexa tem maior risco de neovascularização coroidal (MNV) em comparação com a CSC simples. O coeficiente de concordância entre 10 especialistas em retina é κ=0,57 (moderado), e a classificação continua sendo aprimorada 9).
Paquidrusas são encontradas em mais de 40% dos pacientes com CSC 9). Olhos com CSC e paquidrusas apresentam anormalidades mais extensas da EPR, e diferem morfologicamente e na distribuição das drusas moles convencionais. Foi demonstrada associação entre espessamento da camada de Haller e afinamento dos capilares coroidais 9).
A PBM é uma nova terapia que não utiliza verteporfina, com irradiação combinada de LED amarelo 590 nm e LED vermelho 625 nm 5). É esperada como terapia alternativa em situações de escassez de verteporfina.
A presença de achados de paquicoroide está se tornando cada vez mais importante como fator preditivo de prognóstico nesta doença. No grupo paquicoroide, a taxa de recorrência é maior (31,2% vs 10,4%) e a taxa de resolução espontânea é menor (28,8% vs 48%) em comparação com o grupo não paquicoroide 3). A presença de achados de paquicoroide é um indicador importante na determinação da estratégia de tratamento.
Relatos de casos de início ou recorrência desta doença após vacinação contra COVID-19 estão se acumulando 6). Sugere-se que a ativação do eixo HPA pela vacina e um efeito semelhante ao hormônio esteroide podem estar envolvidos.