RRMS
النمط الانتكاسي-الهاجع (Relapsing-Remitting MS): النمط الفرعي الأكثر شيوعًا. تستمر الانتكاسات لأكثر من 24 ساعة، وتحدث هجوعات كاملة أو جزئية بين النوبات.

التصلب المتعدد (MS) هو مرض التهابي مزيل للميالين يصيب المادة البيضاء في الجهاز العصبي المركزي، ويسبب أعراضًا عصبية متنوعة تتكرر مع فترات انتكاس وهجوع. يتميز بتصلب ندبي ناتج عن التليف الدبقي، وعادة ما يصيب الجهاز العصبي المركزي فقط دون الجهاز العصبي المحيطي.
يقدر معدل الانتشار في الولايات المتحدة بـ 1-1.5 لكل 1000 شخص 1). يصيب المرض 2.1 مليون شخص حول العالم، وهو أكثر شيوعًا في المناطق ذات خطوط العرض العالية في نصفي الكرة الشمالي والجنوبي. متوسط عمر بداية المرض هو 15-45 عامًا، ومتوسط عمر التشخيص 30 عامًا. تتراوح أعمار الإصابة الشائعة بين 15-50 عامًا، وهو أكثر شيوعًا لدى النساء (ذروة في أواخر العشرينات) بنسبة 1:2.9.
يحتوي التصلب المتعدد على أربعة أنماط فرعية رئيسية. يبدأ النمط الانتكاسي-الهاجع (RRMS) عادةً بين سن 25 و29 عامًا، بينما يبدأ النمط التقدمي الثانوي (SPMS) غالبًا بين سن 40 و49 عامًا1).
RRMS
النمط الانتكاسي-الهاجع (Relapsing-Remitting MS): النمط الفرعي الأكثر شيوعًا. تستمر الانتكاسات لأكثر من 24 ساعة، وتحدث هجوعات كاملة أو جزئية بين النوبات.
SPMS
النمط التقدمي الثانوي (Secondary Progressive MS): ينتقل من RRMS. يتراكم العجز تدريجيًا حتى خلال فترات الهجوع.
PPMS
النمط التقدمي الأولي (Primary Progressive MS): يتراكم العجز تدريجيًا منذ البداية. يتقدم ببطء دون انتكاسات.
CIS
المتلازمة المعزولة سريريًا (Clinically Isolated Syndrome): أول نوبة سريرية يمكن أن تؤدي إلى التصلب المتعدد. تتيح بدء العلاج المبكر.
في 75% من المرضى، يكون العرض الأولي شكوى واحدة، حيث تكون 45% أعراضًا حركية أو حسية، و20% أعراضًا بصرية.
الأعراض العينية
الأعراض العصبية العامة
تتفاقم الأعراض بشكل حاد إلى تحت حاد وتستمر من بضعة أيام إلى عدة أشهر. في 85% من الحالات، تتحسن الأعراض أو تختفي، ولكن في 10-15% تبقى آثار متبقية.
غالبًا ما يبدأ كفقدان رؤية مؤلم في عين واحدة. يُلاحظ ألم الحجاج في 92% من الحالات، ويتفاقم مع حركة العين. كما تُلاحظ ظاهرة أوتهوف (Uhthoff phenomenon) حيث تتفاقم الأعراض مؤقتًا مع ارتفاع درجة حرارة الجسم (الاستحمام، التمرين).
السبب الدقيق للتصلب المتعدد غير معروف، لكن يُعتقد أن آليات المناعة الذاتية تشارك في ظهوره.
تلعب العوامل الوراثية دورًا، لكن نسبة التوافق بين التوائم المتماثلة تبلغ 25-30% فقط. تم تحديد تعدد أشكال HLA وأكثر من 100 موضع خطر، لكن يُعتقد أن العوامل البيئية بالإضافة إلى الاستعداد الوراثي تلعب دورًا مهمًا في ظهور المرض.
تُستخدم معايير ماكدونالد 2017 (النسخة المنقحة 2024). الأساس هو إثبات التعدد الزمني والمكاني (DIT/DIS) لآفات إزالة الميالين في الجهاز العصبي المركزي. في مراجعة 2024، تمت إضافة العصب البصري كموقع تشريحي خامس. في اليابان، توجد أيضًا معايير تشخيص التصلب المتعدد الصادرة عن وزارة الصحة والعمل والرفاه لعام 2015.
المواقع التشريحية الخمسة للتعدد المكاني (DIS) هي كما يلي:
إثبات التعدد الزمني (DIT): نوبتان أو أكثر، أو وجود آفات معززة وغير معززة في التصوير بالرنين المغناطيسي في نفس الوقت، أو آفات T2 جديدة، أو يمكن استبدالها بأشرطة قليلة النسق في السائل الدماغي الشوكي 1).
لتشخيص PPMS، بالإضافة إلى تطور الإعاقة لمدة عام أو أكثر، يلزم وجود اثنين أو أكثر من النتائج التالية: آفات T2 في الدماغ، آفات T2 في النخاع الشوكي (اثنتان أو أكثر)، أو أشرطة قليلة النسق في السائل الدماغي الشوكي 1).
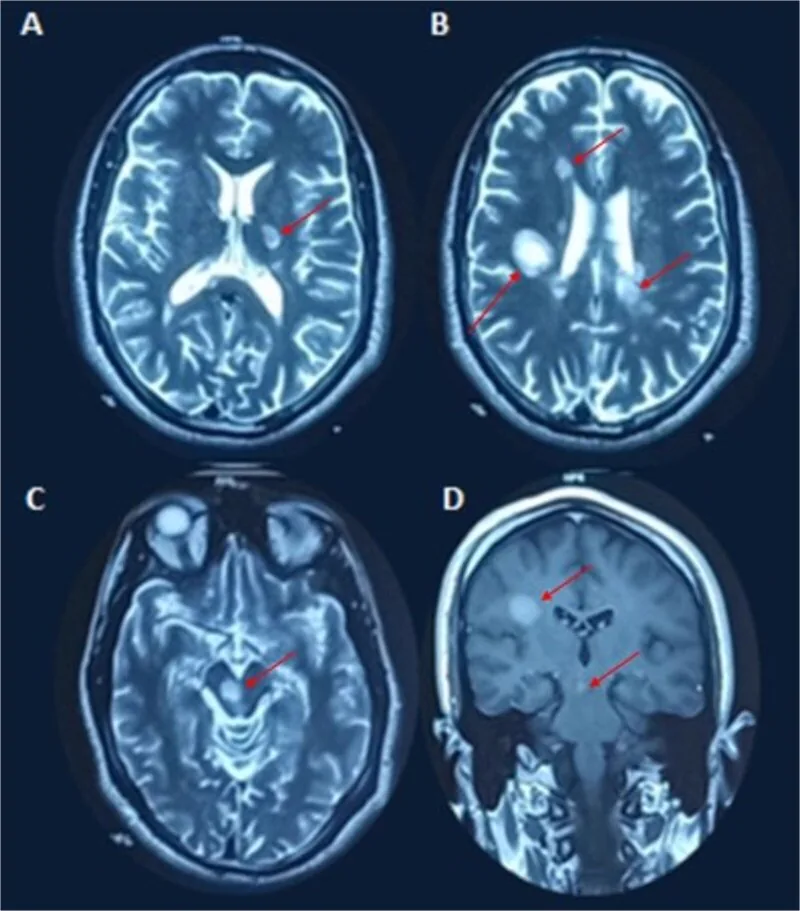
تُكتشف لويحات إزالة الميالين كآفات مفرطة الشدة في T2 أو آفات معززة بالغادولينيوم.
مفيد عندما يكون التصوير بالرنين المغناطيسي غير حاسم أو للتنبؤ بتطور المرض 1). يمكنه الكشف عن إزالة الميالين المبكرة غير العرضية قبل ظهورها في التصوير بالرنين المغناطيسي. في 65% من الحالات، يُلاحظ تطويل زمن الكمون وانخفاض السعة.
من المهم التفريق بين الأمراض التالية، وفي الحالات غير النمطية يتم إجراء فحوصات إضافية.
| فئة المرض | الأمراض التفريقية الرئيسية |
|---|---|
| أمراض إزالة الميالين | NMO (مرض ديفيك)، ADEM، MOGAD |
| معدي | الساركويد، السل، الزهري، داء لايم |
| مناعي ذاتي | الذئبة الحمامية الجهازية، متلازمة شوغرن، مرض بهجت |
| أمراض العصب البصري | اعتلال العصب البصري الإقفاري الأمامي غير الشرياني، الاعتلال العصبي البصري الوراثي ليبر، الاعتلال العصبي البصري السمي/الأيضي |
الفحوصات الإضافية في الحالات غير النمطية: الأجسام المضادة لـ AQP4 (لاستبعاد التهاب النخاع والعصب البصري)، الأجسام المضادة لـ MOG (لاستبعاد مرض الأجسام المضادة لـ MOG)، اختبار NfL في الدم، اختبارات الزهري المصلية (VDRL/RPR/FTA-ABS)، الأجسام المضادة للنواة (للذئبة الحمامية الجهازية)، ACE/lysozyme (للساركويد).
العلاج القياسي في اليابان هو العلاج بالستيرويد النبضي باستخدام ميثيل بريدنيزولون 1000 ملغ/يوم عن طريق الوريد لمدة 3 أيام متتالية. لا يتم إعطاء بريدنيزولون عن طريق الفم بعد التسريب. لا ينبغي إجراء العلاج بالستيرويد الفموي لأنه يزيد من معدل الانتكاس.
حتى بدون علاج، يبدأ تحسن الرؤية في حوالي 80% من الحالات خلال 3 أسابيع من البداية، لكن العلاج النبضي يقصر فترة التحسن. يمكن توقع استعادة الرؤية في أكثر من 90% من حالات التهاب العصب البصري.
إذا كان العلاج النبضي بالستيرويد غير فعال، يتم إجراء علاج تنقية الدم (تبادل البلازما). في الخارج، يُستخدم ميثيل بريدنيزولون 500-1000 ملغ/يوم لمدة 3-5 أيام. في تجربة علاج التهاب العصب البصري (ONTT)، أدى ميثيل بريدنيزولون الوريدي بجرعة عالية إلى تحسين وقت التعافي للوظيفة البصرية وحساسية التباين ورؤية الألوان، لكنه لم يُظهر تحسنًا في النتيجة البصرية النهائية.
بعد تحسن فقدان الرؤية وعيوب المجال البصري، يجب النظر في العلاج المعدل للمرض بالتعاون مع طبيب الأعصاب لمنع الانتكاس.
فيما يلي العلاجات المعدلة للمرض الرئيسية وفعاليتها.
| الدواء | آلية العمل | طريقة الإعطاء | انخفاض الخطر النسبي |
|---|---|---|---|
| إنترفيرون بيتا | تعديل نشاط الخلايا التائية/البائية وإفراز السيتوكينات | حقن ذاتي | تقدم الإعاقة RR 0.71 |
| أسيتات غلاتيرامر | تنظيم الخلايا التائية التنظيمية | حقن ذاتي | الانتكاس RR 0.82 |
| ناتاليزوماب | تثبيط دخول الخلايا الالتهابية إلى الجهاز العصبي المركزي | تسريب وريدي | الانتكاس RR 0.56 |
| فينغوليمود | تعديل مستقبلات S1P | فموي | نسبة خطر الآفات T2 الجديدة 0.65 |
| تيريفلونوميد | تثبيط تخليق البيريميدين | فموي | نسبة خطر تطور الإعاقة 0.76 |
| ثنائي ميثيل فومارات | تقليل الإجهاد التأكسدي والالتهاب | فموي | نسبة خطر الانتكاس 0.64 |
| أليمتوزوماب | جسم مضاد وحيد النسيلة مضاد لـ CD52 | وريدي | نسبة خطر تطور الإعاقة 0.44 |
أصبحت الأجسام المضادة وحيدة النسيلة المضادة لـ CD20 (أوكريليزوماب، ريتوكسيماب، أوفاتوموماب) علاجًا قياسيًا لمرض التصلب المتعدد الانتكاسي 3).
حتى في حالات التهاب العصب البصري دون آفات دماغية، يتطور مرض التصلب المتعدد لدى 25% من المرضى بعد 15 عامًا، بينما تصل النسبة إلى 78% في حالة وجود آفات دماغية.
حتى في حالة عدم وجود آفات في التصوير بالرنين المغناطيسي للدماغ، يتطور مرض التصلب المتعدد لدى 25% بعد 15 عامًا، بينما تصل النسبة إلى 78% في حالة وجود آفات دماغية. يجب على المرضى الذين أصيبوا بالتهاب العصب البصري مناقشة إمكانية استخدام العلاج المعدل للمرض (DMT) للوقاية من الانتكاسات بالتعاون مع طبيب الأعصاب.
يُعتقد أن التصلب المتعدد هو مرض مناعي ذاتي. تتعرف الخلايا اللمفاوية التائية على الميالين كجسم غريب، وتنشط البلاعم والسيتوكينات والأجسام المضادة لتدمير الميالين والمحاور العصبية. يؤدي فقدان الميالين إلى إعاقة توصيل النبضات الكهربائية، مما يضعف نقل الإشارات العصبية.
اللويحة النشطة
البلاعم الرغوية: تراكم البلاعم التي تبتلع الميالين.
الارتشاح حول الأوعية (perivascular cuffing): ارتشاح الخلايا الليمفاوية حول الأوعية الدموية، وهو علامة مميزة.
آفات إزالة الميالين الموضعية الوذمية: تظهر خلال مرحلة التفاقم الحاد.
اللويحة المزمنة
فقدان الميالين: يمكن تأكيده بصبغة Luxol fast blue. يتم الحفاظ على المحاور ولكن إعادة تكون الميالين غير كاملة.
آفات المادة البيضاء الطبيعية المظهر (NAWM): داء نجمي منتشر، تنشيط الخلايا الدبقية الصغيرة، وانهيار الحاجز الدموي الدماغي. ترتبط ارتباطًا أعلى بالضعف السريري مقارنة بآفات المادة البيضاء الموضعية.
تقوم الخلايا الدبقية قليلة التغصن بإعادة تكون الميالين في الجهاز العصبي المركزي 1). تعتمد على الخلايا السلفية للخلايا الدبقية قليلة التغصن البالغة (OPC)، لكن الخلايا الدبقية قليلة التغصن الناضجة الموجودة لا تساهم في إعادة تكون الميالين 1).
الأسباب الرئيسية لفشل إعادة تكون الميالين هي كما يلي 1).
كما يُلاحظ تلف المادة الرمادية في القشرة وتحت القشرة، ومن المعروف أن تكوين بنى لمفاوية شبيهة بجريبات الخلايا البائية في السحايا يؤدي إلى مسار سريري أكثر شدة1).
نهج جديد يثبط CD40L لقطع التحفيز المشترك بين الخلايا التائية والخلايا المقدمة للمستضد (بما في ذلك الخلايا البائية).
في تجربة المرحلة الثانية التي أجراها Vermersch وآخرون (N Engl J Med 2024)، أظهر frexalimab فعالية واضحة مقابل الدواء الوهمي في نتائج التصوير بالرنين المغناطيسي (آفات جديدة معززة بالغادولينيوم بين 8-12 أسبوعًا)، كما لوحظ انخفاض في NfL المصل، وهو مؤشر حيوي لتلف الأنسجة العصبية3). بالنسبة لمرض التصلب المتعدد التقدمي، يُتوقع أيضًا تأثير تعطيل الخلايا الدبقية الصغيرة والبلاعم، ومن الناحية النظرية، يمكن تحقيق الحماية العصبية عن طريق حجب إشارات CD40L في الخلايا الدبقية الصغيرة عند حافة اللويحة3).
يُعتبر إثبات التفوق السريري على العلاجات المعدلة للمرض عالية الفعالية الحالية (مضادات CD20) تحديًا مستقبليًا3).
تم إثبات أن الموت الخلوي الحديدي، وهو موت خلوي معتمد على الحديد، يشارك في موت الخلايا العصبية في مرض التصلب المتعدد.
شرح Tang et al. (2025) دراسة Woo et al. (Cell, 2024) وأبلغ عن سلسلة: السمية المثيرة للجلوتامات → فرط حمل الكالسيوم → إجهاد الشبكة الإندوبلازمية → انفصال STING1 عن STIM1 → تنشيط المسار غير التقليدي → الالتهام الذاتي → تحلل GPX4 (إنزيم تحييد بيروكسيد الدهون) بالالتهام الذاتي → موت الخلايا المبرمج بالحديد 4). تم تأكيد زيادة تعبير STING1 في الخلايا العصبية في كل من عينات التصلب المتعدد البشري ونماذج الفئران. أظهرت مثبطات STING1 (C176، H151) انخفاضًا في تحلل GPX4 المعتمد على الالتهام الذاتي وتأثيرًا وقائيًا عصبيًا في النماذج الحيوانية 4).
في مرحلة البحث، يُعتبر الحماية العصبية من خلال تعطيل الخلايا الدبقية الصغيرة والبلاعم بواسطة مثبط CD40L frexalimab 3) وتثبيط موت الخلايا المبرمج بالحديد (موت الخلايا المعتمد على الحديد) بواسطة تثبيط STING1 4) واعدًا. كلاهما حاليًا في مرحلة التجارب السريرية والبحث، وليس علاجًا قياسيًا.