轻度远视(+3D以下)

远视(包括潜伏远视)
1. 什么是远视?
Section titled “1. 什么是远视?”远视(hyperopia)是指在无调节状态下进入眼内的平行光线聚焦于视网膜后方的屈光状态。另一种表述是,远点在眼后方有限距离的眼,即向眼后方会聚的光线在视网膜上聚焦的屈光状态。
这种情况主要是由于角膜和晶状体的综合屈光力相对于眼轴长度较弱所致。通常+6D以上的强远视称为高度远视,+10D以上的极高度远视有些属于小眼球范畴。
远视的分类(按测量方法)
Section titled “远视的分类(按测量方法)”远视根据测量方法分为以下三种类型。
总远视 = 显性远视 + 潜伏远视 的关系成立。
| 类型 | 定义 |
|---|---|
| 总远视 | 使用阿托品等睫状肌麻痹剂完全消除调节后的远视度数。 |
| 显性远视 | 不使用睫状肌麻痹剂的常规屈光检查中可检测到的远视度数。 |
| 潜伏远视 | 常规检查中潜伏而无法检测,但在睫状肌麻痹下检查才显现的远视度数。儿童较大。 |
按调节代偿的分类
Section titled “按调节代偿的分类”| 类型 | 定义 |
|---|---|
| 随意性远视(facultative hyperopia) | 显性远视中可通过调节代偿的部分。裸眼通过调节也能看清的远视度数。 |
| 绝对远视(absolute hyperopia) | 显性远视中无法通过调节代偿的部分。没有矫正镜片则无法看清。 |
| 相对远视(relative hyperopia) | 与眼位相关:可通过调节看清,但此时会发生内斜视的远视。 |
随着年龄增长,晶状体弹性下降,调节力减弱,因此年轻时作为随意性远视隐藏的成分在中老年以后会以眼疲劳、视力下降的形式显现出来。
| 分类 | 定义 | 主要原因 |
|---|---|---|
| 屈光性远视(refractive hyperopia) | 角膜和晶状体的综合屈光力较弱 | 扁平角膜、晶状体半脱位后移、糖尿病引起的屈光指数变化、无晶状体眼 |
| 轴性远视(axial hyperopia) | 眼轴长度较短 | 先天性(新生儿)、后天性(眼眶肿瘤压迫、视网膜脱离时视网膜隆起等) |
流行病学与自然病程
Section titled “流行病学与自然病程”一般来说,新生儿是远视的,其分布以+2D为中心。到1岁左右,他们变得接近正视。远视度数在7-8岁前增加,之后减少。这称为正视化(emmetropization)。在1892年Herrnheiser的研究中,远视的频率在20岁左右下降,而正视和近视的频率上升。
弱视的患病率在儿童中约为2-4%,其中远视性屈光参差性弱视和远视性双眼弱视占很大比例1)。远视度数+2D以上时,弱视和调节性内斜视的风险特别增加,+6D以上时弱视发病风险显著升高(见表)1)。
纯调节性内斜视的平均远视度数为+5.43D±2.25 D(不伴内斜视的弱视眼为+6.11D±1.84 D),表明高度远视是弱视和内斜视的主要危险因素1)。即使在特殊病例中,如神经纤维瘤病1型(NF1)相关的单侧巨眼症导致的高度屈光参差(-17.50D),如果未早期转诊眼科,也可能导致严重弱视11)。
2. 主要症状与临床所见
Section titled “2. 主要症状与临床所见”远视的症状因程度而异。
中度远视(+3~6D)
高度远视(+6D以上)
临床所见(高度远视)
Section titled “临床所见(高度远视)”高度远视呈现特征性眼底所见。
- 假性视神经炎(pseudopapilledema):视神经乳头边界不清晰。伴有乳头边缘模糊、血管迂曲的拥挤盘表现。
- 后极部视网膜皱襞:因眼轴短导致后极部相对狭窄而产生。
- 浅前房、窄角:成为闭角型青光眼的诱因。
高度远视(特别是+2D以上)容易发生以下并发症。
- 远视性弱视:+2D以上弱视风险增加。+4.5D以上(伴有斜视)或+6D以上(无斜视)时风险特别高1)
- 调节性内斜视:+2~8D的远视容易发生。+2D以上容易发生,+8D以上调节性内斜视罕见。
- 闭角型青光眼:由浅前房、窄角引起。成年后风险持续。
- 葡萄膜渗漏综合征(uveal effusion):常合并小眼球(nanophthalmos),引起渗出性视网膜脱离。
3. 原因与风险因素
Section titled “3. 原因与风险因素”屈光性远视的原因
Section titled “屈光性远视的原因”由于角膜或晶状体的屈光力相对较弱所致。
- 扁平角膜:先天性角膜曲率半径较大,或因翼状胬肉、角膜疾病后天性变扁平
- 晶状体后移:晶状体半脱位导致向后移动时
- 糖尿病:晶状体屈光指数变化可能导致远视化
- 无晶状体眼:晶状体摘除后。通常导致高度远视(+10D以上)
轴性远视的原因
Section titled “轴性远视的原因”由于眼轴长度比正常短所致。
- 先天性:新生儿眼轴较短(约17-18毫米,成人约24毫米),生理性远视。随着成长眼轴延长,趋于正视化
- 后天性:眼眶肿瘤压迫导致眼轴变短,或中心性浆液性脉络膜视网膜病变、视网膜脱离导致视网膜隆起时
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”远视的诊断需要以下检查。
| 检查 | 目的 |
|---|---|
| 客观屈光检查(自动验光仪) | 屈光度定量(参考值) |
| 检影法(视网膜镜) | 儿童客观屈光测量。调节控制优秀。 |
| 主观屈光检查(矫正视力) | 最终处方度数的确定 |
| 睫状肌麻痹下屈光检查 | 检测真正远视量(总远视度)。儿童必需。 |
| 角膜地形图分析和生物测量 | 眼轴长度和前房深度评估。高度远视的解剖学评估。 |
儿童睫状肌麻痹下检查
Section titled “儿童睫状肌麻痹下检查”在幼儿中,由于缺乏正确聚焦远方的注意力,客观屈光检查必须使用睫状肌麻痹眼药水。
首选:1%环喷托酯(赛普乐®)眼药水
每日滴眼1-2次可获得充分的睫状肌麻痹。效果在滴眼后30-60分钟出现,持续约半天。注意副作用(面部潮红、心动过速、兴奋)。
阿托品眼药水(需要更强睫状肌麻痹时)
无论年龄大小,均使用1%阿托品滴眼液,每日2次,连续滴眼7天。这能提供最完全的睫状肌麻痹,并可检测出全部潜伏性远视。由于药效持续1~2周,散瞳和畏光会持续存在,因此对患者的解释很重要。
检测潜伏性远视必须在睫状肌麻痹下进行客观屈光检查,若无睫状肌麻痹,则存在大幅低估远视程度的风险。
婴幼儿正常屈光值(1%环戊通睫状肌麻痹下)
Section titled “婴幼儿正常屈光值(1%环戊通睫状肌麻痹下)”| 年龄 | 正常屈光值 | 需要配镜的屈光值 |
|---|---|---|
| 3个月 | S+4D | S+6D及以上 |
| 1岁 | S+2D | S+4D及以上 |
| 2岁 | S+1D | S+3D及以上 |
| 3岁 | S+1D | S+3D以上 |
如果屈光度比正常值强2D以上,考虑配戴眼镜。
另外,弱视的诊断标准为:3~4岁双眼视力差≥2行或双眼≤20/50,5岁以上双眼视力差≥2行或双眼≤20/401)。
鉴别诊断要点
Section titled “鉴别诊断要点”假性视神经炎与视乳头水肿的鉴别很重要。高度远视时视乳头边界可能不清晰,但荧光眼底造影无渗漏,视野和视力通常正常。
5. 标准治疗方法
Section titled “5. 标准治疗方法”根据睫状肌麻痹药点眼后麻痹状态下的屈光度数,配戴眼镜或隐形眼镜。
儿童眼镜处方
Section titled “儿童眼镜处方”处方度数的选择基于以下原则:
PEDI(小儿眼病研究组)的前瞻性研究表明,3-6岁屈光参差性弱视儿童中,27%仅通过眼镜矫正弱视即治愈,平均改善0.29 logMAR 2)。配镜后,在视力稳定前仅进行屈光矫正是当前的标准方针 2)。
远视性弱视的治疗
Section titled “远视性弱视的治疗”第一步:全天佩戴完全矫正眼镜
根据睫状肌麻痹下屈光检查结果,开具完全矫正眼镜并全天佩戴。仅戴眼镜视力往往会有一定提高。配镜后,在视力稳定前仅进行屈光矫正是当前的标准方针 2)。
第二步:遮盖疗法(贴片)
如果仅戴眼镜视力改善不充分,则在健眼上粘贴遮盖贴片。
第三步:阿托品滴眼液(光学抑制)
在健眼滴用1%阿托品,通过睫状肌麻痹使健眼近视力模糊,促使使用弱视眼。对中度弱视与遮盖疗法效果几乎相同 7)。在遮盖依从性差时作为替代手段有用。
Bangerter滤光片
在健眼镜片上安装半透明滤光片的方法。PEDI研究显示,24周后与遮盖疗法相比,视力改善差异在0.5行以内 1)。
调节性内斜视的治疗
Section titled “调节性内斜视的治疗”对于纯调节性内斜视,使用0.5%阿托品每日三次滴眼,持续3-5天,并让患者佩戴完全矫正眼镜或度数减少0.5D的眼镜。需要注意让患者持续佩戴眼镜,并确保镜框不会滑落。
对于部分调节性内斜视,同样佩戴远视眼镜,但对于残余的内斜视,进行手术或棱镜治疗。
调节性内斜视的分类和处理
| 类型 | 特征 | 治疗 |
|---|---|---|
| 纯调节性内斜视 | 远视矫正后斜视完全消失 | 远视完全矫正眼镜(无需菲涅尔棱镜) |
| 部分调节性内斜视 | 矫正后仍有残余内斜视(>10∆) | 眼镜+手术(针对残余量) |
| 高AC/A型 | 正常远视但近看时内斜视增大 | 远视矫正+双焦点眼镜(近用部+2.5~3.0D的加入) |
| 非屈光性调节性内斜视 | AC/A比值异常增高 | 缩瞳药(依可碘酯)或双焦点眼镜 |
在合并远视性弱视的调节性内斜视中,需要同时进行配镜、弱视治疗和斜视矫正。如果在弱视未治疗的情况下进行斜视手术,术后可能解除眼间抑制而导致复视,因此原则上应优先或同时进行弱视治疗1)。
成人调节性内斜视(不戴眼镜时内斜)中,摘镜可能导致社会和职业限制。在这种情况下,有时会为改善斜视而进行屈光手术(如LASIK)。但屈光手术的主要目的是屈光矫正,对斜视的手术效果是次要的,术前必须充分说明15)。
儿童高度远视
Section titled “儿童高度远视”儿童高度远视(+6D以上)可导致弱视和调节性内斜视。需要早期检测全部远视度数,并通过眼镜等进行屈光矫正。儿童期以后,隐形眼镜也是一种选择。由于眼轴短、前房浅等表现持续存在,需要持续注意成年后并发症(如闭角型青光眼)的风险。在小眼球合并葡萄膜渗漏综合征时,巩膜开窗术有效3)。纳米眼病例建议定期随访3)。
成人(20岁以上,屈光度稳定)可通过准分子激光LASIK(激光原位角膜磨镶术)或PRK(光屈光性角膜切除术)矫正远视。屈光手术指南(第8版)建议远视矫正上限约为+6D(等效球镜),对于更高度的远视,应谨慎考虑适应证4)。
远视LASIK比近视矫正更容易发生回退,尤其是+4D以上的高度远视,长期屈光稳定性趋于下降4)。这与角膜切削模式的特殊性(周边切削、中央保留)有关,并且与年龄相关的角膜形状变化相互作用加速回退。
PRK不制作角膜瓣,因此对于角膜薄或活动度高的患者(运动、职业)可能被选择。但术后上皮下混浊在远视矫正中比近视矫正更常见,可能影响长期矫正精度4)。
有晶状体眼人工晶状体(ICL、IPCL等)矫正远视,适用于高度远视(超过+6D)且不适合LASIK的病例。由于不进行角膜切削,退行风险低,但存在白内障、眼压升高、角膜内皮细胞减少等并发症风险4)。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”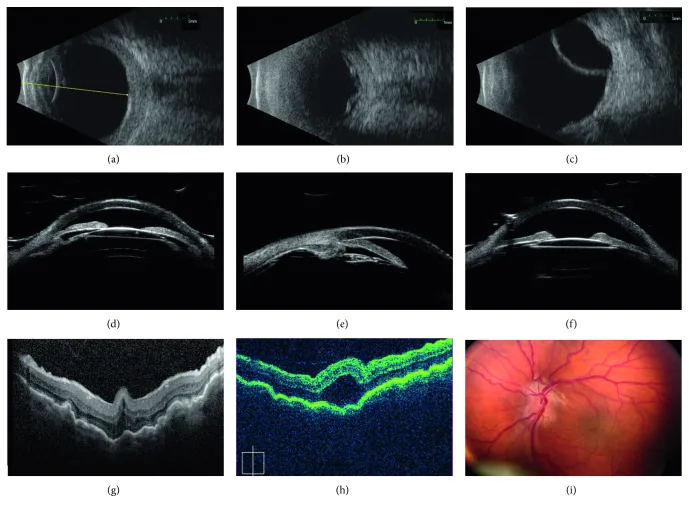
基本光学机制
Section titled “基本光学机制”远视是由于角膜和晶状体的综合屈光力相对于眼轴长度较弱所致。正常眼约58~60D的综合屈光力与约24mm的眼轴长度平衡,平行光线准确聚焦于视网膜上。远视眼这种平衡被打破,焦点形成于视网膜后方。
调节的代偿机制
Section titled “调节的代偿机制”晶状体通过睫状肌收缩增厚以增加屈光力(调节),可代偿远视。在可调节范围内不产生视力下降(随意性远视)。但由于需持续维持调节,易导致调节肌疲劳(视疲劳)。
随着年龄增长,晶状体弹性下降,调节力减弱,年轻时无症状的远视可能在中年以后表现为视疲劳和视力下降。绝对远视的比例增加,需要配戴矫正眼镜。
正视化过程(emmetropization)
Section titled “正视化过程(emmetropization)”新生儿眼轴较短(约17~18mm),存在生理性远视(约+2D)。随着成长眼轴延长(成人约24mm),屈光力与眼轴长度达到平衡而正视化。这一正视化过程由依赖视觉输入的反馈机制调节。
7~8岁左右是远视度数暂时性略有增加的时期,如果在此期间忽视屈光不正的评估,可能会导致弱视和内斜视的漏诊。
儿童潜伏远视的大小
Section titled “儿童潜伏远视的大小”儿童与成人相比,睫状肌张力更强,调节力更大。因此,大部分远视作为潜伏远视隐藏起来,未经睫状肌麻痹的检查无法准确测量远视度数。未检测出潜伏远视而配戴的眼镜会导致矫正不足,削弱弱视治疗和斜视治疗的效果。
高度远视的解剖学特征
Section titled “高度远视的解剖学特征”高度远视的眼球在轴性远视的情况下眼轴长度短,随之前房变浅。前房浅的眼球倾向于房角狭窄,急性闭角型青光眼发作的风险高。此外,由于眼轴短导致后极部相对拥挤,容易发生视神经乳头边界不清(假性视神经炎)和后极部视网膜皱褶。
与葡萄膜渗漏综合征的关系
Section titled “与葡萄膜渗漏综合征的关系”在高度远视的小眼球中,由于巩膜的病理异常,脉络膜系统的引流血管涡静脉在巩膜穿通处受到压迫,可能发生葡萄膜渗漏综合征。眼轴短且高度远视的I型(真性小眼球伴巩膜增厚型)发生渗出性视网膜脱离时,巩膜开窗术有效3)。小眼球病例建议定期随访。
闭角型青光眼风险的管理
Section titled “闭角型青光眼风险的管理”高度远视(特别是+6D以上、轴性远视)的眼球前房浅,房角趋于狭窄。随着年龄增长,晶状体增厚,房角进一步变窄,急性闭角型青光眼的风险增加。
对于AACG的风险管理,推荐以下措施1):
- 定期评估前房深度和房角宽度(UBM、AS-OCT等)
- 需要散瞳时,术前确认前房深度并准备紧急处理
- 对前房浅的高度远视成人考虑预防性激光虹膜周切术
白内障手术将晶状体替换为更薄的人工晶状体,因此可以消除高度远视的闭角风险。对于眼轴极短的高度远视(+8D以上、眼轴<21mm),有时会考虑在发生白内障之前进行预防性晶状体摘除(透明晶状体摘除)以预防闭角型青光眼。
7. 最新研究与未来展望
Section titled “7. 最新研究与未来展望”远视矫正中屈光手术的进展
Section titled “远视矫正中屈光手术的进展”准分子激光远视矫正(LASIK/PRK)相比近视矫正稳定性稍差,易发生回退(屈光近视化)。近年来,角膜切削模式的改进提高了精度,中度远视(约+3D)已报告良好效果。
SMILE(小切口透镜取出术)用于远视的适应症扩展也在研究中。对于超过+6D的高度远视,仍存在局限性,有时需考虑包括有晶状体眼人工晶体(ICL)远视型在内的手术方案13)。KLEx(SMILE)指南明确了近视和近视散光的适应条件,远视矫正仍以LASIK为主流13)。白内障手术中IOL度数计算时远视眼的注意事项(前房深度、晶状体厚度的影响)也很重要,最新公式(如Barrett Universal II)提高了远视眼的精度14)。
儿童远视筛查的效率化
Section titled “儿童远视筛查的效率化”照片筛查(photo screening)设备在集体筛查中已被证明能有效早期发现传统视力表检查难以发现的儿童远视和弱视8)。3岁儿童健康检查中引入照片筛查仪正在普及,有望提高弱视的早期发现率。Spot Vision Screener可测量屈光度、斜视角、瞳孔大小差异和瞳孔间距,当超过弱视风险因素阈值时显示异常8)。
远视性弱视的治疗方案(分步管理)
Section titled “远视性弱视的治疗方案(分步管理)”第1步(0-18周):仅配戴完全矫正眼镜
根据睫状肌麻痹验光配戴完全矫正眼镜,仅戴镜观察直至视力稳定。PEDIG研究显示,仅戴镜矫正可使弱视眼视力平均提高0.29 logMAR,27%脱离弱视标准7)。跳过此步骤直接进行遮盖可能导致过度治疗,因为部分病例仅戴镜即可改善。
第2步(18周后):加用遮盖或阿托品
如果配镜后18周视力不再提高,则加用遮盖或阿托品。对于双眼弱视(等屈光性),无法确定弱视眼,因此不能进行遮盖,主要依靠持续配戴完全矫正眼镜。
第三阶段(视力改善后):逐渐减量、终止与复发监测
当视力恢复正常(或确认平台期后4个月)时,逐渐减少遮盖。弱视的复发率在治疗中断后一年内约为24%,因此定期随访是必要的2)。复发时通常对再次治疗反应良好。
数字治疗与VR在弱视治疗中的应用
Section titled “数字治疗与VR在弱视治疗中的应用”使用Luminopia头戴设备的研究(儿童使用72小时)报告视力改善0.15 logMAR2)。在成人屈光参差性弱视中,也报告了0.15 logMAR(每27小时改善一行)的视力改善2),与传统遮盖疗法的比较研究正在进行中。在VR环境下的分视训练中,44小时的训练使视力从0.05提高到0.5,并获得了立体视觉10)。成人斜视PPP(2023年)也强调了远视性内斜视屈光矫正的重要性,并提出了矫正后仍存在残余斜视时手术适应症的系统管理流程15)。关于学龄前视力筛查中遮盖疗法适当终止时间的研究显示,4岁时视力的预测性很高(r=0.83,p<0.01),表明4岁后继续遮盖并非总是有效9)。此外,在7至17岁未经治疗的弱视儿童中,仅配镜矫正24周后25%视力改善,额外遮盖后53%(7-12岁)改善,表明即使在敏感期后仍有治疗可能性12)。
8. 参考文献
Section titled “8. 参考文献”-
American Academy of Ophthalmology. Amblyopia Preferred Practice Pattern 2022 Update. Ophthalmology. 2023;130(3):P136-P178.
-
Meier K, Tarczy-Hornoch K. Recent treatment advances in amblyopia. Annu Rev Vis Sci. 2022.
-
Carricondo PC, Andrade T, Prasov L, Ayres BM, Moroi SE. Nanophthalmos: A Review of the Clinical Spectrum and Genetics. J Ophthalmol. 2018;2018:2735465. doi:10.1155/2018/2735465
-
日本眼科学会屈折矯正委員会. 屈折矯正手術のガイドライン(第8版). 日眼会誌. 2024;128(2):135-139.
-
Pediatric Eye Disease Investigator Group. A randomized trial of prescribed patching regimens for treatment of severe amblyopia in children. Ophthalmology. 2003;110:2075-2087.
-
Pediatric Eye Disease Investigator Group. A randomized trial of atropine vs. patching for treatment of moderate amblyopia in children. Arch Ophthalmol. 2002;120:268-278.
-
Pediatric Eye Disease Investigator Group. Treatment of anisometropic amblyopia in children with refractive correction. Ophthalmology. 2006;113:895-903.
-
Kanclerz P, Przewłócka K, Arnold RW. Agreement in non-cycloplegic and cycloplegic refraction between a photoscreener and a calibrated autorefractor. BMC Ophthalmol. 2024;24(1):130. doi:10.1186/s12886-024-03375-z. PMID:38528448; PMCID:PMC10962162.
-
Drews-Botsch CD, Cotsonis G, Celano M, et al. Is patching after age 4 beneficial for children born with a unilateral congenital cataract? Ophthalmology. 2025;132:389-396. doi:10.1016/j.ophtha.2024.09.032
-
Halicka J, Bittsansky M, Sivak S, et al. Virtual reality visual training in an adult patient with anisometropic amblyopia: visual and functional magnetic resonance outcomes. Vision. 2021;5(2):22.
-
Mukit FA, Cape HT, Huq SS, et al. An isolated case of unilateral macro-ophthalmia with resultant anisometropic amblyopia in neurofibromatosis 1. Cureus. 2023;15(9):e44679.
-
Pediatric Eye Disease Investigator Group. Randomized trial of treatment of amblyopia in children aged 7 to 17 years. Arch Ophthalmol. 2005;123:437-447.
-
Wang Y, Xie L, Yao K, et al. Evidence-based guidelines for keratorefractive lenticule extraction surgery. Ophthalmology. 2025. doi:10.1016/j.ophtha.2025.
-
Mallareddy V, Daigavane S. Innovations and outcomes in astigmatism correction during cataract surgery: a comprehensive review. Cureus. 2024;16(8):e67828. doi:10.7759/cureus.67828
-
American Academy of Ophthalmology. Adult Strabismus Preferred Practice Pattern. Ophthalmology. 2023.
