干性角结膜炎

系统性红斑狼疮(SLE)的眼部表现
一目了然的要点
Section titled “一目了然的要点”1. 什么是系统性红斑狼疮(SLE)?
Section titled “1. 什么是系统性红斑狼疮(SLE)?”系统性红斑狼疮(SLE)是一种由于免疫系统慢性过度活化而导致全身多器官炎症的自身免疫性疾病。它被列为经典的五大胶原病之一。
好发于2030多岁的女性。男女比例约为1:81:9,女性占绝对多数。亚洲人较多,白种人较少。患病率约为每10万人50~100人。
SLE的诊断标准演变如下。
- 美国风湿病学会(ACR)标准(1997年最终修订):11项临床和免疫学项目中满足4项或以上即可诊断
- SLICC标准(2012年):扩展至17项,满足4项或以上即可诊断
- 欧洲风湿病联盟/美国风湿病学会标准(2019年):抗核抗体(ANA)阳性为必要条件,加权总分≥10分即可诊断
根据美国风湿病学会修订的诊断标准,在病程中满足以下11项中的4项或以上即可诊断:蝶形红斑、盘状红斑、光过敏、口腔溃疡、关节炎、浆膜炎、肾脏病变、神经系统病变、血液学异常、免疫学异常、抗核抗体阳性。
此外,在葡萄膜炎诊疗指南中,SLE被视为胶原病相关葡萄膜炎的鉴别诊断疾病1)。需结合眼部表现和全身症状,并与风湿免疫科协作评估。
不包含。约30%的患者出现眼部症状,但眼部症状本身不属于SLE的诊断标准项目。
2. 主要症状和临床所见
Section titled “2. 主要症状和临床所见”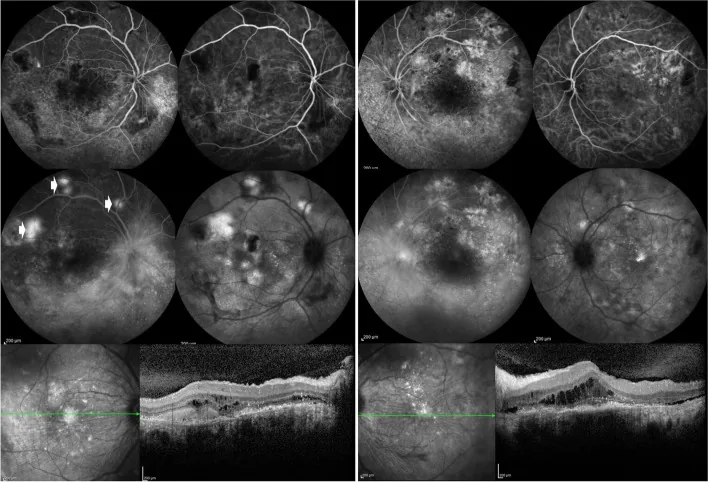
约33%至50%的患者出现眼部主诉。症状从轻度刺激感到严重视力下降不等。
- 干涩感和异物感:最常见的主诉。由继发性干燥综合征引起的干眼症所致。伴有烧灼感、视物模糊,傍晚症状加重。
- 视力下降:见于狼疮性视网膜病变和视神经炎。从无症状的眼底改变到急剧的视力下降,表现多样。
- 眼痛:视神经炎的特征是眼球运动时加重的眼眶周围疼痛。
- 畏光(刺眼):伴随干眼症或眼前段炎症出现。
- 色觉异常:视神经炎几乎全部病例均出现红绿色觉障碍。
SLE的眼部病变多样,可累及眼球几乎全层。
| 部位 | 主要所见 |
|---|---|
| 眼前段 | 干性角结膜炎、巩膜炎、表层巩膜炎 |
| 眼后段 | 软性渗出、视网膜出血、血管闭塞 |
| 神经眼科 | 视神经炎、眼球运动障碍 |
狼疮性视网膜病变是最重要的后段病变。通常为双眼性,多见于疾病活动性高的时期。
- 软性白斑(棉絮斑):最常见的视网膜表现
- 视网膜出血和Roth斑:由局部循环障碍引起
- 微动脉瘤和硬性渗出:基于微血管病变
- 血管迂曲和鞘形成:血管炎的征象
- 动静脉阻塞:也可能发生视网膜中央动脉阻塞(CRAO)和视网膜中央静脉阻塞(CRVO)
- 浆液性视网膜脱离和视网膜色素上皮脱离:推测与脉络膜循环障碍或口服类固醇有关
抗心磷脂抗体阳性与狼疮性视网膜病变,尤其是阻塞性病变相关2)。
神经眼科表现
Section titled “神经眼科表现”- 视神经炎:约1%发生。可见视盘苍白或水肿、相对性传入性瞳孔障碍(RAPD)。
- 眼球运动障碍:中枢神经系统病变导致动眼神经和展神经受损。约30%出现。
合并葡萄膜炎的情况意外地少见。SLE可能合并虹膜睫状体炎,但通常较轻。如果出现葡萄膜炎,应考虑其他原因。
3. 病因与风险因素
Section titled “3. 病因与风险因素”已鉴定出80多个与SLE相关的基因位点变异。易感基因和保护基因的复杂平衡参与发病。
- 紫外线(UV)暴露:作为光过敏诱发SLE发病
- 病毒抗原暴露:感染可成为诱因
- 药物:使用普鲁卡因胺、肼屈嗪、氯丙嗪等
- 其他:手术、外伤、精神压力
女性占绝对多数,提示雌激素及其他激素的参与。育龄期高发支持这一假说。
视网膜病变的风险因素
Section titled “视网膜病变的风险因素”狼疮性视网膜病变与疾病控制不佳相关。抗心磷脂抗体阳性在闭塞性病变的发生中起重要作用2)。
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”SLE的诊断推荐以下检查:
- 血液检查:全血细胞计数(CBC)、基础代谢面板(BMP)
- 免疫学检查:抗核抗体(ANA)、抗dsDNA抗体、抗磷脂抗体
- 炎症标志物:红细胞沉降率(ESR)、CRP、C3/C4水平
- 其他:抗SS-A抗体、抗SS-B抗体(评估继发性干燥综合征)
特别是抗核抗体在活动期大多数病例呈阳性,有助于掌握病情。作为葡萄膜炎筛查,也应确认葡萄膜炎诊疗指南推荐的基本项目(HLA-B27、胸部X线、梅毒血清反应、QFT-3G、ACE、ANA)1)。
干性角结膜炎的评估
Section titled “干性角结膜炎的评估”- 泪液弯月面测量:小于1mm为异常
- 泪膜破裂时间(TBUT):小于10秒为异常
- 角结膜染色:使用荧光素、玫瑰红或丽丝胺绿
- Schirmer试验:无麻醉下≥15mm为正常,表面麻醉下≥5mm为正常
视网膜病变的评估
Section titled “视网膜病变的评估”- 眼底检查:散瞳下评估棉絮斑、出血和血管异常
- 荧光素眼底血管造影(FFA):对评估视网膜血管炎和血管闭塞很重要。可检测渗漏、毛细血管扩张、闭塞和微动脉瘤
- 吲哚青绿(ICG)血管造影:检测FFA无法显示的脉络膜病变,表现为脉络膜高荧光
- OCT-A(光学相干断层扫描血管成像):可能有助于监测亚临床视网膜病变的视网膜结构变化(研究阶段)
视神经炎的评估
Section titled “视神经炎的评估”- 荧光素眼底血管造影:确认视盘周围毛细血管的扩张、充盈缺损和高荧光渗漏
- 钆增强MRI:检测视神经或视交叉的增大和强化
SLE的多种症状需要与其他疾病鉴别。
- 其他自身免疫性疾病:类风湿关节炎、混合性结缔组织病、干燥综合征
- 血管炎:结节性多动脉炎、白塞病
- 视网膜病变的鉴别:糖尿病视网膜病变(HbA1c升高)、高血压视网膜病变(动静脉交叉征)、结节病(常伴葡萄膜炎)
SLE视网膜病变比糖尿病视网膜病变更具闭塞性,更容易引起严重缺血。糖尿病病史或HbA1c升高对鉴别很重要。荧光血管造影显示SLE急性期视网膜血管大量荧光渗漏和微血管异常。
5. 标准治疗方法
Section titled “5. 标准治疗方法”SLE眼部症状的治疗最重要的是控制原发病。与风湿免疫科医生的协作必不可少。
原发病治疗的基础是全身性糖皮质激素给药。
- 无眼或中枢神经系统症状时:泼尼松龙(PSL)30~40 mg/日
- 有眼或中枢神经系统症状时:PSL 1 mg/kg/日,给药3~4周后,根据症状和炎症标志物逐渐减量
- 活动性狼疮视网膜病变:甲泼尼龙1 g/日×3天静脉滴注(冲击疗法),之后从泼尼松片40~60 mg/日开始逐渐减量
对于因视网膜血管炎导致进行性血管闭塞的病例,需要抗凝治疗。华法林片2~5 mg/日,调整至PT-INR 1.5~2。
对于类固醇效果不充分或类固醇抵抗的病例,使用以下药物:
生物制剂(最新)
Section titled “生物制剂(最新)”- 贝利木单抗(Benlysta®):BLyS/BAFF抑制剂。SLE适应症。BLISS-52试验证实可显著降低疾病活动性3)
- 阿尼鲁单抗(Saphnelo®):抗IFNAR1抗体(I型IFN受体抑制剂)。2022年在日本获批。显著改善中重度SLE的疾病活动性4)
- 伏环孢素(钙调神经磷酸酶抑制剂):用于狼疮性肾炎
广泛用于减少SLE的复发。眼科方面需注意视网膜毒性(参见“羟氯喹的眼毒性”一节)。
眼部局部治疗
Section titled “眼部局部治疗”视网膜病变的治疗
Section titled “视网膜病变的治疗”- 视网膜光凝术:荧光眼底造影确认视网膜新生血管时,为预防玻璃体出血立即施行。对广泛的视网膜血管闭塞也进行预防性治疗。
- 玻璃体手术:用于增殖性玻璃体视网膜病变。
- 血浆置换疗法:用于重症病例。
- 浆液性视网膜脱离:通过荧光眼底造影确认视网膜色素上皮层的荧光渗漏点,对该渗漏点进行视网膜光凝术。
视神经炎的治疗
Section titled “视神经炎的治疗”- 甲泼尼龙静脉冲击疗法:每日1克,连用3天,之后口服泼尼松每日1毫克/公斤,逐渐减量。
- 类固醇抵抗:见于多达三分之一的病例。环磷酰胺静脉冲击疗法持续6个月。
- 复发:约37%的患者在类固醇减量过程中出现复发,需要再次治疗。
羟氯喹的眼毒性
Section titled “羟氯喹的眼毒性”羟氯喹与视网膜色素上皮(RPE)中的黑色素结合,可能引起黄斑病变。
黄斑病变的危险因素:
- 终身累积剂量≥1000克(氯喹≥450克)
- 每日剂量≥5毫克/公斤(2016年AAO修订推荐)5)
- 肝功能或肾功能减退
- 肥胖、65岁以上、既往黄斑病变
毒性体征:
- 双侧旁中心视野缺损
- 内节外节连接处消失(SD-OCT上的“飞碟”征)
- 进行性色素改变(经典的“牛眼样”黄斑病变)
筛查建议(AAO 2016年修订)5):
开始治疗后5年内仅需基线检查。5年后建议每年进行Humphrey 10-2视野检查、SD-OCT和眼底自发荧光检查。存在高风险因素时,应在5年前开始筛查。如果发现黄斑病变,应停用药物。
开始治疗后5年内仅需基线检查,但5年后建议每年进行眼底检查。Humphrey 10-2视野检查和SD-OCT是主要的筛查方法。存在高风险因素(肾功能下降、高剂量、长期使用)的患者应更早开始检查5)。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”全身性免疫异常
Section titled “全身性免疫异常”SLE的病理基础是自身耐受丧失和自身抗体过度产生。
- 自身耐受破坏:遗传和环境因素导致对自身抗原的免疫耐受丧失
- T细胞异常:辅助T细胞过度活化,调节性免疫细胞减少
- B细胞成熟异常:B细胞成熟加快,凋亡受抑制。浆细胞寿命延长,产生过量自身抗体
- I型干扰素通路激活:通过BLyS/BAFF介导的B细胞过度活化
- 免疫复合物形成:自身抗体与核、核内和细胞质自身抗原结合,导致炎症细胞因子释放
- 组织损伤:慢性炎症、免疫复合物沉积和凋亡细胞清除缺陷导致组织和器官损伤
血管病变的病理学
Section titled “血管病变的病理学”SLE的病理特征是小血管和毛细血管的纤维素样坏死性血管炎。纤维素样物质由纤维蛋白、免疫复合物和补体组成。
视网膜病变的发病机制
Section titled “视网膜病变的发病机制”狼疮性视网膜病变的病理生理涉及双重机制。
- 免疫复合物型血管炎:免疫复合物沉积在血管内皮上,激活补体并释放炎症介质,导致无灌注和缺血。
- 血栓性机制:抗磷脂抗体综合征的发生导致视网膜血管血栓形成。抗心磷脂抗体阳性与闭塞性狼疮性视网膜病变相关2)。
当无灌注区域扩大时,可能出现新生血管,进而发展为增殖性玻璃体视网膜病变,甚至新生血管性青光眼。
干性角结膜炎的机制
Section titled “干性角结膜炎的机制”除了慢性炎症和免疫复合物沉积外,继发性干燥综合征的发生是主要原因。自身免疫攻击泪腺导致泪液分泌减少。
SLE视网膜病变涉及免疫复合物性血管炎和抗磷脂抗体引起的血栓形成双重机制,因此表现出更强的闭塞性病理。与糖尿病视网膜病变相比,更容易引起严重的缺血,闭塞性血管病变与更差的视力预后相关。
7. 最新研究与未来展望(研究阶段报告)
Section titled “7. 最新研究与未来展望(研究阶段报告)”OCT-A监测亚临床视网膜病变
Section titled “OCT-A监测亚临床视网膜病变”光学相干断层扫描血管成像(OCT-A)是一种新的影像诊断方法,可以无创评估传统荧光眼底造影难以检测的亚临床视网膜微血管变化。它有望应用于SLE视网膜病变的早期发现和监测,但其有效性仍处于尚未充分研究的阶段。
CAR-T疗法
Section titled “CAR-T疗法”在针对难治性SLE的CD19靶向CAR-T疗法中,少数治疗抵抗性患者报告了无药物缓解6)。对眼部并发症的长期影响是未来的课题。
生物制剂的应应用
Section titled “生物制剂的应应用”阿尼鲁单抗(I型IFN受体抑制剂)可改善活动性SLE的疾病控制,并有望对眼部并发症产生间接效果4)。眼科领域的个体疗效数据仍在积累中。
8. 参考文献
Section titled “8. 参考文献”-
日本眼炎症学会. ぶどう膜炎診療ガイドライン. 日眼会誌. 2019;123(6):635-696.
-
Stafford-Brady FJ, Urowitz MB, Gladman DD, Easterbrook M. Lupus retinopathy. Patterns, associations, and prognosis. Arthritis Rheum. 1988;31:1105-1110.
-
Navarra SV, Guzmán RM, Gallacher AE, et al. Efficacy and safety of belimumab in patients with active systemic lupus erythematosus: a randomised, placebo-controlled, phase 3 trial (BLISS-52). Lancet. 2011;377:721-731.
-
Morand EF, Furie R, Tanaka Y, et al. Trial of anifrolumab in active systemic lupus erythematosus. N Engl J Med. 2020;382:211-221.
-
Marmor MF, Kellner U, Lai TYY, et al. Recommendations on screening for chloroquine and hydroxychloroquine retinopathy (2016 Revision). Ophthalmology. 2016;123:1386-1394.
-
Mackensen A, Müller F, Mougiakakos D, et al. Anti-CD19 CAR T cell therapy for refractory systemic lupus erythematosus. Nat Med. 2022;28:2124-2132. doi:10.1038/s41591-022-02017-5.
