梅毒性葡萄膜炎是由 Treponema pallidum 引起的感染性葡萄膜炎 ,作为“伟大的模仿者”呈现多种眼部表现5) 。
约5%的二期梅毒患者发病,约占所有感染性葡萄膜炎 的10%3) 。
近年来日本国内梅毒报告数量急剧增加,对于原因不明的葡萄膜炎 ,应始终考虑梅毒。
最常见的类型是全葡萄膜炎 (75%),93%的患者出现脉络膜 视网膜 炎3) 4) 。
ASP PC(急性梅毒性后极部盘状脉络膜 视网膜 炎)是一种特征性的特殊类型。诊断需结合非梅毒螺旋体试验(RP R)和梅毒螺旋体试验(TPHA/EIA)。RP R ≥16倍且TPHA ≥1280倍提示高活动性10) 。
治疗参照神经梅毒,标准方案为高剂量青霉素G静脉注射(1800万2400万单位/日,共1014天)1) 。
禁止单独使用类固醇 而不使用抗生素,否则可能进展为全层视网膜 坏死4) 。
诊断梅毒时应对所有患者进行HIV检测。HIV合并感染时易出现双眼发病且病情较重1) 。
治疗成功率高达约90%,早期诊断和早期治疗是视力 预后的关键3) 。
梅毒性葡萄膜炎是指梅毒螺旋体(Treponema pallidum )经血行进入眼部引起眼内炎 症的疾病。梅毒是由螺旋体Treponema pallidum 引起的性传播疾病,有症状的显性梅毒分为一期至四期。近年来,三期和四期梅毒已很少见,大多数为无皮肤或黏膜病变的潜伏梅毒。后天性梅毒中,葡萄膜炎 发生于约5%的二期梅毒患者。由于围产期医疗的进步,日本国内几乎看不到先天性梅毒的眼部病变新发病例。
全球范围内,每年报告570万至600万例15~49岁人群的新发梅毒感染1) 5) 。眼梅毒约占所有梅毒病例的0.6%~2%1) 2) ,约占感染性葡萄膜炎 总数的10%3) 。北卡罗来纳州的一项研究显示,在4,232例患者中发现63例(1.5%)眼梅毒,其中38%在一期或二期梅毒时被诊断1) 。
日本国内的感染病例再次增加,2011年报告数不足1,000例,到2017年已超过6,000例。近年来,以MS M(男男性行为者)和HIV合并感染患者为中心呈增加趋势。由于临床表现多样,梅毒被称为“伟大的模仿者”1) 5) 。治疗上参照神经梅毒处理。
Q
眼梅毒发生在哪个病期?
A
眼梅毒可发生于包括一期、二期、三期和潜伏期在内的任何病期。最常见于后天性梅毒二期,以葡萄膜炎 为主。有时眼部症状是梅毒诊断的首个线索,因此对于原因不明的葡萄膜炎 ,应始终考虑梅毒的可能性。
Q
梅毒被称为“伟大的模仿者”是什么意思?
A
梅毒的眼部病变包括前部炎症、葡萄膜炎 、视神经炎 、脉络膜 视网膜 炎等多种表现,与许多其他眼病相似。因此容易延误诊断,这种多样的临床表现正是其被称为“伟大的模仿者”的原因5) 。
梅毒螺旋体 (Treponema pallidum subsp. pallidum ):螺旋体目的专性寄生体1) 。生长缓慢,具有侵入眼、中枢神经系统和胎盘等免疫特权组织的能力1) 。
性接触 :主要传播途径,传播率约60%1) 。经胎盘感染 :导致先天性梅毒1) 。经黏膜或皮肤接触 :经血行播散全身后到达眼组织。
男男性行为者(MS M) :主要风险因素,是近期感染增加的主要原因1) 。玻璃体 液中梅毒抗体阳性的病例均为HIV阳性,CD4细胞计数中位数为228/μL4) 。HIV合并感染 :使眼梅毒风险增加约2倍1) 。易表现为双眼受累,后段受累多见。CD4计数<200 cells/mL、病毒载量>200 copies/mL时患病率升高。免疫缺陷加重眼梅毒,并增加血清学假阴性的风险。多个性伴侣、不使用安全套 8) 。IRIS(免疫重建炎症综合征) :HIV阳性患者启动ART后可能发生11) 。
通过经胎盘感染发生。早期先天性梅毒(出生至生后3个月)表现为脉络膜 视网膜 炎。晚期先天性梅毒以典型的哈钦森三联征(恒牙M型缺损 、感音神经性耳聋、角膜基质炎 )为特征。陈旧性先天性梅毒的眼底可见伴有视网膜色素上皮 细胞增殖的椒盐样眼底(散在的脉络膜 视网膜 萎缩像),有时呈现类似视网膜色素变性 的眼底。
Q
诊断为梅毒后是否需要做HIV检测?
A
HIV合并感染是眼梅毒的重要风险因素,梅毒诊断时推荐所有患者进行HIV检测1) 。HIV阳性时葡萄膜炎 严重程度增加,易双眼受累,临床表现发生变化。此外,在AIDS中血清学检查可能出现假阴性,需注意。
一期
潜伏期 :10~90天。
硬下疳 :接种部位无痛性硬结。约4周后消失。也可发生在结膜 或眼周。
二期
出现时间 :硬下疳出现后4~10周。
全身播散 :血行性侵犯神经、眼、消化道、肝脏。眼部受累约10%。手掌、足底斑丘疹见于70%以上。
眼部表现 :主要为葡萄膜炎 、视网膜 炎、视神经炎 。
潜伏期
分类 :早期(1年内)和晚期(1年后)。
病程 :未经治疗者约1/3进展至三期。即使无症状,眼梅毒也可能显现。
三期
心血管系统 :主动脉炎、主动脉瘤。
神经梅毒 :脑膜梅毒、脑膜血管梅毒、脊髓痨、麻痹性痴呆。
眼部表现 :阿盖尔·罗伯逊瞳孔 、视神经萎缩 、树胶肿。
树胶肿 :良性局限性肉芽肿反应。可发生于全身,包括脉络膜 和虹膜 。
梅毒的病期不同,眼部表现差异很大。
分类 发病时间 主要眼部症状 先天性梅毒(早期) 出生至出生后3个月 视网膜 脉络膜 炎先天性梅毒(晚期) 学龄期及以后 角膜基质炎 、虹膜炎 、泪囊炎 后天性第一期 3周至3个月 眼睑和结膜 下疳 后天二期 4~10周 眼睑炎 、结膜炎 、角膜 炎、虹膜 睫状体 炎、虹膜 结节、巩膜炎 、视网膜 脉络膜 炎、玻璃体 炎、视神经炎 、视网膜血管炎 、渗出性视网膜脱离 后天晚期 数年至数十年 眼睑树胶肿、角膜基质炎 、巩膜炎 、葡萄膜炎 、视神经乳头 炎、阿罗瞳孔 、晶状体 脱位、继发性视网膜色素变性
病型 频率 全葡萄膜炎 75%3) 脉络膜 视网膜 炎93%4) 肉芽肿性虹膜 睫状体 炎 46%1) 前房积脓 6%2)
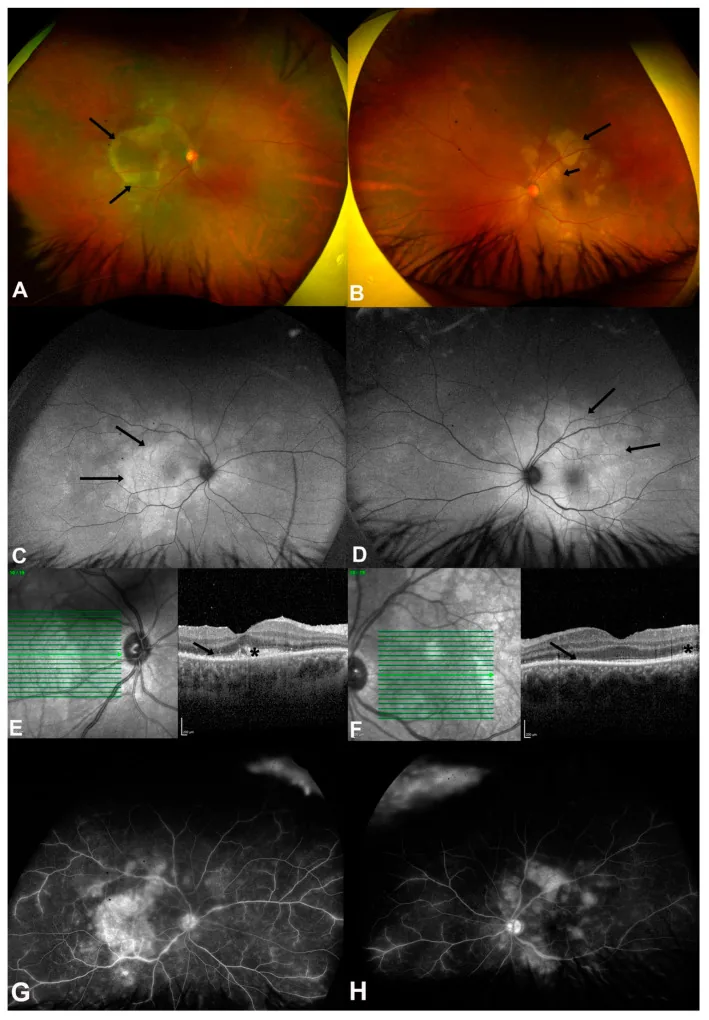
梅毒性葡萄膜炎的眼底、FAF、OCT和荧光眼底造影图像,显示后极部的placoid脉络膜视网膜病变 Ye Z, et al. Syphilis and the Eye: Clinical Features, Diagnostic Challenges, and Evolving Therapeutic Paradigms. Pathogens. 2025. Figure 1. PM
CI D: PMC12472546. License: CC BY.
双眼眼底后极部可见黄白色placoid病变,提示梅毒性后葡萄膜炎 。FAF 、OCT 和荧光眼底造影也证实了病变范围、外层视网膜 损伤、病变染色和视盘高荧光。
视力 下降视物模糊 到严重视力 障碍不等。由视网膜 /脉络膜 病变和玻璃体混浊 引起。飞蚊症 和闪光感 玻璃体混浊 或视网膜 炎出现。眼痛 和充血 葡萄膜炎 、巩膜炎 )。畏光 虹膜 睫状体 炎时加重。单眼或双眼(HIV阳性者多为双眼)2) 。
眼部症状可能是梅毒的首发表现2) 5) 。
眼梅毒的所见因受累部位不同而形态多样。全葡萄膜炎 最为常见(75%)3) ,后段病变中脉络膜 视网膜 炎占93%4) 。
眼前段所见
结膜 结膜炎 ,第三期出现树胶肿。
巩膜 巩膜炎 (多见于第二期),巩膜炎 (多见于第三期)。结节性或弥漫性。
梅毒性角膜基质炎 :免疫介导的非溃疡性、非化脓性基质炎。新生血管 形成→残留鬼影血管。先天性梅毒的哈钦森三联征之一。
肉芽肿性虹膜 睫状体 炎 :梅毒性葡萄膜炎中最常见的眼型(46%)1) 。可能残留虹膜 前粘连和虹膜 萎缩。特征是对局部类固醇 滴眼液耐药。
前房积脓 和角膜 后沉着物(KP)前房积脓 约占6%2) 。可能形成羊脂状KP。
葡萄膜和后节
中间部、后部和全葡萄膜炎 :可表现为前部、后部或全葡萄膜炎 。肉芽肿性或非肉芽肿性。
ASP PC(急性梅毒性后部盘状脉络膜 视网膜 炎)黄斑 至视乳头附近的RPE 水平出现盘状黄色病变。OCT 显示外层视网膜 和RPE 断裂及高反射隆起3) 。FAF 显示高荧光和低荧光斑片。对抗生素治疗反应良好。
视网膜血管炎 和视网膜 炎9) 。无灌注区 可导致增殖性改变。“磨玻璃样视网膜 浸润”和“奶油色小视网膜 表面沉积物”是特征性表现1) 5) 。
严重玻璃体混浊 :通常在青霉素类抗生素给药后数天内迅速消退。
视神经和神经眼科
视神经炎 视神经炎 、视乳头水肿 、神经视网膜 炎、视神经萎缩 。眼梅毒中12-78%有视神经 受累3) 。治疗延迟会导致视神经萎缩 ,影响视力 预后。
阿盖尔·罗伯逊瞳孔 瞳孔 缩小、对光反射消失但近反射保留。多见于第三期,但早期也可出现5) 。
眼球运动异常 :第三期由眶上裂综合征 、脑干梗死或动脉瘤压迫引起。合并神经梅毒时出现复视 。
Q
ASPPC是什么样的表现?
A
ASP PC(急性梅毒性后极部胎盘样脉络膜 视网膜 炎)是梅毒高度特异性的后段表现,在后极部形成大型胎盘样(placoid)黄白色病变5) 。荧光素眼底血管造影 显示特征性的早期低荧光、晚期高荧光。OCT 显示外层视网膜 和RPE 层的断裂及高反射性隆起,对抗菌药物治疗反应良好。
在原因不明的葡萄膜炎 中,应始终考虑梅毒,并保持高度怀疑指数(index of suspicion)。在推进葡萄膜炎 病因检查时,务必进行梅毒血清学检查。
临床上联合使用非梅毒螺旋体试验和特异性梅毒螺旋体试验。
检查类型 代表性检查 特点与用途 非梅毒螺旋体试验(STS) RP R(快速血浆反应素)、VDRL敏感性高,早期阳性。存在生物学假阳性。与感染活动性平行→用于筛查和治疗效果判定 梅毒螺旋体试验(TP抗原法) TPHA、FTA-ABS、TP-PA、EIA 阳性确诊梅毒。治疗后长期持续阳性→不适用于疗效判定
活动性判断 :RP R ≥16倍、TPHA ≥1,280倍 → 活动性高10) 。某病例报告中RP R高达1:2563) 。疗效判断 :RP R ≤8倍或降至初始值的1/4以下 → 驱梅治疗有效10) 。前带现象 :高滴度时非梅毒螺旋体试验可能出现假阴性(需进行稀释试验)。反向序列算法 :先进行梅毒螺旋体试验(EIA/CLIA)→ 阳性后再进行非梅毒螺旋体试验。有利于早期病例的检出1) 。结果不一致时(螺旋体阳性、非螺旋体阴性)用TP-PA复检。
通过EIA检测玻璃体 液中梅毒抗体具有高准确性,灵敏度90.9%,特异度100%4) 。在血清试验可能假阴性的HIV合并感染病例中也有助于诊断。
检测 灵敏度 特异度 血清EIA 高灵敏度(筛查) 高特异度 玻璃体 EIA90.9%4) 100%4)
在眼梅毒中,建议进行脑脊液检查以评估是否合并神经梅毒4) 。如果存在孤立性眼部症状、确认的眼部异常和螺旋体检查阳性,治疗前的脑脊液检查并非必需3) 。当怀疑视神经炎 、眼肌麻痹或脑神经症状时,应进行腰椎穿刺。
CSF-VDRL :特异性高但敏感性低。阳性可确诊神经梅毒。CSF FTA-ABS :敏感性高但特异性低。
荧光素眼底血管造影 (FA )4) )、视盘强荧光,以及ASP PC中的豹纹斑模式1) 。也可用于监测治疗效果。光学相干断层扫描 (OCT )视网膜 改变(EZ /IZ带破坏、RPE 隆起)、囊样黄斑水肿 和视网膜前膜 3) 。89%的病例出现EZ 破坏4) 。自身荧光(FAF ) :在ASP PC中表现为强荧光和弱荧光斑片3) 。超广角眼底成像 :有助于评估周边病变。
Q
玻璃体内抗体检测对哪些病例有用?
A
对于血清梅毒检测易出现假阴性的HIV合并感染者,以及血清学阴性但高度怀疑梅毒性葡萄膜炎的病例,该检测有用4) 。玻璃体 EIA特异性为100%,阳性结果可作为梅毒性葡萄膜炎的诊断依据。
需要与结节病 、结核性葡萄膜炎 、急性视网膜坏死 (ARN )/PORN 、APMPPE 、匍行性脉络膜 炎、巨细胞病毒视网膜炎 、弓形虫视网膜 炎、白塞病 和眼内淋巴瘤等鉴别4) 7) 。由于无法直接检测眼内的T. pallidum ,血清学检查与临床发现的综合判断至关重要10) 。HIV阳性患者需特别注意,AIDS患者血清学检查可能出现假阴性。
口服驱梅治疗 (轻症或门诊管理时):
沙瓦西林片(250 mg)4片,每日4次,分次服用,连续4周10) 。
神经梅毒和眼梅毒(住院静脉治疗):
梅毒性葡萄膜炎常合并神经梅毒,标准治疗为高剂量青霉素静脉注射。首选水溶性青霉素G静脉给药。
方案 剂量和用法 水溶性结晶青霉素G(首选) 1800万2400万单位/天(300万400万单位每4小时静脉注射或持续滴注),共10~14天1) 2) 3) 5) 普鲁卡因青霉素G(替代) 240万单位肌肉注射每日1次,加丙磺舒500 mg口服每日4次,共10~14天1) 2) 头孢曲松(替代) 1~2 g肌肉注射或静脉注射每日1次,共14天1) 4) 6)
治疗成功率报告约为90%3) 。
Nwaobi等人(2023)报告一名46岁男性,RP R 1:64、TPHA 1:512的眼梅毒患者,接受IV PCG 400万单位每4小时一次的神经梅毒治疗,6个月后视力 恢复2) 。
类固醇 滴眼液 + 散瞳 滴眼液(用于前眼部炎症)。炎症严重时加用全身类固醇 。但类固醇 必须在开始使用抗生素后使用。
在使用青霉素类抗生素进行驱梅治疗的同时,对于炎症严重的病例,进行全身类固醇 抗炎治疗。
参考RP R(脂质抗原试验)的变化。抗体滴度降至8倍以下或初始值的1/4以下,可判断为驱梅有效10) 。治疗后仍有复发可能,需定期复查RP R。
首选青霉素脱敏治疗1) 7) 。
头孢曲松:1~2 g 肌注或静注,每日1次,共14天1) 6) 。
多西环素 :200 mg/日(100 mg每日2次),共28天1) 7) 。
Cubelo等(2022)报告了一例HIV阳性、PCG过敏的24岁男性,给予多西环素 100 mg每日2次共14天,RP R从1:1,024降至1:327) 。随后进行了PCG脱敏治疗。
它是在治疗开始后24小时内,对被杀死的梅毒螺旋体来源的炎性脂蛋白的反应而发生的。在眼科方面,可能表现为虹膜炎 的复发(炎症再燃)。
症状 :发热、头痛、肌肉痛、寒战。早期梅毒中发生率为30-70%,神经梅毒中为2% 1) 。也有报告约75%的病例出现 3) 。眼部症状 :已有视力 下降、黄斑水肿 、视盘肿胀、棉絮状斑点的报道。处理 :继续治疗。使用解热镇痛药进行对症治疗。
单独使用类固醇 (无抗菌药物)是绝对禁忌的。感染可能恶化并进展为全层视网膜 坏死 4) 5) 。
类固醇 必须在开始抗菌药物治疗后使用。梅毒性葡萄膜炎可能对类固醇 滴眼液耐药。如果改善不佳,应重新考虑梅毒并进行血清学检查。
获得性梅毒是通过性行为传播的全身感染。注意可能合并HIV感染以及因治疗不充分导致眼部和中枢神经系统复发。
在合并HIV的病例中,需注意免疫恢复相关的IRIS 11) 。
Q
如果对青霉素过敏,如何治疗?
A
首选青霉素脱敏治疗。如果困难,替代药物包括头孢曲松(1-2 g 每日一次,共14天)或多西环素 (200 mg/日,共28天)1) 7) 。但两者对眼梅毒的疗效证据均有限。
Q
如果发生雅里施-赫克斯海默反应,是否应停止治疗?
A
治疗应继续而不中断。全身症状如发热和头痛可使用解热镇痛药进行对症治疗。眼部症状(包括视力 下降、视乳头肿胀等)通常是暂时的,随着继续治疗而改善1) 。
Q
在什么情况下可以使用类固醇?
A
类固醇 仅在充分使用抗生素后炎症仍存在时,才考虑作为辅助治疗。在没有免疫抑制的情况下预先使用类固醇 是禁忌的,因为它可能导致梅毒恶化5) 。
T. pallidum 从原发感染部位经血行播散,到达包括眼组织在内的全身器官。它穿过血-视网膜屏障 ,引起脉络膜 、视网膜 和玻璃体 的炎症。眼梅毒可发生于从一期到晚期的任何阶段,但后段病变在二期后更常见。
梅毒螺旋体通过TLR2/TLR4/TLR5依赖性信号诱导IL-1β、IL-6、IL-12和TNF -α的产生,引起类似迟发型超敏反应的组织损伤1) 。CD4+细胞和巨噬细胞主导一期病变,而CD8+细胞主导二期病变。IFN-γ的产生激活并招募巨噬细胞。
在梅毒性角膜基质炎 中,主要病理不是T. pallidum 本身的直接感染,而是对梅毒螺旋体抗原的免疫反应(角膜基质 中的淋巴细胞浸润和血管侵入)。因此,它对类固醇 有反应,但单用青霉素可能无法消退症状。
梅毒螺旋体增殖缓慢,并具有侵入眼、中枢神经系统和胎盘等免疫豁免组织的能力1) 。通过Fas相关死亡途径诱导CD4+细胞凋亡 ,导致免疫清除不完全,从而建立慢性感染。
在HIV阳性患者中,二期后眼梅毒的进展加速。双眼受累在HIV阳性患者中更常见(62%),而HIV阴性患者为38%(96例研究)1) 。在艾滋病患者中,血清学检查可能出现假阴性,诊断时需注意。
HIV阳性患者患有眼梅毒时,在开始抗逆转录病毒治疗(ART)后可能发生IRIS(免疫重建炎症综合征),导致炎症一过性加重11) 。
ART后发病时间 :中位28天暴露型IRIS :ART开始前未诊断的梅毒变得明显。矛盾型IRIS :治疗中的梅毒暂时恶化。
Pipito等人(2023)的综述报告,IRIS病例在ART前CD4细胞计数较低(中位数196/μL),但ART后恢复至318/μL 11) 。在CD4低值病例中,梅毒血清学检查也有假阴性的风险 11) 。
对青霉素类抗生素的反应通常良好,给药后数天内玻璃体混浊 常迅速消退。治疗成功率报告约为90% 3) 。合并视神经炎 的病例若治疗延迟,可能导致视神经萎缩 ,影响视力 预后。HIV合并感染病例治疗后复发风险高,需要长期监测RP R变化。
Q
HIV阳性患者ART开始后眼炎症恶化应如何处理?
A
如果ART开始后约28天炎症加重,怀疑IRIS。鉴别暴露型和矛盾型,若梅毒治疗不充分,应优先进行青霉素G治疗 11) 。在确立抗梅毒治疗后考虑加用类固醇 。
抗VEGF治疗 炎症性脉络膜新生血管 (iCNV )CNV 极为罕见。Świerczyńska等人(2021)的报告显示,阿柏西普 玻璃体内注射 后,约1/3的患者一次注射即可稳定病情,约2/3的患者两次注射后视力 稳定 6) 。iCNV 仅靠抗生素治疗不能消退,额外进行抗VEGF玻璃体内注射 有效。
静脉优势型梅毒性视网膜血管炎 :通常梅毒性视网膜血管炎 以动脉炎或混合型为主,但在HIV合并感染病例中报告了静脉炎优势型。Mammo等人(2022)报告了一例53岁HIV阳性男性,表现为静脉炎优势的泛葡萄膜炎 ,采用IV PCG 400万单位14天×2疗程治疗 9) 。治疗后进展为旁静脉色素性视网膜 病变。
多模态成像提高诊断准确性 :EDI-OCT 、超广角自发荧光(FAF )和ICG的结合有望提高眼梅毒的诊断准确性1) 3) 。ICG可检测到脉络膜 暗点、热点和模糊的脉络膜 血管。这些多模态成像结果的积累可能有助于与结节病 和结核病的鉴别。
利用眼内液的诊断技术发展 :玻璃体 液中EIA检测梅毒抗体(敏感性90.9%,特异性100%)对血清学假阴性病例和难治性后葡萄膜炎 具有很高的诊断价值4) 。特别是在HIV合并感染或免疫缺陷状态下血清诊断可靠性降低的情况下,眼内液检查正成为一种重要的辅助诊断方法。
IRIS管理的优化 :关于ART启动相关IRIS的发生机制和最佳管理策略的研究正在进展中11) 。在IRIS的预防和治疗中,优化抗梅毒治疗和ART的时机是未来的课题。
Chauhan K, Bhatt DL, Bhardwaj P, et al. Demystifying Ocular Syphilis – A Major Review. Ocul Immunol Inflamm. 2023. DOI:10.1080/09273948.2023.2217246.
Nwaobi S, Nwaobi A, Karunakaran K, et al. Through the Eyes: A Case of Ocular Syphilis. Cureus. 2023;15(11):e48XXX. PMC10694475.
Kayabai M, Doğan R, Kaçar İ, et al. Presentation of Ocular Syphilis with Bilateral Optic Neuropathy : A Rare Case Report. Neuro-Ophthalmology. 2023. PMC10732629.
Fekri S, Golabdar M, Rahimi M, et al. The First Reported Case of Ocular Syphilis in an Iranian Patient Presenting with Intermediate Uveitis. J Ophthalmic Vis Res. 2023. PMC10794801.
Das P, Chakraborty PP, Mondal SK, et al. Ocular syphilis in antibiotic era: A review with case series. Indian J Sex Transm Dis AIDS. 2025. PMC12716672.
Świerczyńska MP, Nowak M, Michalak J, et al. Choroidal neovascularization secondary to ocular syphilis treated with intravitreal aflibercept. Rom J Ophthalmol. 2021;65(4). PMC8764425.
Cubelo M, Almeida MJ, Sobrinho-Simões J, et al. A Case of Ocular Syphilis in an HIV-Positive Patient With Penicillin Allergy. Cureus. 2022;14(9). PMC9574520.
Kiani R, Patel L, Gupta N, et al. Blurry Diagnosis of Ocular Syphilis: A Case Report. Cureus. 2022;14(10). PMC9635406.
Mammo DA, Ober MD, Dansingani KK. Ocular Syphilis With Phlebitis and Paravenous Pigmentary Retinopathy. J VitreoRetinal Dis. 2022. PMC9954775.
日本眼炎症学会ぶどう膜炎診療ガイドライン作成委員会. ぶどう膜炎診療ガイドライン. 日眼会誌. 2019;123(6):635-696(梅毒性ぶどう膜炎の項).
Pipito N, Calcagno A, Caramello P, et al. Immune reconstitution inflammatory syndrome in patients with syphilitic uveitis: a review. J Ophthalmic Inflamm Infect. 2023;13:30.
复制全文后,可以粘贴到你常用的 AI 助手中提问。
打开下面的 AI 助手,并把复制的内容粘贴到聊天框。