脉络膜结核
脉络膜粟粒性结核:黄白色小渗出斑散在于视网膜下。1/2~1/6视盘直径的结节呈多灶性脉络膜炎表现。通常为双眼性,好发于AIDS等细胞免疫低下时。结核菌素反应常为阴性。
脉络膜结核瘤:在后极部附近形成的视盘大小以上的黄白色肿块。是由上皮样细胞和朗汉斯巨细胞组成的肉芽肿,伴有干酪样坏死。非常罕见的病变。

结核性葡萄膜炎(tubercular uveitis; TB-uveitis)是结核菌(Mycobacterium tuberculosis; Mtb)经血行进入眼内,引起以视网膜和脉络膜为主的炎症状态。从眼内直接检测结核菌几乎不可能;临床上重视免疫学检查和对抗结核药物的治疗反应来诊断。仅用抗结核药物就能显著改善的葡萄膜炎的存在,是比细菌学证据更重要的临床发现。
结核性葡萄膜炎在感染性葡萄膜炎中所占比例约为1.4% 3)。在印度、印度尼西亚等亚洲高负担国家,它占感染性葡萄膜炎的22.9%~48.0% 1)。在全球三级医疗中心,所有葡萄膜炎患者中的患病率据报道为0.2%~10.5% 2)。在日本,结核病发病率高于欧美发达国家,尤其在大城市发病率较高。随着来自中国、印度、东南亚等结核病高负担国家的旅行者增加,在葡萄膜炎的鉴别诊断中应始终考虑该病。
结核性葡萄膜炎的视力损害可能很严重。据报道,约三分之一的患者最佳矫正视力低于3/60 1)。葡萄膜黄斑水肿和继发性青光眼发生在约30%的患者中 1)。活动性肺结核合并葡萄膜炎的情况很少见,许多病例肺部表现有限或无异常。
据称约占所有感染性葡萄膜炎的1.4% 3)。由于即使没有活动性肺部病变也可能发生眼结核,因此如果有IGRA阳性等免疫学证据,无论有无肺部病变,都应怀疑眼结核。
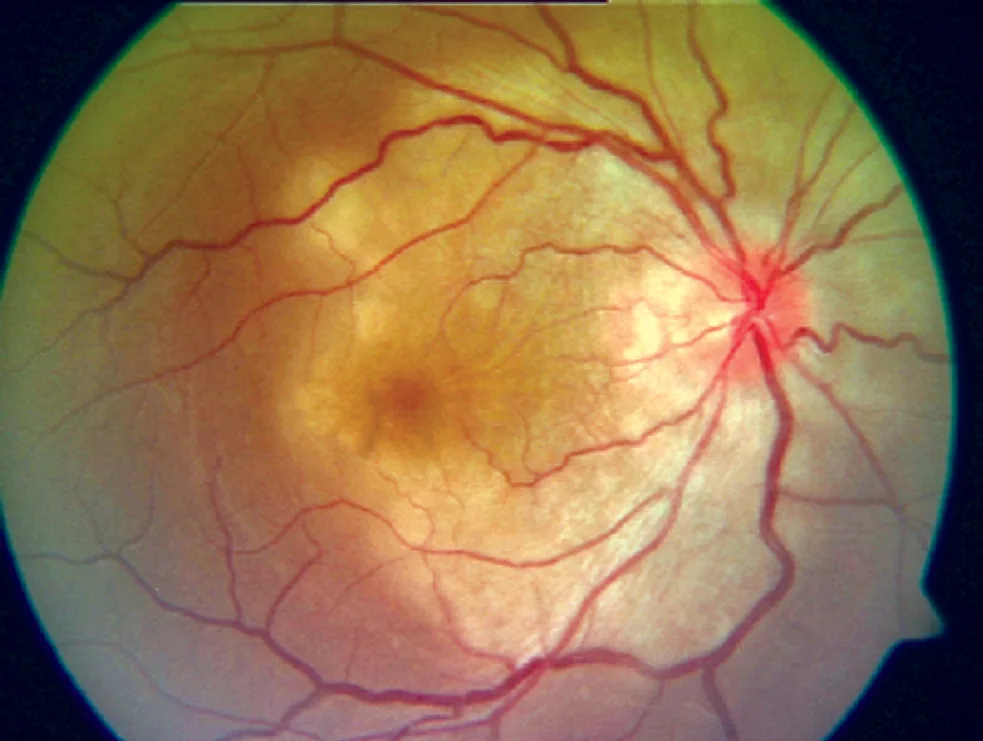
症状因炎症的部位和严重程度而异。
结核性葡萄膜炎可表现为前部、中间部、后部或全葡萄膜炎 1)。后部葡萄膜炎是最常见的临床类型。
SUN(标准化葡萄膜炎命名法)2021年确定了与结核性葡萄膜炎密切相关的五种表型 4)。
脉络膜结核
脉络膜粟粒性结核:黄白色小渗出斑散在于视网膜下。1/2~1/6视盘直径的结节呈多灶性脉络膜炎表现。通常为双眼性,好发于AIDS等细胞免疫低下时。结核菌素反应常为阴性。
脉络膜结核瘤:在后极部附近形成的视盘大小以上的黄白色肿块。是由上皮样细胞和朗汉斯巨细胞组成的肉芽肿,伴有干酪样坏死。非常罕见的病变。
视网膜血管炎 / 脉络膜炎
前葡萄膜炎以肉芽肿性炎症为特征。可见羊脂状角膜后沉着物(mutton fat KP)、虹膜Koeppe结节和Busacca结节、宽基底虹膜后粘连 1)。中间部可出现雪球状玻璃体混浊(snowball)和睫状体扁平部渗出物(snowbank)。
以下按病变部位总结所见。
| 部位 | 代表性所见 |
|---|---|
| 前部 | 虹膜结节(Koeppe和Busacca结节)、羊脂状KP、前房积脓、前部玻璃体炎 |
| 中间部 | 雪球状玻璃体混浊、雪堤、周边视网膜血管鞘形成、周边肉芽肿 |
| 后部/全葡萄膜炎 | 脉络膜粟粒结核、结核瘤、视网膜下脓肿、地图状脉络膜炎、黄斑囊样水肿 |
| 视网膜炎/血管炎 | 视乳头视网膜炎、视神经炎、闭塞性静脉炎 |
| 重症型 | 眼内炎、全眼球炎 |
后葡萄膜炎是最常见的临床类型。脉络膜结核结节、匍行性脉络膜炎和闭塞性视网膜血管炎是典型表现1)。
结核菌从肺部原发感染灶通过血行播散到达眼内(主要是脉络膜),引起炎症。脉络膜血流量大、氧分压高,有利于细菌定植。发病机制有以下三种假说1)。
风险因素:
根据葡萄膜炎诊疗指南,满足以下四个要素时可诊断为结核性葡萄膜炎3)。
由于眼内很少能检测到结核菌,大多数病例基于推定诊断进行治疗。口服异烟肼开始后约1周,如果炎症消退或加重(对药物的某种反应),则视为有效。如果1个月后无效,则视为无效并停药。
| 检查方法 | 特点 | 注意事项 |
|---|---|---|
| 结核菌素试验 | 对结核菌的IV型过敏反应 | 受BCG接种影响;粟粒性结核和艾滋病病例中呈阴性 |
| QFT(QuantiFERON® TB Gold Plus) | 测量致敏CD4/CD8阳性T淋巴细胞的干扰素γ产生。不受BCG影响。 | 潜伏感染也呈阳性 |
| T-SPOT® | ELISPOT法。对检测既往结核感染有用。 | 与干扰素γ释放试验有类似的局限性 |
QuantiFERON® TB Gold Plus(QFT-plus)通过测量对结核分枝杆菌致敏的CD4阳性和CD8阳性T淋巴细胞的细胞免疫反应分泌的干扰素γ,可在不受卡介苗接种影响的情况下进行判定。结合结核菌素试验和IGRA可提高眼结核诊断的敏感性9)。
使用免疫抑制剂期间,结核菌素试验和IGRA可能出现假阴性。如有可能,应在免疫抑制治疗开始前进行检查。在非流行国家,IGRA阳性的葡萄膜炎患者中原因不明的比例显著高于阴性者(59% vs 39%)1)。
使用眼内液(房水、玻璃体液)进行PCR检测。实时PCR法(如IS6110序列)有用,但系统评价中PCR阳性率仅为55%1)。在印度等高流行国家,使用MPB64引物时阳性率最高可达70%1)。眼内液PCR被视为辅助检查。
国际眼结核协作研究(COTS)小组提出了根据表型(匍行性脉络膜炎/结核瘤/多灶性脉络膜炎/血管闭塞性视网膜炎)和流行区/非流行区进行判定的算法2)。对于匍行性脉络膜炎和结核瘤,推荐IGRA或TST任一阳性即开始抗结核治疗。该算法在流行国家和非流行国家设定不同的阈值,便于临床应用。
IGRA或结核菌素试验阳性表明对结核菌有免疫反应,但潜伏感染也可呈阳性,因此不能确诊眼结核。需结合典型眼部表现、排除其他疾病和治疗反应综合诊断1)2)。
在使用TNF-α抑制剂等生物制剂前,必须通过胸部X线、结核菌素试验或IGRA进行潜伏性结核筛查1)。如果潜伏性结核阳性,应在开始生物制剂前至少进行1个月的预防性化疗。即使筛查阴性,也需注意治疗期间结核再激活。
结核性葡萄膜炎的治疗核心是多药联合抗结核治疗(ATT)1)。据报道,ATT可使复发率降低约75%2)。
RIPE四药联合方案:
| 治疗期 | 持续时间 | 药物 | 常用剂量 |
|---|---|---|---|
| 强化期 | 2个月 | 异烟肼(INH)+ 利福平(RFP)+ 吡嗪酰胺(PZA)+ 乙胺丁醇(EB) | INH 300mg/日、RFP 450mg/日、EB 750mg/日、PZA 1.5g/日 |
| 维持期 | 4个月以上 | INH + RFP | 继续上述治疗 |
按商品名处方的例子:异烟肼片(INH 100mg)3片分3次,利福平胶囊(RFP 150mg)3粒早餐前一次,乙胺丁醇片(EB 250mg)3片早晨一次。为预防周围神经炎,联合使用维生素B6复合胶囊B50(VB6)。自2008年起,利福布汀(Fabutin)也获批,加入了联合治疗的选择3)。
治疗持续时间标准至少为6个月,重症或反应不佳的病例可延长至9-12个月1)。作为治疗试验,ATT开始后约1周若炎症消退或加重,则判断为有效。1个月无效则视为无效并停药。若有效,则加用利福平等药物。
COTS的ATT启动标准2):
与ATT联合使用对控制后部炎症有效。通常与ATT同时或紧随其后开始,并在4-6周内逐渐减量。对于匍行性脉络膜炎,COTS指南推荐在开始或之后立即联合口服肾上腺皮质激素2)。球筋膜囊下注射曲安奈德(Kenacort-A®)也是一种选择,但最好在确定抗结核药物有效性后进行。对于迁延或复发病例,考虑加用免疫抑制剂2)。
标准治疗为强化期2个月加维持期4个月,共6个月。重症或反应不佳者可延长至9~12个月1)。治疗期间必须定期进行视功能检查(特别是监测乙胺丁醇的视神经毒性)。
结核性葡萄膜炎的发病机制复杂,涉及直接感染和免疫介导机制两方面1)。
结核菌从肺部原发感染灶经血行播散至眼组织。脉络膜血流量大、氧分压高,有利于细菌定植。组织学上形成由上皮样细胞和朗汉斯巨细胞组成的肉芽肿。伴有干酪样坏死的肉芽肿性炎症是脉络膜结核瘤的组织学特征。在粟粒性结核中,当细胞免疫缺陷(如艾滋病)导致大量结核菌涌入时,可见散在的1/2~1/6视盘直径的脉络膜结节。
结核菌感染时,视网膜色素上皮(RPE)诱导以IFN-α/β为主的先天免疫反应。即使眼内不存在活菌,对结核菌抗原的过度免疫反应也可引起眼内炎症。视网膜血管炎被认为是对结核菌结构蛋白的免疫反应所致。
Putera等人(2024)的综述指出,根据调节性T细胞(Treg)功能异常和I型干扰素刺激基因(ISG)表达,可能对高活动性TB-葡萄膜炎进行分层。C1q+ I型IFN特征作为诊断辅助标志物受到关注1)。
有学者提出结核菌抗原与视网膜抗原之间的分子模拟(antigenic mimicry)导致自身免疫反应。抗视网膜自身免疫反应(IRBP T细胞反应)的激活可能维持和增强眼内炎症1)。据报道,活动性和潜伏性TB-葡萄膜炎患者血清抗视网膜抗体(ARA)阳性率高于健康对照者。
除了传统的ATT,调节宿主免疫反应的方法也在研究中。在耐药结核病增加的背景下,肺结核领域正在研究多种HDT候选药物,其在结核性葡萄膜炎中的应用也受到关注1)。通过ISG特征进行疾病活动性分层可能有助于提高未来ATT适应症判断的准确性。
Putera等人(2024)报告称,ISG(I型干扰素刺激基因)的表达模式可能对高活动性TB-葡萄膜炎进行分层1)。C1q与I型IFN特征的组合被认为是有前景的诊断辅助标志物,未来可能提高ATT适应症判断的准确性。
COTS小组正在基于多中心数据持续审查ATT管理标准2)。特别是针对需要免疫抑制治疗的迁延性和复发性病例,除类固醇以外的免疫抑制药物使用指南也在制定中。
Faneli等人(2026)报告了6例后部眼结核病例5)。病例包括多种临床类型:脉络膜肉芽肿、多灶性脉络膜炎、匍行性脉络膜炎和闭塞性视网膜血管炎。所有病例均通过RIPE疗法联合类固醇使炎症消退。4例有监禁史,仅3例有肺部表现。1例合并脉络膜新生血管的患者加用了抗VEGF治疗。
Hou等人(2025)报告了一例36岁男性患者,其推定眼结核与自身免疫性视网膜病变极为相似6)。在使用类固醇治疗后病情恶化,随后单独使用ATT治疗一个月,视力和黄斑结构显著改善。
Babalola等人(2025)报告了一例15岁男孩的非典型眼结核病例,伴有双侧视神经萎缩和视网膜前膜7)。家族结核病史和脉络膜结节的存在为推定诊断提供了线索。
眼内液实时PCR技术的改进提高了使用MPB64引物时的阳性率。多模态成像与IGRA相结合的非侵入性诊断算法也在建立中。Bruzzone等人(2024)报告了一例在两次结核菌素试验阴性后QFT-plus转为阳性,从而诊断为结核性多灶性脉络膜炎的病例,强调了在免疫抑制开始前进行IGRA的重要性8)。