典型所见
“雾中头灯”:伴有玻璃体炎的白色局限性视网膜炎。是强烈提示本病的所见。
视网膜脉络膜瘢痕:伴有色素沉着的陈旧性瘢痕。复发病灶倾向于出现在其边缘。
玻璃体炎:程度从轻度到重度不等。
视网膜血管炎:见于病灶附近的血管。有时可见伴有Kyrieleis斑的节段性动脉炎。
前葡萄膜炎:继发性非肉芽肿性虹膜睫状体炎。有时可见肉芽肿性、星状的角膜后沉着物。

眼弓形虫病是由专性细胞内寄生原虫 Toxoplasma gondii 感染视网膜引起的视网膜脉络膜炎。它是感染性葡萄膜炎最常见的原因,在一些国家占所有后葡萄膜炎的50%以上7)。
T. gondii 是一种人畜共患感染,猫科动物为终宿主,包括人类在内的几乎所有哺乳动物为中间宿主。通过摄入被猫粪便中排出的卵囊污染的土壤或水,或摄入未煮熟的肉(如猪肉、羊肉、鹿肉)中的组织包囊而感染。全球约三分之一的人口感染7),日本成人血清阳性率为20–30%。眼弓形虫病约占感染性葡萄膜炎病例的1%8)。
该原虫有三种形态:
由眼弓形虫病引起的眼病比例在美国约为2%,巴西为18%,非洲高达43%。热带地区感染率最高,反映了适合原虫生长的温暖潮湿环境。
T. gondii 的群体结构高度克隆化,北美和欧洲以I型、II型和III型三个谱系为主7)。II型占后天性眼病变的大多数,而I型在先天性弓形虫病中更常见。在巴西,I型和非典型型参与后天感染,基因型的差异可能导致临床表现的多样性7)。
先天感染是母亲初次感染时通过胎盘传播给胎儿,典型表现为双眼黄斑部瘢痕病灶。妊娠中晚期胎盘感染率较高,但妊娠早期感染的疾病严重程度往往更高。后天感染是出生后通过污染食物或水新近感染,表现为眼底周边部无陈旧性病灶的局限性脉络膜视网膜炎。详情请参阅“病理生理学”部分。
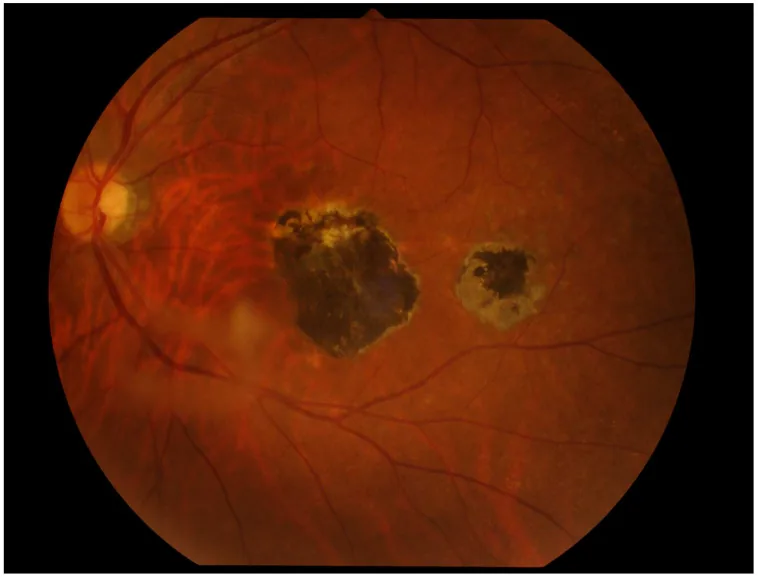
活动性眼弓形虫病可见以下症状:
眼弓形虫病的临床所见大致分为典型所见和非典型所见。
典型所见
“雾中头灯”:伴有玻璃体炎的白色局限性视网膜炎。是强烈提示本病的所见。
视网膜脉络膜瘢痕:伴有色素沉着的陈旧性瘢痕。复发病灶倾向于出现在其边缘。
玻璃体炎:程度从轻度到重度不等。
视网膜血管炎:见于病灶附近的血管。有时可见伴有Kyrieleis斑的节段性动脉炎。
前葡萄膜炎:继发性非肉芽肿性虹膜睫状体炎。有时可见肉芽肿性、星状的角膜后沉着物。
非典型所见
视乳头炎/视神经视网膜炎:视乳头肿胀。有时伴有黄斑星芒状渗出。
点状外层视网膜炎(PORT):深层视网膜的多发性小病变。OCT有时可见巨大外层视网膜囊肿(HORC)2)。
视网膜血管闭塞:可能发生动脉分支闭塞或树枝状血管炎。
巩膜炎/视网膜脱离:重症病例中并发。
多灶性弥漫性坏死性视网膜炎:免疫缺陷患者可能出现严重的双侧病变7)。
先天性感染中,双眼黄斑部可见主要病变为瘢痕性病灶(中心部有灰白色纤维性增殖组织和黑褐色色素沉着混杂,周围伴有脱色素环)。其附近有时可见称为子病灶的小色素性瘢痕。伴有前房炎症和重度玻璃体混浊(“雾中头灯”),与后天感染不同,为双眼性。复发病灶不会同时出现在双眼。后天感染中,眼底周边部可见不伴有陈旧性病灶的局限性白色至灰白色渗出性视网膜脉络膜炎,伴有重度玻璃体混浊和视网膜血管炎。随着愈合,形成伴有色素沉着的边界清晰的萎缩性瘢痕。
视神经乳头周围的病变称为Edmund-Jensen型邻近视乳头视网膜脉络膜炎。荧光眼底造影显示,早期病灶周围组织染色、中央呈阴影缺损,随时间推移缺损部位出现荧光染色,晚期荧光渗漏明显。
非典型病例有时难以与急性视网膜坏死(ARN)或眼内淋巴瘤鉴别5)。在荷兰的一个队列中,18例超过3个视乳头直径的大型病变中有4例最初被诊断为急性视网膜坏死5)。
T. gondii 的感染途径主要有以下三种:
主要风险因素如下:
Kohler等人(2023)报告了4例与食用鹿肉相关的初次感染病例。均为男性,平均年龄56岁,在10-11月狩猎季节暴露,呈现明确的时间序列:全身症状在数周内出现,眼部症状在1-3个月后出现4)。
即使母体发生初次感染,也不一定会导致胎儿感染,大部分为无症状感染。但部分病例会表现为先天性弓形虫病,出现严重的眼部和神经症状(视网膜脉络膜炎、脑积水、颅内钙化、运动神经障碍四联征),因此孕妇的抗体筛查和早期治疗非常重要。
眼弓形虫病的诊断主要基于临床发现。典型的表现为“雾中车灯”样外观和伴有色素沉着的视网膜脉络膜瘢痕,通常可以临床诊断。临床发现和抗弓形虫抗体阳性同时存在时,强烈支持本病的诊断8)。
| 检查 | 意义 | 注意事项 |
|---|---|---|
| IgG抗体 | 确认既往感染 | 阴性可排除感染。阳性率随年龄增长而升高。 |
| IgM抗体 | 提示近期感染 | 可能持续升高超过一年。先天性感染复发时不升高。 |
| IgG亲和力 | 判断感染是新近还是陈旧 | 高亲和力提示慢性感染5) |
免疫功能正常者若IgG抗体完全阴性,基本可排除弓形虫病。但免疫功能低下患者即使抗体阴性也可能存在活动性感染3)。CLL患者低丙种球蛋白血症时需注意假阴性3)。
后天感染时,血清IgM抗体滴度升高,随后下降具有诊断价值。IgG抗体滴度也会升高,但由于亚临床感染多见,高抗体滴度不一定意味着弓形虫脉络膜炎。先天性感染复发时IgM抗体滴度不升高。
房水或玻璃体液的PCR检查对非典型或诊断困难病例有用。
计算眼内液中弓形虫抗体滴度与IgG值的比值(Goldmann-Witmer系数:Q值)也很有用,报道敏感性2981%,特异性83100%5)。联合免疫印迹法三种方法并用时敏感性达85~97%,特异性达93%5)。
Shakha等人(2024)报道一例33岁男性非典型多灶性视网膜炎,通过房水PCR检出T. gondii而确诊。该病例在Tenon囊下注射类固醇后恶化,提示确诊前使用长效类固醇的风险1)。
标准化葡萄膜炎命名(SUN)工作组于2021年发布了弓形虫视网膜炎的分类标准9)。除了局灶性或少量坏死性视网膜炎外,还需要满足PCR阳性或IgM阳性,或特征性临床表现(色素沉着瘢痕、圆形至椭圆形视网膜炎、复发性急性病程)。该标准整合了临床和实验室检查结果,有助于多中心研究和临床试验中的病例识别。
IgG抗体阳性仅表明既往感染,并不一定存在眼部病变。由于亚临床感染常见,诊断眼弓形虫病必须结合临床表现进行综合判断。葡萄膜炎诊疗指南也指出,临床表现与抗体阳性并存可强烈支持本病8)。
并非所有病变都需要治疗。局限于周边视网膜的轻度炎症有自愈倾向。治疗适应症如下:
乙酰螺旋霉素(0.8~1.2克/日,分3~4次)至少给药30天。有时可持续2~3个月直至活动性炎症消失。渗出性病变瘢痕化且弓形虫抗体滴度下降时,可结束治疗。
若玻璃体炎症严重,可联合口服类固醇(从泼尼松20~30毫克/日开始),但最好在开始抗菌药物治疗后等待数天再联合使用8)。联合口服类固醇0.5毫克/公斤/日可加速眼部症状改善。对于后极部病变或大于1/2视盘直径的复发病灶,需要联合抗弓形虫药物和类固醇治疗。
克林霉素1.2克分4次口服,4~6周为一个疗程,也是一种方法。
乙胺嘧啶+磺胺嘧啶+类固醇的三联疗法是经典治疗方法,在美国葡萄膜炎学会的调查中,32%的受访者将其作为首选。由于乙胺嘧啶是叶酸拮抗剂,需联合亚叶酸钙(甲酰四氢叶酸)以预防骨髓抑制。通常给药4~6周。
TMP-SMX(160/800毫克)每日两次,是乙胺嘧啶+磺胺嘧啶的安全有效替代方案7)。副作用少且易于获取。
Kohler等人(2023)用TMP-SMZ单药治疗了4例原发感染,所有病例的视网膜病变均迅速改善。但为防止全身症状复发,需要至少连续给药3个月4)。
玻璃体内注射克林霉素1毫克+地塞米松0.4毫克,疗效与全身给药相当,2年后复发率为6~15%5)。适用于全身治疗禁忌的患者7)。几乎无副作用,消退时间约为2.5±1周5)。
阿奇霉素首剂500毫克,之后250毫克/日,疗效与TMP-SMX相当5)。与乙胺嘧啶联用时可替代磺胺嘧啶,副作用发生率低7)。
Syed Mohd Khomsah等人(2023)对一名35岁女性双眼眼弓形虫病患者给予阿奇霉素500毫克/日和泼尼松龙逐渐减量治疗6周。玻璃体炎和视盘肿胀在4周内消退,但由于乳头黄斑束纤维化和黄斑皱褶,右眼视力不佳6)。
阿托伐醌750 mg每日四次用于对一线药物不耐受的患者5)。治疗开始后1-3周内可获得反应,严重副作用较少。
一项前瞻性随机试验显示,长期给予TMP-SMX(160/800 mg)每周三次,复发率从23.8%降至6.6%7)。另一项随机试验中,隔日一片共311天,6年时复发率为1.4%(安慰剂组27.5%)5)。
弓形虫感染本身无手术指征,但对于并发的视网膜脱离、黄斑前膜(ERM)和玻璃体出血,可行玻璃体切除术5)。
Kohler等人(2023)的病例系列中,4例初发感染中有2例出现并发症:ERM伴囊样黄斑水肿,以及退行性新生血管引起的玻璃体视网膜牵拉4)。ERM病例经玻璃体切除和膜剥离后视力改善。
局限于周边视网膜的小病灶有时可自愈。然而,每次复发都会增加视网膜内包囊数量,因此有人认为应治疗所有复发以最小化未来复发风险。累及后极部或伴有视力下降的病变需要治疗。
T. gondii 主要感染视网膜,也可波及脉络膜、玻璃体和前房7)。脉络膜病变继发于视网膜感染,不会单独出现。
经口摄入的卵囊或组织囊在肠道转变为滋养体(速殖子),并通过血行播散至全身。到达视网膜的途径包括白细胞携带寄生虫以及速殖子直接穿过血管内皮6)。
速殖子感染视网膜多种细胞,其中Müller胶质细胞是最易感的宿主细胞6)。视网膜色素上皮(RPE)感染后,生长因子产生异常,促进邻近未感染RPE细胞增殖。这一机制被认为与特征性色素沉着瘢痕的形成有关。
在坏死性视网膜炎中,血管炎和视网膜破坏进展。组织学上可见伴有Bruch膜坏死的广泛肉芽肿性炎症浸润7)。瘢痕化从边缘向中心进展,色素沉着程度因病例而异。
即使发生经胎盘感染,发病也较少,大部分为亚临床感染。先天性弓形虫病的主要症状为视网膜脉络膜炎、脑积水(或小头畸形)、颅内钙化和精神运动障碍四联征。宫内感染婴儿中约70%出现脉络膜瘢痕病灶(黄斑中心),其中1-2%合并严重视力障碍。复发多见于青春期,约1/3的瘢痕病灶会发生复发。
对430例接受治疗的先天性弓形虫病患者的评估显示,中位随访12年,30%出现眼部病变7)。但严重双眼视力障碍在130例中仅2例,总体功能预后优于文献预测7)。
复发原因尚未完全阐明,但推测与视网膜内休眠包囊破裂7)或外周血中循环的弓形虫有关。治疗后萎缩瘢痕病灶中仍存在耐药包囊,免疫力下降或妊娠可能诱发复发。初次发作后一年内复发风险最高。先天性感染的复发率约为5-30%。
Pidro Miokovic等人(2024)报告一例16岁女性眼弓形虫病,外视网膜出现巨大囊样改变(HORC)2)。HORC仅见于2.5%的眼弓形虫病病例,位于外界膜与RPE内界之间。治疗后2周HORC消退,视力从0.5改善至1.0。
免疫缺陷患者常表现为非典型临床特征,容易导致诊断延迟。由于传统血清学检查可能出现假阴性,PCR检测的作用变得更加重要。
Yazdanpanah等人(2021)报告了一例74岁CLL女性患者,其眼弓形虫病难以与眼内淋巴瘤鉴别3)。玻璃体液流式细胞术和细胞学检查排除了淋巴瘤,使用ITS特异性引物的PCR检测到超过500万拷贝的弓形虫DNA。也有从眼内淋巴瘤细胞中检测到弓形虫DNA的报道,提示两者可能存在关联3)。
Dillon等人(2022)报告了两例表现为广泛多灶性视网膜病变的病例5)。病例1临床诊断为急性视网膜坏死并住院治疗,但玻璃体PCR检测为弓形虫阳性。病例2为鉴别眼内淋巴瘤而行脉络膜视网膜活检,免疫组化显示大量速殖子。两例均为超过3个视盘直径的大型多灶性病变,与典型的1-2个视盘直径的单发病灶显著不同。
在美国明尼苏达州,白尾鹿的弓形虫血清阳性率达到22.5-32.2%,相邻州更高4)。有报告显示,在狩猎季节(秋季)食用未煮熟的鹿肉后,冬季出现眼部症状的模式4)。建议将鹿肉加热至内部温度64°C以上或事先低温保存以确保安全烹饪。