急性期:发病后数小时至数天

内源性细菌性眼内炎
1. 什么是内源性细菌性眼内炎?
Section titled “1. 什么是内源性细菌性眼内炎?”细菌性眼内炎是细菌侵入眼内引起的眼内炎症性疾病,根据感染途径分为外源性和内源性。外源性眼内炎发生于眼科手术、玻璃体内注射或穿孔性眼外伤后,主要致病菌为革兰阳性菌(如凝固酶阴性葡萄球菌、肠球菌)。相比之下,内源性细菌性眼内炎是其他器官的感染灶中的细菌经血行播散至视网膜和脉络膜而发病。常继发于败血症(菌血症),主要致病菌为革兰阴性杆菌。
一般来说,细菌性眼内炎比真菌性眼内炎进展更快,而由革兰阴性杆菌引起的内源性眼内炎进展尤其迅速,预后不良。葡萄膜炎诊疗指南将其归类为感染性眼内炎的一种,根据致病微生物(细菌性 vs 真菌性)和感染途径(外源性 vs 内源性)两方面进行整理1)。
流行病学与发病情况
Section titled “流行病学与发病情况”内源性细菌性眼内炎不会发生于健康人。患者总是存在某种基础疾病或危险因素,好发于老年人、糖尿病、器官脓肿(肺、肝、肾)或接受免疫抑制治疗等易感宿主。
其中,肝脓肿作为眼内炎发病风险最高的基础疾病尤为重要。过去肝脓肿的主要致病菌为大肠杆菌,但自20世纪90年代以来,在东南亚、欧美和日本,肺炎克雷伯菌已占肝脓肿致病菌的80%以上。肺炎克雷伯菌肝脓肿中**3%~8%**会并发眼内炎,需特别注意该菌引起的内源性眼内炎。此外,80%以上的病例为单眼发病。
一项针对342例病例的系统评价显示,内源性细菌性眼内炎的致病菌分布因地区而异,亚洲以革兰阴性杆菌(尤其是肺炎克雷伯菌)为主2)。
| 主要基础疾病/危险因素 | 备注 |
|---|---|
| 肝脓肿(最常见) | 肺炎克雷伯菌占80%以上,眼内炎发生率3%~8% |
| 尿路感染 | 通过革兰阴性杆菌菌血症介导 |
| 肺脓肿 | 从脓肿直接血行播散 |
| 感染性心内膜炎 | 由金黄色葡萄球菌等引起的革兰阳性菌眼内炎 |
| 脑膜炎 | 继发于严重全身感染 |
| 恶性肿瘤 | 免疫功能低下/化疗背景 |
| 糖尿病 | 高血糖导致的中性粒细胞功能障碍 |
| 类固醇/免疫抑制治疗 | 宿主防御功能全面下降 |
| 胶原病 | 疾病本身及治疗药物导致的易感染性 |
最大的区别在于感染途径和致病菌。外源性眼内炎由手术、外伤、玻璃体注射等直接侵入眼内引发,主要致病菌为革兰阳性菌(凝固酶阴性葡萄球菌、肠球菌等)。而内源性眼内炎由肝脓肿、尿路感染等其他器官的感染灶通过血流到达视网膜脉络膜引发,主要致病菌为革兰阴性杆菌(如肺炎克雷伯菌)。外源性眼内炎有明确的手术或外伤史,而内源性眼内炎则以发热等全身感染症状为先导为特征。
2. 主要症状和临床所见
Section titled “2. 主要症状和临床所见”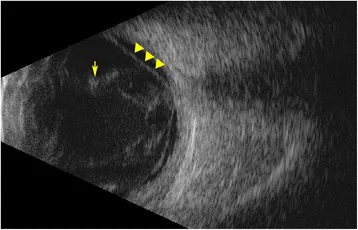
全身症状(前驱症状)
Section titled “全身症状(前驱症状)”内源性眼内炎中,眼部症状之前或同时出现全身感染征象。可见降钙素原(PCT)升高(重症细菌感染的血清标志物)、白细胞计数增加、CRP升高。若基础疾病为糖尿病,则可见高血糖和HbA1c升高。全身状态极差时,患者可能无法识别或主诉眼部症状。
- 发热、全身乏力(作为感染征象必发)
- PCT升高(重症细菌感染的血清标志物)
- 白细胞计数升高和CRP升高(急性炎症标志物)
- 高血糖和HbA1c升高(见于合并糖尿病的患者)
眼部自觉症状
Section titled “眼部自觉症状”早期自觉症状包括飞蚊症、视物模糊和视力下降。急性期除视力下降和畏光外,还会感到眼痛。视力迅速恶化,有时可降至手动或光感水平。
进展期:炎症波及全眼球
玻璃体脓肿形成:一旦形成,常导致全眼球炎,预后极差。
视网膜和视神经损伤:视网膜血管闭塞、视网膜坏死和视神经萎缩导致不可逆的视力丧失1)。
波及眼周组织:炎症可蔓延至眼眶组织,引起眼球突出和眼球运动受限。
紧急手术的必要性:进展为全眼球炎的病例需要紧急手术干预。
3. 原因和风险因素
Section titled “3. 原因和风险因素”内源性细菌性眼内炎的主要致病菌是革兰阴性杆菌。
- 肺炎克雷伯菌:在肝脓肿引起的内源性眼内炎中最为重要。自20世纪90年代以来,在亚洲(包括东南亚和日本)的发病率显著增加,占肝脓肿致病菌的80%以上。由该菌引起的肝脓肿中,3%~8%并发眼内炎。
- 大肠杆菌:以前是肝脓肿和尿路感染的主要致病菌,仍然很重要。
- 铜绿假单胞菌:在免疫功能低下宿主中引起严重感染。
也有报道由金黄色葡萄球菌引起的转移性眼内炎,继发于革兰阳性菌引起的全身感染,如感染性心内膜炎 1)。
在亚洲地区,肺炎克雷伯菌肝脓肿相关眼内炎的发生率高于欧美国家 3)。在东亚的临床实践中,需要考虑到该菌引起的内源性眼内炎。
增加风险的基础疾病
Section titled “增加风险的基础疾病”内源性眼内炎的发生,除了原发感染灶(如肝脓肿、尿路感染)外,几乎总是伴有宿主方面的易感因素。
- 糖尿病:高血糖导致中性粒细胞功能障碍和免疫功能下降,促进感染。
- 恶性肿瘤:肿瘤本身引起的免疫抑制,以及化疗或放疗后的骨髓抑制。
- 胶原病: 疾病活动性和免疫抑制药物两方面均增加易感性
- 长期使用类固醇/免疫抑制治疗: T细胞功能下降和中性粒细胞功能障碍
- 高龄: 随年龄增长免疫功能全面下降(尤其是体液免疫和细胞免疫)
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”诊断基本方针
Section titled “诊断基本方针”当怀疑内源性眼内炎时,原则是不等检查结果,优先治疗。由于急性感染可在数小时内迅速恶化,一旦根据问诊和临床症状怀疑眼内炎,应同时开始眼内液采集和抗菌药物给药。
确诊最重要的检查是眼内液(房水、玻璃体液)的涂片和培养检查。
- 涂片检查(革兰染色等): 有助于早期诊断。可快速了解致病菌类型(革兰阳性或阴性)
- 培养检查: 必须用于鉴定致病菌和确认药敏。玻璃体液比房水检出致病菌的阳性率更高
- PCR法(基因检测): 即使在培养阴性病例中也能检测到致病菌DNA,近年来应用日益普及
全身及辅助检查
Section titled “全身及辅助检查”| 检查 | 目的 |
|---|---|
| B超检查 | 玻璃体混浊导致眼底无法窥见时必须进行。确认玻璃体脓肿的有无及程度 |
| 血培养 | 确认内源性眼内炎和鉴定致病菌所必需1) |
| 血清β-D-葡聚糖 | 有助于鉴别真菌性眼内炎1) |
| 白细胞计数、CRP、PCT | 监测全身感染的严重程度 |
| 血糖、HbA1c | 评估基础疾病(糖尿病) |
| 胸腹部CT | 寻找原发感染灶(如肝脓肿、肺脓肿等) |
| 心脏超声 | 排除感染性心内膜炎 |
内源性眼内炎需与以下疾病进行鉴别。
-
与急性前葡萄膜炎的鉴别:虽然可伴有前房积脓和纤维素,但有以下不同点。
- 老年人急性前葡萄膜炎罕见
- 急性前葡萄膜炎很少引起眼睑肿胀或结膜水肿
- 急性前葡萄膜炎时视力不会降至手动或光感
- 急性前葡萄膜炎时至少可见视盘(内源性眼内炎时玻璃体混浊无法看到)
- 内源性眼内炎先有发热等全身感染症状
-
外源性眼内炎:根据明确的眼科手术、外伤或玻璃体注射史进行鉴别1)
-
真菌性眼内炎:进展相对缓慢(数天至数周),细菌性为数小时至数天。β-D-葡聚糖阳性、视网膜白色渗出病灶(真菌球)为特征1)
-
迟发性(慢性)细菌性眼内炎:由痤疮丙酸杆菌引起,白内障术后1个月或更晚发病。特征为慢性虹膜睫状体炎和复发性前房积脓1)
前房积脓是眼内炎的特征性表现,但也可见于急性前葡萄膜炎(HLA-B27相关、白塞病等)、感染性角膜炎蔓延和糖尿病虹膜炎。鉴别要点包括:①手术或外伤史(与外源性眼内炎鉴别),②发热等全身感染症状(与内源性眼内炎鉴别),③眼睑肿胀和结膜水肿程度,④玻璃体混浊深度和眼底可见性,⑤视力下降速度。眼内炎时伴有全身症状,玻璃体混浊严重,视力下降迅速。若怀疑,应在等待检查结果前开始治疗1)。
5. 标准治疗方法
Section titled “5. 标准治疗方法”治疗基本原则
Section titled “治疗基本原则”一旦怀疑眼内炎,应立即开始抗生素三途径同时给药,无需等待病原菌鉴定。三途径包括:①玻璃体内注射,②频繁滴用抗生素眼药水,③全身给药(静脉滴注)。需与内科(消化科、感染科)协作,同时治疗原发感染灶(如肝脓肿)1)。
药物治疗方案(病原菌不明时)
Section titled “药物治疗方案(病原菌不明时)”| 给药途径 | 药物(商品名) | 用法用量 | 备注 |
|---|---|---|---|
| 玻璃体内注射① | 盐酸万古霉素注射液 | 1 mg/0.1 mL 玻璃体内注射 | 医保外用药 |
| 玻璃体内注射② | 头孢他啶(Modacin®)注射液 | 2 mg/0.1 mL 玻璃体内注射 | 医保外用药。与①同时或紧接其后进行。 |
| 滴眼液① | 左氧氟沙星滴眼液(Cravit®)1.5% | 每日6次滴眼 | 作为频繁滴眼继续使用 |
| 滴眼液② | 头孢甲肟滴眼液(Bestron®)0.5% | 每日6次滴眼 | 与①交替使用 |
| 滴眼③ | 倍他米松滴眼液(Rinderon®)0.1% | 每日6次滴眼 | 用于抑制炎症的联合用药 |
| 全身给药① | 亚胺培南/西司他丁(Tienam®)注射液 | 每次1g,每日2次,静脉滴注,共5天 | 广谱碳青霉烯类 |
| 全身给药② | 左氧氟沙星(Cravit®)片 500mg | 每次1片,每日1次,口服,共5天 | 与全身给药①联合使用 |
全身给药也可选择第四代头孢菌素类如头孢唑兰(Firstcin®)等广谱抗菌药物。药敏结果明确后,应更换为特异性更高的抗菌药物继续治疗。若确认革兰阴性杆菌(如肺炎克雷伯菌),则根据药敏模式从碳青霉烯类、氟喹诺酮类、第三至四代头孢菌素中选择最佳药物。
怀疑眼内炎时(临床判断),并行实施以下措施。
- 采集眼内液(前房水、玻璃体液)→ 涂片、培养、PCR
- 不等检查结果,立即开始三途径同时给药:(1)玻璃体内注射,(2)频繁滴眼,(3)全身给药
- 与内科协作并行实施全身检查和原发感染灶治疗(如肝脓肿引流)
- 药敏结果明确后,更换为特异性更高的抗菌药物
- 药物治疗无效或进展的病例,立即转为玻璃体手术
对药物治疗无反应的病例,在全身状况允许的情况下,应尽早实施玻璃体手术。玻璃体手术可物理清除作为感染介质的玻璃体,并将抗菌药物直接送达眼内。葡萄膜炎诊疗指南推荐,在进展迅速、玻璃体混浊导致眼底无法窥见或存在视网膜下脓肿时,应早期在抗菌药物灌注下进行玻璃体手术1)。
- 适应证:药物治疗无效、眼底无法窥见、视网膜下脓肿形成
- 术式:玻璃体手术。必要时联合晶状体切除术、眼内透镜/晶状体囊摘除
- 灌注液:使用混合抗菌药物(如万古霉素)的灌注液
- 限制:全身状况不佳(如败血症管理中)时常无法进行手术,这是一个挑战
在致病菌不明时,通过三途径同时给予广谱抗菌药物。药敏结果明确后,更换为更特异的药物可提高疗效。但革兰阴性杆菌(如肺炎克雷伯菌)引起的眼内炎进展极快(以小时计),仅用抗菌滴眼液眼内移行不足,必须联合玻璃体内注射和全身给药。若药物治疗后眼底无法窥见的情况未改善或进展,应迅速考虑转为玻璃体手术1)。
6. 病理生理学及详细发病机制
Section titled “6. 病理生理学及详细发病机制”血行播散的机制
Section titled “血行播散的机制”内源性细菌性眼内炎是由于其他器官的感染灶(如肝脓肿、尿路感染等)中的细菌进入血流,经血行播散至视网膜脉络膜而发病。细菌在脉络膜毛细血管床定植后,局部炎症反应迅速进展,从视网膜脉络膜炎波及到玻璃体炎。
多发生于患有恶性肿瘤、糖尿病、胶原病、使用免疫抑制剂等基础疾病的易感宿主。这些宿主血液中细菌清除能力下降,容易发生眼内感染。
革兰阴性杆菌内毒素引起的组织损伤
Section titled “革兰阴性杆菌内毒素引起的组织损伤”当致病菌为革兰阴性杆菌(如肺炎克雷伯菌、大肠杆菌、铜绿假单胞菌等)时,病情进展尤其迅速。革兰阴性杆菌的内毒素(脂多糖,LPS)在眼内组织中引发强烈的炎症反应,并放大炎症级联反应,这是快速恶化的主要原因。由于这一机制,与外源性眼内炎(主要由革兰阳性菌引起)相比,预后往往更差。
病变进展顺序
Section titled “病变进展顺序”- 原发感染灶引起菌血症
- 细菌在脉络膜毛细血管定植 → 形成脉络膜炎和视网膜脉络膜炎
- 炎症波及视网膜和玻璃体腔 → 快速玻璃体混浊和玻璃体炎
- 进展病例:形成玻璃体脓肿 → 波及巩膜和眼眶组织(全眼球炎)
视力预后不良的因素包括视网膜血管闭塞、视网膜坏死和视神经萎缩 1)。如果治疗延迟,许多病例最终会失去光感,治疗开始的速度直接关系到预后。
7. 预后与长期管理
Section titled “7. 预后与长期管理”内源性细菌性眼内炎的视力预后通常较差。当致病菌为革兰阴性杆菌时,进展尤其迅速,预后更差;治疗开始的延迟直接影响视力结果。即使治疗后,也常遗留视神经萎缩、视网膜坏死和视网膜血管白线化等后遗症,许多病例视力预后不良 1)。治愈后也可能合并脉络膜新生血管和黄斑病变 1)。
一项针对342例患者的系统评价显示,大多数患者最终视力为20/200(0.1)或更差,只有少数患者能够维持适当的视力2)。关于肺炎克雷伯菌肝脓肿相关性眼内炎的预后因素研究报道,初诊时的视力和玻璃体混浊程度是最终视力的主要预测因素3)。
在形成玻璃体脓肿或发展为全眼球炎的病例中,有时不得不进行眼球摘除。
基础疾病的长期管理
Section titled “基础疾病的长期管理”从长远来看,基础疾病(肝脓肿、糖尿病、恶性肿瘤等)的适当管理对于预防复发和改善生命预后都至关重要。通过内科和感染科的多学科协作,持续治疗原发感染灶,对眼科预后也有积极影响。从眼科角度而言,术后定期进行眼底检查和OCT检查以随访视网膜和黄斑部非常重要。
患者和医疗团队需要共同认识到,通过多学科协作(眼科、内科、感染科)进行早期诊断和原发感染灶的同步治疗,对于改善视力和生命预后最为重要4)5)。
8. 参考文献
Section titled “8. 参考文献”- 日本眼炎症学会/日本眼科学会. ぶどう膜炎診療ガイドライン. 日眼会誌. 2019;123(6):635-696(「14. 眼内炎」節).
- Jackson TL, Paraskevopoulos T, Georgalas I. Systematic review of 342 cases of endogenous bacterial endophthalmitis. Surv Ophthalmol. 2014;59(6):627-635.
- Ang M, Jap A, Chee SP. Prognostic factors and outcomes in endogenous Klebsiella pneumoniae endophthalmitis. Am J Ophthalmol. 2011;151(2):338-344.
- Durand ML. Bacterial and fungal endophthalmitis. Clin Microbiol Rev. 2017;30(3):597-613.
- Sadiq MA, Hassan M, Agarwal A, et al. Endogenous endophthalmitis: diagnosis, management, and prognosis. J Ophthalmic Inflamm Infect. 2015;5:32.
