急性期:初発から数時間〜数日

内因性細菌性眼内炎(Endogenous Bacterial Endophthalmitis)
1. 内因性細菌性眼内炎とは
Section titled “1. 内因性細菌性眼内炎とは”細菌性眼内炎(bacterial endophthalmitis)は細菌が眼内に侵入して生じる眼内炎症性疾患であり、感染経路により外因性と内因性に大別される。外因性は眼科手術・硝子体注射・穿孔性眼外傷を契機として発症し、グラム陽性菌(コアグラーゼ陰性ブドウ球菌・腸球菌など)が主な起炎菌である。これに対し内因性細菌性眼内炎(endogenous bacterial endophthalmitis)は、他臓器の感染巣から細菌が血行性に網脈絡膜へ播種されることで発症する。敗血症(菌血症)を契機とすることが多く、グラム陰性桿菌が主たる起炎菌となる。
一般に細菌性眼内炎は真菌性眼内炎に比べて進行が速く、起炎菌がグラム陰性桿菌である内因性では特に進行速度が速く予後が不良である。ぶどう膜炎診療ガイドラインでは感染性眼内炎のひとつとして位置づけられており、原因微生物による分類(細菌性・真菌性)と感染経路による分類(外因性・内因性)の両面から整理されている1)。
疫学と発生状況
Section titled “疫学と発生状況”内因性細菌性眼内炎は健常者には発症しない。患者は常に何らかの基礎疾患やリスクファクターを有しており、高齢・糖尿病・臓器膿瘍(肺・肝・腎)・免疫抑制療法中などの易感染性宿主に発症する。
なかでも肝膿瘍は眼内炎発症リスクが最も高い基礎疾患として重要である。かつて肝膿瘍の起炎菌は Escherichia coli が主であったが、1990年代以降は東南アジア・欧米・日本において Klebsiella pneumoniae(肺炎桿菌)が肝膿瘍原因菌の80%以上を占めるようになった。Klebsiella pneumoniae による肝膿瘍では**3〜8%**が眼内炎を合併するとされ、本菌による内因性眼内炎に特に注意が必要である。また、80%以上の症例が片眼性に発症する。
342症例を対象としたシステマティックレビューでは、内因性細菌性眼内炎の起炎菌分布がアジア地域と欧米で異なることが示されており、アジアではグラム陰性桿菌(特に Klebsiella pneumoniae)が優勢であった2)。
| 主な基礎疾患・リスク因子 | 備考 |
|---|---|
| 肝膿瘍(最多) | Klebsiella pneumoniae が80%以上、眼内炎発症率3〜8% |
| 尿路感染症 | グラム陰性桿菌による菌血症を介する |
| 肺膿瘍 | 膿瘍から直接血行播種 |
| 感染性心内膜炎 | Staphylococcus aureus 等によるグラム陽性菌性眼内炎 |
| 髄膜炎 | 重篤な全身感染症に続発 |
| 悪性腫瘍 | 免疫機能低下・化学療法が背景 |
| 糖尿病 | 高血糖による好中球機能障害 |
| ステロイド・免疫抑制療法 | 宿主防御機能の全般的低下 |
| 膠原病 | 疾患自体および治療薬による易感染性 |
最大の違いは感染経路と起炎菌である。外因性は手術・外傷・硝子体注射などの眼への直接的侵入を契機として発症し、グラム陽性菌(コアグラーゼ陰性ブドウ球菌・腸球菌など)が主な起炎菌となる。一方、内因性は肝膿瘍・尿路感染などの他臓器感染巣から細菌が血流を介して網脈絡膜に到達して発症し、グラム陰性桿菌(Klebsiella pneumoniae 等)が主起炎菌となる。外因性では手術・外傷の明確な既往があるが、内因性では発熱などの全身感染症状が先行する点が特徴的である。
2. 主な症状と臨床所見
Section titled “2. 主な症状と臨床所見”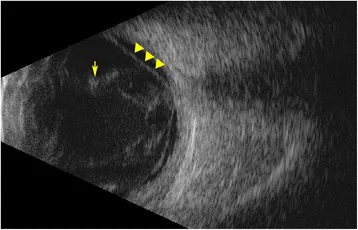
全身症状(先行症状)
Section titled “全身症状(先行症状)”内因性眼内炎では、眼症状に先行または並行して全身の感染徴候が認められる。重症細菌感染症の血清マーカーであるプロカルシトニン(PCT)の上昇、白血球数増加、CRP高値を認める。基礎疾患として糖尿病を有する場合には高血糖・HbA1c高値がみられる。全身状態が著しく不良な場合、患者が眼症状を認識・訴えられないことがある。
- 発熱・全身倦怠感(感染徴候として必発)
- PCT上昇(重症細菌感染症の血清マーカー)
- 白血球数増加・CRP高値(急性炎症マーカー)
- 高血糖・HbA1c高値(糖尿病合併例で認められる)
眼の自覚症状
Section titled “眼の自覚症状”初期の自覚症状は飛蚊症・霧視・視力低下である。急性期には視力低下・羞明に加え眼痛を自覚する。視力は急速に悪化し、手動弁・光覚弁レベルまで低下することもある。
進行期:炎症が全眼球へ波及
3. 原因とリスク要因
Section titled “3. 原因とリスク要因”内因性細菌性眼内炎の主たる起炎菌はグラム陰性桿菌である。
- Klebsiella pneumoniae(肺炎桿菌): 肝膿瘍を原因とする内因性眼内炎で最重要。1990年代以降アジア(東南アジア・日本含む)での増加が著しく、肝膿瘍原因菌の80%以上を占める。本菌による肝膿瘍では3〜8%が眼内炎を合併する
- Escherichia coli(大腸菌): 以前は肝膿瘍・尿路感染の主な原因菌であり、依然として重要
- Pseudomonas aeruginosa(緑膿菌): 易感染性宿主における重篤な感染症を起こす
Staphylococcus aureus(黄色ブドウ球菌)による転移性眼内炎も報告されており、感染性心内膜炎など、グラム陽性菌による全身感染に続発する場合がある1)。
アジア地域では Klebsiella pneumoniae 肝膿瘍関連眼内炎の発生率が欧米より高いことが知られており3)、東アジアの臨床現場では本菌による内因性眼内炎を念頭に置いた診療が求められる。
リスクとなる基礎疾患
Section titled “リスクとなる基礎疾患”内因性眼内炎が発症するには、原発感染巣(肝膿瘍・尿路感染など)に加え、宿主側の易感染性要因が重なることがほとんどである。
- 糖尿病: 高血糖による好中球機能障害・免疫機能低下が感染を助長
- 悪性腫瘍: 腫瘍自体による免疫抑制、化学療法・放射線療法後の骨髄抑制
- 膠原病: 疾患活動性および免疫抑制薬の両面から易感染性が増大
- ステロイド長期使用・免疫抑制療法: T細胞機能低下・好中球機能障害
- 高齢: 加齢に伴う免疫機能全般の低下(特に液性免疫・細胞性免疫)
4. 診断と検査方法
Section titled “4. 診断と検査方法”診断の基本方針
Section titled “診断の基本方針”内因性眼内炎が疑われた場合、検査結果を待たず治療を優先することが原則である。急性感染では数時間単位で急速に増悪するため、問診と臨床症状から眼内炎が疑われた段階で、眼内液採取と抗菌薬投与を並行して開始する。
確定診断のための最重要検査は眼内液(前房水・硝子体液)の塗抹・培養検査である。
- 塗抹検査(グラム染色等): 早期診断に有用。起炎菌の種類(グラム陽性・陰性)を迅速に把握できる
- 培養検査: 起炎菌の同定と薬剤感受性の確認に必須。硝子体液のほうが前房水より起炎菌の検出率が高い
- PCR法(遺伝子検索): 培養陰性例でも起炎菌 DNA の検出が可能であり、近年普及が進んでいる
全身・補助検査
Section titled “全身・補助検査”| 検査 | 目的 |
|---|---|
| 超音波Bモード検査 | 硝子体混濁で眼底透見不能時に必須。硝子体膿瘍の有無・程度を確認する |
| 血液培養 | 内因性眼内炎の確認と起炎菌同定に必須1) |
| 血清β-Dグルカン | 真菌性眼内炎との鑑別に有用1) |
| 白血球数・CRP・PCT | 全身感染の重症度モニタリング |
| 血糖・HbA1c | 基礎疾患(糖尿病)の評価 |
| 胸腹部CT | 原発感染巣(肝膿瘍・肺膿瘍等)の検索 |
| 心臓超音波 | 感染性心内膜炎の除外 |
内因性眼内炎は以下の疾患との鑑別が重要である。
-
急性前部ぶどう膜炎との鑑別: 前房蓄膿・フィブリンを伴い類似するが、以下の点が異なる
-
真菌性眼内炎: 進行が日〜週単位と比較的緩徐(細菌性は時間〜日単位)。β-Dグルカン陽性、網膜白色滲出病巣(fungus ball)が特徴的1)
-
遅発性(慢性)細菌性眼内炎: Cutibacterium acnes(アクネ菌)による白内障術後1か月以降の発症。慢性虹彩毛様体炎・再発性前房蓄膿が特徴的1)
5. 標準的な治療法
Section titled “5. 標準的な治療法”治療の基本原則
Section titled “治療の基本原則”眼内炎が疑われた時点で、起炎菌同定を待たずに抗菌薬の三経路同時投与を即座に開始する。三経路とは①硝子体内注射、②抗菌薬頻回点眼、③全身投与(点滴静注)の組み合わせである。内科(消化器科・感染症科)と連携して原発感染巣(肝膿瘍等)の治療を並行して行うことが不可欠である1)。
薬物療法プロトコル(起炎菌不明時)
Section titled “薬物療法プロトコル(起炎菌不明時)”| 投与経路 | 薬剤(商品名) | 用法・用量 | 備考 |
|---|---|---|---|
| 硝子体内注射① | 塩酸バンコマイシン注 | 1 mg/0.1 mL 硝子体内注射 | 保険適用外 |
| 硝子体内注射② | セフタジジム(モダシン®)注 | 2 mg/0.1 mL 硝子体内注射 | 保険適用外。①と同時または直後に施行 |
| 点眼① | レボフロキサシン点眼液(クラビット®)1.5% | 1日6回 点眼 | 頻回点眼として継続 |
| 点眼② | セフメノキシム点眼液(ベストロン®)0.5% | 1日6回 点眼 | ①と交互に使用 |
| 点眼③ | ベタメタゾン点眼液(リンデロン®)0.1% | 1日6回 点眼 | 炎症抑制目的で併用 |
| 全身投与① | イミペネム/シラスタチン(チエナム®)注 | 1回1 g 1日2回 点滴静注 5日間 | 広域カルバペネム系 |
| 全身投与② | レボフロキサシン(クラビット®)錠 500 mg | 1錠 分1 5日間 経口 | 全身投与①と併用 |
全身投与として、第4世代セフェム系であるセフォゾプラン(ファーストシン®)など広域スペクトルを有する抗菌薬を選択することもある。薬剤感受性が判明した後は、より特異性の高い抗菌薬に変更して治療を継続する。グラム陰性桿菌(Klebsiella pneumoniae 等)が確認された場合は、感受性パターンに応じてカルバペネム系・フルオロキノロン系・第3〜4世代セフェム系の中から最適な薬剤を選択する。
眼内炎を疑った時点(臨床判断)で以下を並行して実施する。
- 眼内液採取(前房水・硝子体液)→ 塗抹・培養・PCR
- 検査結果を待たず三経路同時投与を開始(①硝子体内注射 + ②頻回点眼 + ③全身投与)
- 全身精査・原発感染巣の治療を内科と連携して並行実施(肝膿瘍ドレナージ等)
- 薬剤感受性判明後に特異性の高い抗菌薬へ変更
- 薬物療法不応・進行例では早急な硝子体手術へ移行
薬物療法に反応しない例では、全身状態が許す限り早急に硝子体手術を施行することが望ましい。硝子体手術は感染媒体となる硝子体を物理的に除去し、眼内に抗菌薬を直接届ける効果がある。ぶどう膜炎診療ガイドラインでは、進行が速く硝子体混濁で眼底透見不能または網膜下膿瘍がある場合は早期の抗菌薬灌流下での硝子体手術が推奨されている1)。
- 適応: 薬物療法不応例、眼底透見不能例、網膜下膿瘍形成例
- 術式: 硝子体手術。必要に応じて水晶体切除術・眼内レンズ/水晶体囊摘出を併用
- 灌流液: 抗菌薬(バンコマイシン等)を混合した灌流液を使用
- 制限: 全身状態不良(敗血症の管理中)で手術を行えないことが多い点が課題である
6. 病態生理学・詳細な発症機序
Section titled “6. 病態生理学・詳細な発症機序”血行性播種のメカニズム
Section titled “血行性播種のメカニズム”内因性細菌性眼内炎は、他臓器の感染巣(肝膿瘍・尿路感染症等)から細菌が血流に乗り、血行性に網脈絡膜へ播種されることで発症する。細菌が脈絡膜の毛細血管床に定着すると、局所での炎症反応が急速に進行し、網脈絡膜炎から硝子体炎へと波及する。
多くは悪性腫瘍・糖尿病・膠原病・免疫抑制薬使用などの基礎疾患を有した易感染性宿主に発症する。これらの宿主では細菌の血中クリアランスが低下し、眼内での感染成立が起こりやすい。
グラム陰性桿菌のエンドトキシンによる組織障害
Section titled “グラム陰性桿菌のエンドトキシンによる組織障害”起炎菌がグラム陰性桿菌(Klebsiella pneumoniae、Escherichia coli、Pseudomonas aeruginosa など)の場合、進行が特に速い。グラム陰性桿菌のエンドトキシン(リポ多糖:LPS)が眼内組織に対して強力な炎症反応を惹起し、炎症カスケードを増幅させることが急速な悪化の主要因である。この機序により、外因性眼内炎(グラム陽性菌主体)と比較しても予後が不良となりやすい。
病変の進展順序
Section titled “病変の進展順序”- 原発感染巣からの菌血症(bacteremia)の成立
- 脈絡膜毛細血管への細菌定着 → 脈絡膜炎・網脈絡膜炎の形成
- 網膜・硝子体腔への炎症波及 → 急速な硝子体混濁・硝子体炎
- 進行例:硝子体膿瘍形成 → 強膜・眼窩組織へ波及(全眼球炎)
視力予後不良の要因として、網膜血管閉塞・網膜壊死・視神経萎縮の合併が挙げられる1)。治療が遅れると最終的に光覚なしとなる例も少なくなく、治療開始の速度が予後に直結する。
7. 予後と長期管理
Section titled “7. 予後と長期管理”内因性細菌性眼内炎の視力予後は一般に不良である。起炎菌がグラム陰性桿菌の場合は特に進行が速く予後が不良であり、治療開始の遅れが視力転帰に直結する。治療後も視神経萎縮・網膜壊死・網膜血管白線化などの後遺症が残り、視力予後不良例が多い1)。治癒後に脈絡膜新生血管・黄斑症を合併することもある1)。
342症例を対象としたシステマティックレビューでは、最終視力が20/200(0.1)以下となる例が多数を占め、適切な視力が維持できる例は限られることが示されている2)。Klebsiella pneumoniae 肝膿瘍関連眼内炎の予後因子に関する研究では、初診時視力・初診時硝子体混濁の程度が最終視力の主要予測因子であることが報告されている3)。
硝子体膿瘍を形成した例や全眼球炎に至った例では、眼球摘出を余儀なくされることもある。
基礎疾患の長期管理
Section titled “基礎疾患の長期管理”長期的には基礎疾患(肝膿瘍・糖尿病・悪性腫瘍等)の適切な管理が再発予防と生命予後の両面から不可欠である。内科・感染症科との多科連携による原発感染巣の治療継続が、眼科的予後にも好影響をもたらす。眼科的には術後の定期的な眼底検査・OCT検査による網膜・黄斑部のフォローアップが重要となる。
早急な診断・多科連携(眼科・内科・感染症科)による原発感染巣の同時治療が、視力予後と生命予後の双方の改善に最も重要である点を、患者・医療チームで共有することが求められる4)5)。
8. 参考文献
Section titled “8. 参考文献”- 日本眼炎症学会/日本眼科学会. ぶどう膜炎診療ガイドライン. 日眼会誌. 2019;123(6):635-696(「14. 眼内炎」節).
- Jackson TL, Paraskevopoulos T, Georgalas I. Systematic review of 342 cases of endogenous bacterial endophthalmitis. Surv Ophthalmol. 2014;59(6):627-635.
- Ang M, Jap A, Chee SP. Prognostic factors and outcomes in endogenous Klebsiella pneumoniae endophthalmitis. Am J Ophthalmol. 2011;151(2):338-344.
- Durand ML. Bacterial and fungal endophthalmitis. Clin Microbiol Rev. 2017;30(3):597-613.
- Sadiq MA, Hassan M, Agarwal A, et al. Endogenous endophthalmitis: diagnosis, management, and prognosis. J Ophthalmic Inflamm Infect. 2015;5:32.
