初期:後極部の白色病巣
小円形白色病巣:後極部に単発または多発。境界は比較的明瞭。
小出血斑:病巣周囲に点状出血を伴うことがある。
OCT所見:色素上皮を穿破した隆起像が特徴的。
症状:飛蚊症・軽度の霧視・軽度視力低下が主体。比較的緩徐に進行。

真菌性眼内炎(fungal endophthalmitis)は、各種真菌が眼内に移行し眼内炎を生じて視力障害をきたす疾患である。眼以外の感染巣から血行性に転移する内因性(血行性眼内炎)と、手術や外傷を契機に発症する外因性に分類される。大半は内因性であり、外因性はまれである。感染性ぶどう膜炎の一部を占める1)。
主な起炎菌はカンジダ属(大半)、アスペルギルス属、フザリウム属である。カンジダ血症患者では眼内病変が報告されるが、定義やスクリーニング方法により頻度は大きく異なる。細菌性眼内炎とは異なり、眼底に明瞭な焦点病変を形成しながら比較的緩徐に進行するため、診断が遅れやすい点が特徴である。内因性真菌性眼内炎では両眼性に発症することがある6)。
長期化すると広範な網膜壊死性変化を生じ、治療後の視力予後は不良となる。牽引性網膜剥離を来した場合には手術が必要となるが、視力予後は不良例が多い。早期発見・早期治療が視力予後の鍵である。
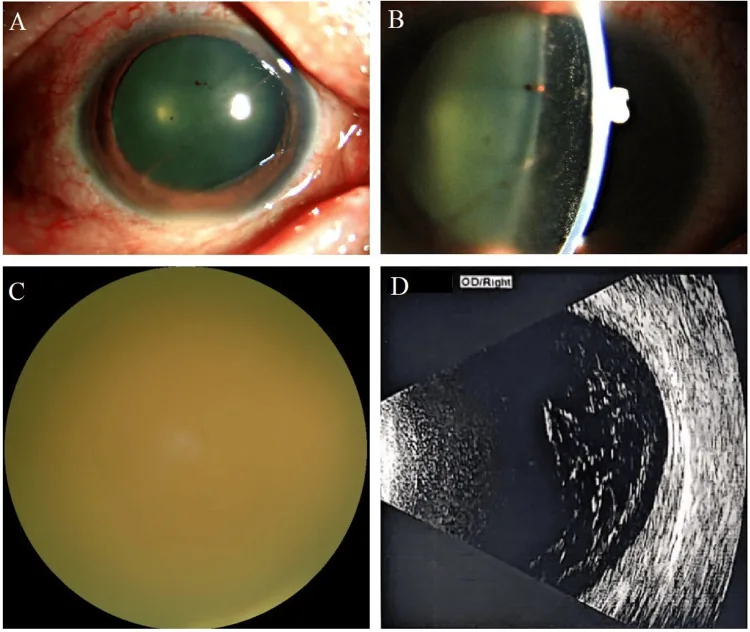
真菌血症(fungemia)に引き続いて真菌性眼内炎が発症するため、発熱は必発である。眼症状の初期には飛蚊症・霧視・軽度の視力低下が出現し、他覚的には微塵状硝子体混濁としてとらえられる。進行に伴い、羞明・眼痛・高度視力低下へ移行する。内因性の30%は両眼性であり、無症状の反対眼にも病変が潜在する場合がある。
初期:後極部の白色病巣
小円形白色病巣:後極部に単発または多発。境界は比較的明瞭。
小出血斑:病巣周囲に点状出血を伴うことがある。
OCT所見:色素上皮を穿破した隆起像が特徴的。
症状:飛蚊症・軽度の霧視・軽度視力低下が主体。比較的緩徐に進行。
中期:硝子体混濁(fungus ball)
多発性病巣:白色病巣が増大・多発する。
羽毛状硝子体混濁(fungus ball):硝子体内に真菌塊が形成される特徴的所見。
進行:視力低下・霧視の増悪。
前房炎症:フィブリン・炎症細胞の集積が出現。
後期:びまん性混濁・増殖
濃いびまん性硝子体混濁:眼底が透見困難となる。
滲出性肉芽腫:脈絡膜・網膜に形成され硝子体内へ突出。
増殖膜→牽引性網膜剥離:視機能の回復が困難になる。
前眼部合併症:前房フィブリン・虹彩後癒着・虹彩ルベオシス→続発緑内障。
急速に進行する細菌性眼内炎(時間〜日単位)とは異なり、真菌性眼内炎は眼底に明瞭な焦点病変を形成しながら週〜月単位で緩徐に進行する。IVH使用歴・発熱・免疫抑制状態などの全身的背景も鑑別に重要である。
| カテゴリ | リスク因子 |
|---|---|
| 医原性(最重要) | IVH(中心静脈栄養)・腹部大手術・尿管カテーテル・免疫抑制薬・抗腫瘍薬・長期ステロイド・放射線療法後 |
| 基礎疾患 | 悪性腫瘍末期・骨髄/臓器移植・血液悪性腫瘍(白血病・悪性リンパ腫)・AIDS・重症感染症・糖尿病・膠原病・心疾患 |
| その他 | 外傷・低栄養・高齢 |
| 外因性(まれ) | 眼内手術後・眼外傷後 |
IVH(中心静脈栄養)は最も重要なリスク因子である。皮膚常在酵母菌が中心静脈カテーテルを介して全身感染し、カンジダ血症を来す。カンジダ血症患者では眼内病変が報告されており、IDSA 2016ガイドラインでは早期の眼科的評価が推奨されている2,3)。
カンジダ血症の治療開始後早期に眼科的評価を行うことが、IDSA 2016ガイドラインで推奨されている2)。
カンジダ血症患者では無症状でも眼内病変がみつかることがあり、IDSA 2016ガイドラインでは治療開始後早期の眼科的評価が推奨されています2)。一方で、スクリーニング対象や眼内炎の定義をめぐっては議論もあり、全身状態と眼症状を踏まえて内科・眼科で判断します6)。
「3徴候(飛蚊症+IVH既往+発熱)」に加え、特徴的な眼底所見(後極部小円形白色病巣・fungus ball・びまん性硝子体混濁)の確認が重要である。細菌性眼内炎と異なり比較的緩徐に進行する点が鑑別の一助となる。IVH終了後しばらく経ってから発症することも多い。
| 検査法 | 検体 | 特徴 |
|---|---|---|
| 真菌培養 | 動脈血・カテーテル先端・硝子体液 | 起炎菌同定・薬剤感受性試験に必須。確定診断となるが結果判明まで時間を要する |
| β-D-グルカン | 血清 | 深在性真菌症の感度の高いスクリーニング指標。培養陰性例でも検出可能 |
| カンジダ抗原(CAND-TEC) | 血清 | カンジダ特異的 |
| アスペルギルス抗原(GM試験) | 血清・BAL | アスペルギルス特異的。好中球減少者で有用 |
| PAS染色 | 硝子体・前房水・組織 | 真菌細胞壁多糖を染色 |
| Grocott染色 | 硝子体・前房水・組織 | 真菌菌糸の確認に優れる |
| ファンギローラY®染色 | 組織 | 蛍光染色法 |
| PCR(真菌) | 前房水・硝子体液 | 感度・特異度が高く微量検体でも有用。起因菌の同定に試みられている |
特にIVHが感染源となる場合、早急にカテーテルを抜去する。感染源が残存している限り、抗真菌薬の効果が十分に得られない。
内科的治療(全身投与)から開始し、治療反応を観察しながら方針を決定する。治療開始後1〜2週間で網膜浸潤巣は徐々に縮小し始め、内服へ切り替えた後も病巣が完全に瘢痕化するまで継続する。通常3週〜3か月の投薬が必要である。
カンジダ眼内炎(第一選択):
アスペルギルス眼内炎:
| 系統 | 一般名(商品名) | 用法・用量 | 主な副作用 |
|---|---|---|---|
| ポリエン系 | アムホテリシンB(ファンギゾン®) | 点滴 0.75 mg/kg/日。硝子体内 5 µg/0.1 mL(保険適用外) | 肝腎障害・貧血・骨髄抑制 |
| トリアゾール系 | フルコナゾール(ジフルカン®) | 200〜400 mg/日 静注または内服。腎機能障害では減量 | 肝機能障害(肝酵素上昇) |
| トリアゾール系 | イトラコナゾール(イトリゾール®) | 100〜200 mg/日 内服。カンジダ属全体・アスペルギルスにスペクトル | 肝機能障害 |
| トリアゾール系 | ボリコナゾール(ブイフェンド®) | 静注→内服切り替え。糸状菌(フザリウム・アスペルギルス等)に有効 | 肝機能障害・視覚障害(可逆性、添付文書記載) |
| キャンディン系 | ミカファンギン(ファンガード®) | 点滴 50〜150 mg/日(1日1回)。アスペルギルス症に有効 | 肝機能障害・急性腎不全 |
全身治療に反応不良な例、または眼内増殖性変化がすでに進行している場合、他科と相談のうえ可能であれば硝子体手術を行う。硝子体混濁が進行する場合、早期診断のうえで積極的な硝子体手術が望ましい。
眼内炎の重症度・起炎菌の種類・治療反応性によって異なるが、全身治療開始後1〜2週間で網膜浸潤巣は徐々に縮小し始める。内服への切り替え後も病巣が完全に瘢痕化するまで継続し、通常3週〜3か月の投薬が必要である。硝子体手術を要した症例では術後も抗真菌薬の継続投与が必要となる。
皮膚・消化管に常在するカンジダ属(特にCandida albicans)は、IVH使用・長期抗菌薬使用・免疫抑制状態などにより腸管粘膜バリアを突破または中心静脈カテーテルを介して血流に入り込む。真菌血症(fungemia)が成立すると、血行性に脈絡膜毛細血管に到達し感染が成立する。
病変の進展順序:
脈絡膜への真菌定着 → 網膜色素上皮を穿破した内網膜への侵入 → 網膜炎の形成 → 硝子体腔への波及 → fungus ball形成 → 炎症増殖膜形成 → 牽引性網膜剥離
免疫機能が保たれている宿主では、真菌性眼内炎は比較的緩徐に進行し、眼底に明瞭な焦点病変を形成する。一方、好中球減少・AIDS・移植後免疫抑制状態では急速に進行し、アスペルギルスやフザリウムなどの糸状菌も発症しやすくなる6)。
フルコナゾール耐性Candida glabrata・Candida kruseiでは、薬剤感受性試験(最小発育阻止濃度:MIC測定)に基づいた抗真菌薬の選択が重要である2,7)。
内因性真菌性眼内炎は両眼に発症することがある。長期化すると広範な網膜壊死性変化を来し、治療後の視力予後は不良となる。全身状態不良患者では真菌血症のコントロールが困難となり、眼症状が繰り返す場合がある。
糸状菌(アスペルギルス・フザリウム)による眼内炎において、硝子体内ボリコナゾール(100 µg/0.1 mL)の単独または全身投与との組み合わせによる使用経験が症例シリーズで報告されている5)。今後の用量最適化データの蓄積が期待される。
カンジダ血症患者に対する一律の眼科スクリーニングについては、システマティックレビューで有用性と過剰診断・介入の可能性が議論されている8)。無症状例を含めた評価の対象、時期、定義をどう標準化するかが今後の課題である。
フルコナゾール耐性カンジダ属に対応するため、培養同定とMICに基づく個別化治療の重要性が高まっている2,7)。眼内検体が得られる場合は、培養や分子診断を全身検査と組み合わせて起炎菌同定に用いる。