テント状剥離
形成機序:新生血管の根元(epicenter)や網膜血管に沿って牽引が生じた場合に形成される。
特徴:剝離部が逆アール状(テント状)を呈する。可動性がなく、剝離の高さは限局的であることが多い。PDR初期〜中期に典型的。

牽引性網膜剥離(Tractional Retinal Detachment; TRD)は、後部硝子体剝離が不完全な状態で網膜に硝子体の強い牽引力が生じることにより発生する網膜剥離である。網膜上の増殖性組織あるいは硝子体の牽引によって生じる非裂孔原性の網膜剥離であり、剝離範囲は限局的で、扁平あるいはテント状を呈することが多く、可動性がほとんどないことが特徴である。
TRDは原因により以下の2つに大別される。
線維性血管膜(新生血管を含む)による牽引:代表疾患は増殖糖尿病網膜症(PDR)、網膜静脈閉塞症(RVO)、未熟児網膜症(ROP)である。眼内虚血に対する新生血管形成を基盤とし、線維性血管膜の収縮が牽引力を生じる。
新生血管を欠く硝子体網膜牽引:代表疾患は黄斑硝子体牽引症候群と穿孔性眼外傷である。炎症・外傷後の増殖を基盤とする。
網膜剥離は一般に裂孔原性・牽引性・滲出性の3型に分類される。牽引性は可動性がない限局した剝離として、胞状・可動性を有する裂孔原性、および滲出性と臨床的に区別される。網膜裂孔を合併しているケースもあり、その場合は combined tractional-rhegmatogenous RD(裂孔合併牽引性網膜剥離)と呼ばれる。Combined RDはより緊急性の高い病態であり、牽引性のみの場合と管理が異なる。
増殖性硝子体網膜症(PVR)は裂孔原性網膜剝離術後に二次的に生じる増殖過程であり、TRDの原因の一つともなりうる。
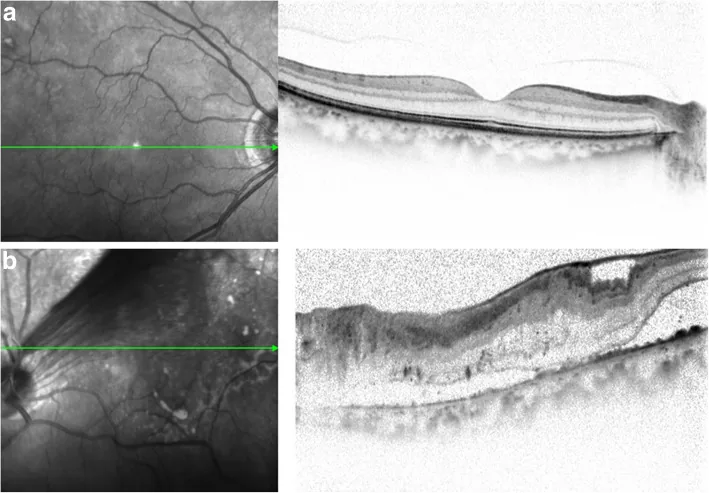
TRDの自覚症状は剝離の部位・範囲によって大きく異なる。
糖尿病網膜症(DR)に伴うTRDでは、硝子体出血を合併することが多く、これにより急激な視力低下が生じることがある1)。
TRDに特徴的な形態所見を以下に示す。
テント状剥離
形成機序:新生血管の根元(epicenter)や網膜血管に沿って牽引が生じた場合に形成される。
特徴:剝離部が逆アール状(テント状)を呈する。可動性がなく、剝離の高さは限局的であることが多い。PDR初期〜中期に典型的。
テーブルトップ剥離
形成機序:線維血管膜と網膜の癒着が広範囲に及ぶ場合に形成される。富士山型とも呼ばれる。
特徴:広い平坦な剝離面を形成する。可動性がなく、黄斑部全体を覆う場合は視力予後が不良となる。
可動性の評価:牽引性RDは可動性がない点が重要な所見である。剝離にドーム状の形態や可動性が認められる場合は、裂孔原性RDの併発(combined RD)を考慮する必要がある。
線維血管膜(fibrovascular membrane)の存在:PDR由来TRDでは眼底の新生血管と線維組織が融合した膜構造が観察される。膜の活動性(血管成分の豊富さ・出血傾向)が手術難易度に影響する。
硝子体出血の合併:増殖期の糖尿病網膜症では、線維血管膜からの出血により視界が遮られることがある。この場合、眼底観察が困難となるため超音波Bモード検査が必要となる。
牽引性網膜分離症:増殖糖尿病網膜症などで網膜表面に強い牽引が生じると、網膜内層と外層が分離する網膜分離症を呈することがある。表面形状はテント状を示し、OCTが診断に有効である。
TRDは以下の原因疾患によって生じる。
1. 増殖糖尿病網膜症(PDR):TRDの中で最も頻度が高い原因疾患。網膜虚血に対する代償として新生血管が形成され、線維性血管膜が網膜上に増殖・収縮することでTRDが生じる。糖尿病網膜症診療ガイドライン(第1版)では牽引性網膜剝離はPDRの重篤な合併症の一つとして明記されている1)。
2. 未熟児網膜症(ROP):Stage 4(部分的TRD)およびStage 5(全TRD)でTRDが生じる4)。網膜血管が発達していない無血管帯を有する未熟な網膜に、出生後の高酸素環境が相対的虚血を引き起こし新生血管が形成される。
3. 穿孔性眼外傷:眼球穿孔創からの炎症細胞浸潤と血液網膜関門(BRB)の破綻により眼内増殖が進行し、増殖膜形成・牽引を生じる。
4. 増殖性硝子体網膜症(PVR):裂孔原性網膜剝離術後に二次的に生じた増殖が牽引性要素を追加することで、TRD様の病態に至る場合がある。
5. 網膜静脈閉塞症(RVO):新生血管形成を伴う重症例では、PDRと同様の機序でTRDが生じうる。
6. その他:Eales病(特発性周辺部静脈周囲炎)、鎌状赤血球症、Coats病の一部でもTRDが生じることがある。
以下に各原因疾患とリスク因子をまとめる。
| リスク因子 | 関連疾患 |
|---|---|
| 糖尿病罹病期間・血糖コントロール不良 | PDR |
| 低出生体重・早産(在胎週数32週未満) | ROP |
| 穿孔性眼外傷 | 外傷後TRD |
| 裂孔原性網膜剥離手術既往 | PVR |
| 汎網膜光凝固未施行・不完全 | PDR |
| 網膜静脈閉塞症 | 虚血型RVO由来TRD |
未熟児網膜症に対する抗VEGF療法については、日本未熟児網膜症研究会の手引きが参考となる7)。
倒像検眼鏡・細隙灯顕微鏡(前置レンズ)による眼底観察がTRD診断の基本である。
OCTは牽引性網膜分離症の診断に特に有効である。牽引がテント状の表面形状を形成していることを断層像で描出できる。黄斑部への牽引の程度・網膜内層と外層の分離・黄斑への剝離進展の有無を定量的に評価できる。
硝子体出血や高度な白内障により眼底観察ができない場合に必須の検査である。網膜剝離の有無・範囲・形態・牽引の程度を評価できる。増殖膜が高輝度エコーとして描出される場合がある。
新生血管の活動性評価および無灌流領域(NPA)の検出に有用である1)。PDR由来TRDでは、術前に無灌流領域の広さを把握することが、術中光凝固計画に役立つ。
以下にTRDと類似する病態の鑑別診断をまとめる。
| 鑑別疾患 | 特徴 | 可動性 | 形態 |
|---|---|---|---|
| 裂孔原性RD | 裂孔あり | あり | 胞状 |
| 牽引性RD | 増殖膜あり | なし | テント状・テーブルトップ |
| 滲出性RD | 裂孔・増殖膜なし | なし〜軽度 | 滑らかなドーム状 |
| Combined TRD-RRD | 裂孔+増殖膜 | あり | テント状+胞状混合 |
TRDの手術適応を以下に示す。
| 病態 | 方針 |
|---|---|
| 黄斑部をおびやかす牽引性網膜剝離 | 手術適応1, 2) |
| 裂孔併発型牽引性網膜剝離(combined RD) | 手術適応(より緊急性高)1, 2) |
| 黄斑偏位を起こしうる増殖膜がある場合 | 手術を考慮1) |
| 黄斑部外の限局的TRD(進行なし) | 経過観察可 |
黄斑部外の限局的TRDでは、剝離範囲の拡大や黄斑偏位が認められない場合、定期的な眼底検査・OCT検査によるモニタリングを行いながら経過観察が可能である。ただし、進行の徴候を認めた場合は早期に手術を検討する1)。
TRDの根本治療は硝子体手術による牽引除去である。近年は25G・27G小切開硝子体手術(MIVS)が主流であり、広角観察システム下での手術が標準となっている1)。
手術の基本手順は以下のとおりである。
術前の抗VEGF硝子体内注射は術中出血の軽減・医原性裂孔の減少・手術時間短縮に寄与する可能性がある3)。PDRに伴うTRDで線維血管膜の活動性が高い場合に考慮される。
未熟児網膜症に伴うTRDの手術方針は病期によって異なる4)。
抗VEGF療法が重症ROPの一次治療として用いられる場合があるが7)、Stage 4-5のTRDに対しては硝子体手術が原則となる。
黄斑部に進行するリスクがなければ経過観察が可能である。ただし、剝離範囲の拡大や黄斑偏位を生じうる増殖膜が認められる場合は、より早期の手術を検討する。定期的な眼底検査・OCT検査で進行の有無をモニタリングすることが重要である。
増殖糖尿病網膜症に由来するTRDは、以下の段階を経て発症する。
PDR由来TRDの病態
虚血→VEGF→新生血管の連鎖が基盤となる。
線維性血管膜の収縮が網膜に牽引力を生じ、TRDへと至る。血液網膜関門(BRB)破綻によるサイトカイン漏出が増殖を促進する。
ROP由来TRDの病態
網膜血管の未熟性→無血管帯→虚血→新生血管が基盤となる。
出生後の高酸素環境が相対的虚血を生じ、ridge上の線維血管増殖が硝子体内へ進展してStage 4-5のTRDへ至る。
TRDの基盤には血液網膜関門(BRB)の破綻がある。BRBが破綻すると、眼内の炎症性・血管新生性環境が強まり、線維血管増殖が進行する。RPE、グリア細胞、マクロファージ、線維芽細胞などが増殖膜形成に関与する9)。
増殖膜にはRPEのみならず、グリア細胞・マクロファージ・線維芽細胞なども複雑に関与する。コラーゲンの収縮により網膜への牽引が生じ、TRDが発症する。
穿孔性眼外傷後のTRDでは、穿孔創からの炎症細胞浸潤とBRB破綻により眼内増殖が進行する。線維芽細胞・RPEの増殖により増殖膜が形成され、これが収縮することで牽引が生じてTRDに至る。
糖尿病性重度硝子体出血に対する早期硝子体手術の有効性を検討したDRVS(Diabetic Retinopathy Vitrectomy Study)は、TRD管理の基盤となるエビデンスを提供している。1型糖尿病の重度硝子体出血では、早期硝子体手術群で2年後に矯正視力20/40以上が達成される割合が25%(経過観察群15%)であり、1型糖尿病では36% vs 12%と有意な差が示された5)。2型糖尿病では有意差は認められなかった5)。
糖尿病性硝子体出血に対するアフリベルセプト硝子体内注射と硝子体手術+汎網膜光凝固(PRP)を比較した試験では、24週時点の視力改善に有意差は認められなかった。ただし硝子体出血の消退は手術群のほうが速かった(4週 vs 36週)2)。
術前抗VEGF投与の有用性を検討したメタ解析では、術中出血量の減少・医原性裂孔の減少が報告されている3)。ただし抗VEGF注射後に牽引が一時的に増悪する可能性が指摘されており、注射後1〜2週以内の早期手術が推奨される2)。
25G・27Gシステムおよび広角観察システムの普及により、PDR由来TRDに対する低侵襲硝子体手術の適応が拡大している1)。小切開術式は術後炎症の軽減・早期回復に寄与し、外来手術への適応が増加している8, 9)。
DRCR Protocol S では、抗VEGF(ラニビズマブ)がPRPに対して2年時点で非劣性を示した2)。しかしTRDへの進展率に有意差はなく、TRDが既に存在する場合は抗VEGF単独では対処できない。抗VEGFはTRDの予防的観点では考慮されるが、TRD発症後は硝子体手術が根本的な治療となる。
抗VEGF注射単独でTRDが改善することは通常期待できない。抗VEGFは新生血管の退縮には有効だが、既存の線維性増殖膜の収縮を制御できず、むしろ注射後に牽引が悪化する報告もある2)。TRDの治療は硝子体手術が原則である。術前補助としての抗VEGF投与は有用な場合があり、術中出血の軽減や医原性裂孔の減少に寄与する可能性が示されている3)。