網膜分離症は神経網膜 が内網状層または外網状層で分離した状態であり、網膜剥離 (視細胞 層が色素上皮層から剥離)とは病態が異なる。
3つの病型がある。①加齢性(40歳以上の7〜30%に発症、下耳側周辺部に70%が好発)、②X連鎖性(男児・学童期、5,000〜25,000人に1人)、③近視 性中心窩 分離症(強度近視 眼)。
加齢性は大多数が無症状で経過観察のみ;網膜剥離 への進行リスクは年間約0.05%ときわめて低い2) 。
X連鎖性(XLRS)はRS1 遺伝子変異によるX染色体劣性遺伝疾患;ERG の陰性b波(b波振幅 < a波)が診断に特徴的2) 。
XLRSに対する炭酸脱水酵素阻害薬 (ドルゾラミド 点眼・アセタゾラミド 内服)で分離腔改善の報告がある;確立した根治療法はない。
近視 性中心窩 分離症は強度近視 眼に伴い発症し、硝子体手術 (ILM 剥離)が基本的治療となる。XLRSに対するRS1遺伝子治療 は臨床試験段階にあり、眼内炎 症などの安全性上の課題が残る3) 。
網膜分離症(retinoschisis)は、神経網膜 が内網状層または外網状層で分離した状態である。視細胞 層が色素上皮層から剥離する網膜剥離 とは病態が根本的に異なる。
病型 好発年齢・性別 好発部位 有病率・罹患率 加齢性(後天性)網膜分離症 40歳以上;男女問わず 下耳側周辺部(70%) 40歳以上の7〜30% X連鎖性(先天性)網膜分離症 学童期;ほぼ男性のみ 中心窩 (ほぼ全例)+周辺部(約半数)5,000〜25,000人に1人2) 近視 性網膜 中心窩 分離症中年以降;強度近視 後極部・黄斑部 強度近視 眼の一定割合
Q
網膜分離症と網膜剥離は別の疾患か?
A
網膜分離症は神経網膜 の「層内」で分離が生じる病態であり、網膜剥離 (網膜 全層が色素上皮から剥離)とは全く異なる。分離症では網膜色素上皮 との連絡は保たれているため、網膜剥離 に比べて視力 予後は一般に良好である。ただし内外両層に孔が生じると、網膜剥離 へ進行する可能性がある。
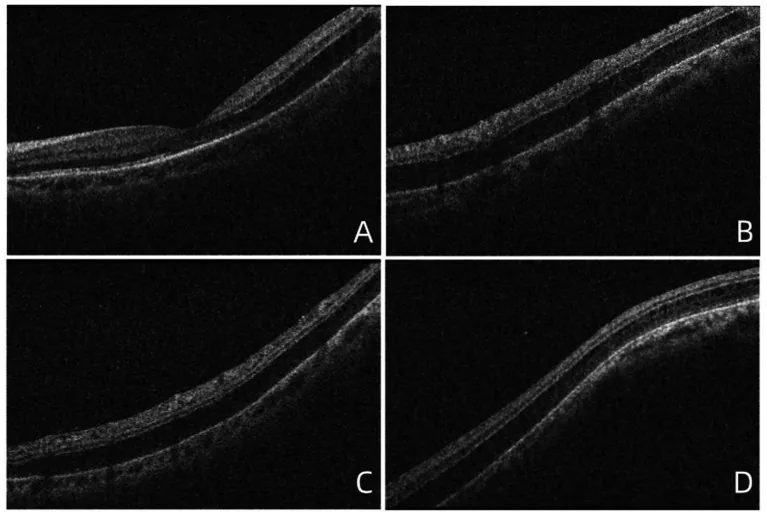
網膜分離症のOCT像 Wang N, et al. Case Report: A case of unexplained retinoschisis. Front Med (Lausanne). 2025. Figure 1. PM
CI D: PMC12518284. License: CC BY.
OCT 画像は網膜分離症を示しており、(A)黄斑部 における外網状層の分離、(B)上網膜 血管弓付近の分離、(C)下網膜 血管弓付近の分離、(D)黄斑 耳側の網膜 分離を捉えている。本文「2. 後天性(加齢性)網膜分離症」の項で扱う網膜 分離に対応する。
加齢性網膜分離症 は、成人周辺部網膜 の生理的嚢胞様変性(Blessig-Iwanoff嚢胞)が融合・拡大して外叢状層または内顆粒層に分離が生じる病態である。
有病率は1.65〜7%2) とされ、40歳以上に多く、両眼性が約70%にみられる。下耳側網膜 周辺部に70%が好発し、隆起表面は平滑である。遺伝性はなく、加齢に伴い発症する。
続発性の網膜分離症は増殖膜 ・硝子体 牽引、嚢胞性変化、網膜 内出血・滲出・炎症が原因となりうる。具体的な原因疾患として糖尿病網膜症 、陳旧性網膜剥離 、加齢黄斑変性 、未熟児網膜症 (ROP )、Coats病が知られている。
大多数は無症状であり、後極まで進展することはまれで視力 は正常のことが多い。病変が赤道部を越えると視野欠損 等の自覚症状を生じることがある。
所見 特徴 鑑別への意義 ドーム状隆起 平滑・透明な半球状;固定・不動 体位変換で移動しない water silk appearance 内層の波打つ光沢 本症に特徴的 snowflakes(雪片状混濁) 分離層内層裏面の黄白色顆粒状混濁 変性の指標
外層孔が生じ網膜 外層剥離を生じても危険性は低い。内・外孔が生じ剥離に進行した場合は通常の裂孔原性網膜剥離 に対する手術加療が必要となる。
加齢による外叢状層のHenle線維の嚢胞様変性が融合・拡大することが主な病態である。絶対暗点の機序は、外叢状層での層間分離がシナプス結合部での組織断裂をもたらし、光刺激の信号伝達が遮断されるためである1) 。
リスク要因として加齢・遠視 が挙げられる2) 。遺伝的素因は同定されていない2) 。
OCT による診断2) 。分離腔の広がり・深さ・層間の柱状構造物(垂直な組織架橋)を描出し、外叢状層での層間分離を直接確認できる。
網膜剥離 との鑑別
特徴 網膜分離症 網膜剥離 隆起の移動性 固定・不動 体位変換で移動 透過性 高い(透明) 低い(混濁) 暗点の性質 絶対暗点 相対暗点 表面の性状 平滑(water silk) 不整・波打ち
原則的に経過観察である。網膜剥離 への進展リスクは年間約0.05%と低く、大多数の症例は無症状で安定している。
バリケードレーザー光凝固 :後方進展を阻止する目的で施行。適応は進行性拡大、後方境界が後極に近接、内外両層裂孔がある場合黄斑 浸潤例への硝子体手術 硝子体手術 (ILM 剥離・気体充填)により視力 改善が得られた1) 。黄斑部 に進展した症例では手術が選択肢となる
後方進展リスク
基本方針 :経過観察
バリケードレーザー適応 :進行性拡大、後極への近接
治療目的 :さらなる後方進展の阻止
外層裂孔形成
基本方針 :経過観察
注意点 :外層裂孔は剥離リスクを高める
適応を慎重に評価 :内層孔を同時に持つ場合は要注意
分離症性剥離
基本方針 :通常の裂孔原性網膜剥離 に準じた手術
手術適応 :内・外両層に孔が生じ剥離進行した場合
予後 :一般的には良好
黄斑浸潤例
基本方針 :硝子体手術 の検討
術式 :ILM 剥離+気体充填
エビデンス :症例報告レベル1)
外叢状層での層間分離がシナプス結合部での組織断裂をもたらし、絶対暗点が生じる1) 。Henle線維が加齢に伴う嚢胞様変性の融合で引き離されることが分離の原因と考えられている。SD-OCT による三次元的評価で分離腔の広がりや内外層の薄さを精密に評価できるようになり、長期的な自然経過と進行予測因子の同定が進んでいる2) 。
Q
なぜ絶対暗点が生じるのか?
A
加齢性網膜分離症 では外叢状層での層間分離が生じる。この部位では視細胞 と神経節細胞の間のシナプス結合が存在しており、分離によりシナプスが断絶されると光刺激が双極細胞・神経節細胞へ伝わらなくなる1) 。このため、分離領域では光を当てても電気信号が伝導されず、絶対暗点として自覚される。
Q
加齢性網膜分離症は将来必ず悪化するのか?
A
ほとんどの加齢性網膜分離症 は安定した経過をたどる。網膜剥離 への進展リスクは年間約0.05%と極めて低い。ただし内外両層に孔が生じた場合は剥離リスクが高まるため、定期的な眼底検査 での経過観察が重要である2) 。
X連鎖性網膜分離症(XLRS)は、RS1遺伝子変異によるX染色体劣性遺伝の先天性網膜 疾患である。比較的まれな硝子体 網膜 変性疾患で、罹患率は5,000〜25,000人に1人とされる2) 。通常男性のみが発症し、女性は保因者となる。
原因遺伝子 :RS1遺伝子(Xp22.2)2) コードタンパク :レチノスキシン(retinoschisin; RS)機能 :視細胞 ・双極細胞に発現する細胞外マトリクスタンパク;ホモオリゴマー複合体を形成し、細胞接着・シナプス形成・網膜 の分化と機能に重要な役割を果たす2) 変異数 :200以上の疾患原因変異が同定されている表現型 :表現型の多様性が顕著;同一変異内でも重症度が異なる;非症候群性疾患(網膜 のみに限局)
Q
女性がX連鎖網膜分離症になることはあるか?
A
通常は男性のみが発症する。X染色体劣性遺伝であるため、女性は1本のX染色体にのみ変異があれば保因者となり通常は無症状である。稀に、X染色体不活化の偏りや片親性ダイソミーにより、女性でも軽度の表現型が出現することが報告されている2) 。
自覚症状 :
視力 低下視力 低下(0.3〜0.8程度)を自覚する場合が多い2) 。重症例では生後から視力 不良遠視 が多いとされる;弱視 ・斜視 ・眼振 (乳児期〜就学前に出現することがある)視力 0.6程度あれば通常の大学進学が可能。年齢とともに黄斑 萎縮をきたすと視力 0.1に低下中等度の視力 (0.2〜0.7)を長期に保つことが多い
臨床所見 :
黄斑部所見
中心窩 分離(ほぼ全例)OCT 上の嚢胞と架橋構造)
黄斑 萎縮嚢胞様黄斑浮腫 にみえる例も多い
蛍光造影 :嚢胞様黄斑浮腫 と異なり蛍光漏出なし(中心窩 は正常かwindow defect)
周辺部所見
周辺部網膜 分離 (約半数):下耳側に好発;大きな網膜 内層孔を伴うことがある
金箔様反射 :周辺網膜 に特徴的な所見;網膜 血管の白線化を伴う
硝子体 ベール硝子体 は未剥離で網膜 と強く接着
合併症 :網膜剥離 (5〜20%)・硝子体出血 ・分離腔内出血
遺伝的背景 :RS1遺伝子変異によるレチノスキシンのホモオリゴマー複合体崩壊が、特徴的な分離腔と網膜 シグナル伝達障害をもたらす2) 合併症リスク :
男児両眼性の嚢胞様黄斑浮腫 をみたら本症を疑う ことが重要な診断の入口となる。
OCT 中心窩 嚢胞・架橋構造(柱状のMüller細胞残骸)・分離の範囲を評価;韓国人83例のコホート研究ではSD-OCT ・ffERG ・眼底写真の総合評価が有用とされる2) ERG (網膜電図 )2) 。a波が保持されるがb波の振幅がa波より小さい(陰性b波);幼少時から認められ、眼底全体の網膜 中層機能不全を反映;一部の患者では正常〜準正常の波形を呈する蛍光眼底造影 嚢胞様黄斑浮腫 との鑑別に有用;XLRSでは花弁状蛍光漏出なし遺伝子検査 :RS1遺伝子の変異解析で確定診断;200以上の疾患原因変異が同定
鑑別診断 :
疾患 鑑別のポイント 裂孔原性網膜剥離 通常片眼性;demarcation line形成;格子状変性 を伴う 嚢胞様黄斑浮腫 蛍光造影で花弁状漏出あり;XLRSでは漏出なし 加齢性(変性性)網膜分離症 高齢者に発生;周辺部限局;b波正常 Goldman-Favre症候群 夜盲 ・色素沈着を伴う
Q
嚢胞様黄斑浮腫との違いは何か?
A
嚢胞様黄斑浮腫 (CME )では蛍光眼底造影 で花弁状の蛍光漏出・貯留が認められる。一方、XLRSでは中心窩 の分離腔は存在するが血液網膜関門 は正常であり、蛍光造影では漏出がなく、窓欠損(window defect)のみを呈する。この違いがOCT と蛍光造影を組み合わせた鑑別において重要である。
確立した根治療法はない。
薬物療法 :
炭酸脱水酵素阻害薬 (CAI)OCT 上の分離腔を改善させる効果が報告されている
ドルゾラミド 点眼(局所投与)アセタゾラミド 内服(全身投与)効果には個人差があり、視力 とOCT 上の嚢胞状液体の変化でモニタリングが必要
外科的治療 :
硝子体手術
周辺部網膜 分離が網膜剥離 に進行した場合(主要な適応)
中心窩 大嚢胞の平坦化(視力 ・ERG 改善は期待しにくい)後部硝子体剥離 の誘発(将来の周辺網膜 分離予防の可能性)小児では硝子体 と網膜 が広範囲に癒着しており手術は危険なため慎重に適応を判断する
強膜バックリング術 網膜剥離 例に適用レーザー光凝固 術網膜剥離 予防目的で検討されることがあるが、医原性裂孔のリスクがあり議論がある
患者管理 :
アセタゾラミド 内服は電解質異常・腎石灰化・血球減少などの全身副作用を生じうる。長期服用時は定期的な採血が必要硝子体手術 は視力 ・ERG の根本的改善は期待しにくいことが多い。手術の目的と期待できる結果について術前に十分な説明が必要未成年患者では網膜 と硝子体 の癒着が強く、手術リスクが成人より高い
Q
年齢が上がると分離は消えるか?
A
成長とともに中心窩 の嚢胞様変化が自然に軽減することがある2) 。しかし黄斑 萎縮へ移行する例もあり、消退が必ずしも視力 改善を意味しない。一部の症例では後部硝子体剥離 の発生後に周辺部分離が軽減することも報告されている。
RS1遺伝子がコードするレチノスキシンは224アミノ酸からなる分泌蛋白であり、ディスコイジンドメインを介してホモオリゴマー複合体を形成する2) 。視細胞 ・双極細胞への結合を通じて網膜 の構造的・シナプス的完全性を維持している。RS1変異により複合体が崩壊すると、特徴的な分離腔と網膜 シグナル伝達障害が生じる2) 。
組織病理学的には網膜 分離は主に神経線維層で生じる。OCT では中心窩 とその周辺で外網状層と内顆粒層での分離が認められる。形態学的な分離が限局していても、電気生理学的には網膜 全体の機能障害が存在することが、陰性b波から示される。
遺伝子型と表現型の相関 (韓国人83例コホート、Lee et al. 2025)2) :
RS1蛋白の分泌能を持つ変異群は非分泌群より有意に良好な最終BCVA(P=0.021)
非分泌群では楕円体帯(EZ )の障害頻度が有意に高い(P=0.030)
短縮型変異とミスセンス変異の間ではBCVA・OCT ・ERG パラメータに有意差なし
RS1蛋白の分泌能が変異の種類より表現型を規定する重要因子となりうる
XLRSの分離腔液を分析した研究では、光受容体間レチノイド結合蛋白(IRBP)が分離腔液中に同定されており、分離腔内の網膜 代謝異常を示す可能性が報告されている2) 。またXLRSでは通常みられない滲出性黄斑 症が合併する例も報告されており、同一診断下での多彩な表現型の存在が示されている2) 。
RS1遺伝子治療 の臨床試験が進行中である2) 3) 。動物モデルおよび早期臨床試験で網膜電図 応答の部分的な回復と網膜 解剖の改善が報告されている。
主要な臨床試験:
NEI試験(NCT 02317887) :AAV-RS1ベクターの硝子体 内投与安全性評価。高用量投与群の1例で分離腔の閉鎖が認められたが、眼内炎 症も惹起されたAGTC試験(NCT 02416622) :rAAV2tYF-CB-hRS1ベクターの安全性・有効性試験。炎症の発生と臨床的な治療効果の欠如により試験は中止。高用量群を中心に投与後早期の眼内炎 症が観察されており、安全性面の課題が残る3)
現在の課題:XLRSでは網膜 の脆弱性が増加しており、後部硝子体 膜の剥離と網膜 下注射が技術的に非常に困難である3) 。硝子体 内投与が望ましい場合があるが、硝子体 炎のリスクを許容する必要がある。
Q
遺伝子治療は現在受けられるか?
A
XLRSに対する遺伝子治療 はまだ臨床試験段階にあり、一般的な病院での治療として承認されていない。いくつかの臨床試験では眼内炎 症などの安全性上の課題が明らかになり、一部の試験は中止されている3) 。参加を希望する場合は専門施設への相談が必要である。
近視 性網膜 中心窩 分離症(myopic foveoschisis)は、強度近視 眼に伴う後極部の網膜 内層分離である。古くから強度近視 眼に伴う後極部網膜剥離 として記載され、現在は黄斑円孔 を合併するものも含める概念となっている。
病態には以下の要素が複合的に関与する:
眼軸 延長・後部ぶどう腫 形成網膜 が引き延ばされ、内側へ引き込まれる力が働く硝子体 ・内境界膜 (ILM )・網膜 血管の牽引硝子体 膜、硬化した内境界膜 、ならびに赤道部に比して相対的に短い網膜 血管が、後極部の網膜 内層を引き離す方向に作用する
自覚症状 :視力 低下・中心暗点 ・歪視(metamorphopsia)・霧視 。強度近視 では自覚症状に乏しいこともある。
診断(OCT ) :
網膜 内層分離と網膜 間隙に架橋構造(内境界膜 ・Müller細胞の残骸)を認める黄斑円孔 ・黄斑部 剥離を伴うこともある鑑別:黄斑円孔 網膜剥離 (全層で剥離)
治療 :硝子体手術 が基本である。
術式 :ILM 剥離が基本;inverted ILM flap technique、レンズ形成ILM flap法など術後の網膜 復位まで数か月以上要することがある
予後 :
術前に黄斑部 剥離を伴うものが最も視力 予後良好
術前黄斑円孔 ・術後黄斑円孔 形成では視力 予後不良
適切なタイミングでの手術介入が視機能予後を左右する
Desjarlais EB , Barineau W, Shah CP. Surgical treatment of macula-involving degenerative retinoschisis. Retin Cases Brief Rep. 2022;16(1):73-76.
Yang YP, Chen YP, Yang CM. Clinical manifestation and current therapeutics in X-linked juvenile retinoschisis. J Chin Med Assoc. 2022;85(3):276-278. doi:10.1097/JCMA.0000000000000666.
van der Veen I, Stingl K, Kohl S, et al. The road towards gene therapy for X-linked retinoschisis: a systematic review of preclinical and clinical findings. Int J Mol Sci. 2024;25(2):1267. doi:10.3390/ijms25021267.
記事の全文をコピーして、お好みのAIに貼り付けて質問できます
下のAIを開いて、チャット欄に貼り付け(ペースト)してください