帳篷狀剝離
形成機轉:當牽引發生在新生血管根部(epicenter)或沿視網膜血管時形成。
特徵:剝離區域呈反拱形(帳篷狀)。無活動性,剝離高度通常侷限。典型於PDR早期至中期。

牽引性視網膜剝離(TRD)是在後玻璃體剝離不完全的狀態下,玻璃體對視網膜產生強烈牽引力而發生的視網膜剝離。它是由視網膜上的增殖性組織或玻璃體牽引引起的非裂孔源性視網膜剝離,剝離範圍常為局限性,呈扁平或帳篷狀,特徵為幾乎無活動性。
TRD根據原因大致分為以下兩類。
纖維血管膜(包括新生血管)牽引:代表性疾病為增殖性糖尿病視網膜病變(PDR)、視網膜靜脈阻塞(RVO)和早產兒視網膜病變(ROP)。以眼內缺血引起的新生血管形成為基礎,纖維血管膜的收縮產生牽引力。
無新生血管的玻璃體視網膜牽引:代表性疾病為黃斑玻璃體牽引症候群和穿孔性眼外傷。以炎症或外傷後的增殖為基礎。
視網膜剝離一般分為裂孔源性、牽引性和滲出性三種類型。牽引性剝離表現為無活動性的侷限性剝離,臨床上與呈泡狀、有活動性的裂孔源性剝離和滲出性剝離區別。部分病例合併視網膜裂孔,稱為合併牽引性-裂孔源性視網膜剝離(combined tractional-rhegmatogenous RD)。合併RD是更緊急的病變,其處理與單純牽引性不同。
增殖性玻璃體視網膜病變(PVR)是裂孔源性視網膜剝離術後繼發的增殖過程,也可成為TRD的原因之一。
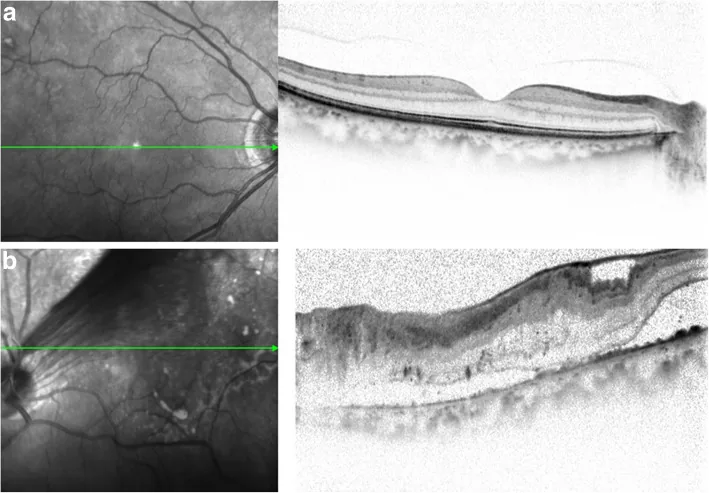
TRD的自覺症狀因剝離的部位和範圍而異。
糖尿病視網膜病變(DR)相關的牽引性視網膜剝離(TRD)常合併玻璃體出血,可能導致視力突然下降1)。
TRD的特徵性形態所見如下。
帳篷狀剝離
形成機轉:當牽引發生在新生血管根部(epicenter)或沿視網膜血管時形成。
特徵:剝離區域呈反拱形(帳篷狀)。無活動性,剝離高度通常侷限。典型於PDR早期至中期。
桌面狀剝離
形成機轉:當纖維血管膜與視網膜廣泛粘連時形成。也稱為富士山型。
特徵:形成寬廣平坦的剝離面。無活動性,若覆蓋整個黃斑部,視力預後不良。
活動性評估:牽引性RD無活動性是重要所見。若剝離呈圓頂狀或有活動性,需考慮合併裂孔源性RD(combined RD)。
纖維血管膜的存在:PDR來源的TRD可見眼底新生血管與纖維組織融合形成的膜結構。膜的活動性(血管成分豐富程度、出血傾向)影響手術難度。
合併玻璃體出血:增殖性糖尿病視網膜病變中,纖維血管膜出血可能遮擋視野。此時眼底觀察困難,需行B型超音波檢查。
牽引性視網膜裂:增殖性糖尿病視網膜病變等導致視網膜表面強烈牽引時,視網膜內層與外層可分離,表現為視網膜裂。表面形態呈帳篷狀,OCT有助於診斷。
TRD由以下原因疾病引起。
1. 增殖性糖尿病視網膜病變(PDR):TRD中最常見的原因疾病。作為視網膜缺血的代償,形成新生血管,纖維血管膜在視網膜上增殖和收縮,導致TRD。糖尿病視網膜病變診療指引(第1版)明確指出牽引性視網膜剝離是PDR的嚴重併發症之一1)。
2. 早產兒視網膜病變(ROP):在第4期(部分TRD)和第5期(全TRD)發生TRD4)。在視網膜血管未發育的無血管區的未成熟視網膜上,出生後的高氧環境引起相對缺血,形成新生血管。
3. 穿孔性眼外傷:眼球穿孔傷的炎症細胞浸潤和血-視網膜屏障(BRB)破壞導致眼內增殖,形成增殖膜並產生牽引。
4. 增殖性玻璃體視網膜病變(PVR):裂孔源性視網膜剝離術後繼發的增殖增加了牽引成分,可能導致類似TRD的病理狀態。
5. 視網膜靜脈阻塞(RVO):伴有新生血管形成的重症病例中,可能通過類似PDR的機制發生TRD。
6. 其他:Eales病(特發性周邊靜脈周圍炎)、鐮狀細胞病、Coats病的一部分也可能發生TRD。
下表總結各原因疾病和風險因素。
| 風險因素 | 相關疾病 |
|---|---|
| 糖尿病病程、血糖控制不良 | PDR |
| 低出生體重、早產(胎齡<32週) | ROP |
| 穿孔性眼外傷 | 外傷後TRD |
| 裂孔性視網膜剝離手術病史 | PVR |
| 全視網膜光凝術未執行或不完全 | PDR |
| 視網膜靜脈阻塞 | 缺血型RVO引起的TRD |
關於早產兒視網膜病變的抗VEGF治療,可參考日本早產兒視網膜病變研究會的指引7)。
使用間接檢眼鏡或裂隙燈顯微鏡(前置鏡)進行眼底觀察是診斷TRD的基礎。
OCT對診斷牽引性視網膜劈裂特別有效。它可以在斷層影像上顯示由牽引形成的帳篷狀表面形態。可以定量評估黃斑部牽引程度、視網膜內層與外層的分離以及剝離向黃斑進展的情況。
當玻璃體出血或嚴重白內障導致無法觀察眼底時,這是必需的檢查。可以評估視網膜剝離的有無、範圍、形態和牽引程度。增殖膜有時表現為高回音。
FA有助於評估新生血管活動性和檢測無灌流區(NPA)1)。在PDR相關的TRD中,術前了解無灌流區的範圍有助於規劃術中光凝治療。
以下總結了與TRD相似疾病的鑑別診斷。
| 鑑別診斷 | 特徵 | 可動性 | 形態 |
|---|---|---|---|
| 裂孔源性RD | 有裂孔 | 有 | 泡狀 |
| 牽引性RD | 有增殖膜 | 無 | 帳篷狀或桌面狀 |
| 滲出性RD | 無裂孔或增殖膜 | 無至輕度 | 光滑的圓頂狀 |
| 混合性TRD-RRD | 裂孔+增殖膜 | 有 | 帳篷狀與大泡狀混合 |
TRD的手術適應症如下所示。
| 病態 | 方針 |
|---|---|
| 威脅黃斑部的牽引性視網膜剝離 | 手術適應症1, 2) |
| 合併裂孔的牽引性視網膜剝離(合併RD) | 手術適應症(更緊急)1, 2) |
| 可能導致黃斑位移的增殖膜 | 考慮手術1) |
| 黃斑部外的局限性TRD(無進展) | 可觀察 |
對於黃斑部外的局限性TRD,如果剝離範圍無擴大且無黃斑位移,可透過定期眼底檢查和OCT檢查進行監測觀察。但若發現進展徵象,應儘早考慮手術1)。
TRD的根本治療是透過玻璃體手術解除牽引。近年來,25G和27G微切口玻璃體手術(MIVS)已成為主流,在廣角觀察系統下進行手術是標準做法1)。
手術的基本步驟如下。
術前玻璃體內注射抗VEGF可能有助於減少術中出血、醫源性裂孔和手術時間3)。在PDR伴TRD且纖維血管膜活動性高時考慮使用。
早產兒視網膜病變相關牽引性視網膜剝離的手術方針因分期而異4)。
抗VEGF療法可作為重症ROP的第一線治療7),但對於第4-5期TRD,玻璃體手術為原則。
如果沒有向黃斑部進展的風險,可以觀察。但如果出現剝離範圍擴大或可能導致黃斑部偏移的增殖膜,應考慮早期手術。定期眼底檢查和OCT監測進展很重要。
增殖性糖尿病視網膜病變引起的TRD經由以下階段發生。
PDR引起的TRD之病理
缺血→VEGF→新生血管的連鎖反應是基礎。
纖維血管膜的收縮對視網膜產生牽引力,導致TRD。血-視網膜屏障(BRB)破壞導致的細胞激素滲漏促進增殖。
ROP引起的TRD之病理
視網膜血管未成熟→無血管區→缺血→新生血管是基礎。
出生後的高氧環境導致相對缺血,嵴上的纖維血管增殖向玻璃體內進展,導致第4-5期TRD。
TRD的基礎是血-視網膜屏障(BRB)的破壞。當BRB被破壞時,眼內炎症和新生血管環境增強,纖維血管增生進展。RPE、膠質細胞、巨噬細胞、纖維母細胞等參與增生膜的形成9)。
增生膜不僅涉及RPE,還複雜地涉及膠質細胞、巨噬細胞、纖維母細胞等。膠原蛋白的收縮導致對視網膜的牽引,從而引發TRD。
在穿孔性眼外傷後的TRD中,由於穿孔傷口的炎症細胞浸潤和BRB破壞,眼內增生進展。纖維母細胞和RPE的增生形成增生膜,該膜收縮產生牽引,導致TRD。
評估早期玻璃體手術治療糖尿病性重度玻璃體出血有效性的DRVS(Diabetic Retinopathy Vitrectomy Study)為TRD管理提供了基礎證據。在1型糖尿病的重度玻璃體出血中,早期玻璃體手術組2年後矯正視力達到20/40或以上的比例為25%(觀察組15%),在1型糖尿病中為36% vs 12%,顯示出顯著差異5)。2型糖尿病中未觀察到顯著差異5)。
在比較阿柏西普玻璃體內注射與玻璃體手術聯合全視網膜光凝(PRP)治療糖尿病性玻璃體出血的試驗中,24週時視力改善無顯著差異。但玻璃體出血的消退在手術組更快(4週 vs 36週)2)。
評估術前抗VEGF給藥有效性的統合分析報告了術中出血量和醫源性裂孔的減少3)。但有人指出抗VEGF注射後牽引可能暫時加重,建議注射後1-2週內早期手術2)。
隨著25G和27G系統以及廣角觀察系統的普及,PDR源性TRD的微創玻璃體手術適應症已擴大1)。小切口技術有助於減少術後炎症和早期恢復,其在門診手術中的應用正在增加8, 9)。
在DRCR Protocol S中,抗VEGF(ranibizumab)在2年時顯示對PRP的非劣效性2)。然而,進展為TRD的比率無顯著差異,且已存在TRD時無法單獨使用抗VEGF處理。抗VEGF在預防TRD方面可考慮,但TRD發生後,玻璃體手術是根本治療。
通常不能期望僅靠抗VEGF注射改善TRD。抗VEGF對新生血管消退有效,但無法控制現有纖維增殖膜的收縮,甚至有報告指出注射後牽引惡化2)。TRD的治療原則是玻璃體手術。術前輔助使用抗VEGF可能有用,有研究顯示可減少術中出血和醫源性裂孔3)。