前节所见
羊脂状角膜后沉着物(KP):整齐密集排列覆盖整个角膜内皮,或呈下方为主的Arlt三角模式。随时间推移可伴有色素。
前房炎症:可见炎症细胞和房水闪辉。虹膜前后粘连和虹膜萎缩少见。
眼压升高:HSV ARN中发生率高且程度重(平均约35 mmHg)。VZV ARN中约半数有高眼压(平均约25 mmHg)。即使无高眼压的病例,与对侧健眼相比也常显示6 mmHg以上的眼压差。

急性视网膜坏死(ARN)是一种坏死性疱疹性视网膜病变,于1971年由浦山等人首次报道为“桐泽型葡萄膜炎”。2) 当时描述了6例前所未有的暴发性葡萄膜炎,成为ARN这一疾病概念的全球起点。
其特点是发生于免疫功能正常的健康个体,病原体为HSV-1、HSV-2和VZV。发病后出现快速视网膜坏死和眼压升高,若不治疗会导致失明,因此被归类为眼科急症。根据葡萄膜炎诊疗指南(2019年)的全国调查,2002年调查报告41例(占所有葡萄膜炎的1.3%),2009年调查报告53例(1.4%)。1)
在免疫功能低下患者中,同一疱疹病毒可引起不同疾病类型。CMV视网膜炎和进行性外层视网膜坏死(PORN)是免疫功能低下者的疾病,而ARN被定位为免疫功能正常者的疾病。
流行病学上,年发病率为0.5~0.63/百万人(英国)11),多见于50~70岁的免疫功能正常成人。发病形式三分之二为单眼,三分之一为双眼(双侧ARN;BARN)13)。近年来,有报道与免疫检查点抑制剂(ICI)12)、那他珠单抗13)、富马酸二甲酯(DMF)14)等免疫抑制药物相关。也有白内障手术15)和COVID-19感染16)作为触发因素的病例报道。
这是急性视网膜坏死(ARN)的别名,是1971年浦山等人以其恩师桐泽长德的名字命名的历史名称。即使现在国际疾病名称ARN已确立,特别是在日本,有时仍使用桐泽型葡萄膜炎这一术语。
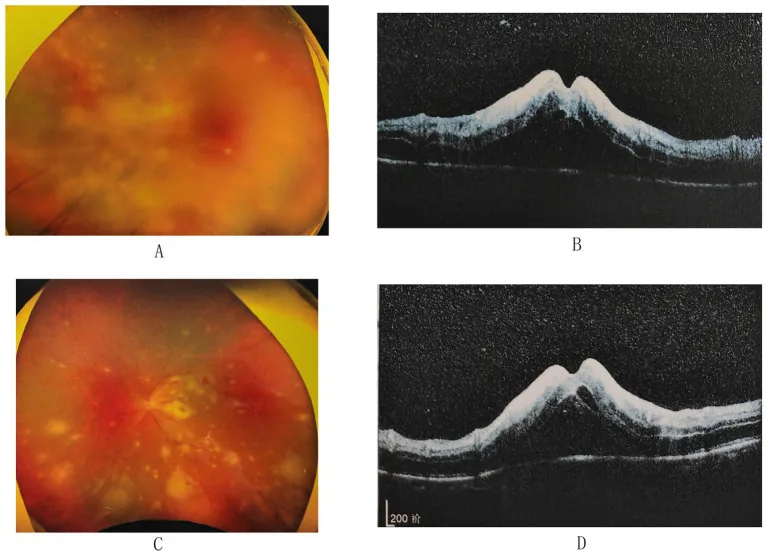
突然发作的充血、眼痛、畏光、视物模糊、飞蚊症和视力下降。初期以前部葡萄膜炎症状(充血、眼痛、畏光)为先导,随着视网膜病变进展,视力迅速下降。
前节所见
羊脂状角膜后沉着物(KP):整齐密集排列覆盖整个角膜内皮,或呈下方为主的Arlt三角模式。随时间推移可伴有色素。
前房炎症:可见炎症细胞和房水闪辉。虹膜前后粘连和虹膜萎缩少见。
眼压升高:HSV ARN中发生率高且程度重(平均约35 mmHg)。VZV ARN中约半数有高眼压(平均约25 mmHg)。即使无高眼压的病例,与对侧健眼相比也常显示6 mmHg以上的眼压差。
眼底及视网膜所见
周边视网膜黄白色颗粒状病变:出现在多个部位,向全周和后极迅速扩大。抗病毒治疗后约1周停止进展,转变为融合的地图状白色病变。
视网膜动脉炎:血管鞘和闭塞。特征性的棒状静脉旁出血。
其他:视乳头充血肿胀、炎性玻璃体混浊。棒状静脉旁出血、扇形边缘(scalloped edges)和Kyrieleis动脉炎(小动脉旁的黄白色病变)也是特征性表现。
荧光眼底血管造影显示闭塞性动脉炎模式和视乳头强荧光。OCT检查显示坏死性视网膜炎部位相应的脉络膜增厚(厚脉络膜),如报道所述18),作为新的诊断性发现受到关注。
视网膜周边的黄白色颗粒状病变(病毒增殖部位)会向全周和后极方向扩展,但使用抗病毒药物等治疗后,其进展约在1周内停止。随后,各颗粒状病变融合成浓厚、边界清晰的地图状白色病变(病毒直接损伤+闭塞性血管炎导致的循环障碍的复合作用)。
治疗开始后约1周,前房症状减轻,眼压恢复正常,但前房炎症可能持续数年。发病后约3~4周,玻璃体机化导致不完全性后玻璃体脱离,极度变薄、脆弱的视网膜坏死部位受到玻璃体的强烈牵拉,形成多发裂孔。结果,约70%的病例发生视网膜脱离。
| 致病病毒 | 特征性患者群体 | 相关全身疾病 |
|---|---|---|
| HSV-1 | 中老年人 | 有疱疹性脑炎病史或合并 |
| HSV-2 | 年轻人 | 与脑膜炎相关 |
| VZV | 中老年人 | 有合并脑膜炎的报道 |
约70%的病例发生视网膜脱离,最终三分之二的眼睛视力降至0.1以下,是一种预后不良的疾病。但与首发眼相比,后发病的另眼(约15%发病)的病灶扩散有限,视力预后相对较好。
ARN由疱疹病毒在眼内再激活引起。初次感染后,潜伏在三叉神经节和脊神经后根神经节的病毒,在宿主免疫平衡改变时再激活,通过神经轴突到达眼部。
病理机制包括病毒直接细胞损伤,以及为清除病毒而募集的炎症细胞引起的闭塞性血管炎和视网膜缺血,从而加重组织损伤。5)
| 项目 | 内容 |
|---|---|
| 1a | 前房炎症细胞或羊脂状角膜后沉着物 |
| 1b | 周边视网膜一处或多处黄白色病变(初期呈颗粒状至斑片状,逐渐融合) |
| 1c | 视网膜动脉炎 |
| 1d | 视盘充血 |
| 1e | 炎症性玻璃体混浊 |
| 1f | 眼压升高 |
| 2a | 视网膜病变快速沿圆周方向扩展 |
| 2b | 发生视网膜裂孔或视网膜脱离 |
| 2c | 视网膜血管闭塞 |
| 2d | 视神经萎缩 |
| 2e | 对抗病毒药物有反应 |
| 3 | 眼内液PCR或抗体比值(Q值)检测HSV-1、HSV-2或VZV任一阳性 |
确诊(病毒确认组):存在初期眼部表现1a和1b,且满足至少1项临床病程项目+病毒检测阳性。
临床诊断(病毒未确认组):至少4项包括初期眼部表现1a和1b,且满足至少2项临床病程项目。
该标准由Takase等人(2015)开发并验证。4)
眼内液(房水或玻璃体液)PCR是病毒鉴定中敏感性和特异性最高的诊断方法。1) 多重PCR(先进医疗)可鉴定多种病毒,有助于鉴别诊断。
抗体比值(Q值:Goldmann-Witmer系数)也用作辅助诊断。但发病10天内眼内抗体产生不足,易出现假阴性,此期间应优先进行PCR。仅凭血清抗体滴度无法进行病因诊断。1)
| 疾病 | 免疫状态 | 主要特征 |
|---|---|---|
| PORN(进行性外层视网膜坏死) | 严重免疫缺陷(如HIV CD4 <50) | 前房炎症轻微、后极部为主、快速进展 |
| CMV视网膜炎 | 免疫缺陷 | 伴出血的缓慢扩大、早期前房炎症轻微 |
| 眼弓形虫病 | 免疫功能正常至缺陷 | 局灶性肉芽肿性视网膜炎、邻近瘢痕 |
| 眼内淋巴瘤/肿瘤性病变 | 中老年人 | 玻璃体细胞、视网膜下浸润、脑病变。罕见情况下转移性肿瘤可表现为ARN样 17) |
| 儿童非典型病例 | 儿童 | 有渗出性视网膜脱离等非典型表现的病例报告,若偏离典型表现应扩大鉴别诊断 19) |
是的。如果符合临床诊断标准(病毒未确认组),无需等待PCR结果即可开始抗病毒治疗。发病10天内PCR假阴性率高,且病变进展迅速,因此根据ASAP原则,如果诊断确信,立即开始治疗是标准做法。
遵循ASAP原则,参考国内指南和已报道的治疗系列,尽快开始四大支柱治疗。1, 5, 6)
| 药物 | 剂量和用法 | 疗程 |
|---|---|---|
| 阿昔洛韦注射液(舒维疗注射液) | 10 mg/kg 溶于至少200 mL液体中,静脉滴注2小时以上,每日3次 | 初始2周 |
| 伐昔洛韦片(维德思)[无法静脉滴注时] | 500 mg,6片,分3次 | 初始2周 |
| 伐昔洛韦片(维德思)[持续治疗] | 500 mg,6片,分3次 | 初始治疗后额外2周 |
| 倍他米松滴眼液(Rinderon 0.1%) | 每日6次 → 炎症减轻后每日2-4次 | 炎症期间 |
| 美多丽M滴眼液(0.4%) | 每日1次 | 前房炎症期间 |
| 倍他米松注射液(Rinderon注射液) | 8 mg/日×5天 → 6 mg×4天 → 4 mg×4天,静脉滴注 | 抗病毒药物开始后24-48小时起 |
| 法莫替丁片(高舒达20 mg) | 2片,分2次,早晚服用 | 全身使用类固醇期间 |
| 阿司匹林肠溶片(拜阿司匹灵100 mg) | 1片,每日1次 | 4周 |
除全身给药外,联合玻璃体内注射膦甲酸钠(2.4 mg/0.1 mL)可改善视力结局并降低视网膜脱离率。7, 8) 尤其在重症病例或视力受到紧迫威胁时考虑使用。5)
手术步骤:
并非必须。有时会进行屏障激光(在坏死病变的后极侧进行光凝),但目前有限证据表明其能确实预防视网膜脱离。考虑到坏死区域的脆弱性和牵拉力,一旦发生脱离,玻璃体手术(硅油填充)是根本的治疗方法。
ARN的发病是由于疱疹病毒(HSV-1、HSV-2、VZV)潜伏感染三叉神经节或脊神经后根神经节,在某些触发因素(免疫低下、衰老、压力等)下再激活并到达眼内所致。
病毒的直接细胞损伤:病毒在视网膜细胞内复制并导致细胞溶解。病毒增殖的部位肉眼可见为黄白色颗粒状病变。
闭塞性血管炎导致的缺血:为清除病毒而发生的炎症细胞浸润引起视网膜动脉周围的血管炎,导致血管闭塞和视网膜缺血。闭塞性血管炎引起的水肿和循环障碍形成边界清晰的地图状白色病变。
这两种机制共同作用,导致视网膜快速坏死、变薄和脆弱化。5)
发病后3-4周,玻璃体发生机化,导致不完全性玻璃体后脱离。此时,极度变薄和脆弱的坏死视网膜受到来自玻璃体的强烈牵引,形成多发裂孔。坏死区域的变薄和牵引力的共同作用导致约70%的病例发生视网膜脱离。
传统的标准治疗是静脉注射阿昔洛韦的住院治疗,但已有病例系列报告显示口服伐昔洛韦或泛昔洛韦可使活动性视网膜炎消退。9) AAO报告也指出口服或静脉注射抗病毒药物的初始治疗是有效的,但根据重症程度和全身状态,通常优先考虑静脉滴注。5)
一项回顾性研究显示,玻璃体内注射膦甲酸钠(2.4 mg/0.1 mL)联合全身治疗,特别是在VZV ARN中,添加玻璃体内注射可能改善视力预后。7) 它可能实现高局部浓度同时最小化全身毒性,重症病例的诱导治疗标准化是研究课题。
通过眼内液定量PCR监测病毒载量,据报道不仅有助于诊断,还可能有助于评估治疗反应。10) 然而,重复采样的侵入性和测量方法的标准化等问题仍存在,将其纳入日常诊疗面临挑战。
OCT上的脉络膜增厚(厚脉络膜)已被报道为反映急性视网膜坏死活动性的表现。在一例继发性VZV-ARN病例中,OCT上的厚脉络膜与坏死性视网膜炎区域一致出现,提示其可能作为治疗后随访中的活动性标志物。18)
有报告称,一例对阿昔洛韦和更昔洛韦耐药的EBV-ARN病例,膦甲酸钠4800 mg/日静脉注射有效。20) 当病原体是VZV或HSV以外的病毒时,标准治疗可能效果不佳,通过PCR鉴定病原病毒对确定治疗方案很重要。
随着免疫检查点抑制剂(ICI)的普及,需要注意VZV再激活导致ARN发病的风险。12) 此外,COVID-19感染后HSV/VZV再激活导致ARN的报告相继出现,与免疫抑制治疗相关的ARN未来可能继续增加。14)16)
日本眼炎症学会ぶどう膜炎診療ガイドライン作成委員会. ぶどう膜炎診療ガイドライン. 日眼会誌. 2019;123(6):635-796.
Urayama A, Yamada N, Sasaki T, et al. Unilateral acute uveitis with periarteritis and retinal detachment. Jpn J Clin Ophthalmol. 1971;25:607-619.
Standardization of Uveitis Nomenclature (SUN) Working Group. Classification criteria for acute retinal necrosis syndrome. Ophthalmology. 2021;128(12):1974-1980. doi:10.1016/j.ophtha.2021.11.011. PMID: 34807625.
Takase H, Okada AA, Goto H, et al. Development and validation of new diagnostic criteria for acute retinal necrosis. Jpn J Ophthalmol. 2015;59(1):14-20. doi:10.1007/s10384-014-0362-0. PMID: 25492579.
Schoenberger SD, Kim SJ, Thorne JE, et al. Diagnosis and Treatment of Acute Retinal Necrosis: A Report by the American Academy of Ophthalmology. Ophthalmology. 2017;124(3):382-392. doi:10.1016/j.ophtha.2016.11.007. PMID: 28094044.
Tibbetts MD, Shah CP, Young LH, et al. Treatment of acute retinal necrosis. Ophthalmology. 2010;117(4):818-824. doi:10.1016/j.ophtha.2009.09.001. PMID: 20110127.
Wong R, Pavesio CE, Laidlaw DA, et al. Acute retinal necrosis: the effects of intravitreal foscarnet and virus type on outcome. Ophthalmology. 2010;117(3):556-560. doi:10.1016/j.ophtha.2009.08.003. PMID: 20031221.
Flaxel CJ, Yeh S, Lauer AK. Combination systemic and intravitreal antiviral therapy in the management of acute retinal necrosis syndrome. Ophthalmic Surg Lasers Imaging Retina. 2013;44(6):521-526.
Aizman A, Johnson MW, Elner SG. Treatment of acute retinal necrosis syndrome with oral antiviral medications. Ophthalmology. 2007;114(2):307-312. doi:10.1016/j.ophtha.2006.06.058. PMID: 17123607.
Asano S, Yoshikawa T, Kimura H, et al. Monitoring herpesvirus DNA in three cases of acute retinal necrosis by real-time PCR. J Clin Virol. 2004;29(3):206-209. PMID: 15002491.
Cochrane TF, Silvestri G, McDowell C, et al. Acute retinal necrosis in the United Kingdom: results of a prospective surveillance study. Eye (Lond). 2012;26(3):370-377.
Wang P, An M, Zhang M, et al. Acute retinal necrosis in a patient with cervical malignant tumor treated with sintilimab: a case report and literature review. Front Immunol. 2024;15:1301329.
Cheraqpour K, Ahmadraji A, Rashidinia A, et al. Acute retinal necrosis caused by co-infection with multiple viruses in a natalizumab-treated patient: a case report and brief review of literature. BMC Ophthalmol. 2021;21:337.
Paisey C, Curtin K, Epps SJ, et al. Acute retinal necrosis associated with dimethyl fumarate. Mult Scler J. 2025;31(12):1506-1508.
Luo T, Wang L, Zhang L, et al. Acute retinal necrosis following cataract surgery: a case of VZV reactivation and successful management. BMC Ophthalmol. 2025;25:131.
Gonzalez MP, Rios R, Pappaterra M, et al. Reactivation of acute retinal necrosis following SARS-CoV-2 infection. Case Rep Ophthalmol Med. 2021;2021:7336488.
Rahman EZ, Shah P, Shah R. Metastatic squamous cell carcinoma masquerading as acute retinal necrosis. Am J Ophthalmol Case Rep. 2023;32:101934.
Harbeck K, Ericksen C, Johnson W, et al. Pachychoroid associated with acute retinal necrosis secondary to varicella zoster virus. J Vitreoretinal Dis. 2024;8(2):196-199.
Perhiar BA, Siddiqui MAR, Ibrahim S. Acute retinal necrosis with exudative retinal detachment in a child. BMJ Case Rep. 2021;14:e245984.
Suzuki K, Namba K, Hase K, et al. A case of Epstein-Barr virus acute retinal necrosis successfully treated with foscarnet. Am J Ophthalmol Case Rep. 2022;25:101363.