จอประสาทตา อักเสบชนิดเฉียบพลันเนื้อตาย (ARN ) คือ โรคจอประสาทตา จากเชื้อเฮอร์ปีส์ชนิดเนื้อตาย รายงานครั้งแรกโดย Urayama และคณะในปี 1971 ภายใต้ชื่อ “ม่านตาอักเสบ ชนิดคิริซาวะ” 2) มีการอธิบายผู้ป่วย 6 รายว่าเป็นม่านตาอักเสบ ชนิดรุนแรงที่ไม่เคยพบมาก่อน และกลายเป็นจุดเริ่มต้นระดับโลกของแนวคิดโรค ARN
มีลักษณะเฉพาะคือเกิดในบุคคลที่มีสุขภาพดีและมีภูมิคุ้มกันปกติ ไวรัสที่ก่อโรคคือ HS V-1, HS V-2 และ VZV หลังจากเริ่มเกิดโรค จะเกิดเนื้อตายของจอประสาทตา อย่างรวดเร็วและความดันลูกตา สูง และจัดเป็นภาวะฉุกเฉินทางจักษุวิทยา เพราะทำให้ตาบอดหากไม่รักษา ตามการสำรวจระดับชาติของแนวทางการรักษาม่านตาอักเสบ (2019) มีรายงาน 41 รายในการสำรวจปี 2002 (1.3% ของม่านตาอักเสบ ทั้งหมด) และ 53 รายในการสำรวจปี 2009 (1.4%) 1)
ในผู้ป่วยที่มีภูมิคุ้มกันบกพร่อง ไวรัสเฮอร์ปีส์ชนิดเดียวกันทำให้เกิดรูปแบบโรคที่แตกต่างกัน จอประสาทตาอักเสบจาก CMV และจอประสาทตา อักเสบชนิดเนื้อตายชั้นนอกแบบลุกลาม (PORN ) เป็นโรคของผู้มีภูมิคุ้มกันบกพร่อง ในขณะที่ ARN เป็นโรคของบุคคลที่มีภูมิคุ้มกันปกติ
ทางระบาดวิทยา อุบัติการณ์รายปีคือ 0.5-0.63 ต่อล้านคน (สหราชอาณาจักร) 11) และพบบ่อยที่สุดในผู้ใหญ่ที่มีภูมิคุ้มกันปกติอายุ 50-70 ปี ประมาณสองในสามของกรณีเป็นตาเดียว หนึ่งในสามเป็นตาสองข้าง (BARN ) 13) ในช่วงไม่กี่ปีที่ผ่านมา มีรายงานความสัมพันธ์กับสารยับยั้งจุดตรวจสอบภูมิคุ้มกัน (ICI ) 12) , natalizumab 13) และ dimethyl fumarate (DMF) 14) นอกจากนี้ยังมีรายงานกรณีที่ถูกกระตุ้นโดยการผ่าตัดต้อกระจก 15) หรือการติดเชื้อ COVID-19 16)
Q
ม่านตาอักเสบชนิดคิริซาวะคืออะไร?
A
เป็นอีกชื่อหนึ่งของจอประสาทตา อักเสบชนิดเฉียบพลันเนื้อตาย (ARN ) ตั้งชื่อโดย Urayama และคณะในปี 1971 เพื่อเป็นเกียรติแก่ครูของพวกเขา Kirisawa Chotoku แม้ว่าชื่อสากล ARN จะเป็นที่ยอมรับแล้ว แต่คำว่าม่านตาอักเสบ ชนิดคิริซาวะยังคงใช้เป็นครั้งคราว โดยเฉพาะในญี่ปุ่น
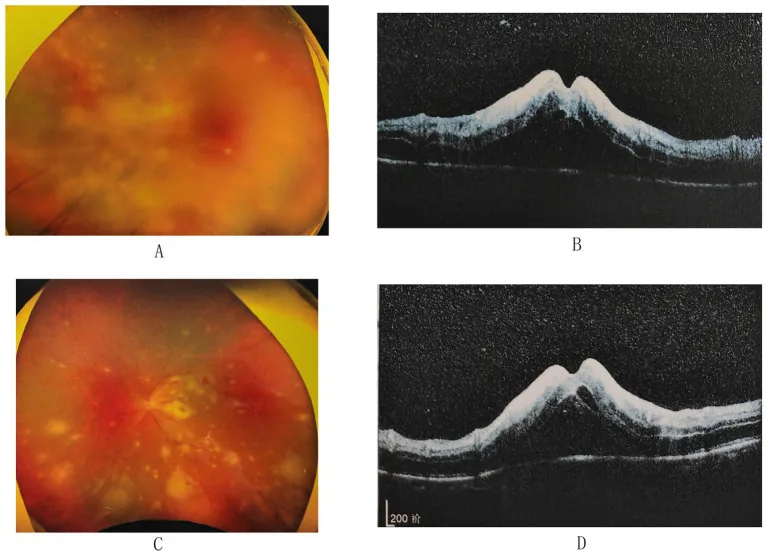
ภาพถ่ายจอตาและ OCT ของจอตาตายเฉียบพลัน แสดงรอยโรคจอตาสีขาวเหลือง, บวมของหัวประสาทตา, การเปลี่ยนแปลงของหลอดเลือดแบบอุดตัน, จอตาบวมน้ำ Zhu W, et al. Atypical presentation of acute retinal necrosis mimicking Vogt-Koyanagi-Harada disease leading to misdiagnosis: a case report. Front Med (Lausanne). 2024. Figure 2. PM
CI D: PMC11620890. License: CC BY.
ภาพถ่ายจอตาแสดงรอยโรคจอตาตายสีขาวเหลืองกระจาย, บวมของหัวประสาทตา, เลือดออกในจอตา, และเส้นเลือดขาว OCT แสดงจอตาหนาตัวและของเหลวในและใต้จอตา ซึ่งเป็นลักษณะทางคลินิกของจอตาตายเฉียบพลัน
อาการเริ่มต้นอย่างฉับพลัน: ตาแดง , ปวดตา , กลัวแสง, ตาพร่า , เห็นจุดลอย, และสายตาลดลง ในระยะแรกจะมีอาการของม่านตาอักเสบ ส่วนหน้า (ตาแดง , ปวดตา , กลัวแสง) นำมาก่อน จากนั้นสายตาจะลดลงอย่างรวดเร็วเมื่อรอยโรคจอตาดำเนินไป
อาการของส่วนหน้าของตา
ตะกอนที่กระจกตา แบบมันหมู (KP) : เรียงตัวหนาแน่นเป็นระเบียบปกคลุมผิวด้านหลังของกระจกตา ทั้งหมด หรือเป็นรูปสามเหลี่ยมของ Arlt ด้านล่าง เมื่อเวลาผ่านไปจะมีเม็ดสี
การอักเสบในช่องหน้าตา : พบเซลล์อักเสบและ flare การยึดติดของม่านตา ทั้งด้านหน้าและด้านหลังและการฝ่อของม่านตา พบได้น้อย
ความดันลูกตา สูงARN จาก HS V พบบ่อยและสูง (เฉลี่ย 35 mmHg) ใน ARN จาก VZV ครึ่งหนึ่งของกรณีมีความดันลูกตา สูง (เฉลี่ย 25 mmHg) แม้ในกรณีที่ไม่มีความดันลูกตา สูง มักมีความแตกต่าง ≥6 mmHg เมื่อเทียบกับตาข้างปกติ
อาการของจอตาและอวัยวะภายในลูกตา
รอยโรคเม็ดเล็กสีขาวเหลืองที่จอตาส่วนปลาย : ปรากฏในหลายตำแหน่ง ขยายตัวอย่างรวดเร็วทั้งในแนวรอบและไปทางขั้วหลัง หยุดขยายตัวหลังจากให้ยาต้านไวรัสประมาณ 1 สัปดาห์ เปลี่ยนเป็นรอยโรคสีขาวแบบแผนที่ที่รวมตัวกัน
หลอดเลือดแดงจอตาอักเสบ : ปลอกหุ้มหลอดเลือดและการอุดตัน เลือดออกตามหลอดเลือดดำรูปกระบองเป็นลักษณะเฉพาะ
อื่นๆ : หัวประสาทตาแดง และบวม, ขุ่นของวุ้นตา จากการอักเสบ เลือดออกตามหลอดเลือดดำรูปกระบอง, ขอบหยักเป็นคลื่น (scalloped edges), และ Kyrieleis’ Arteriolitis (รอยโรคสีขาวเหลืองตามหลอดเลือดแดงเล็ก) ก็เป็นลักษณะเฉพาะเช่นกัน
การตรวจหลอดเลือดด้วยฟลูออเรสซีน แสดงรูปแบบหลอดเลือดแดงอักเสบแบบอุดตันและการเรืองแสงเกินของหัวประสาทตา ในการตรวจ OCT มีรายงานการหนาตัวของคอรอยด์ (pachychoroid) ที่สอดคล้องกับตำแหน่งของจอตาอักเสบแบบตาย 18) ซึ่งกำลังเป็นที่สนใจในฐานะลักษณะการวินิจฉัยใหม่
รอยโรคแบบเม็ดสีเหลืองขาวบริเวณจอประสาทตา ส่วนปลาย (บริเวณที่มีการเพิ่มจำนวนของไวรัส) จะขยายตัวเป็นวงรอบไปทางขั้วหลัง แต่การดำเนินโรคจะหยุดภายในประมาณ 1 สัปดาห์หลังจากให้ยาต้านไวรัส หลังจากนั้น รอยโรคแบบเม็ดจะรวมตัวกันกลายเป็นรอยโรคสีขาวหนาแน่นขอบเขตชัดเจนคล้ายแผนที่ (เป็นการรวมกันของความเสียหายโดยตรงจากไวรัสและความผิดปกติของการไหลเวียนจากหลอดเลือดอักเสบชนิดอุดตัน)
ประมาณ 1 สัปดาห์หลังจากเริ่มการรักษา อาการในช่องหน้าม่านตา จะลดลงและความดันลูกตา จะกลับสู่ปกติ แต่อาการอักเสบในช่องหน้าม่านตา อาจคงอยู่นานหลายปี ประมาณ สัปดาห์ที่ 3-4 หลังจากเริ่มมีอาการ จะเกิดภาวะวุ้นตา หลุดแบบไม่สมบูรณ์เนื่องจากวุ้นตา กลายเป็นพังผืด ทำให้เกิดการดึงรั้งอย่างรุนแรงจากวุ้นตา บนบริเวณจอประสาทตา ที่ตายและบางมาก เกิดเป็นรอยฉีกขาดหลายแห่ง ผลที่ตามมาคือ จอประสาทตาลอก ในประมาณ 70% ของผู้ป่วย
ไวรัสที่เป็นสาเหตุ กลุ่มผู้ป่วยที่มีลักษณะเฉพาะ โรคทางระบบที่เกี่ยวข้อง HS V-1วัยกลางคนขึ้นไป ประวัติหรือภาวะแทรกซ้อนของโรคสมองอักเสบจากเริม HS V-2ผู้ป่วยอายุน้อย ความสัมพันธ์กับเยื่อหุ้มสมองอักเสบ VZV วัยกลางคนขึ้นไป รายงานภาวะแทรกซ้อนของเยื่อหุ้มสมองอักเสบ
Q
การมองเห็นลดลงมากน้อยเพียงใด?
A
ประมาณ 70% ของผู้ป่วยเกิดจอประสาทตาลอก และในที่สุดสองในสามของดวงตามีค่าการมองเห็น 0.1 หรือน้อยกว่า ทำให้เป็นโรคที่มีการพยากรณ์โรคไม่ดี อย่างไรก็ตาม เมื่อเทียบกับดวงตาข้างแรกที่เกิดโรค การขยายตัวของรอยโรคในดวงตาข้างที่สอง (ซึ่งเกิดขึ้นประมาณ 15% ของผู้ป่วย) มีจำกัด และการพยากรณ์โรคด้านการมองเห็น ค่อนข้างดี
ARN เกิดจากการกระตุ้นเชื้อไวรัสเริมภายในดวงตาอีกครั้ง หลังการติดเชื้อครั้งแรก ไวรัสจะแฝงตัวอยู่ในปมประสาทไทรเจมินัลและปมประสาทรากหลังของไขสันหลัง จากนั้นจะถูกกระตุ้นอีกครั้งเมื่อสมดุลภูมิคุ้มกันของโฮสต์เปลี่ยนแปลง และเดินทางไปยังดวงตาผ่านแอกซอนของเส้นประสาท
HS V-2HS V-1 และ VZVARN ที่เกิดจาก HS V-1 มักเกิดในผู้ป่วยที่มีประวัติหรือภาวะแทรกซ้อนของโรคสมองอักเสบจากเริมARN ที่เกิดจาก HS V-2 และ VZV สัมพันธ์กับเยื่อหุ้มสมองอักเสบ
การติดเชื้อเริมในปัจจุบันหรือประวัติ : แม้แต่ประวัติโรคงูสวัดเมื่อกว่า 30 ปีที่แล้วก็สามารถทำให้เกิด ARN จากการกระตุ้น VZV อีกครั้ง ประวัติโรคสมองอักเสบจากเริมก็เป็นสาเหตุได้เช่นกันสเตียรอยด์ เฉพาะที่สเตียรอยด์ เฉพาะที่ดวงตาเป็นเวลานานอาจเป็นตัวกระตุ้นที่พบได้น้อยอายุมาก : สัมพันธ์กับความเสี่ยงของ ARN จาก VZVยากดภูมิคุ้มกัน : การลดลงของเซลล์ T CD8+ และภูมิคุ้มกันของเซลล์ T ที่จำเพาะต่อไวรัสถือเป็นกุญแจสำคัญในการกระตุ้นอีกครั้ง และมีรายงานเกี่ยวกับยาต่อไปนี้:
natalizumab (ยารักษาโรคปลอกประสาทเสื่อมแข็ง): ยับยั้งการเคลื่อนย้ายเม็ดเลือดขาวเข้าสู่ระบบประสาทส่วนกลาง ทำให้อัตราส่วน CD4/CD8 ลดลง13)
DMF (ไดเมทิลฟูมาเรต): ภูมิคุ้มกันของเซลล์ T CD8+ และเซลล์ T ที่จำเพาะต่อ VZV ลดลง 14)
ICI (ยาสกัดกั้นจุดตรวจภูมิคุ้มกัน ): การกระตุ้น VZV อีกครั้งโดยซินทิลิแมบ 12)
การผ่าตัดต้อกระจก : อาจกระตุ้นให้ VZV กลับมาทำงานอีกครั้งในฐานะตัวกระตุ้นทางกายภาพ 15)
การติดเชื้อ COVID-19: การกระตุ้น HS V อีกครั้งเนื่องจากภาวะลิมโฟไซต์ T CD3+ CD8+ ต่ำ 16)
สมมติฐานว่ามีภูมิคุ้มกันปกติ: หากมีภาวะภูมิคุ้มกันบกพร่อง (การติดเชื้อ HIV หรือการใช้ยากดภูมิคุ้มกัน) ให้พิจารณาจอประสาทตาอักเสบจาก CMV หรือ PORN ก่อน
พยาธิสรีรวิทยาคือความเสียหายของเซลล์โดยตรงจากไวรัส ร่วมกับหลอดเลือดอักเสบอุดตันและจอประสาทตา ขาดเลือดจากเซลล์อักเสบที่ถูกเรียกมาเพื่อกำจัดไวรัส ซึ่งเพิ่มความเสียหายของเนื้อเยื่อ 5)
รายการ เนื้อหา 1a เซลล์อักเสบในช่องหน้าหรือคราบไขมันคล้ายมันหมูบนผิวด้านหลังของกระจกตา 1b รอยโรคสีเหลืองขาวหนึ่งจุดหรือมากกว่าที่จอประสาทตา ส่วนปลาย (ระยะแรกเป็นเม็ดเล็กถึงเป็นปื้น จากนั้นรวมตัวกัน) 1c หลอดเลือดแดงจอประสาทตา อักเสบ 1d จานประสาทตา แดง1e วุ้นตา ขุ่นจากการอักเสบ1f ความดันลูกตา สูง2a รอยโรคจอประสาทตา ขยายตัวอย่างรวดเร็วในแนวเส้นรอบวง 2b เกิดจอประสาทตาฉีกขาด หรือจอประสาทตาลอก 2c หลอดเลือดจอประสาทตา อุดตัน 2d ประสาทตาฝ่อ 2e ตอบสนองต่อยาต้านไวรัส 3 PCR ของเหลวในลูกตาหรืออัตราส่วนแอนติบอดี (ค่า Q) ให้ผลบวกต่อ HS V-1, HS V-2 หรือ VZV อย่างใดอย่างหนึ่ง
การวินิจฉัยที่แน่นอน (กลุ่มที่ยืนยันไวรัส) : พบอาการทางตาเริ่มต้น 1a และ 1b ร่วมกับรายการในประวัติโรคอย่างน้อย 1 รายการ และผลตรวจไวรัสเป็นบวก
การวินิจฉัยทางคลินิก (กลุ่มที่ไม่ยืนยันไวรัส) : พบอาการอย่างน้อย 4 รายการรวมถึงอาการทางตาเริ่มต้น 1a และ 1b ร่วมกับรายการในประวัติโรคอย่างน้อย 2 รายการ
เกณฑ์นี้ได้รับการพัฒนาและตรวจสอบโดย Takase (2015) และคณะ 4)
ข้อบังคับ : จอประสาทตา อักเสบชนิดเนื้อตายที่ส่งผลต่อจอประสาทตา ส่วนปลายข้อกำหนดเพิ่มเติมอย่างใดอย่างหนึ่งต่อไปนี้:
PCR ของเหลวในช่องหน้าหรือวุ้นตา ให้ผลบวกต่อ HS V หรือ VZV
ลักษณะทางคลินิกที่จำเพาะ (จอประสาทตา อักเสบแบบรอบด้านหรือแบบรวมตัว, ปลอกหุ้มหลอดเลือดหรือการอุดตัน, วุ้นตา อักเสบมากกว่าเล็กน้อย)
PCR โดยใช้ของเหลวในลูกตา (ของเหลวในช่องหน้าหรือวุ้นตา ) เป็นวิธีการวินิจฉัยที่ดีที่สุดในแง่ความไวและความจำเพาะสำหรับการระบุไวรัส 1) PCR แบบหลายเชื้อ (การแพทย์ขั้นสูง) ช่วยให้ระบุไวรัสหลายชนิดได้และมีประโยชน์ในการวินิจฉัยแยกโรค
อัตราส่วนแอนติบอดี (ค่า Q: สัมประสิทธิ์ Goldmann-Witmer) ยังใช้เป็นการวินิจฉัยเสริม อย่างไรก็ตาม ภายใน 10 วันแรก หลังเริ่มมีอาการ การผลิตแอนติบอดีในลูกตายังไม่เพียงพอ ทำให้เกิดผลลบปลอมได้ง่าย ในช่วงนี้ควรใช้ PCR เป็นหลัก ไม่สามารถใช้ระดับแอนติบอดีในซีรั่มเพียงอย่างเดียวในการวินิจฉัยสาเหตุได้ 1)
โรค ภาวะภูมิคุ้มกัน ลักษณะสำคัญ PORN (เนื้อตายของจอประสาทตา ชั้นนอกแบบลุกลาม)ภาวะภูมิคุ้มกันบกพร่องรุนแรง (เช่น HIV CD4 <50) การอักเสบส่วนหน้าน้อย, เด่นที่ขั้วหลัง, ดำเนินโรคเร็ว จอประสาทตาอักเสบจาก CMV ภาวะภูมิคุ้มกันบกพร่อง ขยายขนาดช้าๆ ร่วมกับเลือดออก, การอักเสบส่วนหน้าน้อยในช่วงแรก ท็อกโซพลาสโมซิสที่ตา ภูมิคุ้มกันปกติถึงบกพร่อง จอประสาทตา อักเสบชนิดแกรนูโลมาที่จำเพาะจุด, แผลเป็นข้างเคียงมะเร็งต่อมน้ำเหลืองในลูกตา / รอยโรคเนื้องอก วัยกลางคนถึงสูงอายุ เซลล์ในวุ้นตา , การแทรกซึมใต้จอประสาทตา , รอยโรคในสมอง. พบไม่บ่อยที่เนื้องอกแพร่กระจายมีลักษณะคล้าย ARN 17) กรณีไม่ปกติในเด็ก เด็ก มีรายงานกรณีที่มีจอประสาทตาลอก แบบมีน้ำใต้จอประสาทตา และลักษณะอื่นที่ไม่ปกติ; หากแตกต่างจากภาพทั่วไป ควรขยายการวินิจฉัยแยกโรค 19)
ARN เป็นภาวะฉุกเฉินทางจักษุวิทยา หากพบจอประสาทตา อักเสบแบบเนื้อตาย (necrotizing retinitis) ภาวะวุ้นตา อักเสบ (vitritis) หรือจอประสาทตา อักเสบของหลอดเลือด (retinal vasculitis) ที่เริ่มจากบริเวณรอบนอก ควรเริ่มการรักษาด้วยยาต้านไวรัสทันทีโดยไม่รอผลการตรวจ
Q
เราจะเริ่มการรักษาหรือไม่แม้ว่า PCR จะเป็นลบ?
A
ใช่ หากเข้าเกณฑ์การวินิจฉัยทางคลินิก (กลุ่มที่ไม่ยืนยันไวรัส) เราจะเริ่มการรักษาด้วยยาต้านไวรัสโดยไม่รอผล PCR เนื่องจากอัตราผลลบปลอมของ PCR สูงในช่วง 10 วันแรกของการเกิดโรค และรอยโรคดำเนินไปอย่างรวดเร็ว หลักการคือเริ่มการรักษาทันทีเมื่อวินิจฉัยได้แน่ชัดตามหลักการ ASAP
ตามหลักการ ASAP โดยอ้างอิงแนวทางปฏิบัติของประเทศและชุดการรักษาที่มีรายงาน เริ่มการรักษาสี่เสาหลักโดยเร็วที่สุด 1, 5, 6)
A: Aciclovir (การรักษาด้วยยาต้านไวรัส)S: Steroid (การรักษาด้วยยาต้านการอักเสบ)A: Aspirin (การรักษาด้วยยาต้านการแข็งตัวของเลือด )P: Prophylaxis for retinal detachment (การป้องกันจอประสาทตาลอก )
ยา ขนาดและวิธีใช้ ระยะเวลา อะไซโคลเวียร์ชนิดฉีด (Zovirax ชนิดฉีด) 10 มก./กก. ละลายในสารละลายอย่างน้อย 200 มล. ให้ทางหลอดเลือดดำนาน 2 ชั่วโมงขึ้นไป วันละ 3 ครั้ง 2 สัปดาห์แรก ยาเม็ดวาลาไซโคลเวียร์ (Valtrex) [เมื่อไม่สามารถให้ทางหลอดเลือดดำได้] 500 มก. จำนวน 6 เม็ด แบ่งให้ 3 ครั้ง 2 สัปดาห์แรก ยาเม็ดวาลาไซโคลเวียร์ (Valtrex) [ต่อเนื่อง] 500 มก. จำนวน 6 เม็ด แบ่งให้ 3 ครั้ง เพิ่มอีก 2 สัปดาห์หลังการรักษาเริ่มต้น ยาหยอดตาเบตาเมทาโซน (Rinderon 0.1%) 6 ครั้ง/วัน → 2-4 ครั้ง/วันเมื่อการอักเสบลดลง ระหว่างที่มีการอักเสบ ยาหยอดตาไมดริน เอ็ม (0.4%) 1 ครั้ง/วัน ระหว่างที่มีการอักเสบของช่องหน้าลูกตา ยาฉีดเบตาเมทาโซน (Rinderon ฉีด) 8 มก./วัน × 5 วัน → 6 มก. × 4 วัน → 4 มก. × 4 วัน ให้ทางหลอดเลือดดำ 24-48 ชั่วโมงหลังจากเริ่มยาต้านไวรัส ยาเม็ดฟาโมทิดีน (Gaster 20 มก.) ครั้งละ 2 เม็ด วันละ 2 เวลา เช้า-เย็น ระหว่างการให้สเตียรอยด์ ทั่วร่างกาย ยาเม็ดแอสไพรินเคลือบลำไส้ (Bayer Aspirin 100 มก.) ครั้งละ 1 เม็ด วันละ 1 ครั้ง นาน 4 สัปดาห์
ประมาณ 15% ของผู้ป่วยจะเกิดรอยโรคที่ตาอีกข้างระหว่างดำเนินโรค เนื่องจากช่วงเวลาการเกิดระหว่างตาทั้งสองข้างมักอยู่ภายใน 1 เดือน จึงให้ยาต้านไวรัส (วาลาไซโคลเวียร์) ต่ออีก 2 สัปดาห์หลังจากสิ้นสุดการรักษาเริ่มต้น 2 สัปดาห์ รอยโรคที่ตาข้างหลังมักมีขอบเขตจำกัด และพยากรณ์โรคทางสายตาดีกว่าตาข้างแรก
นอกจากการให้ยาทั่วร่างกายแล้ว มีรายงานว่าการฉีดฟอสคาร์เนท (2.4 มก./0.1 มล.) เข้าแก้วตาร่วมด้วยช่วยให้ผลลัพธ์ทางสายตาดีขึ้นและลดอัตราจอประสาทตาลอก 7, 8) พิจารณาใช้โดยเฉพาะในกรณีรุนแรงหรือเมื่อใกล้จะกระทบต่อการมองเห็น 5)
การจี้เลเซอร์กั้นป้องกัน : อาจทำในระยะเม็ดเล็กทางด้านหลังของรอยโรคเนื้อตาย แต่หลักฐานเกี่ยวกับประสิทธิภาพในการป้องกันจอประสาทตาลอก มีจำกัด และยังไม่ได้รับการยืนยัน 5) การจี้ทำเป็น 3-4 แถวถัดจากด้านหลังของรอยโรคเม็ดเล็ก โดยไม่จี้ที่รอยโรคหรือด้านปลายการตัดแก้วตา : ทำเมื่อเกิดจอประสาทตาลอก (ประมาณ 70%)
ขั้นตอนการผ่าตัด :
การสลายเลนส์ด้วยคลื่นเสียงความถี่สูง
การล้างน้ำวุ้นตา ด้วยน้ำยาล้างที่เติมอะไซโคลเวียร์ 40 ไมโครกรัม/มิลลิลิตร (อยู่นอกเหนือการคุ้มครองของประกัน)
การตัดน้ำวุ้นตา (ตัดออกอย่างหมดจดเพื่อป้องกันการดึงรั้งจากน้ำวุ้นตา ที่เหลือ)
การจี้แสงในลูกตา: จี้ 3-4 แถวทางด้านหลังของรอยโรคแบบเม็ดทันที (ไม่จี้ที่รอยโรคหรือด้านรอบข้าง)
การรัดรอบด้วยยางซิลิโคนขนาด 9 มม.
การใส่น้ำมันซิลิโคน
ความดันลูกตาต่ำ หลังการใส่น้ำมันซิลิโคนความดันลูกตาต่ำ หลังการเอาน้ำมันออก สาเหตุเชื่อว่าเกิดจากความผิดปกติของซิลิอารีบอดี ้เนื่องจากการอักเสบรุนแรง บางครั้งจำเป็นต้องใส่น้ำมันซิลิโคนซ้ำ ควรพิจารณาเวลาที่เหมาะสมและข้อบ่งชี้ในการเอาน้ำมันออกอย่างรอบคอบการหดตัวของถุงเลนส์ที่เหลือ : หลังการผ่าตัดน้ำวุ้นตา การหดตัวของถุงเลนส์เกิดขึ้นเกือบทุกครั้ง จำเป็นต้องตัดถุงเลนส์ด้วยเลเซอร์แต่เนิ่นๆการใช้สเตียรอยด์ เฉพาะที่เพียงอย่างเดียวอันตราย : การใช้สเตียรอยด์ เฉพาะที่โดยไม่มีการรักษาด้วยยาต้านไวรัสอาจทำให้จอประสาทตา อักเสบดำเนินไปอย่างรวดเร็วและสูญเสียการมองเห็น ควรใช้ด้วยความระมัดระวัง
Q
จำเป็นต้องทำเลเซอร์จี้แสงเพื่อป้องกันเสมอหรือไม่?
A
ไม่จำเป็น บางครั้งอาจทำเลเซอร์กั้น (จี้แสงทางด้านหลังของรอยโรคเนื้อตาย) แต่หลักฐานที่แน่ชัดในการป้องกันจอประสาทตาลอก ยังมีจำกัด เมื่อพิจารณาถึงความเปราะบางของเนื้อตายและแรงดึงรั้ง หากเกิดจอประสาทตาลอก การผ่าตัดน้ำวุ้นตา (ใส่น้ำมันซิลิโคน) เป็นวิธีการรักษาที่ถาวร
ARN เกิดจากเชื้อไวรัสเริม (HS V-1, HS V-2, VZV) ติดเชื้อแฝงอยู่ที่ปมประสาทไทรเจมินัลหรือปมประสาทรากหลังของไขสันหลัง จากนั้นถูกกระตุ้นอีกครั้งโดยปัจจัยบางอย่าง (ภูมิคุ้มกันต่ำ อายุมากขึ้น ความเครียด ฯลฯ) และเดินทางไปถึงลูกตา
การทำลายเซลล์โดยตรงจากไวรัส : การเพิ่มจำนวนของไวรัสภายในเซลล์จอประสาทตา และการสลายเซลล์ บริเวณที่ไวรัสเพิ่มจำนวนจะสังเกตเห็นเป็นรอยโรคแบบเม็ดสีเหลืองขาวด้วยตาเปล่า
ภาวะขาดเลือดจากหลอดเลือดอักเสบอุดตัน : การแทรกซึมของเซลล์อักเสบเพื่อกำจัดไวรัสทำให้เกิดหลอดเลือดอักเสบรอบหลอดเลือดแดงจอตา นำไปสู่การอุดตันของหลอดเลือดและจอตาขาดเลือด อาการบวมน้ำและความผิดปกติของการไหลเวียนจากหลอดเลือดอักเสบอุดตันทำให้เกิดรอยโรคสีขาวคล้ายแผนที่ขอบเขตชัดเจน
การรวมกันของกลไกทั้งสองนี้ทำให้เกิดเนื้อตายเร็ว จอตาบางลง และเปราะบางมากขึ้น 5)
ในสัปดาห์ที่ 3-4 หลังเริ่มมีอาการ วุ้นลูกตาจะเกิดการจัดระเบียบและเกิดภาวะวุ้นลูกตาหลุดออกจากจอตาส่วนหลังแบบไม่สมบูรณ์ ในเวลานี้ แรงดึงที่รุนแรงจากวุ้นลูกตาบนจอตาที่เนื้อตายบางและเปราะบางอย่างมากทำให้เกิดรอยฉีกขาดหลายจุด การรวมกันของความบางของบริเวณเนื้อตายและแรงดึงทำให้เกิดจอตาลอกในประมาณ 70% ของกรณี
ARN จาก HS V-1 มีแนวโน้มเกิดขึ้นเมื่อมีประวัติหรือโรคร่วมของสมองอักเสบจากเริม และอาจแสดงเป็นอาการทางตาหลังสมองอักเสบARN จาก HS V-2 มีความสัมพันธ์กับเยื่อหุ้มสมองอักเสบ โดยเฉพาะต้องระวังในผู้ป่วยอายุน้อยARN จาก VZV มีระดับของหลอดเลือดอักเสบอุดตันและความถี่ของการเกี่ยวข้องกับเส้นประสาทตา สูงกว่า ARN จาก HS V และพยากรณ์โรคแย่กว่าความเสี่ยงของการเกิดในตาอีกข้างประมาณ 15% ช่วงเวลาการเริ่มต้นระหว่างสองตามักอยู่ใน 1 เดือน แต่การขยายของรอยโรคในตาที่เกิดทีหลังมีจำกัด และพยากรณ์การมองเห็น ดีกว่าตาแรก
ARN ที่เกี่ยวข้องกับ ICI (ยับยั้ง PD-1/PD-L1)12) ARN ที่เกี่ยวข้องกับ COVID-19HS V ที่แฝงอยู่ 16) ARN ที่เกี่ยวข้องกับ natalizumab13) ARN ที่เกี่ยวข้องกับ DMF (dimethyl fumarate)14)
การรักษามาตรฐานเดิมคือการรักษาในโรงพยาบาลด้วยอะไซโคลเวียร์ทางหลอดเลือดดำ แต่มีรายงานชุดผู้ป่วยที่จอประสาทตา อักเสบแบบแอคทีฟทุเลาลงด้วยวาลาไซโคลเวียร์ชนิดรับประทานหรือแฟมไซโคลเวียร์ 9) รายงานของ AAO ยังระบุว่าการรักษาเริ่มต้นด้วยยาต้านไวรัสชนิดรับประทานหรือทางหลอดเลือดดำมีประสิทธิผล แต่ในกรณีรุนแรงหรือขึ้นอยู่กับสภาพร่างกาย มักให้ความสำคัญกับการให้สารน้ำทางหลอดเลือดดำ 5)
ในการศึกษาย้อนหลังของการฉีดฟอสคาร์เน็ตในน้ำวุ้นตา (2.4 มก./0.1 มล.) ร่วมกับการรักษาทั่วร่างกาย พบว่าการเพิ่มการฉีดในน้ำวุ้นตา อาจช่วยพยากรณ์การมองเห็น ได้ดีขึ้น โดยเฉพาะใน ARN จาก VZV 7) สามารถบรรลุความเข้มข้นเฉพาะที่สูงในขณะที่ลดความเป็นพิษต่อร่างกาย และการกำหนดมาตรฐานของการรักษาเหนี่ยวนำในกรณีรุนแรงเป็นหัวข้อวิจัย
การติดตามปริมาณไวรัสด้วย PCR เชิงปริมาณของของเหลวในลูกตาได้รับการรายงานว่าช่วยในการวินิจฉัยและประเมินการตอบสนองต่อการรักษา 10) อย่างไรก็ตาม ยังมีความท้าทายในการนำมาใช้ในเวชปฏิบัติประจำวัน เช่น การรุกล้ำของการเก็บตัวอย่างซ้ำและการกำหนดมาตรฐานของวิธีการวัด
ความหนาของคอรอยด์ (pachychoroid) ในการตรวจ OCT ได้รับรายงานว่าเป็นสิ่งที่สะท้อนกิจกรรมของจอประสาทตาตายเฉียบพลัน ในกรณี ARN ทุติยภูมิจาก VZV พบว่า pachychoroid ในการตรวจ OCT เกิดขึ้นสอดคล้องกับบริเวณจอประสาทตา อักเสบแบบเนื้อตาย และชี้ให้เห็นถึงศักยภาพในการใช้เป็นเครื่องหมายกิจกรรมระหว่างการติดตามผลหลังการรักษา 18)
มีรายงานผู้ป่วย ARN จาก EB V หนึ่งรายที่ดื้อต่ออะไซโคลเวียร์และแกนซิโคลเวียร์ตอบสนองต่อฟอสคาร์เน็ต 4800 มก./วัน ทางหลอดเลือดดำ 20) เมื่อสาเหตุมาจากไวรัสอื่นที่ไม่ใช่ VZV/HS V การรักษามาตรฐานอาจไม่ได้ผลดี และการระบุไวรัสก่อโรคด้วย PCR มีความสำคัญในการกำหนดแผนการรักษา
ด้วยการแพร่หลายของสารยับยั้งจุดตรวจภูมิคุ้มกัน จำเป็นต้องระวังความเสี่ยงของการเกิด ARN จากการกระตุ้น VZV อีกครั้ง 12) นอกจากนี้ มีรายงาน ARN หลังการติดเชื้อ COVID-19 จากการกระตุ้น HS V/VZV อีกครั้งอย่างต่อเนื่อง และ ARN ที่เกี่ยวข้องกับการรักษาด้วยการกดภูมิคุ้มกัน มีแนวโน้มเพิ่มขึ้นในอนาคต 14) 16)
日本眼炎症学会ぶどう膜炎診療ガイドライン作成委員会. ぶどう膜炎診療ガイドライン. 日眼会誌. 2019;123(6):635-796.
Urayama A, Yamada N, Sasaki T, et al. Unilateral acute uveitis with periarteritis and retinal detachment. Jpn J Clin Ophthalmol. 1971;25:607-619.
Standardization of Uveitis Nomenclature (SUN) Working Group. Classification criteria for acute retinal necrosis syndrome. Ophthalmology. 2021;128(12):1974-1980. doi:10.1016/j.ophtha.2021.11.011. PMID: 34807625.
Takase H, Okada AA, Goto H, et al. Development and validation of new diagnostic criteria for acute retinal necrosis. Jpn J Ophthalmol. 2015;59(1):14-20. doi:10.1007/s10384-014-0362-0. PMID: 25492579.
Schoenberger SD, Kim SJ, Thorne JE, et al. Diagnosis and Treatment of Acute Retinal Necrosis: A Report by the American Academy of Ophthalmology. Ophthalmology. 2017;124(3):382-392. doi:10.1016/j.ophtha.2016.11.007. PMID: 28094044.
Tibbetts MD, Shah CP, Young LH, et al. Treatment of acute retinal necrosis. Ophthalmology. 2010;117(4):818-824. doi:10.1016/j.ophtha.2009.09.001. PMID: 20110127.
Wong R, Pavesio CE, Laidlaw DA, et al. Acute retinal necrosis: the effects of intravitreal foscarnet and virus type on outcome. Ophthalmology. 2010;117(3):556-560. doi:10.1016/j.ophtha.2009.08.003. PMID: 20031221.
Flaxel CJ, Yeh S, Lauer AK. Combination systemic and intravitreal antiviral therapy in the management of acute retinal necrosis syndrome. Ophthalmic Surg Lasers Imaging Retina. 2013;44(6):521-526.
Aizman A, Johnson MW, Elner SG. Treatment of acute retinal necrosis syndrome with oral antiviral medications. Ophthalmology. 2007;114(2):307-312. doi:10.1016/j.ophtha.2006.06.058. PMID: 17123607.
Asano S, Yoshikawa T, Kimura H, et al. Monitoring herpesvirus DNA in three cases of acute retinal necrosis by real-time PCR. J Clin Virol. 2004;29(3):206-209. PMID: 15002491.
Cochrane TF, Silvestri G, McDowell C, et al. Acute retinal necrosis in the United Kingdom: results of a prospective surveillance study. Eye (Lond). 2012;26(3):370-377.
Wang P, An M, Zhang M, et al. Acute retinal necrosis in a patient with cervical malignant tumor treated with sintilimab: a case report and literature review. Front Immunol. 2024;15:1301329.
Cheraqpour K, Ahmadraji A, Rashidinia A, et al. Acute retinal necrosis caused by co-infection with multiple viruses in a natalizumab-treated patient: a case report and brief review of literature. BMC Ophthalmol. 2021;21:337.
Paisey C, Curtin K, Epps SJ, et al. Acute retinal necrosis associated with dimethyl fumarate. Mult Scler J. 2025;31(12):1506-1508.
Luo T, Wang L, Zhang L, et al. Acute retinal necrosis following cataract surgery: a case of VZV reactivation and successful management. BMC Ophthalmol. 2025;25:131.
Gonzalez MP, Rios R, Pappaterra M, et al. Reactivation of acute retinal necrosis following SARS-CoV-2 infection. Case Rep Ophthalmol Med. 2021;2021:7336488.
Rahman EZ , Shah P, Shah R. Metastatic squamous cell carcinoma masquerading as acute retinal necrosis. Am J Ophthalmol Case Rep. 2023;32:101934.
Harbeck K, Ericksen C, Johnson W, et al. Pachychoroid associated with acute retinal necrosis secondary to varicella zoster virus. J Vitreoretinal Dis. 2024;8(2):196-199.
Perhiar BA, Siddiqui MAR, Ibrahim S. Acute retinal necrosis with exudative retinal detachment in a child. BMJ Case Rep. 2021;14:e245984.
Suzuki K, Namba K, Hase K, et al. A case of Epstein-Barr virus acute retinal necrosis successfully treated with foscarnet. Am J Ophthalmol Case Rep. 2022;25:101363.