前眼部所見

急性網膜壊死(桐沢型ぶどう膜炎)
1. 急性網膜壊死とは
Section titled “1. 急性網膜壊死とは”急性網膜壊死(ARN: Acute Retinal Necrosis)は、1971年に浦山らが「桐沢型ぶどう膜炎」として報告した壊死性ヘルペス性網膜症である。2) それまでに類をみない劇症ぶどう膜炎として6例が記載され、ARNという疾患概念の世界的な起点となった。
免疫正常の健常者に発症するのが特徴であり、原因ウイルスはHSV-1・HSV-2・VZVである。発症後に急速な網膜壊死と眼圧上昇をきたし、放置すれば失明に至るため眼科的緊急疾患に分類される。ぶどう膜炎診療ガイドライン(2019年)の全国調査では、2002年調査で41例(ぶどう膜炎全体の1.3%)、2009年調査で53例(同1.4%)が報告されている。1)
免疫不全患者では、同じヘルペスウイルスによっても病型が異なる。CMV網膜炎や進行性外層壊死性網膜炎(PORN)は免疫不全者の疾患であり、ARNは免疫正常者の疾患として位置づけられる。
疫学的には年間発症率は0.5〜0.63/100万人(英国)と報告され11)、50〜70代の免疫正常成人に多い。発症形式は2/3が片眼性で、1/3が両眼性(Bilateral ARN; BARN)である13)。近年では免疫チェックポイント阻害薬(ICI)12)、natalizumab13)、ジメチルフマル酸塩(DMF)14)など免疫抑制薬との関連が報告されている。また白内障手術15)やCOVID-19感染16)がトリガーとなった事例も報告されている。
2. 主な症状と臨床所見
Section titled “2. 主な症状と臨床所見”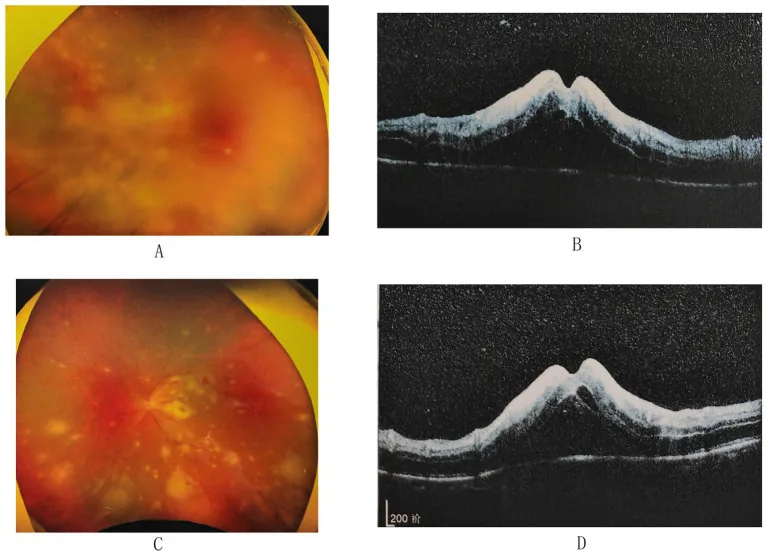
突然発症の充血・眼痛・羞明・霧視・飛蚊症・視力低下を呈する。初期は前部ぶどう膜炎症状(充血・眼痛・羞明)が先行し、網膜病変の進行とともに視力が急速に低下する。
眼底・網膜所見
周辺網膜の黄白色顆粒状病変:複数箇所に出現し、全周性・後極側へ急速拡大。抗ウイルス薬投与後約1週間で進展停止し、融合した地図状白色病変へと変化する。
網膜動脈炎:血管鞘走・閉塞。棍棒状の静脈沿い出血が特徴的。
その他:視神経乳頭発赤・腫脹、炎症性硝子体混濁。棍棒状の静脈沿い出血、波状の縁(scalloped edges)、Kyrieleis’ Arteriolitis(細動脈沿いの黄白色病変)も特徴的な所見である。
蛍光眼底造影検査では閉塞性動脈炎パターンと乳頭過蛍光が確認される。OCT検査では、壊死性網膜炎部位に一致した脈絡膜肥厚(パキコロイド)が生じることが報告されており18)、新たな診断的所見として注目されている。
網膜周辺部の黄白色顆粒状病変(ウイルス増殖部位)は全周性・後極側へ拡大するが、抗ウイルス薬などの投与によりその進展は約1週間で停止する。その後、各顆粒状病変は融合して濃厚で境界明瞭な地図状白色病変へと変化する(ウイルスによる直接障害+閉塞性血管炎による循環障害の複合)。
治療開始後約1週間で前房症状は軽減し眼圧も正常化するが、前房炎症は年余にわたって持続することがある。発症後約3〜4週目に硝子体の器質化による不完全後部硝子体剥離が生じ、極度に菲薄化・脆弱化した網膜壊死部に硝子体からの強い牽引がかかり多発裂孔が形成される。その結果、約70%の症例で網膜剥離が発生する。
| 原因ウイルス | 特徴的な患者層 | 関連全身疾患 |
|---|---|---|
| HSV-1 | 中高年 | ヘルペス脳炎の既往・合併 |
| HSV-2 | 若年者 | 髄膜炎との関連 |
| VZV | 中高年 | 髄膜炎の合併報告 |
約70%で網膜剥離が発生し、最終的に3分の2の眼で視力0.1以下となる予後不良疾患です。ただし最初に発症した眼(先発眼)に比べ、後から発症する僚眼(約15%で発症)の病巣拡大は限定的で、視力予後は比較的良好とされています。
3. 原因とリスク要因
Section titled “3. 原因とリスク要因”ARNはヘルペスウイルスの眼内再活性化によって発症する。初感染後に三叉神経節・脊髄後根神経節に潜伏したウイルスが、宿主の免疫バランスの変化を契機に再活性化し、神経軸索を介して眼に到達する。
原因ウイルスと患者層
Section titled “原因ウイルスと患者層”- HSV-2: 若年者に多い。性器ヘルペスの既往と関連する。
- HSV-1・VZV: 中高年に多い。帯状疱疹既往・顔面帯状疱疹との関連がある。
- HSV-1によるARNはヘルペス脳炎の既往・合併がある場合に発症しやすい。
- HSV-2・VZVによるARNでは髄膜炎との関連が指摘されている。
- ヘルペス感染の現症または既往歴: 帯状疱疹の既往は30年以上前でもVZV再活性化によるARNを引き起こすことがある。HSV脳炎の既往も原因となりうる。
- 局所ステロイド: 眼局所ステロイドの長期使用が稀な誘因となることがある。
- 高齢: VZVによるARNリスクと関連。
- 免疫抑制薬: CD8+ T細胞やウイルス特異的T細胞免疫の低下が再活性化の鍵とされており、以下の薬剤での報告がある。
- 免疫正常が前提: 免疫不全(HIV感染・免疫抑制薬使用)があればCMV網膜炎・PORNを優先して考慮する。
病態はウイルスの直接細胞障害に加え、ウイルス排除のために動員された炎症細胞による閉塞性血管炎・網膜虚血が組織障害を増大させる点にある。5)
4. 診断と検査方法
Section titled “4. 診断と検査方法”日本の診断基準
Section titled “日本の診断基準”| 項目 | 内容 |
|---|---|
| 1a | 前房炎症細胞または豚脂様角膜後面沈着物 |
| 1b | 周辺網膜に1つまたは複数の黄白色病変(初期は顆粒状〜斑状、次第に融合) |
| 1c | 網膜動脈炎 |
| 1d | 視神経乳頭発赤 |
| 1e | 炎症性硝子体混濁 |
| 1f | 眼圧上昇 |
| 2a | 網膜病変が急速に円周方向に拡大 |
| 2b | 網膜裂孔あるいは網膜剥離の発生 |
| 2c | 網膜血管閉塞 |
| 2d | 視神経萎縮 |
| 2e | 抗ウイルス薬に反応 |
| 3 | 眼内液PCRまたは抗体率(Q値)でHSV-1・HSV-2・VZVのいずれかが陽性 |
確定診断(ウイルス確認群): 初期眼所見1aと1bを認め、かつ臨床経過項目のうち1項目以上+ウイルス検査陽性
臨床診断(ウイルス未確認群): 初期眼所見1aと1bを含む4項目以上、かつ臨床経過項目のうち2項目以上
本基準はTakase(2015)らによって開発・検証された。4)
SUN 2021 ARN診断基準3)
Section titled “SUN 2021 ARN診断基準3)”- 必須: 周辺部網膜を侵す壊死性網膜炎
- 以下のいずれかを追加要件とする:
- 前房水・硝子体PCRでHSV・VZVのいずれかが陽性
- 特徴的臨床像(全周性または融合性網膜炎、血管鞘走・閉塞、軽度を超える硝子体炎)
眼内液(前房水・硝子体液)を用いたPCRがウイルス同定において感度・特異度ともに最も優れた診断法である。1) 多項目PCR(先進医療)では複数ウイルスの同定が可能であり鑑別に有用である。
抗体率(Q値: Goldmann-Witmer係数)も補助診断として用いる。ただし発症10日以内は眼内での抗体産生が不十分なため偽陰性となりやすく、この時期はPCRを優先する。血清抗体価のみでは病因診断を行うことはできない。1)
| 疾患 | 免疫状態 | 主な特徴 |
|---|---|---|
| PORN(進行性外層網膜壊死) | 高度免疫不全(HIV CD4 <50 など) | 前部炎症乏しい・後極優位・急速進行 |
| CMV網膜炎 | 免疫不全 | 出血を伴う徐々の拡大・前部炎症初期には乏しい |
| 眼トキソプラズマ症 | 免疫正常〜不全 | 局所性肉芽腫性網膜炎・隣接瘢痕 |
| 眼内リンパ腫・腫瘍性病変 | 中高年 | 硝子体細胞・網膜下浸潤・脳病変。まれに転移性腫瘍がARN様にみえる症例もある17) |
| 小児の非典型例 | 小児 | 滲出性網膜剥離など非典型的な所見を伴う症例報告があり、典型像から外れる場合は鑑別を広げる19) |
はい。臨床診断基準(ウイルス未確認群)を満たせば、PCR結果を待たずに抗ウイルス療法を開始します。発症10日以内はPCRの偽陰性率が高く、また病変の進行が急速であるため、ASAP原則にのっとり診断の確信があれば即座に治療を始めることが標準です。
5. 標準的な治療法
Section titled “5. 標準的な治療法”ASAP原則に従い、国内ガイドラインと既報の治療シリーズを参考にしながら、可及的速やかに4本柱の治療を開始する。1, 5, 6)
- A: Aciclovir(抗ウイルス療法)
- S: Steroid(抗炎症療法)
- A: Aspirin(抗血栓療法)
- P: Prophylaxis for retinal detachment(網膜剥離予防)
薬物療法レジメン
Section titled “薬物療法レジメン”| 薬剤 | 用量・用法 | 期間 |
|---|---|---|
| アシクロビル注(ゾビラックス注) | 10 mg/kg を補液200 mL以上に溶解し2時間以上かけて点滴静注 1日3回 | 初期2週間 |
| バラシクロビル錠(バルトレックス)[点滴不可時] | 500 mg 6錠 分3 | 初期2週間 |
| バラシクロビル錠(バルトレックス)[継続] | 500 mg 6錠 分3 | 初期療法後さらに2週間 |
| ベタメタゾン点眼(リンデロン0.1%) | 1日6回 → 炎症軽減で1日2〜4回 | 炎症期間中 |
| ミドリンM点眼(0.4%) | 1日1回 | 前房炎症期間中 |
| ベタメタゾン注(リンデロン注) | 8 mg/日×5日間 → 6 mg×4日 → 4 mg×4日 点滴静注 | 抗ウイルス薬導入24〜48時間後から |
| ファモチジン錠(ガスター20 mg) | 2錠 分2 朝夕 | ステロイド全身投与中 |
| アスピリン腸溶錠(バイアスピリン100 mg) | 1錠 分1 | 4週間 |
硝子体内抗ウイルス薬注射
Section titled “硝子体内抗ウイルス薬注射”全身投与に加え、ホスカルネット(2.4 mg/0.1 mL)の硝子体内注射を併用することで視力転帰の改善・網膜剥離率の低下が報告されている。7, 8) 特に重症例・視力への影響が切迫している例では考慮する。5)
網膜剥離予防(手術療法)
Section titled “網膜剥離予防(手術療法)”- 予防的バリアレーザー光凝固: 壊死病変の後極側に顆粒状病変期に施行することがあるが、網膜剥離抑制効果のエビデンスは限定的であり、有効性は確立していない。5) 顆粒状病変のすぐ後極側に3〜4列で凝固を行い、病変自体や周辺側には凝固しない。
- 硝子体切除術: 網膜剥離が発生した場合(約70%)に施行する。
手術ステップ:
- 超音波水晶体乳化吸引
- アシクロビル 40 μg/mL を添加した灌流液で硝子体灌流(保険適用外)
- 硝子体切除(残存硝子体による牽引を防ぐため徹底的に郭清)
- 眼内光凝固: 顆粒状病変のすぐ後極側に3〜4列で凝固(病変自体・周辺側には凝固しない)
- 9 mmシリコーンタイヤによる輪状締結
- シリコーンオイル充填
必須ではありません。バリアレーザー(壊死病変の後極側への光凝固)を施行することはありますが、網膜剥離の発生を確実に抑制するエビデンスは現時点では限定的です。壊死部の脆弱性・牽引力を考慮すると、発生した場合は硝子体手術(シリコーンオイル充填)が根本的な対処法となります。
6. 病態生理学・詳細な発症機序
Section titled “6. 病態生理学・詳細な発症機序”ARNの発症はヘルペスウイルス(HSV-1・HSV-2・VZV)が三叉神経節または脊髄後根神経節に潜伏感染し、何らかのトリガー(免疫低下・加齢・ストレスなど)で再活性化して眼内に到達することによる。
網膜障害の2機序
Section titled “網膜障害の2機序”-
ウイルスの直接細胞障害: 網膜細胞内でのウイルス増殖と細胞溶解。ウイルスが増殖している部位が黄白色顆粒状病変として肉眼的に観察される。
-
閉塞性血管炎による虚血: ウイルス排除のための炎症細胞浸潤が網膜動脈周囲の血管炎を引き起こし、血管閉塞・網膜虚血を招く。閉塞性血管炎による浮腫・循環障害が境界明瞭な地図状白色病変を形成する。
これら2つの機序の複合により、網膜の急速壊死・菲薄化・脆弱化が進行する。5)
網膜剥離の発生機序
Section titled “網膜剥離の発生機序”発症後3〜4週目に硝子体が器質化して不完全後部硝子体剥離が生じる。このとき極度に菲薄化・脆弱化した壊死網膜に硝子体からの強い牽引がかかり多発裂孔が形成される。壊死部の菲薄化と牽引力の複合により、約70%の症例で網膜剥離が発生する。
ウイルス種別による差異
Section titled “ウイルス種別による差異”- HSV-1 ARNはヘルペス脳炎の既往・合併がある場合に発症しやすく、脳炎先行後の眼症状として現れることもある
- HSV-2 ARNでは髄膜炎との関連が指摘されており、特に若年者で注意を要する
- VZV ARNは閉塞性血管炎の程度・視神経侵犯の頻度がHSV ARNより高く、予後がより不良とされる
- 僚眼発症リスクは約15%。左右眼の発症間隔は1か月以内が多いが、後発眼の病巣拡大は限定的であり視力予後は先発眼より良好である
免疫抑制薬・新興感染症関連ARNの特殊機序
Section titled “免疫抑制薬・新興感染症関連ARNの特殊機序”- ICI(PD-1/PD-L1阻害薬)関連ARN: 免疫関連有害事象(IRIS類似機序)、自己寛容の障害、眼の免疫特権喪失などが示唆されている12)
- COVID-19関連ARN: SARS-CoV-2感染によるCD3+ CD8+ Tリンパ球の著明な減少が、潜伏HSVの再活性化を促進するとされている16)
- natalizumab関連ARN: 白血球のCNS移行阻害作用によるCD4/CD8比低下がウイルス特異的免疫を低下させる13)
- DMF(ジメチルフマル酸塩)関連ARN: CD8+ T細胞およびVZV特異的T細胞免疫の低下が再活性化リスクを高める14)
7. 最新の研究と今後の展望(研究段階の報告)
Section titled “7. 最新の研究と今後の展望(研究段階の報告)”経口バラシクロビル導入療法の有効性
Section titled “経口バラシクロビル導入療法の有効性”従来の標準治療はアシクロビルの静脈内投与による入院治療であったが、経口バラシクロビルまたはファムシクロビルで活動性網膜炎が消退した症例シリーズが報告されている。9) AAO報告でも経口または静注の抗ウイルス薬による初期治療は有効とされるが、重症例や全身状態に応じて点滴静注を優先することが多い。5)
硝子体内抗ウイルス薬の有効性
Section titled “硝子体内抗ウイルス薬の有効性”ホスカルネット硝子体内注射(2.4 mg/0.1 mL)を全身療法と併用した後ろ向き研究では、特にVZV ARNにおいて硝子体内注射の追加が視力予後を改善する可能性が示されている。7) 全身毒性を最小限に抑えながら高い局所濃度を達成できる可能性があり、重症例での導入療法標準化が研究課題となっている。
定量PCRによる疾患活動性モニタリング
Section titled “定量PCRによる疾患活動性モニタリング”眼内液の定量PCRによるウイルス量モニタリングは、診断補助に加えて治療反応判定に役立つ可能性が報告されている。10) ただし反復採取の侵襲性や測定法の標準化など、日常診療への組み込みには課題が残る。
パキコロイドのARN活動性マーカーとしての可能性
Section titled “パキコロイドのARN活動性マーカーとしての可能性”OCTでの脈絡膜肥厚(パキコロイド)が急性網膜壊死の活動性を反映する所見として報告されている。二次性VZV-ARNの症例で、OCT上のパキコロイドが壊死性網膜炎部位に一致して生じ、治療後の経過観察において活動性のマーカーとして活用できる可能性が示唆された。18)
EBV-ARNに対するfoscarnetの有効性
Section titled “EBV-ARNに対するfoscarnetの有効性”アシクロビル・ガンシクロビルに抵抗性を示したEBV-ARNの1例に対し、foscarnet 4800 mg/日 IVが奏効したとの報告がある。20) VZV・HSV以外のウイルスが原因の場合、標準的な治療が効きにくい場合があり、PCRによる原因ウイルスの同定が治療方針の決定に重要である。
免疫抑制薬・新興感染症とARNの関連
Section titled “免疫抑制薬・新興感染症とARNの関連”免疫チェックポイント阻害薬(ICI)の普及に伴い、VZV再活性化によるARN発症リスクへの注意が求められている。12) また、COVID-19感染後のHSV/VZV再活性化によるARN報告が相次いでおり、免疫抑制療法関連のARNは今後も増加する可能性がある。14)16)
8. 参考文献
Section titled “8. 参考文献”-
日本眼炎症学会ぶどう膜炎診療ガイドライン作成委員会. ぶどう膜炎診療ガイドライン. 日眼会誌. 2019;123(6):635-796.
-
Urayama A, Yamada N, Sasaki T, et al. Unilateral acute uveitis with periarteritis and retinal detachment. Jpn J Clin Ophthalmol. 1971;25:607-619.
-
Standardization of Uveitis Nomenclature (SUN) Working Group. Classification criteria for acute retinal necrosis syndrome. Ophthalmology. 2021;128(12):1974-1980. doi:10.1016/j.ophtha.2021.11.011. PMID: 34807625.
-
Takase H, Okada AA, Goto H, et al. Development and validation of new diagnostic criteria for acute retinal necrosis. Jpn J Ophthalmol. 2015;59(1):14-20. doi:10.1007/s10384-014-0362-0. PMID: 25492579.
-
Schoenberger SD, Kim SJ, Thorne JE, et al. Diagnosis and Treatment of Acute Retinal Necrosis: A Report by the American Academy of Ophthalmology. Ophthalmology. 2017;124(3):382-392. doi:10.1016/j.ophtha.2016.11.007. PMID: 28094044.
-
Tibbetts MD, Shah CP, Young LH, et al. Treatment of acute retinal necrosis. Ophthalmology. 2010;117(4):818-824. doi:10.1016/j.ophtha.2009.09.001. PMID: 20110127.
-
Wong R, Pavesio CE, Laidlaw DA, et al. Acute retinal necrosis: the effects of intravitreal foscarnet and virus type on outcome. Ophthalmology. 2010;117(3):556-560. doi:10.1016/j.ophtha.2009.08.003. PMID: 20031221.
-
Flaxel CJ, Yeh S, Lauer AK. Combination systemic and intravitreal antiviral therapy in the management of acute retinal necrosis syndrome. Ophthalmic Surg Lasers Imaging Retina. 2013;44(6):521-526.
-
Aizman A, Johnson MW, Elner SG. Treatment of acute retinal necrosis syndrome with oral antiviral medications. Ophthalmology. 2007;114(2):307-312. doi:10.1016/j.ophtha.2006.06.058. PMID: 17123607.
-
Asano S, Yoshikawa T, Kimura H, et al. Monitoring herpesvirus DNA in three cases of acute retinal necrosis by real-time PCR. J Clin Virol. 2004;29(3):206-209. PMID: 15002491.
-
Cochrane TF, Silvestri G, McDowell C, et al. Acute retinal necrosis in the United Kingdom: results of a prospective surveillance study. Eye (Lond). 2012;26(3):370-377.
-
Wang P, An M, Zhang M, et al. Acute retinal necrosis in a patient with cervical malignant tumor treated with sintilimab: a case report and literature review. Front Immunol. 2024;15:1301329.
-
Cheraqpour K, Ahmadraji A, Rashidinia A, et al. Acute retinal necrosis caused by co-infection with multiple viruses in a natalizumab-treated patient: a case report and brief review of literature. BMC Ophthalmol. 2021;21:337.
-
Paisey C, Curtin K, Epps SJ, et al. Acute retinal necrosis associated with dimethyl fumarate. Mult Scler J. 2025;31(12):1506-1508.
-
Luo T, Wang L, Zhang L, et al. Acute retinal necrosis following cataract surgery: a case of VZV reactivation and successful management. BMC Ophthalmol. 2025;25:131.
-
Gonzalez MP, Rios R, Pappaterra M, et al. Reactivation of acute retinal necrosis following SARS-CoV-2 infection. Case Rep Ophthalmol Med. 2021;2021:7336488.
-
Rahman EZ, Shah P, Shah R. Metastatic squamous cell carcinoma masquerading as acute retinal necrosis. Am J Ophthalmol Case Rep. 2023;32:101934.
-
Harbeck K, Ericksen C, Johnson W, et al. Pachychoroid associated with acute retinal necrosis secondary to varicella zoster virus. J Vitreoretinal Dis. 2024;8(2):196-199.
-
Perhiar BA, Siddiqui MAR, Ibrahim S. Acute retinal necrosis with exudative retinal detachment in a child. BMJ Case Rep. 2021;14:e245984.
-
Suzuki K, Namba K, Hase K, et al. A case of Epstein-Barr virus acute retinal necrosis successfully treated with foscarnet. Am J Ophthalmol Case Rep. 2022;25:101363.
