前節所見

急性視網膜壞死(桐澤型葡萄膜炎)
1. 什麼是急性視網膜壞死?
Section titled “1. 什麼是急性視網膜壞死?”急性視網膜壞死(ARN)是一種壞死性皰疹性視網膜病變,於1971年由浦山等人首次報告為「桐澤型葡萄膜炎」。2) 當時描述了6例前所未有的暴發性葡萄膜炎,成為ARN疾病概念的全球起點。
其特點是發生於免疫功能正常的健康個體,病原體為HSV-1、HSV-2和VZV。發病後出現快速視網膜壞死和眼壓升高,若不治療會導致失明,因此被歸類為眼科急症。根據葡萄膜炎診療指引(2019年)的全國調查,2002年調查報告41例(佔所有葡萄膜炎的1.3%),2009年調查報告53例(1.4%)。1)
在免疫功能低下患者中,同一皰疹病毒可引起不同疾病類型。CMV視網膜炎和進行性外層壞死性視網膜炎(PORN)是免疫功能低下者的疾病,而ARN被定位為免疫功能正常者的疾病。
流行病學上,年發生率為0.5~0.63/百萬人(英國)11),多見於50~70歲的免疫功能正常成人。發病形式三分之二為單眼,三分之一為雙眼(雙側ARN;BARN)13)。近年來,有報告與免疫檢查點抑制劑(ICI)12)、那他珠單抗13)、富馬酸二甲酯(DMF)14)等免疫抑制藥物相關。也有白內障手術15)和COVID-19感染16)作為觸發因素的病例報告。
2. 主要症狀和臨床所見
Section titled “2. 主要症狀和臨床所見”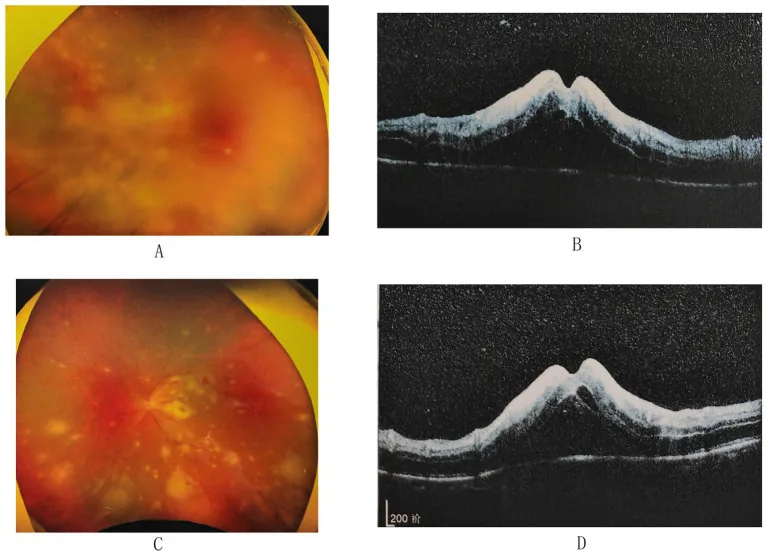
突然發作的充血、眼痛、畏光、視物模糊、飛蚊症和視力下降。初期以前部葡萄膜炎症狀(充血、眼痛、畏光)為先導,隨著視網膜病變進展,視力迅速下降。
眼底及視網膜所見
周邊視網膜黃白色顆粒狀病變:出現在多個部位,向全周和後極迅速擴大。抗病毒治療後約1週停止進展,轉變為融合的地圖狀白色病變。
視網膜動脈炎:血管鞘和閉塞。特徵性的棒狀靜脈旁出血。
其他:視乳頭充血腫脹、炎性玻璃體混濁。棒狀靜脈旁出血、扇形邊緣(scalloped edges)和Kyrieleis動脈炎(小動脈旁的黃白色病變)也是特徵性表現。
螢光眼底血管造影顯示閉塞性動脈炎模式和視乳頭強螢光。OCT檢查顯示壞死性視網膜炎部位相應的脈絡膜增厚(厚脈絡膜),如報導所述18),作為新的診斷性發現受到關注。
視網膜周邊的黃白色顆粒狀病變(病毒增殖部位)會向全周和後極方向擴展,但使用抗病毒藥物等治療後,其進展約在1週內停止。隨後,各顆粒狀病變融合成濃厚、邊界清晰的地圖狀白色病變(病毒直接損傷+閉塞性血管炎導致的循環障礙的複合作用)。
治療開始後約1週,前房症狀減輕,眼壓恢復正常,但前房炎症可能持續數年。發病後約3~4週,玻璃體機化導致不完全性後玻璃體剝離,極度變薄、脆弱的視網膜壞死部位受到玻璃體的強烈牽拉,形成多發裂孔。結果,約70%的病例發生視網膜剝離。
| 致病病毒 | 特徵性患者群體 | 相關全身疾病 |
|---|---|---|
| HSV-1 | 中老年人 | 有疱疹性腦炎病史或合併 |
| HSV-2 | 年輕人 | 與腦膜炎相關 |
| VZV | 中老年人 | 有合併腦膜炎的報導 |
約70%的病例發生視網膜剝離,最終三分之二的眼睛視力降至0.1以下,是一種預後不良的疾病。但與先發眼相比,後發病的另一眼(約15%發病)的病灶擴散有限,視力預後相對較好。
3. 原因與風險因素
Section titled “3. 原因與風險因素”ARN由疱疹病毒在眼內再活化引起。初次感染後,潛伏在三叉神經節和脊神經後根神經節的病毒,在宿主免疫平衡改變時再活化,通過神經軸突到達眼部。
致病病毒與患者族群
Section titled “致病病毒與患者族群”- HSV-2:多見於年輕人。與生殖器疱疹病史相關。
- HSV-1和VZV:多見於中老年人。與帶狀疱疹或面部帶狀疱疹病史相關。
- HSV-1引起的ARN在有疱疹性腦炎病史或合併症的患者中較易發生。
- HSV-2和VZV引起的ARN與腦膜炎有關。
- 當前或既往疱疹感染:即使30多年前的帶狀疱疹病史,也可能因VZV再活化引起ARN。HSV腦炎病史也可能是原因。
- 局部類固醇:長期使用眼部局部類固醇可能成為罕見誘因。
- 高齡:與VZV引起的ARN風險相關。
- 免疫抑制藥物:CD8+ T細胞和病毒特異性T細胞免疫的降低是再活化的關鍵,以下藥物有相關報告:
- 免疫功能正常為前提:若存在免疫缺陷(HIV感染、使用免疫抑制劑),應優先考慮CMV視網膜炎和PORN。
病理機轉包括病毒直接細胞損傷,以及為清除病毒而募集的發炎細胞引起的閉塞性血管炎和視網膜缺血,從而加重組織損傷。5)
4. 診斷與檢查方法
Section titled “4. 診斷與檢查方法”日本診斷標準
Section titled “日本診斷標準”| 項目 | 內容 |
|---|---|
| 1a | 前房發炎細胞或羊脂狀角膜後沉著物 |
| 1b | 周邊視網膜一處或多處黃白色病變(初期呈顆粒狀至斑片狀,逐漸融合) |
| 1c | 視網膜動脈炎 |
| 1d | 視神經盤充血 |
| 1e | 發炎性玻璃體混濁 |
| 1f | 眼壓升高 |
| 2a | 視網膜病變快速沿圓周方向擴展 |
| 2b | 發生視網膜裂孔或視網膜剝離 |
| 2c | 視網膜血管阻塞 |
| 2d | 視神經萎縮 |
| 2e | 對抗病毒藥物有反應 |
| 3 | 眼內液PCR或抗體比值(Q值)檢測HSV-1、HSV-2或VZV任一陽性 |
確診(病毒確認組):存在初期眼部表現1a和1b,且符合至少1項臨床病程項目+病毒檢測陽性。
臨床診斷(病毒未確認組):至少4項包括初期眼部表現1a和1b,且符合至少2項臨床病程項目。
該標準由Takase等人(2015)開發並驗證。4)
SUN 2021 ARN診斷標準3)
Section titled “SUN 2021 ARN診斷標準3)”- 必要條件:累及周邊視網膜的壞死性視網膜炎。
- 以下任一附加條件:
- 房水或玻璃體PCR檢測HSV或VZV陽性。
- 特徵性臨床表現(環形或融合性視網膜炎、血管鞘/閉塞、超過輕度的玻璃體炎)。
眼內液(房水或玻璃體液)PCR是病毒鑑定中敏感性和特異性最高的診斷方法。1) 多重PCR(先進醫療)可鑑定多種病毒,有助於鑑別診斷。
抗體比值(Q值:Goldmann-Witmer係數)也用作輔助診斷。但發病10天內眼內抗體產生不足,易出現偽陰性,此期間應優先進行PCR。僅憑血清抗體效價無法進行病因診斷。1)
| 疾病 | 免疫狀態 | 主要特徵 |
|---|---|---|
| PORN(進行性外層視網膜壞死) | 嚴重免疫不全(如HIV CD4 <50) | 前房發炎輕微、後極部為主、快速進展 |
| CMV視網膜炎 | 免疫不全 | 伴出血的緩慢擴大、早期前房發炎輕微 |
| 眼弓形蟲症 | 免疫功能正常至不全 | 局部肉芽腫性視網膜炎、鄰近疤痕 |
| 眼內淋巴瘤/腫瘤性病變 | 中老年人 | 玻璃體細胞、視網膜下浸潤、腦病變。罕見情況下轉移性腫瘤可表現為ARN樣 17) |
| 兒童非典型病例 | 兒童 | 有滲出性視網膜剝離等非典型表現的病例報告,若偏離典型表現應擴大鑑別診斷 19) |
是的。如果符合臨床診斷標準(病毒未確認組),無需等待PCR結果即可開始抗病毒治療。發病10天內PCR偽陰性率高,且病變進展迅速,因此根據ASAP原則,如果診斷確信,立即開始治療是標準做法。
5. 標準治療方法
Section titled “5. 標準治療方法”遵循ASAP原則,參考國內指引和已報導的治療系列,盡快開始四大支柱治療。1, 5, 6)
- A: 阿昔洛韋(抗病毒治療)
- S: 類固醇(抗炎治療)
- A: 阿斯匹靈(抗血栓治療)
- P: 視網膜剝離預防
藥物治療方案
Section titled “藥物治療方案”| 藥物 | 劑量與用法 | 療程 |
|---|---|---|
| 阿昔洛韋注射液(Zovirax注射液) | 10 mg/kg 溶於至少200 mL液體中,靜脈滴注2小時以上,每日3次 | 初始2週 |
| 伐昔洛韋錠(Valtrex)[無法點滴時] | 500 mg,6錠,分3次 | 初始2週 |
| 伐昔洛韋錠(Valtrex)[持續治療] | 500 mg,6錠,分3次 | 初始治療後額外2週 |
| 倍他米松眼藥水(Rinderon 0.1%) | 每日6次 → 炎症減輕後每日2-4次 | 炎症期間 |
| 美多麗M眼藥水(0.4%) | 每日1次 | 前房炎症期間 |
| 倍他米松注射液(Rinderon注射液) | 8 mg/日×5天 → 6 mg×4天 → 4 mg×4天,靜脈點滴 | 抗病毒藥物開始後24-48小時起 |
| 法莫替丁錠(胃適妥20 mg) | 2錠,分2次,早晚服用 | 全身性類固醇使用期間 |
| 阿斯匹靈腸溶錠(拜耳阿斯匹靈100 mg) | 1錠,每日1次 | 4週 |
玻璃體內抗病毒藥物注射
Section titled “玻璃體內抗病毒藥物注射”除全身給藥外,合併玻璃體內注射磷甲酸鈉(2.4 mg/0.1 mL)可改善視力結果並降低視網膜剝離率。7, 8) 尤其在重症病例或視力受到緊迫威脅時考慮使用。5)
視網膜剝離的預防(手術治療)
Section titled “視網膜剝離的預防(手術治療)”- 預防性屏障雷射光凝固:可在壞死病灶後極側的顆粒狀病變期進行,但預防視網膜剝離的證據有限,有效性尚未確立。5) 在顆粒狀病變緊鄰的後極側進行3~4排光凝固,避免對病灶本身及周邊側進行光凝固。
- 玻璃體切除術:在發生視網膜剝離時(約70%)進行。
手術步驟:
- 超音波晶體乳化術
- 使用添加阿昔洛韋 40 μg/mL 的灌注液進行玻璃體灌注(仿單標示外使用)
- 玻璃體切除術(徹底清除殘留玻璃體以防止牽引)
- 眼內光凝固:在顆粒狀病變緊鄰的後極側進行3~4排凝固(不凝固病變本身及周邊側)
- 使用9 mm矽膠帶進行環紮
- 矽油填充
並非必須。有時會進行屏障雷射(在壞死病變的後極側進行光凝固),但目前有限證據顯示其能確實預防視網膜剝離。考慮到壞死區域的脆弱性和牽引力,一旦發生剝離,玻璃體手術(矽油填充)是根本的治療方法。
6. 病理生理學與詳細發病機制
Section titled “6. 病理生理學與詳細發病機制”ARN的發病是由於皰疹病毒(HSV-1、HSV-2、VZV)潛伏感染三叉神經節或脊神經後根神經節,在某些觸發因素(免疫低下、老化、壓力等)下再激活並到達眼內所致。
視網膜損傷的兩種機制
Section titled “視網膜損傷的兩種機制”-
病毒的直接細胞損傷:病毒在視網膜細胞內複製並導致細胞溶解。病毒增殖的部位肉眼可見為黃白色顆粒狀病變。
-
阻塞性血管炎導致的缺血:為清除病毒而發生的發炎細胞浸潤引起視網膜動脈周圍的血管炎,導致血管阻塞和視網膜缺血。阻塞性血管炎引起的水腫和循環障礙形成邊界清晰的地圖狀白色病變。
這兩種機制共同作用,導致視網膜快速壞死、變薄和脆弱化。5)
視網膜剝離的發生機轉
Section titled “視網膜剝離的發生機轉”發病後3-4週,玻璃體發生機化,導致不完全性玻璃體後剝離。此時,極度變薄和脆弱的壞死視網膜受到來自玻璃體的強烈牽引,形成多發裂孔。壞死區域的變薄和牽引力的共同作用導致約70%的病例發生視網膜剝離。
不同病毒類型的差異
Section titled “不同病毒類型的差異”- HSV-1 ARN在有單純疱疹病毒腦炎病史或合併症的患者中較易發生,也可能在腦炎後出現眼部症狀。
- HSV-2 ARN與腦膜炎有關,尤其在年輕患者中需注意。
- VZV ARN的阻塞性血管炎程度和視神經侵犯頻率高於HSV ARN,預後更差。
- 對側眼發病風險約為15%。左右眼發病間隔多在1個月內,但後發眼的病灶擴散有限,視力預後優於先發眼。
免疫抑制劑和新興感染相關ARN的特殊機轉
Section titled “免疫抑制劑和新興感染相關ARN的特殊機轉”- ICI(PD-1/PD-L1抑制劑)相關ARN:提示與免疫相關不良事件(類似IRIS機轉)、自身耐受障礙和眼部免疫特權喪失有關。12)
- COVID-19相關ARN:SARS-CoV-2感染導致CD3+ CD8+ T淋巴細胞顯著減少,被認為促進潛伏HSV的再活化。16)
- 那他珠單抗相關ARN:抑制白血球向中樞神經系統遷移導致CD4/CD8比值降低,從而降低病毒特異性免疫。13)
- DMF(富馬酸二甲酯)相關ARN:CD8+ T細胞和VZV特異性T細胞免疫降低增加再活化風險。14)
7. 最新研究與未來展望(研究階段報告)
Section titled “7. 最新研究與未來展望(研究階段報告)”口服伐昔洛韋誘導治療的有效性
Section titled “口服伐昔洛韋誘導治療的有效性”傳統的標準治療是靜脈注射阿昔洛韋的住院治療,但已有病例系列報告顯示口服伐昔洛韋或泛昔洛韋可使活動性視網膜炎消退。9) AAO報告也指出口服或靜脈注射抗病毒藥物的初始治療是有效的,但根據重症程度和全身狀態,通常優先考慮靜脈滴注。5)
玻璃體內抗病毒藥物的有效性
Section titled “玻璃體內抗病毒藥物的有效性”一項回顧性研究顯示,玻璃體內注射膦甲酸鈉(2.4 mg/0.1 mL)聯合全身治療,特別是在VZV ARN中,添加玻璃體內注射可能改善視力預後。7) 它可能實現高局部濃度同時最小化全身毒性,重症病例的誘導治療標準化是研究課題。
通過定量PCR監測疾病活動性
Section titled “通過定量PCR監測疾病活動性”通過眼內液定量PCR監測病毒量,據報導不僅有助於診斷,還可能有助於評估治療反應。10) 然而,重複取樣的侵入性和測量方法的標準化等問題仍存在,將其納入日常診療面臨挑戰。
厚脈絡膜作為ARN活動性標誌物的可能性
Section titled “厚脈絡膜作為ARN活動性標誌物的可能性”OCT上的脈絡膜增厚(厚脈絡膜)已被報導為反映急性視網膜壞死活動性的表現。在一例繼發性VZV-ARN病例中,OCT上的厚脈絡膜與壞死性視網膜炎區域一致出現,提示其可能作為治療後追蹤中的活動性標誌物。18)
膦甲酸鈉對EBV-ARN的有效性
Section titled “膦甲酸鈉對EBV-ARN的有效性”有報告稱,一例對阿昔洛韋和更昔洛韋耐藥的EBV-ARN病例,膦甲酸鈉4800 mg/日靜脈注射有效。20) 當病原體是VZV或HSV以外的病毒時,標準治療可能效果不佳,通過PCR鑑定病原病毒對確定治療方案很重要。
免疫抑制藥物和新興傳染病與ARN的關聯
Section titled “免疫抑制藥物和新興傳染病與ARN的關聯”隨著免疫檢查點抑制劑(ICI)的普及,需要注意VZV再激活導致ARN發病的風險。12) 此外,COVID-19感染後HSV/VZV再激活導致ARN的報告相繼出現,與免疫抑制治療相關的ARN未來可能繼續增加。14)16)
8. 參考文獻
Section titled “8. 參考文獻”-
日本眼炎症学会ぶどう膜炎診療ガイドライン作成委員会. ぶどう膜炎診療ガイドライン. 日眼会誌. 2019;123(6):635-796.
-
Urayama A, Yamada N, Sasaki T, et al. Unilateral acute uveitis with periarteritis and retinal detachment. Jpn J Clin Ophthalmol. 1971;25:607-619.
-
Standardization of Uveitis Nomenclature (SUN) Working Group. Classification criteria for acute retinal necrosis syndrome. Ophthalmology. 2021;128(12):1974-1980. doi:10.1016/j.ophtha.2021.11.011. PMID: 34807625.
-
Takase H, Okada AA, Goto H, et al. Development and validation of new diagnostic criteria for acute retinal necrosis. Jpn J Ophthalmol. 2015;59(1):14-20. doi:10.1007/s10384-014-0362-0. PMID: 25492579.
-
Schoenberger SD, Kim SJ, Thorne JE, et al. Diagnosis and Treatment of Acute Retinal Necrosis: A Report by the American Academy of Ophthalmology. Ophthalmology. 2017;124(3):382-392. doi:10.1016/j.ophtha.2016.11.007. PMID: 28094044.
-
Tibbetts MD, Shah CP, Young LH, et al. Treatment of acute retinal necrosis. Ophthalmology. 2010;117(4):818-824. doi:10.1016/j.ophtha.2009.09.001. PMID: 20110127.
-
Wong R, Pavesio CE, Laidlaw DA, et al. Acute retinal necrosis: the effects of intravitreal foscarnet and virus type on outcome. Ophthalmology. 2010;117(3):556-560. doi:10.1016/j.ophtha.2009.08.003. PMID: 20031221.
-
Flaxel CJ, Yeh S, Lauer AK. Combination systemic and intravitreal antiviral therapy in the management of acute retinal necrosis syndrome. Ophthalmic Surg Lasers Imaging Retina. 2013;44(6):521-526.
-
Aizman A, Johnson MW, Elner SG. Treatment of acute retinal necrosis syndrome with oral antiviral medications. Ophthalmology. 2007;114(2):307-312. doi:10.1016/j.ophtha.2006.06.058. PMID: 17123607.
-
Asano S, Yoshikawa T, Kimura H, et al. Monitoring herpesvirus DNA in three cases of acute retinal necrosis by real-time PCR. J Clin Virol. 2004;29(3):206-209. PMID: 15002491.
-
Cochrane TF, Silvestri G, McDowell C, et al. Acute retinal necrosis in the United Kingdom: results of a prospective surveillance study. Eye (Lond). 2012;26(3):370-377.
-
Wang P, An M, Zhang M, et al. Acute retinal necrosis in a patient with cervical malignant tumor treated with sintilimab: a case report and literature review. Front Immunol. 2024;15:1301329.
-
Cheraqpour K, Ahmadraji A, Rashidinia A, et al. Acute retinal necrosis caused by co-infection with multiple viruses in a natalizumab-treated patient: a case report and brief review of literature. BMC Ophthalmol. 2021;21:337.
-
Paisey C, Curtin K, Epps SJ, et al. Acute retinal necrosis associated with dimethyl fumarate. Mult Scler J. 2025;31(12):1506-1508.
-
Luo T, Wang L, Zhang L, et al. Acute retinal necrosis following cataract surgery: a case of VZV reactivation and successful management. BMC Ophthalmol. 2025;25:131.
-
Gonzalez MP, Rios R, Pappaterra M, et al. Reactivation of acute retinal necrosis following SARS-CoV-2 infection. Case Rep Ophthalmol Med. 2021;2021:7336488.
-
Rahman EZ, Shah P, Shah R. Metastatic squamous cell carcinoma masquerading as acute retinal necrosis. Am J Ophthalmol Case Rep. 2023;32:101934.
-
Harbeck K, Ericksen C, Johnson W, et al. Pachychoroid associated with acute retinal necrosis secondary to varicella zoster virus. J Vitreoretinal Dis. 2024;8(2):196-199.
-
Perhiar BA, Siddiqui MAR, Ibrahim S. Acute retinal necrosis with exudative retinal detachment in a child. BMJ Case Rep. 2021;14:e245984.
-
Suzuki K, Namba K, Hase K, et al. A case of Epstein-Barr virus acute retinal necrosis successfully treated with foscarnet. Am J Ophthalmol Case Rep. 2022;25:101363.
