ชนิดเม็ดเล็กบริเวณรอบนอก
ลักษณะ: แทบไม่มีเลือดออก มีจุดขาวขุ่นแบบเม็ดเล็กสะสมเป็นรูปพัด
ผลต่อการมองเห็น: หากหลีกเลี่ยงจุดรับภาพ (macula) การมองเห็นจะคงอยู่ค่อนข้างดี
การดำเนินโรค: ชนิดที่พบบ่อยที่สุด ค่อยๆ ลุกลามจากรอบนอกเข้าสู่ศูนย์กลาง

Human herpesvirus 5 หรือชื่อสามัญ cytomegalovirus (CMV) เป็นไวรัสที่ใหญ่ที่สุดในวงศ์ herpesvirus มี DNA สายคู่ ไวรัสมีความสัมพันธ์กับเนื้อเยื่อต่างๆ ในร่างกายมนุษย์ และผ่านการติดเชื้อครั้งแรก การติดเชื้อซ้ำ หรือการกลับมาทำงานที่จอประสาทตา ทำให้เกิดจอประสาทตาอักเสบจาก CMV ซึ่งมีลักษณะเด่นคือการตายและบวมของจอประสาทตาทุกชั้น
อัตราการมีแอนติบอดีต่อ CMV สูง (70-90%) และการติดเชื้อส่วนใหญ่ไม่มีอาการในวัยทารก จอประสาทตาอักเสบจาก CMV ในผู้ใหญ่ส่วนใหญ่เป็นการติดเชื้อฉวยโอกาสจากการกลับมาทำงานของไวรัส1)
หากมารดามีการติดเชื้อครั้งแรกหรือการกลับมาทำงานในช่วงต้นของการตั้งครรภ์ 20-40% ของกรณีจะติดต่อสู่ทารกผ่านรก ทำให้เกิดจอประสาทตาอักเสบจาก CMV แต่กำเนิดซึ่งเป็นส่วนหนึ่งของกลุ่มอาการ TORCH
ระบาดวิทยา:
โดยหลักการแล้ว พบได้น้อยมากในผู้ที่มีภูมิคุ้มกันปกติ อย่างไรก็ตาม ในช่วงไม่กี่ปีที่ผ่านมา รายงานของกลุ่มอาการส่วนหน้าของตาจาก CMV ที่แสดงเป็นม่านตาอักเสบส่วนหน้าหรือเยื่อบุผิวดอกระจกตาอักเสบในผู้ที่มีภูมิคุ้มกันปกติมีเพิ่มขึ้น (ดูหัวข้อแยก “ม่านตาอักเสบส่วนหน้าจาก CMV”) จอประสาทตาอักเสบจาก CMV (รอยโรคส่วนหลัง) ส่วนใหญ่เป็นการติดเชื้อฉวยโอกาสในภาวะภูมิคุ้มกันบกพร่อง 1) และพบน้อยมากในผู้ที่มีสุขภาพดี ปัจจัยพื้นฐานรวมถึงการใช้สเตียรอยด์เป็นเวลานาน การทำงานของภูมิคุ้มกันลดลงจากเบาหวาน และภาวะชราภาพของระบบภูมิคุ้มกัน 11, 12)
ได้ ในการศึกษาย้อนหลัง มีรายงานว่า 15% ของผู้ป่วยจอประสาทตาอักเสบจาก CMV ที่ติดเชื้อ HIV ไปพบจักษุแพทย์ก่อนการวินิจฉัย HIV และใน 9% จอประสาทตาอักเสบจาก CMV เป็นเกณฑ์การวินิจฉัยโรคเอดส์เพียงอย่างเดียว 13) เมื่อสงสัยจอประสาทตาอักเสบจาก CMV ควรทำการตรวจ HIV อย่างจริงจัง
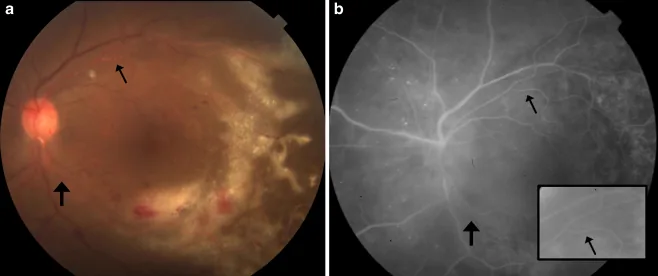
แตกต่างกันไปตามตำแหน่งและขนาดของรอยโรค
ในระยะแรก แทบไม่พบการอักเสบของช่องหน้าตาหรือวุ้นตา และอาการเหล่านี้จะปรากฏเมื่อรอยโรคขยายใหญ่ขึ้น ซึ่งเป็นลักษณะเฉพาะและเป็นจุดแยกสำคัญจาก ARN
จอประสาทตาอักเสบจาก CMV แบ่งเป็น 3 ชนิดตามลักษณะเฉพาะของจอตา ในทางปฏิบัติทางคลินิก ชนิดเหล่านี้มักปะปนกัน และตำแหน่งและขนาดของรอยโรคมีความสำคัญมากกว่าสำหรับการพยากรณ์โรค
ชนิดเม็ดเล็กบริเวณรอบนอก
ลักษณะ: แทบไม่มีเลือดออก มีจุดขาวขุ่นแบบเม็ดเล็กสะสมเป็นรูปพัด
ผลต่อการมองเห็น: หากหลีกเลี่ยงจุดรับภาพ (macula) การมองเห็นจะคงอยู่ค่อนข้างดี
การดำเนินโรค: ชนิดที่พบบ่อยที่สุด ค่อยๆ ลุกลามจากรอบนอกเข้าสู่ศูนย์กลาง
ชนิดหลอดเลือดอักเสบที่ขั้วหลัง
ลักษณะ: มีจุดขาวขุ่นสีเหลือง-ขาวร่วมกับเลือดออกในจอตาและบวมน้ำตามแนวหลอดเลือดที่ขั้วหลัง มีเนื้อตายและเลือดออกกว้างขวางคล้าย “พิซซ่าไพ” เป็นลักษณะเฉพาะ
ผลต่อการมองเห็น: กระทบจุดรับภาพและประสาทตา ทำให้การมองเห็นลดลงอย่างชัดเจน
การดำเนินโรค: ชนิดที่มีการพยากรณ์การมองเห็นแย่ที่สุด การเริ่มรักษาอย่างรวดเร็วเป็นสิ่งสำคัญ
ชนิดหลอดเลือดอักเสบแบบกิ่งไม้เยือกแข็ง
ลักษณะ: หลอดเลือดจอตากลายเป็นสีขาวคล้ายหลอดเลือดอักเสบแบบกิ่งไม้เยือกแข็ง (frosted branch angiitis; FBA) โดยเฉพาะรอบหลอดเลือดใหญ่
ความถี่: ชนิดที่พบได้ค่อนข้างน้อย อาจปรากฏเป็นสัญญาณของ CMV-IRIS10)
ข้อควรระวัง: ในทางปฏิบัติทางคลินิก ทั้งสามชนิดมักปะปนกัน และตำแหน่งและขนาดของรอยโรคมีความสำคัญต่อการพยากรณ์โรค
การแบ่งโซนรอยโรคมีความสำคัญในการพิจารณาความเร่งด่วนของการรักษา
| โซน | ขอบเขต | ความสำคัญทางคลินิก |
|---|---|---|
| โซน 1 | ภายใน 1 DD ของจานประสาทตา และ 2 DD ของจอประสาทตา | เริ่มการรักษาทันที |
| โซน 2 | จากเส้นศูนย์สูตรถึงหลอดเลือดดำวอร์ติโคส | พิจารณาการรักษา |
| โซน 3 | ส่วนปลายสุด | สามารถสังเกตอาการได้ |
จอประสาทตาลอก (RD) เป็นภาวะแทรกซ้อนที่รุนแรง ยิ่งรอยโรคมีขอบเขตกว้างมากเท่าใด ความเสี่ยงต่อจอประสาทตาลอกชนิดมีรอยฉีกขาดก็ยิ่งสูงขึ้น แม้ว่าจะลดลงหลังจากการแพร่หลายของ ART แต่ยังคงต้องเฝ้าระวังในระยะยาวแม้หลังการรักษา 3).
Tang และคณะ (2021) รายงานผู้ป่วย HIV ที่เกิดหลอดเลือดจอประสาทตาอักเสบแบบน้ำค้างแข็ง 35 วันหลังจากเริ่ม HAART 10) IL-6 ในอารมณ์ขันน้ำเพิ่มขึ้นเป็น 2,845 pg/mL และ IL-8 เป็น 967.8 pg/mL บ่งชี้ถึงจอประสาทตาอักเสบจาก CMV ในรูปแบบ IRIS แบบ unmasking การอักเสบดีขึ้นด้วยการรักษาด้วยยาต้านไวรัสเท่านั้น
ในรอยโรคจอประสาทตาอักเสบจาก CMV เรื้อรัง จอประสาทตาทุกชั้นจะตายและบางลงเป็นรูปร่างคล้ายลูกไม้ เมื่อมีแรงดึงของวุ้นตา จะเกิดรอยฉีกขาดหลายแห่งและจอประสาทตาลอกได้ง่าย ดังนั้นแม้จอประสาทตาอักเสบจะสงบลงแล้ว ก็ยังต้องติดตามผลในระยะยาว
ชั้นจอประสาทตาที่ตายจะบางลงเหมือนลูกไม้ เมื่อมีแรงดึงของวุ้นตา จะเกิดรอยฉีกขาดหลายแห่งได้ง่าย โดยเฉพาะที่ขอบของเนื้อตาย การบางลงจะรุนแรงและมีความเสี่ยงสูงต่อการเกิดรอยฉีกขาด แม้จอประสาทตาอักเสบจะสงบลงหลังการรักษา จอประสาทตาที่บางยังคงอยู่ จึงจำเป็นต้องติดตามผลในระยะยาว
จอประสาทตาอักเสบจาก CMV ส่วนใหญ่เป็นการติดเชื้อฉวยโอกาสในภาวะภูมิคุ้มกันบกพร่อง ในผู้ป่วยผู้ใหญ่ การตรวจสอบโรคพื้นเดิมที่ทำให้เกิดภูมิคุ้มกันบกพร่อง เช่น กลุ่มอาการภูมิคุ้มกันบกพร่องที่ได้มา (เอดส์) หรือประวัติการใช้ยากดภูมิคุ้มกันเป็นจุดเริ่มต้นของการวินิจฉัย 1).
ปัจจัยเสี่ยงหลัก:
ไม่มีเกณฑ์การวินิจฉัยที่ชัดเจนสำหรับจอประสาทตาอักเสบจาก CMV แต่เนื่องจากมีรอยโรคจอประสาทตาที่มีลักษณะเฉพาะ จึงสามารถวินิจฉัยทางคลินิกได้โดยการรวมประวัติผู้ป่วย (ภาวะภูมิคุ้มกันบกพร่อง) และผลการตรวจอวัยวะภายในตา
| การตรวจ/การประเมิน | เนื้อหา |
|---|---|
| ผลการตรวจอวัยวะภายในตา | ยืนยันสามรูปแบบ (ชนิดเม็ดเล็กบริเวณรอบนอก, ชนิดหลอดเลือดอักเสบที่ขั้วหลัง, ชนิดหลอดเลือดอักเสบแบบกิ่งไม้) ในระยะแรก การอักเสบของช่องหน้าม่านตาและวุ้นตาแก้วตาอักเสบมีน้อย |
| PCR เชิงปริมาณของของเหลวในลูกตา (แบบเรียลไทม์) | มีความไวและความจำเพาะสูง ใช้สำหรับการวินิจฉัยที่แน่นอน อาจตรวจไม่พบในระยะแรกเมื่อไม่มีเซลล์อักเสบในช่องหน้าม่านตา1) |
| PCR หลายรายการ (การแพทย์ขั้นสูง) | การค้นหาไวรัสหลายชนิดอย่างครอบคลุมด้วยตัวอย่างปริมาณน้อย มีประโยชน์ในการแยกความแตกต่างจาก ARN1) |
| การตรวจ CMV แอนติเจนในเลือดและ PCR เลือด | ค่า参考สำหรับการวินิจฉัยเสริม สำหรับการวินิจฉัยที่แน่นอน ควรใช้ PCR เฉพาะที่ของตา |
| การยืนยันประวัติผู้ป่วย | ค่า CD4, ประวัติการใช้ยากดภูมิคุ้มกัน, สถานะการรักษาด้วย ART เป็นต้น |
เกณฑ์ ACTG (AIDS Clinical Trials Group)1):
เกณฑ์ ACTG (AIDS Clinical Trials Group)1):
Next-generation sequencing (NGS) ได้รับรายงานว่าเป็นเครื่องมือช่วยวินิจฉัยในกรณีที่วินิจฉัยยากด้วย PCR และมีตัวอย่างการใช้ในกรณีหลัง CAR-T8) ในผู้ป่วยภูมิคุ้มกันกด HIV-negative การวินิจฉัยมักล่าช้า ดังนั้นไม่ควรตัดออกโดยอาศัยการตรวจซีรั่มเพียงอย่างเดียว แต่ควรใช้ลักษณะทางตาและการตรวจของเหลวในลูกตาร่วมกัน7, 9)
ในการแยกจาก cotton-wool spot ขนาดของรอยโรคอาจช่วยได้ รอยโรค <750 μm บ่งชี้ cotton-wool spot ในขณะที่รอยโรคที่ใหญ่กว่าบ่งชี้ CMV retinitis
การวินิจฉัยแยกโรค:
การวินิจฉัยทางคลินิกขึ้นอยู่กับลักษณะเฉพาะของจอตา (หนึ่งใน 3 แบบ) และประวัติผู้ป่วย (ภาวะภูมิคุ้มกันบกพร่อง) สำหรับการวินิจฉัยที่แน่นอน การตรวจ PCR แบบเรียลไทม์เชิงปริมาณของของเหลวในลูกตา (อารมณ์ขันในช่องหน้าหรือวุ้นตา) มีความไวและความจำเพาะสูงที่สุด 1) PCR หลายเชื้อโรค (การแพทย์ขั้นสูง) มีข้อดีในการแยกแยะไวรัสหลายชนิดจากตัวอย่างขนาดเล็ก ซึ่งมีประโยชน์อย่างยิ่งในการแยกความแตกต่างจากจอประสาทตาอักเสบชนิดเนื้อตายเฉียบพลัน
การรักษาด้วยยาต้าน CMV คือการให้แกนซิโคลเวียร์ทางหลอดเลือดดำเป็นทางเลือกแรก และขึ้นอยู่กับตำแหน่งและขนาดของรอยโรคและการมีผลข้างเคียง อาจใช้วาลแกนซิโคลเวียร์ชนิดรับประทานหรือฟอสคาร์เนททางหลอดเลือดดำหรือการฉีดเข้าแก้วตาเพียงอย่างเดียวหรือร่วมกัน จอประสาทตาอักเสบจาก CMV มักเกิดร่วมกับการติดเชื้อ CMV แฝงในหลายอวัยวะ ดังนั้นพื้นฐานของการรักษาด้วยยาต้านไวรัสคือการรักษาทั่วร่างกาย
ต่อไปนี้เป็นใบสั่งยาหลัก:
| ยา | ชื่อผลิตภัณฑ์ | ขนาดยาเริ่มต้น | ขนาดยาบำรุงรักษา |
|---|---|---|---|
| แกนซิโคลเวียร์ฉีดเข้าหลอดเลือดดำ | ดีโนซินสำหรับฉีดเข้าหลอดเลือดดำ (500 มก.) | 5 มก./กก./ครั้ง วันละ 2 ครั้ง | 5 มก./กก./ครั้ง วันละ 1 ครั้ง |
| วาลแกนซิโคลเวียร์ชนิดรับประทาน | ยาเม็ดวาลิกซา (450 มก.) | 4 เม็ด (1,800 มก.) แบ่งให้ 2 ครั้งหลังอาหาร | 2 เม็ด (900 มก.) ครั้งเดียวหลังอาหาร |
| ฟอสคาร์เนทฉีดเข้าหลอดเลือดดำ | ยาฉีดฟอสคาเวียร์ (24 มก./มล.) | 90 มก./กก./ครั้ง วันละ 2 ครั้ง | 90 มก./กก./ครั้ง วันละ 1 ครั้ง |
การรักษาแบบเหนี่ยวนำโดยทั่วไปจะดำเนินการเป็นเวลา 2-3 สัปดาห์ หลังจากนั้นจะรักษาแบบประคับประคองต่อไป ฟอสคาร์เนทเป็นทางเลือกเมื่อมีการกดไขกระดูกจากแกนซิโคลเวียร์อย่างรุนแรง แต่ต้องระวังพิษต่อไต
ในกรณีที่มีปัญหาผลข้างเคียงหรือรอยโรคอยู่ที่ขั้วหลัง อาจทำการฉีด GCV หรือฟอสคาร์เนทเข้าแก้วตา (นอกประกัน)
ฟอสคาร์เนทและซิโดโฟเวียร์เป็นทางเลือกที่สองเมื่อไม่ทนหรือดื้อต่อ GCV/VGCV ซิโดโฟเวียร์ให้สัปดาห์ละครั้ง (เหนี่ยวนำ) → ทุก 2 สัปดาห์ (ประคับประคอง) มีผลข้างเคียงคือความดันลูกตาลดลง (ถึง 50%) ม่านตาอักเสบส่วนหน้า และพิษต่อไต จึงต้องให้โพรเบเนซิดก่อน
หลังจากเริ่ม HAART ในระหว่างที่ CD4 ฟื้นตัว อาจเกิดการตอบสนองทางภูมิคุ้มกันที่มากเกินไปต่อแอนติเจน CMV ที่เหลืออยู่ (เกิดขึ้นใน 10-17% ของ CMV ส่วนใหญ่ภายใน 3 เดือนหลังจากเริ่ม HAART) การจัดการมีดังนี้:
หลังจากสิ้นสุดการรักษาแบบ induction ให้รักษาแบบ maintenance ต่อ ในผู้ป่วย HIV/AIDS ให้การรักษาด้วยยาต้านไวรัสอย่างน้อย 6 เดือน และหากจำนวน CD4+ T cell >100/μL คงอยู่นาน 4-6 เดือน ให้พิจารณาหยุด การติดตามผล: ระหว่าง induction สัปดาห์ละครั้ง ระหว่าง maintenance ทุก 2 สัปดาห์ด้วยการตรวจ fundus ผ่านม่านตาขยาย หลังจากคงที่แล้วเดือนละครั้ง
ในกรณีที่มีจอประสาทตาลอกชนิด rhegmatogenous ให้การรักษาโดยการผ่าตัด ขึ้นอยู่กับขนาดของรอยโรคและระดับของการลอก ให้ผสมผสานดังนี้:
หากได้รับการรักษาในเวลาที่เหมาะสม การพยากรณ์โรคไม่เลวร้ายเท่ากับจอประสาทตาตายเฉียบพลัน
การหยุดการกดภูมิคุ้มกันเป็นการรักษาที่รากฐาน ในผู้ติดเชื้อ HIV การเริ่มหรือรักษาการรักษาด้วยยาต้านไวรัส (ART) เพื่อฟื้นฟู CD4 เป็นพื้นฐานสำคัญในการป้องกันการกลับเป็นซ้ำของจอประสาทตาอักเสบจาก CMV ต้องระวังการเกิดม่านตาอักเสบจากการฟื้นคืนภูมิคุ้มกัน (IRU) หลังจากเริ่ม ART (→ ดูหัวข้อ “พยาธิสรีรวิทยา/กลไกการเกิดโรคโดยละเอียด”)
ไม่ได้ผล CMV มีความไวต่ออะไซโคลเวียร์และวาลาไซโคลเวียร์ต่ำ ยารักษา HSV/VZV ไม่เพียงพอ สำหรับ CMV แกนซิโคลเวียร์หรือวัลแกนซิโคลเวียร์เป็นตัวเลือกแรก หากใช้แกนซิโคลเวียร์ได้ยากเนื่องจากผลข้างเคียง เช่น การกดไขกระดูก ให้ใช้ฟอสคาร์เนทเป็นทางเลือก
CMV เป็นไวรัส DNA สายคู่ที่ใหญ่ที่สุดในวงศ์ Herpesviridae หลังการติดเชื้อครั้งแรก ไวรัสจะแฝงตัวในเซลล์ต้นกำเนิดไมอีลอยด์ โมโนไซต์ และแมคโครฟาจ เมื่อการทำงานของภูมิคุ้มกันลดลง ไวรัสจะกลับมากระตุ้นและแพร่กระจายทางเลือดเข้าสู่ดวงตา ทำให้เกิดจอประสาทตาอักเสบจาก CMV
CMV ติดเชื้อทุกชั้นของจอประสาทตา และการทำลายเซลล์โดยตรงจากไวรัสเป็นสาเหตุหลักที่ทำให้เกิดเนื้อตายที่จอประสาทตา การอักเสบที่เกิดจากภูมิคุ้มกันอย่างรุนแรงเช่นใน ARN พบได้น้อย และเนื่องจากการตอบสนองทางภูมิคุ้มกันอ่อนแอ ทำให้อาการอักเสบไม่ชัดเจน นี่คือสาเหตุที่การอักเสบของช่องหน้าม่านตาและวุ้นตาแทบไม่พบในระยะแรก
CMV ผลิตอินเตอร์ลิวคิน-10 ของไวรัส (cmvIL-10) เพื่อกดภูมิคุ้มกัน โปรตีน pp65 ยับยั้งเส้นทางสัญญาณ cGAS-STING และโมเลกุลคล้าย MHC-I หลบเลี่ยงการโจมตีของเซลล์ NK 14) กลไกการหลบหลีกภูมิคุ้มกันเหล่านี้เป็นพื้นฐานของการติดเชื้อเรื้อรังแบบต่อเนื่อง นอกจากนี้ยังพบว่า CMV เพิ่มการแสดงออกของตัวรับ ACE2 ซึ่งอาจส่งเสริมการติดเชื้อร่วมกับ SARS-CoV-2 14)
การติดเชื้อร่วม CMV กับ VZV และ EBV มีการพยากรณ์โรคที่แย่กว่าการติดเชื้อเดี่ยว
Kondo และคณะ (2025) รายงานผู้ป่วยจอประสาทตาอักเสบจาก CMV ทั้งสองข้างที่มีการติดเชื้อร่วม EBV และ VZV 15) การตรวจ PCR เชิงปริมาณพบระดับสูงของ CMV 6.7×10⁷ ชุด/มล. และ VZV 1.3×10⁸ ชุด/มล. ซึ่งนำไปสู่จอประสาทตาลอกในทั้งสองข้าง
เมื่อจำนวนลิมโฟไซต์ที CD4+ เพิ่มขึ้นอย่างรวดเร็วหลังจากเริ่มการรักษาด้วยยาต้านไวรัส (ART) อาจเกิดการแย่ลงของการติดเชื้อฉวยโอกาสที่มีอยู่หรือเกิดรอยโรคใหม่ ภาวะนี้เรียกว่ากลุ่มอาการฟื้นฟูภูมิคุ้มกัน (IRIS) ในจักษุวิทยา เป็นที่รู้จักกันว่า IRU เกิดขึ้นในตาที่มีประวัติจอประสาทตาอักเสบจาก CMV ที่สงบแล้วหลังจากเริ่ม ART ทำให้เกิดวุ้นตาอักเสบ 1)
กลไกของ IRU: ทฤษฎีหลักคือเมื่อ ART ฟื้นฟูการตอบสนองของทีเซลล์ที่จำเพาะต่อ CMV แอนติเจน CMV ที่เหลือซึ่งจำลองแบบเล็กน้อยภายในเซลล์ที่ขอบของรอยโรคจอประสาทตาอักเสบจาก CMV ที่สงบแล้วจะกระตุ้นให้เกิดม่านตาอักเสบผ่านการตอบสนองทางภูมิคุ้มกัน IRIS ชนิด “เปิดโปง” เป็นภาวะที่การติดเชื้อที่เคยควบคุมได้ปรากฏชัดขึ้นทันทีหลังจากเริ่ม HAART 10)
อาการและการวินิจฉัย IRU: นอกจากรอยโรคเริ่มต้นเช่นม่านตาอักเสบร่วมกับซิลิอารีบอดีและวุ้นตาอักเสบแล้ว อาจเกิดภาวะแทรกซ้อนเช่นจอประสาทตาบวมน้ำและต้อกระจก ประวัติการเริ่ม ART และการเพิ่มขึ้นของจำนวนลิมโฟไซต์ที CD4+ เป็นสิ่งจำเป็นสำหรับการวินิจฉัย
การรักษา IRU: แตกต่างกันไปตามความรุนแรงและระยะเวลา ตั้งแต่การหายเองตามธรรมชาติด้วยการสังเกตไปจนถึงกรณีที่ต้องหยุด ART ให้สเตียรอยด์ทั้งตัว หรือการผ่าตัด แต่การเริ่มการรักษาด้วยยาต้าน CMV อีกครั้งสำหรับเชื้อที่เหลือเป็นพื้นฐาน 1)
ในขณะที่จอประสาทตาอักเสบจาก CMV ในผู้ป่วยเอดส์ลดลงอย่างมากเนื่องจากการแพร่หลายของ ART รายงานในผู้ป่วยภูมิคุ้มกันบกพร่องที่ไม่ใช่เอดส์ เช่น หลังปลูกถ่ายอวัยวะ การบำบัดด้วยเซลล์ CAR-T และผู้ใช้สารชีวภาพกำลังเพิ่มขึ้น 7, 9) ความหลากหลายของสาเหตุของภูมิคุ้มกันบกพร่องเป็นความท้าทายในการกำหนดมาตรฐานของข้อบ่งชี้ ระยะเวลา และการเลือกยาสำหรับการป้องกัน CMV ต้องระวังการวินิจฉัยที่ล่าช้าในผู้ป่วยที่ติดเชื้อ HIV ลบ 7, 9)
ในจอประสาทตาอักเสบจาก CMV ที่ดื้อยาหรือกลับเป็นซ้ำ การทำความเข้าใจการตอบสนองทางภูมิคุ้มกันของโฮสต์นอกเหนือจากยาต้านไวรัสเป็นสิ่งสำคัญ Li และคณะ (2022) รายงานถึงความเป็นไปได้ของการระดมทีเซลล์ที่จำเพาะต่อ CMV ไม่เพียงพอในจอประสาทตาอักเสบจาก CMV ในบุคคลที่มีภูมิคุ้มกันปกติ 16) และการอธิบายกลไกการหลบหลีกภูมิคุ้มกันเฉพาะที่อาจนำไปสู่การพัฒนาการรักษาในอนาคต ปัจจุบัน การรักษาที่เกี่ยวข้องกับทีเซลล์อยู่ในขั้นตอนการวิจัยและไม่ใช่การรักษามาตรฐาน
เลเทอร์โมเวียร์ (letermovir) และมาริบาเวียร์ (maribavir) เป็นยาต้านไวรัสชนิดใหม่ที่แสดงประสิทธิภาพต่อ CMV ที่ดื้อต่อ GCV/ฟอสคาร์เนท โดยเฉพาะมาริบาเวียร์ได้รับการอนุมัติจาก FDA สำหรับการติดเชื้อ CMV ที่ดื้อหรือไม่ตอบสนองหลังการปลูกถ่ายเซลล์ต้นกำเนิดเม็ดเลือด (HSCT) หลักฐานสำหรับจอประสาทตาอักเสบจาก CMV ยังมีจำกัด แต่คาดว่าจะนำไปใช้ในกรณีที่ดื้อยาหลายชนิด
Zu และคณะ (2022) รายงานกรณีแรกของโลกของจอประสาทตาอักเสบจาก CMV หลังการรักษาด้วยเซลล์ CAR-T 8) การลดลงอย่างรุนแรงของภูมิคุ้มกันแบบฮิวโมรัลจากการรักษาด้วย CAR-T เชื่อว่ากระตุ้นการกลับมาทำงานของ CMV และใช้ NGS ในการวินิจฉัย ซึ่งบ่งชี้ถึงความจำเป็นในการตรวจคัดกรอง CMV หลังผ่าตัดและการติดตามทางจักษุวิทยาในผู้ป่วยที่ได้รับการรักษาด้วย CAR-T
CMV อาจเอื้อต่อการติดเชื้อร่วมกับ SARS-CoV-2 โดยเพิ่มการแสดงออกของ ACE2 14) นอกจากนี้ยังมีรายงานการกลับมาทำงานของ CMV หลังจาก COVID-19 ที่รุนแรง 14) ในผู้ป่วยที่มีภูมิคุ้มกันบกพร่องซึ่งมี COVID-19 รุนแรง ควรพิจารณาการประเมินทางจักษุวิทยา
การระบุความหลากหลายทางพันธุกรรมของโฮสต์ที่ส่งผลต่อความไวต่อ CMV กำลังก้าวหน้า 14) ในอนาคต การตรวจคัดกรองทางพันธุกรรมของผู้ป่วยที่มีความเสี่ยงสูงอาจถูกนำมาใช้ในกลยุทธ์การป้องกัน
การติดตามระยะยาวโดย Studies of Ocular Complications of AIDS (SOCA) แสดงให้เห็นว่าการพยากรณ์ความคมชัดของการมองเห็นของผู้ป่วยจอประสาทตาอักเสบจาก CMV ในยุค ART ดีขึ้น แต่อาการบวมน้ำที่จุดรับภาพ ต้อกระจก และจอประสาทตาเสื่อมชนิดโปรลิเฟอเรทีฟวุ้นตาจาก IRU เป็นสาเหตุหลักของการมองเห็นลดลง 3)
ในช่วงไม่กี่ปีที่ผ่านมา มีรายงานม่านตาอักเสบและเยื่อบุกระจกตาอักเสบจาก CMV (ม่านตาอักเสบส่วนหน้าจาก CMV) ในผู้ที่มีภูมิคุ้มกันปกติ ซึ่งขยายขอบเขตของการติดเชื้อ CMV ในลูกตา รายงาน TITAN 2 นำเสนอฉันทามติระหว่างประเทศสำหรับการจัดการม่านตาอักเสบส่วนหน้าจาก CMV และคาดว่าจะมีการสะสมหลักฐานในอนาคต 2)
การวิจัยเกี่ยวกับการแทรกแซงตั้งแต่เนิ่นๆ เพื่อปรับปรุงการพยากรณ์โรคระยะยาวของภาวะแทรกซ้อนทางจักษุวิทยาของการติดเชื้อ CMV แต่กำเนิด (จอประสาทตาอักเสบจาก CMV และฝ่อของเส้นประสาทตา) กำลังดำเนินอยู่ การเริ่มต้นการรักษาด้วยยาต้านไวรัสตั้งแต่เนิ่นๆ อาจช่วยปรับปรุงการพยากรณ์การทำงานของการมองเห็น