周辺部顆粒型
特徴:出血をほとんど伴わず、白色顆粒状の滲出斑が扇形に集積する。
視力への影響:黄斑部を避ければ視力は比較的保たれる。
経過:最も多い病型。周辺部から徐々に中央へ進行する。

ヒトヘルペスウイルス5、一般名サイトメガロウイルス(cytomegalovirus:CMV)は2本鎖DNAをもつヘルペスウイルス科最大のウイルスである。ヒトの体内では広範な組織に親和性があり、網膜への初感染・再感染または再活性化により、網膜全層の壊死と浮腫を主体とするCMV網膜炎を発症する。
CMV抗体保有率は70〜90%と高く、ほとんどが乳幼児期に不顕性感染している。成人にみられるCMV網膜炎はウイルスの再活性化に伴う日和見感染が大多数を占める1)。
妊娠初期に母体が初感染または再活性化をきたすと、20〜40%が経胎盤的に胎児に感染し、TORCH症候群の一つである先天性CMV感染症としてCMV網膜炎を発症することもある。
疫学:
原則として健常免疫正常者への発症はまれである。ただし近年、免疫正常者に前部ぶどう膜炎・角膜内皮炎として発症するCMV前部眼症候群の報告が増えている(別項「CMV前部ぶどう膜炎」参照)。CMV網膜炎(後部病変)は免疫不全下の日和見感染が主体であり1)、健常者では極めてまれである。長期ステロイド使用・糖尿病による免疫機能低下・免疫老化(immunosenescence)などが背景として挙げられる11, 12)。
ある。後ろ向き研究では、HIV陽性CMV網膜炎患者の15%がHIV診断前に眼科を受診しており、9%ではCMV網膜炎がAIDSの唯一の診断基準疾患であったと報告されている13)。CMV網膜炎を疑った場合は、HIV検査を積極的に行うべきである。
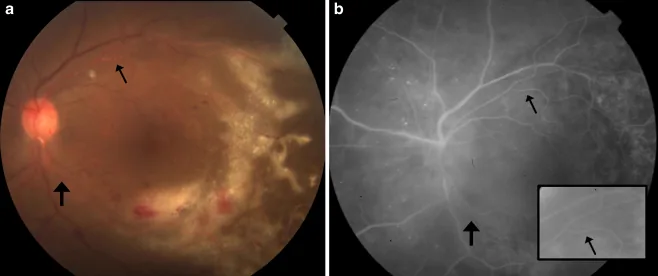
病変の部位と大きさにより多彩である。
初期に前房炎症・硝子体炎はほとんどみられず、病変の拡大とともにこれらの所見が出現する点が特徴的で、ARNとの重要な鑑別点となる。
CMV網膜炎は特徴的な眼底所見から3病型に分類される。実臨床ではこれらが混在することが多く、病巣の出現部位と大きさのほうが予後予測に重要となる。
周辺部顆粒型
特徴:出血をほとんど伴わず、白色顆粒状の滲出斑が扇形に集積する。
視力への影響:黄斑部を避ければ視力は比較的保たれる。
経過:最も多い病型。周辺部から徐々に中央へ進行する。
後極部血管炎型
特徴:後極部の血管に沿って網膜出血と浮腫を伴う黄白色滲出斑が出現する。「ピザパイ状(pizza pie)」と形容される広範な壊死・出血が特徴的。
視力への影響:黄斑部・視神経を侵すため視力低下が顕著。
経過:視力予後が最も悪い病型。迅速な治療開始が重要。
樹水状血管炎型
特徴:大血管を中心に網膜血管が樹水状血管炎様に白鞘化する(霜枝状血管炎・frosted branch angiitis; FBA)。
頻度:比較的まれな病型。CMV-IRISの徴候として出現することがある10)。
注意:実臨床では3病型が混在することも多く、病巣の部位と大きさが予後予測に重要。
病変のゾーン分類は治療の緊急度を判断するうえで重要である。
| ゾーン | 範囲 | 臨床的意義 |
|---|---|---|
| Zone 1 | 視神経乳頭1DD以内・黄斑2DD以内 | 即座に治療開始 |
| Zone 2 | 赤道部〜渦静脈膨大部 | 治療を考慮 |
| Zone 3 | 最周辺部 | 経過観察も可 |
網膜剥離(RD)は重篤な合併症である。病変範囲が広いほど裂孔原性網膜剥離のリスクが高く、ART普及後は以前より減少したものの、治療後も長期に注意が必要である3)。
Tangら(2021)は、HAART開始35日後に霜枝状血管炎を発症したHIV患者を報告した10)。房水中IL-6は2,845 pg/mL、IL-8は967.8 pg/mLと著明に上昇しており、unmaskingタイプのIRISとしてのFBAであった。抗ウイルス療法のみで炎症が改善した。
陳旧性CMV網膜炎病巣部は網膜全層が壊死に至りレース状に菲薄化し、硝子体の牽引が加わると容易に多発裂孔を生じ、網膜剥離をきたす。そのため網膜炎が鎮静化したあとも長期的な経過観察が必要である。
壊死した網膜全層が菲薄化してレース状になる。そこに硝子体牽引が加わると容易に多発裂孔を生じる。特に壊死縁では菲薄化が著しく裂孔形成のリスクが高い。治療で網膜炎が鎮静化した後も、菲薄化した網膜が残存するため長期にわたる経過観察が必要である。
CMV網膜炎は免疫不全下での日和見感染が大多数を占める。成人患者の背景として後天性免疫不全症候群(AIDS)をはじめとした免疫不全をきたす基礎疾患や薬剤投与歴を確認することが診断の出発点となる1)。
主なリスク因子:
CMV網膜炎に対する明確な診断基準はないが、特徴的な網膜病変を呈することから、患者背景(免疫不全状態)と眼底所見を組み合わせた臨床診断が可能である。
| 検査・評価 | 内容 |
|---|---|
| 眼底所見 | 3病型(周辺部顆粒型・後極部血管炎型・樹水状血管炎型)の確認。初期は前房炎症・硝子体炎が乏しい |
| 眼内液定量PCR(リアルタイム) | 感度・特異度ともに高く、確定診断に用いられる。前房内炎症細胞がない初期は検出されないことあり1) |
| 多項目PCR(先進医療) | 少量サンプルで複数ウイルスを網羅検索。ARNとの鑑別に有用1) |
| CMVアンチゲネミア法・血液PCR | 補助診断として参考値程度。確定診断には眼局所PCRが優先 |
| 患者背景確認 | CD4値・免疫抑制薬使用歴・ART治療状況など |
ACTG(エイズ臨床試験グループ)基準1):
ACTG(エイズ臨床試験グループ)基準1):
次世代シーケンシング(NGS)はPCRで診断困難な症例の補助診断として報告されており、CAR-T後症例でも活用例がある8)。HIV陰性免疫抑制患者では診断が遅れやすく、血清検査だけで否定せず眼所見と眼内液検査を組み合わせて判断する7, 9)。
綿花状白斑(cotton-wool spot)との鑑別では病変サイズが参考になる。750μm未満は綿花状白斑、それを超えるものはCMV網膜炎を疑う。
鑑別疾患:
特徴的な眼底所見(3病型のいずれか)と患者背景(免疫不全状態)による臨床診断が基本となる。確定診断には眼内液(前房水・硝子体液)の定量リアルタイムPCRが最も感度・特異度ともに優れている1)。多項目PCR(先進医療)は少量サンプルで複数ウイルスを鑑別できる利点があり、ARNとの鑑別に特に有用である。
抗CMV療法はガンシクロビルの点滴静注が第一選択となり、病巣の発症部位や大きさ、副作用の有無に応じてバルガンシクロビル経口投与やホスカルネットの点滴静注、硝子体内注射を単独または併用する。CMV網膜炎は多臓器の潜在的なCMV感染症を生じている可能性が高く、抗ウイルス療法の基本は全身治療である。
以下に主要な処方を示す。
| 薬剤 | 製品名 | 導入量 | 維持量 |
|---|---|---|---|
| ガンシクロビル点滴静注 | デノシン点滴静注用(500mg) | 5 mg/kg/回 1日2回 | 5 mg/kg/回 1日1回 |
| バルガンシクロビル内服 | バリキサ錠(450mg) | 4錠(1,800mg)分2食後 | 2錠(900mg)分1食後 |
| ホスカルネット点滴静注 | ホスカビル注(24mg/mL) | 90 mg/kg/回 1日2回 | 90 mg/kg/回 1日1回 |
導入療法は原則2〜3週間施行する。以後、維持療法を継続する。ホスカルネットはガンシクロビルによる骨髄抑制が強い場合の代替薬であるが、腎毒性への注意が必要である。
副作用の問題がある場合や病変が後極部に存在する場合には、GCVまたはホスカルネットの硝子体内注射を行うことがある(保険適用外)。
ホスカルネットとシドフォビルはGCV/VGCVに不耐容または耐性を示す場合の第二選択薬である。シドフォビルは週1回(導入)→2週1回(維持)で投与し、眼圧低下(50%まで)・前部ぶどう膜炎・腎毒性の副作用があるため、プロベネシドの前投与が必要である。
HAART開始後にCD4が回復する過程で、残存するCMV抗原に対する過剰な免疫応答が生じることがある(サイトメガロウイルス10〜17%に発症、多くはHAART開始後3ヶ月以内)。対応は以下の通りである。
導入療法終了後は維持療法を継続する。HIV/AIDS患者では抗ウイルス療法を少なくとも6ヶ月継続し、CD4陽性T細胞数が100個/μL超を4〜6ヶ月維持できれば中止を検討する。経過観察は導入中は週1回、維持中は2週に1回の散瞳眼底検査を行い、安定後は月1回とする。
裂孔原性網膜剥離を合併した場合は外科治療の適応となる。病巣の大きさや剥離の程度に応じて、以下を組み合わせる。
適切な時期に治療が施行されれば予後は急性網膜壊死ほど悪くない。
免疫抑制の解除が根本的な治療である。HIV感染者ではARTの開始・継続によってCD4を回復させることがCMV網膜炎再発防止の根幹となる。ART開始後のIRU(免疫回復ぶどう膜炎)発症に注意が必要である(→「病態生理学・詳細な発症機序」の項参照)。
効かない。CMVはアシクロビルやバラシクロビルに対して感受性が低く、HSV/VZV治療薬では不十分である。CMVにはガンシクロビルまたはバルガンシクロビルが第一選択薬となる。ガンシクロビルが骨髄抑制などの副作用で使用困難な場合はホスカルネットが代替薬として用いられる。
CMVはヘルペスウイルス科最大の2本鎖DNAウイルスで、初感染後は骨髄系前駆細胞・単球・マクロファージに潜伏感染する。免疫機能が低下した状態でウイルスが再活性化し、血行性に眼内へ播種されてCMV網膜炎を発症する。
CMVは網膜全層に感染し、ウイルス直接細胞障害が主体となって網膜壊死をきたす。ARNでみられるような強い免疫介在性炎症は乏しく、免疫応答が弱いため炎症所見も目立たない。これが初期に前房炎症・硝子体炎がほとんどみられない理由である。
CMVはウイルス性インターロイキン-10(cmvIL-10)を産生して免疫を抑制し、pp65タンパクがcGAS-STINGシグナル経路を阻害し、MHC-I様分子でNK細胞の攻撃を回避する14)。これらの免疫回避機構が慢性持続感染の基盤となる。CMVはACE2受容体の発現を上昇させることも示されており、SARS-CoV-2との共感染を促進する可能性が指摘されている14)。
CMVとVZV・EBVの共感染は単独感染より予後が悪い。
Kondoら(2025)は両眼性CMV網膜炎にEBV・VZVが共感染した症例を報告した15)。定量PCRではCMV 6.7×10⁷コピー/mL・VZV 1.3×10⁸コピー/mLと高値であり、網膜剥離を両眼に来した。
ART開始後にCD4陽性Tリンパ球数が急激に上昇すると、既存の日和見感染症の悪化や新たな病変の出現などがみられることがある。これを免疫再構築症候群(IRIS)とよぶ。眼科領域では、ART開始後に鎮静化したCMV網膜炎の既往眼に硝子体炎が生じるIRUが知られている1)。
IRUの発症機序:ARTによりCMV特異的T細胞の反応が回復すると、すでに鎮静化したCMV網膜炎病巣辺縁の細胞内でわずかに複製される残存CMV抗原が、免疫反応によりぶどう膜炎を顕在化させるとの説が有力である。「unmaskingタイプ」のIRISは、HAART開始直後にそれまで制御されていた感染が顕在化する病態である10)。
IRUの症状・診断:虹彩毛様体炎・硝子体炎などの初期病変のほか、続発する黄斑浮腫・白内障などが生じる。ART導入歴とCD4陽性Tリンパ球数の上昇が診断には必須である。
IRUの治療:重症度や時期により異なる。経過観察により自然寛解するものから、ARTの中断やステロイドの全身投与が必要となる症例、外科的治療を要する症例まで様々であるが、残存病原体に対する抗CMV療法の再開が基本となる1)。
ARTの普及によりAIDS患者のCMV網膜炎は大きく減少した一方、臓器移植後・CAR-T細胞療法後・生物学的製剤使用者など非AIDS免疫抑制患者での報告が増えている7, 9)。免疫不全の原因が多様化しており、CMV予防投与の適応・期間・薬剤選択の標準化が課題となっている。HIV陰性患者では診断の遅れに注意が必要である7, 9)。
薬剤抵抗性・再発性CMV網膜炎では、抗ウイルス薬だけでなく宿主免疫応答の理解も重要である。Liら(2022)は免疫正常者のCMV網膜炎でCMV特異的T細胞の動員が十分でない可能性を報告しており16)、局所免疫回避機構の解明が今後の治療開発につながる可能性がある。現時点ではT細胞関連治療は研究段階であり、標準治療ではない。
レテルモビル(letermovir)・マリバビル(maribavir)はGCV/ホスカルネット耐性CMVに対して有効性が示されている新規抗ウイルス薬である。特にマリバビルはHSCT後の難治性・耐性CMV感染症に対してFDA承認を取得している。CMV網膜炎に対するエビデンスはまだ限られているが、多剤耐性例への応用が期待される。
Zuら(2022)はCAR-T細胞療法後に発症した世界初のCMV網膜炎症例を報告した8)。CAR-T療法による深刻な液性免疫低下がCMV再活性化を促進したと考えられ、診断にはNGSが活用された。CAR-T療法を受けた患者では術後のCMVスクリーニングと眼科的モニタリングの必要性が示唆される。
CMVはACE2発現を上昇させることによりSARS-CoV-2との共感染を助長する可能性がある14)。また、CMV自体がCOVID-19重症化後に再活性化する症例も報告されている14)。免疫抑制患者のCOVID-19重症化時には眼科的評価も検討すべきとされる。
CMV感受性に影響する宿主遺伝子多型の同定が進んでいる14)。将来的にはハイリスク患者の遺伝的スクリーニングが予防戦略に活用される可能性がある。
Studies of Ocular Complications of AIDS(SOCA)による長期追跡では、ART時代のCMV網膜炎患者の視力予後は改善しているものの、IRUに起因する黄斑浮腫・白内障・増殖性硝子体網膜症が視力低下の主因となっていることが示されている3)。
近年、免疫正常者においてCMVによる虹彩毛様体炎・角膜内皮炎(CMV前部ぶどう膜炎)が報告されており、CMV感染の眼内スペクトラムは拡大しつつある。TITAN Report 2はCMV前部ぶどう膜炎管理の国際コンセンサスを提示しており、今後のエビデンス集積が期待される2)。
先天性CMV感染症における眼科合併症(CMV網膜炎・視神経萎縮)の長期予後改善に向けた早期介入の研究が進んでいる。抗ウイルス療法の早期開始が視機能予後を改善する可能性が示唆されている。