Periferik Granüler Tip
Özellik: Neredeyse hiç kanama olmaz, beyaz granüler eksüda lekeleri yelpaze şeklinde birikir.
Görme üzerine etkisi: Makula korunursa görme nispeten korunur.
Seyir: En sık görülen tip. Periferden yavaşça merkeze ilerler.

İnsan herpes virüsü 5, genel adıyla sitomegalovirüs (CMV), çift sarmallı DNA’ya sahip herpes virüs ailesinin en büyük virüsüdür. İnsan vücudunda geniş doku afinitesi vardır ve retinada primer enfeksiyon, reenfeksiyon veya reaktivasyon yoluyla, retina katmanlarının nekrozu ve ödemi ile karakterize CMV retinitine neden olur.
CMV antikor prevalansı %70-90 gibi yüksektir ve çoğu kişi bebeklik döneminde asemptomatik olarak enfekte olur. Erişkinlerde görülen CMV retiniti çoğunlukla virüsün reaktivasyonu ile ilişkili fırsatçı enfeksiyondur1).
Gebeliğin erken döneminde annede primer enfeksiyon veya reaktivasyon olursa, %20-40 oranında transplasental yolla fetüse bulaşır ve TORCH sendromlarından biri olan konjenital CMV enfeksiyonu olarak CMV retiniti gelişebilir.
Epidemiyoloji:
Prensip olarak, sağlıklı ve bağışıklığı normal bireylerde hastalığın ortaya çıkması nadirdir. Ancak son yıllarda, bağışıklığı normal kişilerde ön üveit ve kornea endoteliti olarak ortaya çıkan CMV ön segment sendromu raporları artmaktadır (bkz. “CMV ön üveiti” bölümü). CMV retiniti (arka segment lezyonu) esas olarak immün yetmezlik altında fırsatçı bir enfeksiyondur 1) ve sağlıklı bireylerde son derece nadirdir. Uzun süreli steroid kullanımı, diyabete bağlı immün fonksiyon bozukluğu ve immün yaşlanma (immunosenescence) gibi faktörler zemin hazırlayıcı olarak sayılabilir 11, 12).
Evet. Retrospektif bir çalışmada, HIV pozitif CMV retiniti hastalarının %15’inin HIV tanısından önce göz doktoruna başvurduğu ve %9’unda CMV retinitinin AIDS için tek tanı kriteri hastalığı olduğu bildirilmiştir 13). CMV retinitinden şüphelenildiğinde, aktif olarak HIV testi yapılmalıdır.
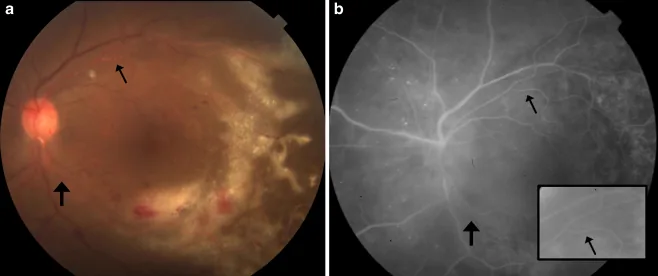
Belirtiler lezyonun yeri ve büyüklüğüne göre değişkendir.
Erken dönemde ön kamara inflamasyonu ve vitrit hemen hemen hiç görülmez; bu bulgular lezyonun genişlemesiyle ortaya çıkar ve bu özellik ARN’den ayırt edici önemli bir noktadır.
CMV retiniti, karakteristik fundus bulgularına göre üç klinik tipe ayrılır. Klinik pratikte bu tipler sıklıkla bir arada bulunur ve lezyonun yeri ve büyüklüğü prognoz tahmininde daha önemlidir.
Periferik Granüler Tip
Özellik: Neredeyse hiç kanama olmaz, beyaz granüler eksüda lekeleri yelpaze şeklinde birikir.
Görme üzerine etkisi: Makula korunursa görme nispeten korunur.
Seyir: En sık görülen tip. Periferden yavaşça merkeze ilerler.
Arka Kutup Vaskülit Tipi
Özellik: Arka kutuptaki damarlar boyunca retina kanaması ve ödem ile birlikte sarı-beyaz eksüda lekeleri görülür. «Pizza payı» olarak tanımlanan yaygın nekroz ve kanama karakteristiktir.
Görme üzerine etkisi: Makula ve optik siniri etkilediği için görme azalması belirgindir.
Seyir: En kötü görme prognozuna sahip tiptir. Hızlı tedavi başlangıcı önemlidir.
Dendritik-Akıntılı Vaskülit Tipi
Özellik: Büyük damarlar başta olmak üzere retina damarları dendritik-akıntılı vaskülit benzeri beyaz kılıflanma gösterir (FBA).
Sıklık: Nispeten nadir bir tip. CMV-IRIS belirtisi olarak ortaya çıkabilir10).
Dikkat: Klinik pratikte üç tip sıklıkla bir arada bulunur ve lezyonun yeri ve büyüklüğü prognoz tahmininde önemlidir.
Lezyonun bölge sınıflandırması tedavi aciliyetini belirlemede önemlidir.
| Bölge | Aralık | Klinik Önem |
|---|---|---|
| Zone 1 | Optik disk 1DD içi ve makula 2DD içi | Hemen tedavi başlanır |
| Zone 2 | Ekvator’dan vorteks ven ampullerine kadar | Tedavi düşünülür |
| Zone 3 | En periferik alan | Takip edilebilir |
Retina dekolmanı (RD) ciddi bir komplikasyondur. Lezyon alanı ne kadar genişse, regmatojen retina dekolmanı riski o kadar yüksektir. ART yaygınlaştıktan sonra bu risk azalmış olsa da, tedavi sonrası uzun süreli dikkat gereklidir3).
Tang ve ark. (2021), HAART başlangıcından 35 gün sonra frost branch vaskülit gelişen bir HIV hastası bildirdi10). Aköz hümörde IL-6 2845 pg/mL, IL-8 967.8 pg/mL gibi belirgin yüksekti ve bu, unmasking tip IRIS olarak FBA idi. Sadece antiviral tedavi ile inflamasyon düzeldi.
Eski CMV retiniti lezyonlarında retina tüm katları nekroza uğrar ve dantel gibi incelir. Vitreus traksiyonu eklendiğinde kolayca çoklu yırtıklar oluşur ve retina dekolmanı gelişir. Bu nedenle retinit sakinleştikten sonra bile uzun süreli takip gereklidir.
Nekrotik retina tüm katları incelir ve dantel görünümü alır. Vitreus traksiyonu ile kolayca çoklu yırtıklar oluşur. Özellikle nekroz kenarında incelme belirgindir ve yırtık riski yüksektir. Tedavi ile retinit sakinleştikten sonra bile incelmiş retina kaldığı için uzun süreli takip gereklidir.
CMV retiniti çoğunlukla immün yetmezlik durumunda fırsatçı bir enfeksiyondur. Erişkin hastalarda edinilmiş immün yetmezlik sendromu (AIDS) gibi immün yetmezliğe yol açan altta yatan hastalıkların ve ilaç kullanım öyküsünün sorgulanması tanının başlangıç noktasıdır 1).
Başlıca risk faktörleri:
CMV retiniti için kesin bir tanı kriteri olmamakla birlikte, karakteristik retina lezyonları nedeniyle hasta geçmişi (immün yetmezlik durumu) ve fundus bulgularının birleşimiyle klinik tanı mümkündür.
| Test/Değerlendirme | İçerik |
|---|---|
| Fundus Bulguları | Üç tipin (periferik granüler tip, posterior kutup vaskülit tipi, dendritik vaskülit tipi) doğrulanması. Erken evrede ön kamara inflamasyonu ve vitrit azdır. |
| Göz İçi Sıvı Kantitatif PCR (Real-time) | Duyarlılık ve özgüllük yüksektir ve kesin tanı için kullanılır. Ön kamarada inflamatuar hücre olmayan erken evrede tespit edilemeyebilir1) |
| Çoklu PCR (İleri Tıp) | Az miktarda örnekle birden fazla virüsün kapsamlı taranması. ARN’den ayırt etmede faydalıdır1) |
| CMV Antijenemi Yöntemi / Kan PCR | Yardımcı tanı olarak referans değer. Kesin tanı için göz lokal PCR tercih edilir |
| Hasta Geçmişi Kontrolü | CD4 değeri, immünosupresif ilaç kullanım öyküsü, ART tedavi durumu vb. |
ACTG (AIDS Klinik Deney Grubu) kriterleri1):
ACTG (AIDS Klinik Deney Grubu) kriterleri1):
Yeni nesil dizileme (NGS), PCR ile tanı konulamayan vakalarda yardımcı tanı aracı olarak rapor edilmiştir ve CAR-T sonrası vakalarda da kullanım örnekleri vardır8). HIV negatif immün süprese hastalarda tanı sıklıkla gecikir; serolojik testlerle dışlanmamalı, göz bulguları ve göz içi sıvı testleri birlikte değerlendirilmelidir7, 9).
Pamuk yünü lekesi (cotton-wool spot) ile ayırıcı tanıda lezyon boyutu yardımcıdır. 750 μm’den küçük lezyonlar pamuk yünü lekesi, daha büyük olanlar CMV retiniti olarak değerlendirilir.
Ayırıcı tanılar:
Karakteristik fundus bulguları (üç tipten herhangi biri) ve hasta öyküsü (immün yetmezlik durumu) ile klinik tanı esastır. Kesin tanı için göz içi sıvısında (aköz hümör veya vitreus) kantitatif gerçek zamanlı PCR, hem duyarlılık hem de özgüllük açısından en iyisidir 1). Çoklu PCR (ileri tıp), küçük bir örnekle birden fazla virüsü ayırt etme avantajına sahiptir ve özellikle ARN’den ayırt etmede faydalıdır.
Anti-CMV tedavisinde ilk seçenek intravenöz gansiklovirdir ve lezyonun yeri ve boyutuna, yan etkilerin varlığına göre oral valgansiklovir, intravenöz foskarnet veya intravitreal enjeksiyon tek başına veya kombine olarak kullanılır. CMV retiniti, çoklu organlarda potansiyel CMV enfeksiyonu olasılığı yüksektir ve antiviral tedavinin temeli sistemik tedavidir.
Aşağıda ana reçeteler gösterilmiştir.
| İlaç | Ürün Adı | Yükleme Dozu | İdame Dozu |
|---|---|---|---|
| Gansiklovir intravenöz infüzyon | Denosin intravenöz infüzyon (500 mg) | 5 mg/kg/doz günde 2 kez | 5 mg/kg/doz günde 1 kez |
| Oral valgansiklovir | Valiksa tablet (450 mg) | 4 tablet (1800 mg) günde 2 kez yemek sonrası | 2 tablet (900 mg) günde 1 kez yemek sonrası |
| Foskarnet intravenöz infüzyon | Foskavir enjeksiyon (24 mg/mL) | 90 mg/kg/doz günde 2 kez | 90 mg/kg/doz günde 1 kez |
İndüksiyon tedavisi genellikle 2-3 hafta süreyle uygulanır. Ardından idame tedavisine devam edilir. Foskarnet, gansiklovire bağlı şiddetli kemik iliği baskılanması durumunda alternatiftir, ancak nefrotoksisiteye dikkat edilmelidir.
Yan etki sorunları varsa veya lezyon arka kutupta yer alıyorsa, GCV veya foskarnetin intravitreal enjeksiyonu yapılabilir (sigorta kapsamı dışı).
Foskarnet ve sidofovir, GCV/VGCV’ye intolerans veya direnç durumlarında ikinci basamak ilaçlardır. Sidofovir haftada 1 kez (indüksiyon) → 2 haftada 1 kez (idame) uygulanır. Göz içi basıncında düşme (%50’ye kadar), ön üveit ve nefrotoksisite gibi yan etkileri vardır; probenesid ön tedavisi gereklidir.
HAART başladıktan sonra CD4 düzelirken, kalan CMV antijenlerine karşı aşırı immün yanıt oluşabilir (sitomegalovirüs vakalarının %10-17’sinde, çoğunlukla HAART başlangıcından sonraki 3 ay içinde). Yönetim şu şekildedir:
İndüksiyon tedavisi sonrası idame tedavisine devam edilir. HIV/AIDS hastalarında antiviral tedavi en az 6 ay sürdürülür ve CD4+ T hücre sayısı 4-6 ay boyunca >100 hücre/μL olursa kesilmesi düşünülür. Takip: indüksiyonda haftada bir, idamede iki haftada bir dilate fundus muayenesi, stabilizasyon sonrası ayda bir.
Regmatojen retina dekolmanı eşlik ediyorsa cerrahi tedavi endikedir. Lezyon büyüklüğü ve dekolman derecesine göre aşağıdakiler kombine edilir:
Uygun zamanda tedavi edilirse prognoz akut retina nekrozu kadar kötü değildir.
Temel tedavi immünosupresyonun kaldırılmasıdır. HIV enfeksiyonu olanlarda, ART’nin başlatılması ve sürdürülmesi ile CD4’ün geri kazanılması, CMV retinitinin nüksünü önlemenin temelini oluşturur. ART başlangıcından sonra IRU (immün rekonstitüsyon üveiti) gelişimine dikkat edilmelidir (→ «Patofizyoloji ve detaylı gelişim mekanizması» bölümüne bakınız).
Etkili değildir. CMV, asiklovir ve valasiklovire karşı düşük duyarlılığa sahiptir ve HSV/VZV tedavi ilaçları yetersiz kalır. CMV için gansiklovir veya valgansiklovir birinci basamak ilaçlardır. Gansiklovir kemik iliği baskılanması gibi yan etkiler nedeniyle kullanılamazsa, foskarnet alternatif olarak kullanılır.
CMV, herpes virüs ailesinin en büyük çift sarmallı DNA virüsüdür. Primer enfeksiyondan sonra miyeloid progenitör hücreler, monositler ve makrofajlarda latent olarak kalır. Bağışıklık fonksiyonunun azaldığı durumlarda virüs reaktive olur ve hematojen yolla göz içine yayılarak CMV retinitine neden olur.
CMV, retinanın tüm katmanlarını enfekte eder ve doğrudan viral hücre hasarı retina nekrozuna yol açar. ARN’de görülen güçlü immün aracılı inflamasyon burada nadirdir ve bağışıklık yanıtı zayıf olduğu için inflamatuar bulgular da belirgin değildir. Bu, erken dönemde ön kamara inflamasyonu ve vitritin neredeyse hiç görülmemesinin nedenidir.
CMV, viral interlökin-10 (cmvIL-10) üreterek bağışıklığı baskılar, pp65 proteini cGAS-STING sinyal yolunu inhibe eder ve MHC-I benzeri moleküllerle NK hücre saldırısından kaçar14). Bu immün kaçış mekanizmaları kronik persistan enfeksiyonun temelini oluşturur. CMV’nin ACE2 reseptör ekspresyonunu artırdığı da gösterilmiştir ve bu, SARS-CoV-2 ile ko-enfeksiyonu kolaylaştırabileceği öne sürülmüştür14).
CMV ile VZV ve EBV koenfeksiyonu, tek başına enfeksiyondan daha kötü prognoza sahiptir.
Kondo ve ark. (2025), bilateral CMV retinitinde EBV ve VZV koenfeksiyonu olan bir olgu bildirmiştir15). Kantitatif PCR’de CMV 6.7×10⁷ kopya/mL ve VZV 1.3×10⁸ kopya/mL gibi yüksek değerler saptanmış ve her iki gözde retina dekolmanı gelişmiştir.
ART başlandıktan sonra CD4+ T lenfosit sayısının hızla yükselmesi, mevcut fırsatçı enfeksiyonların kötüleşmesine veya yeni lezyonların ortaya çıkmasına neden olabilir. Buna immün rekonstitüsyon sendromu (IRIS) denir. Göz alanında, ART sonrası sakinleşmiş CMV retiniti öyküsü olan gözlerde vitrit gelişen IRU bilinmektedir1).
IRU’nun patogenezi: ART ile CMV’ye özgü T hücre yanıtının düzelmesiyle, sakinleşmiş CMV retiniti lezyonlarının kenarındaki hücrelerde hafifçe replike olan kalıntı CMV antijenlerinin immün yanıtla üveiti ortaya çıkardığı görüşü hakimdir. «Unmasking» tip IRIS, HAART başlangıcından hemen sonra daha önce kontrol altındaki enfeksiyonun belirgin hale gelmesidir10).
IRU’nun belirtileri ve tanısı: İridosiklit, vitrit gibi başlangıç lezyonlarının yanı sıra sekonder makula ödemi, katarakt gibi durumlar ortaya çıkar. Tanı için ART öyküsü ve CD4+ T lenfosit sayısında artış gereklidir.
IRU tedavisi: Şiddet ve evreye göre değişir. İzlemle kendiliğinden düzelen olgulardan ART’nin kesilmesi veya sistemik steroid gerektiren olgulara, hatta cerrahi tedavi gerektiren olgulara kadar çeşitlilik gösterir, ancak temel tedavi kalıntı patojene karşı anti-CMV tedavisinin yeniden başlatılmasıdır1).
ART’nin yaygınlaşmasıyla AIDS hastalarında CMV retiniti büyük ölçüde azalırken, organ nakli sonrası, CAR-T hücre tedavisi sonrası ve biyolojik ajan kullanıcıları gibi AIDS dışı immünsüpresif hastalarda bildirimler artmaktadır7, 9). İmmün yetmezlik nedenleri çeşitlenmiştir ve CMV profilaksisinin endikasyonu, süresi ve ilaç seçiminin standardizasyonu bir sorun haline gelmiştir. HIV negatif hastalarda tanı gecikmesine dikkat edilmelidir7, 9).
İlaca dirençli veya tekrarlayan CMV retinitinde, antiviral ilaçların yanı sıra konak immün yanıtının anlaşılması da önemlidir. Li ve ark. (2022), immün kompetan bireylerde CMV retinitinde CMV’ye özgü T hücrelerinin yeterince mobilize olmayabileceğini bildirmiştir16) ve lokal immün kaçış mekanizmalarının aydınlatılması gelecekteki tedavi gelişimine yol açabilir. Şu anda T hücre ilişkili tedaviler araştırma aşamasındadır ve standart tedavi değildir.
Letermovir ve maribavir, GCV/foskarnet dirençli CMV’ye karşı etkinliği gösterilmiş yeni antiviral ilaçlardır. Özellikle maribavir, HSCT sonrası dirençli ve tedavisi zor CMV enfeksiyonu için FDA onayı almıştır. CMV retiniti için kanıtlar hala sınırlı olsa da, çoklu ilaç direnci olan vakalarda kullanımı umut vaat etmektedir.
Zu ve ark. (2022), CAR-T hücre tedavisi sonrası gelişen dünyadaki ilk CMV retiniti vakasını bildirmiştir 8). CAR-T tedavisine bağlı ciddi humoral immün yetmezliğin CMV reaktivasyonunu tetiklediği düşünülmekte ve tanıda NGS kullanılmıştır. CAR-T tedavisi alan hastalarda postoperatif CMV taraması ve oftalmolojik izlemin gerekliliğini düşündürmektedir.
CMV, ACE2 ekspresyonunu artırarak SARS-CoV-2 ile ko-enfeksiyonu kolaylaştırabilir 14). Ayrıca, şiddetli COVID-19 sonrası CMV reaktivasyonu vakaları da bildirilmiştir 14). İmmünsüprese hastalarda şiddetli COVID-19 sırasında oftalmolojik değerlendirme de düşünülmelidir.
CMV duyarlılığını etkileyen konak gen polimorfizmlerinin tanımlanması ilerlemektedir 14). Gelecekte, yüksek riskli hastaların genetik taraması önleme stratejilerinde kullanılabilir.
Studies of Ocular Complications of AIDS (SOCA) tarafından yapılan uzun süreli takip, ART döneminde CMV retiniti hastalarında görme prognozunun iyileştiğini, ancak IRU’ya bağlı makula ödemi, katarakt ve proliferatif vitreoretinopatinin görme kaybının ana nedenleri olduğunu göstermiştir 3).
Son yıllarda, immünokompetan bireylerde CMV’ye bağlı iridosiklit ve kornea endoteliti (CMV ön üveit) bildirilmekte olup, CMV’nin intraoküler spektrumu genişlemektedir. TITAN Report 2, CMV ön üveit yönetimi için uluslararası bir fikir birliği sunmuş olup, gelecekte daha fazla kanıt birikmesi beklenmektedir 2).
Konjenital CMV enfeksiyonunda oküler komplikasyonların (CMV retiniti, optik atrofi) uzun dönem prognozunu iyileştirmek için erken müdahale araştırmaları devam etmektedir. Antiviral tedavinin erken başlatılmasının görsel prognozu iyileştirebileceği düşünülmektedir.