النمط الحبيبي المحيطي
الخصائص: لا يصاحبه نزيف تقريبًا، وتظهر بقع نضحية بيضاء حبيبية متجمعة بشكل مروحي.
التأثير على الرؤية: إذا تم تجنب البقعة الصفراء، تبقى الرؤية محفوظة نسبيًا.
المسار: النمط الأكثر شيوعًا. يتقدم تدريجيًا من المحيط نحو المركز.

فيروس الهربس البشري 5، المعروف باسم الفيروس المضخم للخلايا (CMV)، هو أكبر فيروس في عائلة فيروسات الهربس، وله حمض نووي مزدوج الشريط. له ألفة واسعة للأنسجة في جسم الإنسان، ويسبب التهاب الشبكية المضخم للخلايا، الذي يتميز بنخر ووذمة في جميع طبقات الشبكية، نتيجة العدوى الأولية أو إعادة العدوى أو إعادة التنشيط في الشبكية.
معدل انتشار الأجسام المضادة لـ CMV مرتفع (70-90%)، وتحدث معظم الإصابات بدون أعراض في مرحلة الطفولة المبكرة. الغالبية العظمى من حالات التهاب الشبكية المضخم للخلايا لدى البالغين هي عدوى انتهازية ناتجة عن إعادة تنشيط الفيروس1).
إذا أصيبت الأم بعدوى أولية أو إعادة تنشيط في بداية الحمل، فإن 20-40% من الحالات تنتقل إلى الجنين عبر المشيمة، مما يؤدي إلى التهاب الشبكية المضخم للخلايا الخلقي كجزء من متلازمة TORCH.
الوبائيات:
من حيث المبدأ، نادر حدوثه لدى الأشخاص ذوي المناعة الطبيعية. ومع ذلك، في السنوات الأخيرة، ازدادت تقارير متلازمة الجزء الأمامي للعين بالفيروس المضخم للخلايا التي تظهر كالتهاب العنبية الأمامي أو التهاب البطانة القرنية لدى الأشخاص ذوي المناعة الطبيعية (انظر القسم المنفصل “التهاب العنبية الأمامي بالفيروس المضخم للخلايا”). التهاب الشبكية بالفيروس المضخم للخلايا (الآفة الخلفية) هو بشكل رئيسي عدوى انتهازية في حالات نقص المناعة 1)، ونادر جدًا لدى الأصحاء. تشمل العوامل المساهمة الاستخدام طويل الأمد للستيرويدات، ضعف المناعة بسبب السكري، والشيخوخة المناعية 11, 12).
نعم. في دراسة بأثر رجعي، أفيد أن 15% من مرضى التهاب الشبكية بالفيروس المضخم للخلايا المصابين بفيروس نقص المناعة البشرية زاروا طبيب العيون قبل تشخيص فيروس نقص المناعة البشرية، وفي 9% كان التهاب الشبكية بالفيروس المضخم للخلايا هو المعيار التشخيصي الوحيد للإيدز 13). عند الاشتباه في التهاب الشبكية بالفيروس المضخم للخلايا، يجب إجراء اختبار فيروس نقص المناعة البشرية بنشاط.
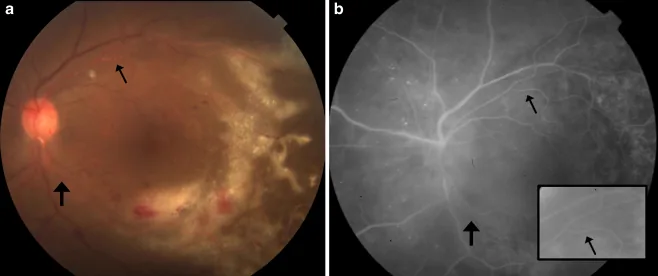
تختلف الأعراض حسب موقع وحجم الآفة.
في المراحل المبكرة، لا يُلاحظ التهاب الغرفة الأمامية أو التهاب الجسم الزجاجي تقريبًا، وتظهر هذه النتائج مع توسع الآفة، وهي سمة مميزة ونقطة فارقة مهمة عن التهاب الشبكية الحاد الناخر.
يُصنف التهاب الشبكية بالفيروس المضخم للخلايا (CMV) إلى ثلاثة أنماط بناءً على مظهر قاع العين المميز. في الممارسة السريرية، غالبًا ما تختلط هذه الأنماط، ويكون موقع وحجم الآفات أكثر أهمية للتنبؤ بالنتيجة.
النمط الحبيبي المحيطي
الخصائص: لا يصاحبه نزيف تقريبًا، وتظهر بقع نضحية بيضاء حبيبية متجمعة بشكل مروحي.
التأثير على الرؤية: إذا تم تجنب البقعة الصفراء، تبقى الرؤية محفوظة نسبيًا.
المسار: النمط الأكثر شيوعًا. يتقدم تدريجيًا من المحيط نحو المركز.
النمط الوعائي الالتهابي للقطب الخلفي
الخصائص: تظهر بقع نضحية صفراء-بيضاء مصحوبة بنزيف شبكي ووذمة على طول الأوعية في القطب الخلفي. يتميز بنخر ونزيف واسع النطاق يُوصف بأنه “فطيرة البيتزا”.
التأثير على الرؤية: يؤثر على البقعة الصفراء والعصب البصري، مما يؤدي إلى انخفاض ملحوظ في الرؤية.
المسار: النمط ذو أسوأ تشخيص بصري. البدء السريع بالعلاج مهم.
النمط الوعائي الشجري المتجمد
الخصائص: تصبح الأوعية الشبكية مغلفة بغمد أبيض على شكل التهاب وعائي شجري متجمد (التهاب الأوعية المتجمد الفرعي)، خاصة حول الأوعية الكبيرة.
التكرار: نمط نادر نسبيًا. قد يظهر كعلامة على متلازمة استعادة المناعة للفيروس المضخم للخلايا (CMV-IRIS)10).
ملاحظة: في الممارسة السريرية، غالبًا ما تختلط الأنماط الثلاثة، ويكون موقع وحجم الآفات مهمًا للتنبؤ بالنتيجة.
تصنيف الآفات حسب المنطقة مهم لتحديد مدى إلحاح العلاج.
| المنطقة | النطاق | الأهمية السريرية |
|---|---|---|
| المنطقة 1 | ضمن قطر حلمة العصب البصري (1 DD) وضمن قطرين (2 DD) من البقعة | بدء العلاج فورًا |
| المنطقة 2 | من خط الاستواء إلى أمبولة الوريد الدوامي | النظر في العلاج |
| المنطقة 3 | أقصى المحيط | يمكن المتابعة |
انفصال الشبكية (RD) هو أحد المضاعفات الخطيرة. كلما اتسع نطاق الآفة، زاد خطر انفصال الشبكية الناتج عن التمزق. على الرغم من انخفاضه بعد انتشار العلاج المضاد للفيروسات القهقرية (ART)، إلا أنه لا يزال يتطلب مراقبة طويلة الأمد حتى بعد العلاج 3).
أبلغ تانغ وآخرون (2021) عن مريض مصاب بفيروس نقص المناعة البشرية أصيب بالتهاب الأوعية الدموية الشبكية الشبيه بالصقيع بعد 35 يومًا من بدء العلاج المضاد للفيروسات القهقرية عالي الفعالية (HAART) 10). ارتفع مستوى IL-6 في الخلط المائي إلى 2,845 بيكوغرام/مل و IL-8 إلى 967.8 بيكوغرام/مل، مما يشير إلى التهاب الشبكية بالفيروس المضخم للخلايا (CMV) كمتلازمة إعادة بناء المناعة الالتهابية (IRIS) من النوع غير المعلن. تحسنت الالتهابات بالعلاج المضاد للفيروسات فقط.
في مناطق التهاب الشبكية بالفيروس المضخم للخلايا (CMV) المزمن، يحدث نخر كامل لطبقات الشبكية، مما يؤدي إلى ترقق يشبه الدانتيل. عند إضافة الجر الزجاجي، تتشكل تمزقات متعددة بسهولة، مما يؤدي إلى انفصال الشبكية. لذلك، حتى بعد هدوء التهاب الشبكية، تكون المتابعة طويلة الأمد ضرورية.
تصبح طبقات الشبكية النخرية رقيقة مثل الدانتيل. عند إضافة الجر الزجاجي، تتشكل تمزقات متعددة بسهولة. خاصة عند حواف النخر، يكون الترقق شديدًا ويكون خطر تكوين التمزق مرتفعًا. حتى بعد هدوء التهاب الشبكية بالعلاج، تبقى الشبكية الرقيقة، مما يستلزم متابعة طويلة الأمد.
التهاب الشبكية بالفيروس المضخم للخلايا (CMV) هو في الغالب عدوى انتهازية في حالات نقص المناعة. بالنسبة للمرضى البالغين، فإن التحقق من وجود أمراض كامنة تسبب نقص المناعة مثل متلازمة نقص المناعة المكتسب (الإيدز) أو تاريخ استخدام الأدوية المثبطة للمناعة هو نقطة البداية للتشخيص 1).
عوامل الخطر الرئيسية:
لا توجد معايير تشخيصية واضحة لالتهاب الشبكية بالفيروس المضخم للخلايا، ولكن نظرًا لظهور آفات شبكية مميزة، يمكن التشخيص السريري من خلال الجمع بين خلفية المريض (حالة نقص المناعة) ونتائج فحص قاع العين.
| الفحص/التقييم | المحتوى |
|---|---|
| نتائج فحص قاع العين | تأكيد الأنواع الثلاثة (النوع الحبيبي المحيطي، النوع الوعائي الالتهابي للقطب الخلفي، النوع الوعائي الالتهابي الشجري). في المراحل المبكرة، يكون التهاب الغرفة الأمامية والتهاب الجسم الزجاجي ضئيلًا. |
| PCR الكمي للسائل داخل العين (الوقت الحقيقي) | حساسية ونوعية عالية، ويستخدم للتشخيص النهائي. قد لا يتم اكتشافه في المراحل المبكرة عندما لا توجد خلايا التهابية في الغرفة الأمامية1) |
| PCR متعدد العوامل (الطب المتقدم) | فحص شامل لفيروسات متعددة بعينة صغيرة. مفيد للتمييز عن التهاب الشبكية الحاد الناخر1) |
| مقايسة مستضد CMV وPCR الدم | قيمة مرجعية كتشخيص مساعد. للتشخيص النهائي، يُفضل PCR الموضعي للعين. |
| تأكيد خلفية المريض | قيمة CD4، تاريخ استخدام مثبطات المناعة، حالة العلاج المضاد للفيروسات القهقرية، إلخ. |
معايير مجموعة التجارب السريرية للإيدز (ACTG)1):
معايير مجموعة التجارب السريرية للإيدز (ACTG)1):
تم الإبلاغ عن التسلسل من الجيل التالي (NGS) كأداة تشخيصية مساعدة للحالات التي يصعب تشخيصها بواسطة PCR، وهناك حالات استخدام بعد علاج CAR-T8). في المرضى المثبطين مناعياً غير المصابين بفيروس نقص المناعة البشرية، غالباً ما يتأخر التشخيص، لذا يجب عدم الاعتماد فقط على الاختبارات المصلية، بل الجمع بين نتائج العين وفحص السائل داخل العين7, 9).
في التمييز عن البقع القطنية (cotton-wool spots)، يمكن أن يكون حجم الآفة مفيداً. الآفات التي يقل حجمها عن 750 ميكرومتر تشير إلى بقع قطنية، بينما الآفات الأكبر تشير إلى التهاب الشبكية CMV.
التشخيص التفريقي:
يعتمد التشخيص السريري على النتائج المميزة لقاع العين (أي من الأنواع الثلاثة) وخلفية المريض (حالة نقص المناعة). للتشخيص النهائي، يعتبر تفاعل البوليميراز المتسلسل الكمي في الوقت الحقيقي للسائل داخل العين (الخلط المائي أو الزجاجي) الأكثر حساسية ونوعية 1). تفاعل البوليميراز المتسلسل متعدد العوامل (الطب المتقدم) له ميزة التمييز بين فيروسات متعددة من عينة صغيرة، وهو مفيد بشكل خاص للتمييز عن التهاب الشبكية الحاد الناخر.
العلاج المضاد للفيروس المضخم للخلايا هو الحقن الوريدي للغانسيكلوفير كخيار أول، ويتم استخدام فالجانسيكلوفير عن طريق الفم أو الحقن الوريدي للفوسكارنيت أو الحقن داخل الزجاجي بمفرده أو بالاشتراك حسب موقع الآفة وحجمها ووجود آثار جانبية. من المحتمل أن التهاب الشبكية بالفيروس المضخم للخلايا يصاحبه عدوى كامنة بالفيروس المضخم للخلايا في أعضاء متعددة، وبالتالي فإن أساس العلاج المضاد للفيروسات هو العلاج الجهازي.
فيما يلي الوصفات الرئيسية:
| الدواء | اسم المنتج | جرعة التحميل | جرعة الصيانة |
|---|---|---|---|
| غانسيكلوفير حقن وريدي | دينوسين للحقن الوريدي (500 مجم) | 5 مجم/كجم/جرعة مرتين يوميًا | 5 مجم/كجم/جرعة مرة واحدة يوميًا |
| فالغانسيكلوفير عن طريق الفم | أقراص فاليکسا (450 مجم) | 4 أقراص (1800 مجم) مقسمة على جرعتين بعد الأكل | قرصان (900 مجم) جرعة واحدة بعد الأكل |
| فوسكارنيت عن طريق الوريد | حقن فوسكافير (24 مجم/مل) | 90 مجم/كجم/جرعة مرتين يوميًا | 90 مجم/كجم/جرعة مرة واحدة يوميًا |
يتم إجراء العلاج التمهيدي لمدة 2-3 أسابيع بشكل عام. بعد ذلك، يستمر العلاج الصيانة. الفوسكارنيت هو بديل عندما يكون تثبيط نخاع العظم الناتج عن غانسيكلوفير شديدًا، ولكن يجب الانتباه إلى السمية الكلوية.
في حالة وجود مشاكل في الآثار الجانبية أو وجود الآفة في القطب الخلفي، يمكن إجراء حقن داخل الزجاجي من GCV أو فوسكارنيت (خارج التغطية التأمينية).
الفوسكارنيت والسيدوفوفير هما الخياران الثانيان في حالة عدم التحمل أو المقاومة لـ GCV/VGCV. يُعطى سيدوفوفير مرة واحدة في الأسبوع (تمهيدي) → مرة كل أسبوعين (صيانة)، وله آثار جانبية مثل انخفاض ضغط العين (حتى 50%)، التهاب العنبية الأمامي، والسمية الكلوية، مما يستلزم إعطاء بروبينيسيد مسبقًا.
عندما يتعافى CD4 بعد بدء HAART، قد يحدث استجابة مناعية مفرطة تجاه مستضدات الفيروس المضخم للخلايا المتبقية (يحدث في 10-17% من حالات الفيروس المضخم للخلايا، غالبًا في غضون 3 أشهر من بدء HAART). الإجراءات كالتالي:
بعد انتهاء العلاج التعريفي، يستمر العلاج الصيانة. في مرضى HIV/AIDS، يستمر العلاج المضاد للفيروسات لمدة 6 أشهر على الأقل، وإذا استمر عدد خلايا CD4+ T أكثر من 100 خلية/ميكرولتر لمدة 4-6 أشهر، يمكن النظر في إيقافه. المتابعة: أثناء العلاج التعريفي مرة واحدة في الأسبوع، وأثناء الصيانة مرة كل أسبوعين بفحص قاع العين بعد توسيع الحدقة، وبعد الاستقرار مرة واحدة شهريًا.
في حالة حدوث انفصال الشبكية الناتج عن تمزق، يكون العلاج الجراحي مناسبًا. اعتمادًا على حجم الآفة ودرجة الانفصال، يتم الجمع بين ما يلي:
إذا تم العلاج في الوقت المناسب، فإن التشخيص ليس سيئًا مثل نخر الشبكية الحاد.
إزالة كبت المناعة هو العلاج الأساسي. في مرضى فيروس نقص المناعة البشرية، يعد بدء أو استمرار العلاج المضاد للفيروسات القهقرية (ART) لاستعادة CD4 حجر الزاوية لمنع تكرار التهاب الشبكية بالفيروس المضخم للخلايا (CMV). يجب الانتباه إلى حدوث التهاب القزحية الناتج عن استعادة المناعة (IRU) بعد بدء ART (انظر قسم “الفيزيولوجيا المرضية وآلية الحدوث التفصيلية”).
غير فعالين. الفيروس المضخم للخلايا (CMV) لديه حساسية منخفضة للأسيكلوفير وفالاسيكلوفير، وأدوية علاج فيروس الهربس البسيط/فيروس الحماق النطاقي غير كافية. بالنسبة للفيروس المضخم للخلايا، يعتبر غانسيكلوفير أو فالغانسيكلوفير الخيار الأول. إذا كان غانسيكلوفير صعب الاستخدام بسبب الآثار الجانبية مثل تثبيط نقي العظم، يستخدم فوسكارنيت كبديل.
الفيروس المضخم للخلايا (CMV) هو أكبر فيروس DNA مزدوج الشريط في عائلة فيروسات الهربس. بعد العدوى الأولية، يظل كامنًا في الخلايا السلفية النخاعية والوحيدات والبلاعم. عندما تنخفض وظيفة المناعة، يعاد تنشيط الفيروس وينتشر دمويًا إلى العين، مما يسبب التهاب الشبكية بالفيروس المضخم للخلايا.
يصيب الفيروس المضخم للخلايا جميع طبقات الشبكية، ويحدث تلف الخلايا المباشر بالفيروس بشكل رئيسي مما يؤدي إلى نخر الشبكية. الالتهاب المناعي القوي كما يحدث في التهاب الشبكية الحاد الناخر (ARN) نادر، وبسبب ضعف الاستجابة المناعية، تكون العلامات الالتهابية غير واضحة. هذا هو السبب في أن التهاب الغرفة الأمامية والتهاب الجسم الزجاجي نادران في المراحل المبكرة.
ينتج الفيروس المضخم للخلايا إنترلوكين-10 فيروسيًا (cmvIL-10) لتثبيط المناعة، ويمنع بروتين pp65 مسار إشارات cGAS-STING، ويتجنب هجوم الخلايا القاتلة الطبيعية عبر جزيئات شبيهة بـ MHC-I 14). تشكل آليات الهروب المناعي هذه أساس العدوى المزمنة المستمرة. كما ثبت أن الفيروس المضخم للخلايا يزيد من تعبير مستقبل ACE2، مما قد يعزز العدوى المشتركة مع SARS-CoV-2 14).
العدوى المشتركة بـ CMV و VZV و EBV لها تشخيص أسوأ من العدوى الفردية.
أبلغ Kondo وآخرون (2025) عن حالة من التهاب الشبكية المضخم للخلايا الثنائي مع عدوى مشتركة بـ EBV و VZV 15). أظهر PCR الكمي مستويات عالية من CMV 6.7×10⁷ نسخة/مل و VZV 1.3×10⁸ نسخة/مل، مما أدى إلى انفصال الشبكية في كلتا العينين.
عندما يرتفع عدد الخلايا اللمفاوية التائية CD4+ بشكل حاد بعد بدء العلاج المضاد للفيروسات القهقرية (ART)، قد يحدث تفاقم للعدوى الانتهازية الموجودة أو ظهور آفات جديدة. يُسمى هذا متلازمة إعادة بناء المناعة (IRIS). في طب العيون، يُعرف التهاب العنبية الناتج عن استعادة المناعة (IRU) الذي يحدث في العيون التي لديها تاريخ من التهاب الشبكية المضخم للخلايا الهادئ بعد بدء ART، مما يؤدي إلى التهاب الجسم الزجاجي 1).
آلية IRU: النظرية السائدة هي أنه عندما يستعيد ART استجابة الخلايا التائية الخاصة بـ CMV، فإن مستضدات CMV المتبقية التي تتكاثر بشكل طفيف داخل الخلايا على حافة آفات التهاب الشبكية المضخم للخلايا الهادئة تؤدي إلى التهاب العنبية من خلال الاستجابة المناعية. IRIS من النوع “الكاشف” هو حالة تظهر فيها العدوى التي كانت مسيطر عليها سابقًا بعد بدء HAART مباشرة 10).
أعراض وتشخيص IRU: بالإضافة إلى الآفات المبكرة مثل التهاب القزحية والجسم الهدبي والتهاب الجسم الزجاجي، قد تحدث مضاعفات مثل الوذمة البقعية وإعتام عدسة العين. تاريخ بدء ART وارتفاع عدد الخلايا اللمفاوية التائية CD4+ ضروريان للتشخيص.
علاج IRU: يختلف حسب الشدة والتوقيت. يتراوح من الشفاء التلقائي مع المراقبة إلى الحالات التي تتطلب إيقاف ART أو إعطاء الستيرويدات الجهازية أو العلاج الجراحي، لكن إعادة العلاج المضاد لـ CMV للممرض المتبقي هو الأساس 1).
بينما انخفض التهاب الشبكية المضخم للخلايا لدى مرضى الإيدز بشكل كبير بسبب انتشار ART، زادت التقارير عن المرضى غير المصابين بالإيدز والمثبطين مناعياً مثل بعد زرع الأعضاء، بعد العلاج بخلايا CAR-T، ومستخدمي العوامل البيولوجية 7, 9). تنوع أسباب نقص المناعة يجعل توحيد معايير مؤشرات العلاج الوقائي لـ CMV ومدته واختيار الدواء تحديًا. يجب الانتباه إلى تأخر التشخيص في المرضى سلبيي HIV 7, 9).
في التهاب الشبكية المضخم للخلايا المقاوم للأدوية أو المتكرر، من المهم فهم الاستجابة المناعية للمضيف بالإضافة إلى الأدوية المضادة للفيروسات. أبلغ Li وآخرون (2022) عن احتمال عدم كفاية تجنيد الخلايا التائية الخاصة بـ CMV في التهاب الشبكية المضخم للخلايا لدى الأفراد ذوي المناعة الطبيعية 16)، وقد يؤدي توضيح آليات الهروب المناعي المحلي إلى تطوير علاجات مستقبلية. حاليًا، العلاجات المرتبطة بالخلايا التائية هي في مرحلة البحث وليست علاجًا قياسيًا.
ليترمورفير (letermovir) وماريبافير (maribavir) هما عقاران مضادان للفيروسات جديدان أثبتا فعاليتهما ضد CMV المقاوم لـ GCV/فوسكارنيت. حصل ماريبافير على موافقة إدارة الغذاء والدواء الأمريكية (FDA) لعلاج عدوى CMV المقاومة والمستعصية بعد زرع الخلايا الجذعية المكونة للدم (HSCT). الأدلة على التهاب الشبكية CMV لا تزال محدودة، لكن من المتوقع تطبيقه في الحالات متعددة المقاومة.
أبلغ Zu وآخرون (2022) عن أول حالة في العالم لالتهاب الشبكية CMV بعد العلاج بالخلايا CAR-T 8). يُعتقد أن الانخفاض الحاد في المناعة الخلطية الناجم عن العلاج بـ CAR-T عزز إعادة تنشيط CMV، واستُخدم التسلسل من الجيل التالي (NGS) في التشخيص. يُشير ذلك إلى ضرورة فحص CMV بعد الجراحة والمراقبة العينية للمرضى الذين تلقوا العلاج بـ CAR-T.
قد يسهل CMV العدوى المشتركة مع SARS-CoV-2 عن طريق زيادة تعبير ACE2 14). كما تم الإبلاغ عن حالات إعادة تنشيط CMV بعد شدة COVID-19 14). يُوصى بالنظر في التقييم العيني لدى المرضى المثبطين مناعياً عند شدة COVID-19.
يتقدم تحديد تعدد الأشكال الجينية للمضيف التي تؤثر على القابلية للإصابة بـ CMV 14). في المستقبل، قد يُستخدم الفحص الجيني للمرضى عالي الخطورة في استراتيجيات الوقاية.
أظهرت المتابعة طويلة الأمد لدراسات مضاعفات العين للإيدز (SOCA) أن تشخيص حدة البصر لمرضى التهاب الشبكية CMV في عصر ART قد تحسن، لكن الوذمة البقعية وإعتام عدسة العين واعتلال الشبكية الزجاجي التكاثري الناتج عن التهاب القزحية الناتج عن إعادة التنشيط المناعي (IRU) هي الأسباب الرئيسية لانخفاض حدة البصر 3).
في السنوات الأخيرة، تم الإبلاغ عن التهاب القزحية والجسم الهدبي والتهاب بطانة القرنية الناجم عن CMV (التهاب العنبية الأمامي CMV) لدى الأفراد ذوي المناعة الطبيعية، مما يوسع طيف عدوى CMV داخل العين. يقدم تقرير TITAN 2 إجماعاً دولياً حول إدارة التهاب العنبية الأمامي CMV، ومن المتوقع تراكم الأدلة في المستقبل 2).
تتقدم الأبحاث حول التدخل المبكر لتحسين التشخيص طويل الأمد للمضاعفات العينية لعدوى CMV الخلقية (التهاب الشبكية CMV وضمور العصب البصري). يُشير إلى أن البدء المبكر بالعلاج المضاد للفيروسات قد يحسن تشخيص الوظيفة البصرية.