نوع دانهای محیطی
ویژگی: تقریباً بدون خونریزی، لکههای اگزوداتیو سفید دانهای به صورت بادبزنی تجمع مییابند.
تأثیر بر بینایی: اگر ماکولا درگیر نشود، بینایی نسبتاً حفظ میشود.
سیر: شایعترین نوع. از محیط به تدریج به سمت مرکز پیشرفت میکند.

ویروس هرپس انسانی 5، با نام عمومی سیتومگالوویروس (CMV)، بزرگترین ویروس خانواده هرپسویروس با DNA دو رشتهای است. در بدن انسان تمایل گستردهای به بافتها دارد و از طریق عفونت اولیه، عفونت مجدد یا فعالسازی مجدد در شبکیه، باعث رتینیت CMV میشود که با نکروز و ادم تمام لایههای شبکیه مشخص میشود.
نرخ آنتیبادی CMV 70 تا 90 درصد بالا است و بیشتر افراد در دوران نوزادی بدون علامت آلوده میشوند. رتینیت CMV در بزرگسالان عمدتاً ناشی از عفونت فرصتطلب همراه با فعالسازی مجدد ویروس است1).
اگر مادر در اوایل بارداری دچار عفونت اولیه یا فعالسازی مجدد شود، 20 تا 40٪ موارد عفونت از طریق جفت به جنین منتقل میشود و به عنوان عفونت مادرزادی CMV، یکی از سندرمهای TORCH، ممکن است رتینیت CMV ایجاد شود.
اپیدمیولوژی:
در اصل، بروز بیماری در افراد سالم با ایمنی طبیعی نادر است. با این حال، در سالهای اخیر، گزارشهای سندرم قدامی CMV که به صورت یووئیت قدامی و اندوتلیت قرنیه در افراد با ایمنی طبیعی ظاهر میشود، افزایش یافته است (به بخش «یووئیت قدامی CMV» مراجعه کنید). رتینیت CMV (ضایعه خلفی) عمدتاً یک عفونت فرصتطلب در شرایط نقص ایمنی است 1) و در افراد سالم بسیار نادر است. استفاده طولانی مدت از استروئیدها، کاهش عملکرد ایمنی ناشی از دیابت، و پیری ایمنی (immunosenescence) از جمله عوامل زمینهای هستند 11, 12).
بله. در یک مطالعه گذشتهنگر، ۱۵٪ از بیماران مبتلا به رتینیت CMV با HIV مثبت، قبل از تشخیص HIV به چشمپزشک مراجعه کرده بودند و در ۹٪ موارد، رتینیت CMV تنها معیار تشخیصی ایدز بود 13). در صورت مشکوک شدن به رتینیت CMV، باید آزمایش HIV به طور فعال انجام شود.
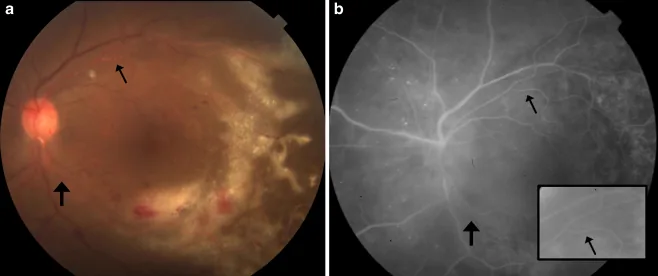
علائم بسته به محل و اندازه ضایعه متفاوت است.
در مراحل اولیه، التهاب اتاق قدامی و ویتریت تقریباً دیده نمیشود و این یافتهها با گسترش ضایعه ظاهر میشوند که این ویژگی، نکته مهمی در افتراق از ARN است.
رتینیت CMV بر اساس یافتههای مشخص فوندوس به سه نوع بالینی طبقهبندی میشود. در عمل بالینی، این انواع اغلب با هم مخلوط میشوند و محل و اندازه ضایعه برای پیشآگهی مهمتر است.
نوع دانهای محیطی
ویژگی: تقریباً بدون خونریزی، لکههای اگزوداتیو سفید دانهای به صورت بادبزنی تجمع مییابند.
تأثیر بر بینایی: اگر ماکولا درگیر نشود، بینایی نسبتاً حفظ میشود.
سیر: شایعترین نوع. از محیط به تدریج به سمت مرکز پیشرفت میکند.
نوع واسکولیت قطب خلفی
ویژگی: لکههای اگزوداتیو زرد-سفید همراه با خونریزی و ادم شبکیه در امتداد عروق قطب خلفی ظاهر میشوند. نکروز و خونریزی گسترده که به «پیتزا پای» تشبیه میشود، مشخصه است.
تأثیر بر بینایی: به دلیل درگیری ماکولا و عصب بینایی، کاهش بینایی قابل توجه است.
سیر: بدترین پیشآگهی بینایی. شروع سریع درمان حیاتی است.
نوع واسکولیت درختی-آبی
ویژگی: عروق شبکیه به ویژه عروق بزرگ، به صورت واسکولیت درختی-آبی غلاف سفید میشوند (FBA).
شیوع: نوع نسبتاً نادر. ممکن است به عنوان نشانه CMV-IRIS ظاهر شود10).
توجه: در عمل بالینی، سه نوع اغلب با هم مخلوط میشوند و محل و اندازه ضایعه برای پیشآگهی مهم است.
طبقهبندی ناحیهای ضایعه برای تعیین فوریت درمان مهم است.
| ناحیه | محدوده | اهمیت بالینی |
|---|---|---|
| Zone 1 | درون 1DD از دیسک بینایی و درون 2DD از ماکولا | شروع فوری درمان |
| Zone 2 | از خط استوا تا آمپول وریدهای گردابی | درمان در نظر گرفته شود |
| Zone 3 | دورترین ناحیه محیطی | پیگیری قابل قبول است |
جداشدگی شبکیه (RD) یک عارضه جدی است. هرچه ناحیه درگیر وسیعتر باشد، خطر جداشدگی رگماتوژن شبکیه بیشتر است. اگرچه پس از رواج ART این خطر نسبت به گذشته کاهش یافته، اما حتی پس از درمان نیز نیاز به پیگیری طولانیمدت وجود دارد3).
Tang و همکاران (2021) یک بیمار HIV را گزارش کردند که 35 روز پس از شروع HAART دچار واسکولیت شاخههای یخزده شد10). IL-6 در زلالیه 2845 pg/mL و IL-8 برابر 967.8 pg/mL بود که افزایش قابل توجهی داشت و به عنوان FBA از نوع IRIS آشکارساز (unmasking) تشخیص داده شد. التهاب تنها با درمان ضد ویروسی بهبود یافت.
در نواحی قدیمی رتینیت CMV، تمام لایههای شبکیه دچار نکروز شده و نازک و توریمانند میشوند. با کشش زجاجیه، به راحتی پارگیهای متعدد ایجاد شده و جداشدگی شبکیه رخ میدهد. بنابراین حتی پس از فروکش کردن رتینیت، پیگیری طولانیمدت ضروری است.
لایههای نکروز شده شبکیه نازک و توریمانند میشوند. با کشش زجاجیه، به راحتی پارگیهای متعدد ایجاد میشود. به ویژه در لبه نکروز که نازکتر است، خطر ایجاد پارگی بیشتر است. حتی پس از فروکش التهاب با درمان، شبکیه نازک باقی میماند و نیاز به پیگیری طولانیمدت دارد.
CMV رتینیت در اکثر موارد یک عفونت فرصتطلب در شرایط نقص ایمنی است. بررسی سابقه بیماریهای زمینهای مانند سندرم نقص ایمنی اکتسابی (ایدز) که منجر به نقص ایمنی میشوند و همچنین سابقه مصرف داروهای سرکوبکننده ایمنی در بیماران بزرگسال، نقطه شروع تشخیص است 1).
عوامل خطر اصلی:
اگرچه معیار تشخیصی قطعی برای رتینیت CMV وجود ندارد، اما با توجه به ضایعات مشخص شبکیه، تشخیص بالینی بر اساس ترکیب زمینه بیمار (وضعیت نقص ایمنی) و یافتههای فوندوس امکانپذیر است.
| آزمایش/ارزیابی | محتوا |
|---|---|
| یافتههای فوندوس | تأیید سه نوع (نوع دانهای محیطی، نوع واسکولیت قطب خلفی، نوع واسکولیت دندریتیک). در مراحل اولیه، التهاب اتاق قدامی و زجاجیه اندک است. |
| PCR کمی مایع داخل چشمی (Real-time) | حساسیت و ویژگی بالا دارد و برای تشخیص قطعی استفاده میشود. ممکن است در مراحل اولیه که سلولهای التهابی اتاق قدامی وجود ندارند، شناسایی نشود1) |
| PCR چندگانه (پزشکی پیشرفته) | جستجوی جامع چندین ویروس با نمونه کوچک. برای افتراق از ARN مفید است1) |
| روش آنتیژنمی CMV / PCR خون | به عنوان کمک تشخیصی، مقدار مرجع. برای تشخیص قطعی، PCR موضعی چشم اولویت دارد |
| بررسی زمینه بیمار | مقدار CD4، سابقه مصرف داروهای سرکوبکننده ایمنی، وضعیت درمان ART و غیره |
معیارهای ACTG (گروه کارآزمایی بالینی ایدز)1):
معیارهای ACTG (گروه کارآزمایی بالینی ایدز)1):
توالییابی نسل بعد (NGS) به عنوان کمک تشخیصی برای مواردی که تشخیص با PCR دشوار است گزارش شده است و در موارد پس از CAR-T نیز کاربرد دارد8). در بیماران سرکوبایمنی HIV منفی، تشخیص اغلب به تأخیر میافتد و نباید تنها با آزمایش سرم رد شود، بلکه باید با ترکیب یافتههای چشمی و آزمایش مایع داخل چشمی قضاوت کرد7, 9).
در افتراق از لکه پنبهای (cotton-wool spot)، اندازه ضایعه کمککننده است. ضایعات کوچکتر از 750 میکرومتر احتمالاً لکه پنبهای و بزرگتر از آن احتمالاً رتینیت CMV هستند.
تشخیصهای افتراقی:
تشخیص بالینی بر اساس یافتههای مشخص فوندوس (هر یک از سه نوع) و زمینه بیمار (وضعیت نقص ایمنی) اساس کار است. برای تشخیص قطعی، PCR کمی بلادرنگ مایع داخل چشمی (زلالیه یا زجاجیه) از نظر حساسیت و ویژگی بهترین است 1). PCR چندعاملی (پزشکی پیشرفته) مزیت تشخیص چندین ویروس را با نمونه کوچک دارد و به ویژه برای افتراق از ARN مفید است.
درمان ضد CMV با تزریق داخل وریدی گانسیکلوویر به عنوان خط اول است و بسته به محل و اندازه ضایعه و وجود عوارض جانبی، از والگانسیکلوویر خوراکی، تزریق داخل وریدی فوسکارنت یا تزریق داخل زجاجیه به تنهایی یا ترکیبی استفاده میشود. رتینیت CMV احتمال عفونت نهفته CMV در چندین اندام را دارد و اساس درمان ضد ویروسی، درمان سیستمیک است.
در زیر نسخههای اصلی آورده شده است.
| دارو | نام محصول | دوز شروع | دوز نگهدارنده |
|---|---|---|---|
| گانسیکلوویر تزریق داخل وریدی | دنوسین تزریق داخل وریدی (۵۰۰ میلیگرم) | ۵ میلیگرم/کیلوگرم/نوبت دو بار در روز | ۵ میلیگرم/کیلوگرم/نوبت یک بار در روز |
| والگانسیکلوویر خوراکی | قرص والیکسا (450 میلیگرم) | 4 قرص (1800 میلیگرم) دو بار در روز بعد از غذا | 2 قرص (900 میلیگرم) یک بار در روز بعد از غذا |
| فوسکارنت تزریق وریدی | ویال فوسکاویر (24 میلیگرم/میلیلیتر) | 90 میلیگرم/کیلوگرم/دوز دو بار در روز | 90 میلیگرم/کیلوگرم/دوز یک بار در روز |
درمان القایی معمولاً به مدت 2 تا 3 هفته انجام میشود. پس از آن، درمان نگهدارنده ادامه مییابد. فوسکارنت جایگزینی برای موارد سرکوب شدید مغز استخوان ناشی از گانسیکلوویر است، اما باید به سمیت کلیوی آن توجه کرد.
در صورت وجود مشکلات عوارض جانبی یا قرارگیری ضایعه در قطب خلفی، ممکن است تزریق داخل زجاجیهای GCV یا فوسکارنت انجام شود (خارج از پوشش بیمه).
فوسکارنت و سیدوفوویر داروهای خط دوم در موارد عدم تحمل یا مقاومت به GCV/VGCV هستند. سیدوفوویر یک بار در هفته (القایی) و سپس هر دو هفته یک بار (نگهدارنده) تجویز میشود. عوارض جانبی شامل کاهش فشار چشم (تا 50%)، یووئیت قدامی و سمیت کلیوی است و نیاز به پیشدرمانی با پروبنسید دارد.
پس از شروع HAART و در طی بهبود CD4، ممکن است پاسخ ایمنی بیش از حد به آنتیژنهای باقیمانده CMV رخ دهد (در ۱۰ تا ۱۷٪ موارد سیتومگالوویروس، اغلب در ۳ ماه اول پس از HAART). مدیریت به شرح زیر است:
پس از پایان درمان القایی، درمان نگهدارنده ادامه مییابد. در بیماران HIV/AIDS، درمان ضد ویروسی حداقل ۶ ماه ادامه یابد و در صورت تداوم CD4+ > 100 سلول/میکرولیتر به مدت ۴-۶ ماه، قطع آن در نظر گرفته شود. پیگیری: در طول القا هفتهای یک بار، در طول نگهداری هر دو هفته یک بار معاینه فوندوس با گشاد کردن مردمک، و پس از تثبیت ماهانه یک بار.
در صورت جداشدگی رگماتوژن شبکیه، درمان جراحی اندیکاسیون دارد. با توجه به اندازه ضایعه و میزان جداشدگی، ترکیبی از موارد زیر استفاده میشود:
در صورت درمان به موقع، پیشآگهی به اندازه نکروز حاد شبکیه بد نیست.
درمان اساسی، رفع سرکوب ایمنی است. در افراد مبتلا به HIV، شروع و ادامه ART برای بازگرداندن CD4 و جلوگیری از عود رتینیت CMV اساسی است. باید مراقب بروز IRU (یووئیت ناشی از بازیابی ایمنی) پس از شروع ART بود (← به بخش «پاتوفیزیولوژی و مکانیسم دقیق بروز» مراجعه کنید).
خیر، مؤثر نیستند. CMV حساسیت کمی به آسیکلوویر و والاسیکلوویر دارد و داروهای ضد HSV/VZV کافی نیستند. برای CMV، گانسیکلوویر یا والگانسیکلوویر داروهای خط اول هستند. اگر گانسیکلوویر به دلیل عوارضی مانند سرکوب مغز استخوان قابل استفاده نباشد، فوسکارنت به عنوان داروی جایگزین استفاده میشود.
CMV بزرگترین ویروس DNA دو رشتهای در خانواده هرپسویروسها است. پس از عفونت اولیه، در سلولهای پیشساز میلوئید، مونوسیتها و ماکروفاژها به صورت نهفته باقی میماند. در شرایط کاهش عملکرد ایمنی، ویروس دوباره فعال شده و از طریق خون به داخل چشم منتشر میشود و باعث رتینیت CMV میگردد.
CMV تمام لایههای شبکیه را آلوده میکند و آسیب مستقیم سلولی ویروسی اصلیترین عامل نکروز شبکیه است. برخلاف ARN، التهاب شدید با واسطه ایمنی در این بیماری نادر است و به دلیل پاسخ ایمنی ضعیف، علائم التهابی نیز قابل توجه نیستند. این دلیل عدم وجود التهاب اتاق قدامی و زجاجیه در مراحل اولیه است.
CMV با تولید اینترلوکین-10 ویروسی (cmvIL-10) ایمنی را سرکوب میکند، پروتئین pp65 مسیر سیگنالدهی cGAS-STING را مهار میکند و با مولکولهای شبه MHC-I از حمله سلولهای NK جلوگیری میکند14). این مکانیسمهای فرار ایمنی زمینهساز عفونت مزمن پایدار هستند. همچنین نشان داده شده است که CMV بیان گیرنده ACE2 را افزایش میدهد که ممکن است عفونت همزمان با SARS-CoV-2 را تسهیل کند14).
عفونت همزمان CMV با VZV و EBV پیشآگهی بدتری نسبت به عفونت تکویروسی دارد.
کوندو و همکاران (2025) موردی از رتینیت CMV دوطرفه همراه با عفونت همزمان EBV و VZV را گزارش کردند15). PCR کمی مقادیر بالای CMV 6.7×10⁷ کپی/میلیلیتر و VZV 1.3×10⁸ کپی/میلیلیتر را نشان داد و جداشدگی شبکیه در هر دو چشم رخ داد.
پس از شروع ART، افزایش ناگهانی تعداد لنفوسیتهای T CD4+ ممکن است باعث تشدید عفونتهای فرصتطلب موجود یا ظهور ضایعات جدید شود. این سندرم بازسازی ایمنی (IRIS) نامیده میشود. در چشمپزشکی، IRU به عنوان التهاب زجاجیه در چشمهایی با سابقه رتینیت CMV که پس از ART فروکش کرده است، شناخته میشود1).
مکانیسم IRU: نظریه غالب این است که پس از ART، پاسخ سلولهای T اختصاصی CMV بازیابی میشود و آنتیژنهای باقیمانده CMV که در سلولهای حاشیه ضایعات رتینیت CMV فروکشیافته به مقدار کم تکثیر میشوند، از طریق واکنش ایمنی باعث یووئیت آشکار میشوند. IRIS از نوع «unmasking» وضعیتی است که در آن عفونت قبلاً کنترلشده بلافاصله پس از شروع HAART آشکار میشود10).
علائم و تشخیص IRU: علاوه بر ضایعات اولیه مانند ایریدوسیکلیت و ویتریت، عوارض ثانویه مانند ادم ماکولا و آب مروارید رخ میدهد. سابقه شروع ART و افزایش تعداد لنفوسیتهای T CD4+ برای تشخیص ضروری است.
درمان IRU: بسته به شدت و زمان متفاوت است. موارد از بهبود خودبهخودی با پیگیری تا نیاز به قطع ART یا تجویز سیستمیک استروئید و حتی درمان جراحی متغیر است، اما اساس درمان، ازسرگیری درمان ضد CMV علیه پاتوژن باقیمانده است1).
با گسترش ART، رتینیت CMV در بیماران ایدزی به شدت کاهش یافته است، در حالی که گزارشها در بیماران غیر ایدزی با نقص ایمنی مانند پس از پیوند عضو، پس از درمان با سلولهای CAR-T و مصرفکنندگان داروهای بیولوژیک در حال افزایش است7, 9). علل نقص ایمنی متنوع شدهاند و استانداردسازی اندیکاسیون، مدت و انتخاب دارو برای پروفیلاکسی CMV به یک چالش تبدیل شده است. در بیماران HIV منفی باید به تأخیر در تشخیص توجه کرد7, 9).
در رتینیت CMV مقاوم به دارو یا عودکننده، درک پاسخ ایمنی میزبان علاوه بر داروهای ضدویروسی مهم است. لی و همکاران (2022) احتمال عدم بسیج کافی سلولهای T اختصاصی CMV را در رتینیت CMV افراد با ایمنی طبیعی گزارش کردند16) و کشف مکانیسمهای فرار ایمنی موضعی ممکن است به توسعه درمانهای آینده کمک کند. در حال حاضر، درمانهای مرتبط با سلولهای T در مرحله تحقیقاتی هستند و درمان استاندارد محسوب نمیشوند.
لترموویر (letermovir) و ماریباویر (maribavir) داروهای ضد ویروسی جدیدی هستند که اثربخشی خود را در برابر CMV مقاوم به GCV/فوسکارنت نشان دادهاند. به ویژه ماریباویر برای عفونت CMV مقاوم و دشوار پس از HSCT تأیید FDA را دریافت کرده است. اگرچه شواهد برای رتینیت CMV هنوز محدود است، اما انتظار میرود در موارد مقاوم به چند دارو کاربرد داشته باشد.
زو و همکاران (2022) اولین مورد رتینیت CMV را پس از درمان با سلولهای CAR-T گزارش کردند 8). کاهش شدید ایمنی هومورال ناشی از درمان CAR-T احتمالاً باعث فعالسازی مجدد CMV شده است و برای تشخیص از NGS استفاده شد. این یافته نشاندهنده نیاز به غربالگری CMV و پایش چشمی پس از درمان در بیماران تحت CAR-T است.
CMV با افزایش بیان ACE2 ممکن است عفونت همزمان با SARS-CoV-2 را تسهیل کند 14). همچنین مواردی از فعالسازی مجدد CMV پس از COVID-19 شدید گزارش شده است 14). در بیماران دچار نقص ایمنی با COVID-19 شدید، ارزیابی چشمی نیز باید مد نظر قرار گیرد.
شناسایی پلیمورفیسمهای ژنتیکی میزبان که بر حساسیت به CMV تأثیر میگذارند در حال پیشرفت است 14). در آینده، غربالگری ژنتیکی بیماران پرخطر ممکن است در استراتژیهای پیشگیری استفاده شود.
پیگیری طولانیمدت توسط Studies of Ocular Complications of AIDS (SOCA) نشان داده است که اگرچه پیشآگهی بینایی در بیماران مبتلا به رتینیت CMV در عصر ART بهبود یافته است، اما ادم ماکولا، آب مروارید و رتینوپاتی پرولیفراتیو ناشی از IRU علل اصلی کاهش بینایی هستند 3).
اخیراً، مواردی از ایریدوسیکلیت و اندوتلیت قرنیه ناشی از CMV (یووئیت قدامی CMV) در افراد با ایمنی طبیعی گزارش شده است و طیف عفونت CMV داخل چشمی در حال گسترش است. گزارش TITAN Report 2 یک اجماع بینالمللی برای مدیریت یووئیت قدامی CMV ارائه کرده است و انتظار میرود شواهد بیشتری جمعآوری شود 2).
تحقیقات در مورد مداخله زودهنگام برای بهبود پیشآگهی بلندمدت عوارض چشمی عفونت مادرزادی CMV (رتینیت CMV و آتروفی عصب بینایی) در حال پیشرفت است. شروع زودهنگام درمان ضد ویروسی ممکن است پیشآگهی بینایی را بهبود بخشد.