โรคท็อกโซพลาสโมซิสทางตา คือ จอประสาทตา อักเสบร่วมกับคอรอยด์ อักเสบที่เกิดจาก Toxoplasma gondii ซึ่งเป็นสาเหตุที่พบบ่อยที่สุดของม่านตาอักเสบ ส่วนหลังชนิดติดเชื้อ
ประมาณหนึ่งในสามของประชากรโลกติดเชื้อ และสัดส่วนของโรคตาอยู่ระหว่าง 2-43% ขึ้นอยู่กับภูมิภาค ในญี่ปุ่น โรคนี้คิดเป็นประมาณ 1% ของม่านตาอักเสบ ชนิดติดเชื้อ
ลักษณะทั่วไปคือ จอประสาทตา อักเสบแบบโฟกัสสีขาวร่วมกับวุ้นตา เสื่อม (สัญญาณ “ไฟหน้ารถในหมอก”) และแผลเป็นของคอรอยด์ และจอประสาทตา ที่มีเม็ดสี
ในการติดเชื้อแต่กำเนิด จะมีแผลเป็นที่จุดภาพชัด ทั้งสองข้าง และอาจเกิดการกลับเป็นซ้ำได้โดยเฉพาะในช่วงวัยรุ่น
การรักษาทั่วไปคือ การให้อะเซทิลสไปรามัยซิน 0.8-1.2 กรัม/วัน เป็นเวลา 30 วันขึ้นไป ส่วนในต่างประเทศใช้การรักษาแบบสามตัวร่วมกันคือ ไพริเมธามีน + ซัลฟาไดอะซีน + สเตียรอยด์
สำหรับการป้องกันการกลับเป็นซ้ำ การใช้ไตรเมโทพริม-ซัลฟาเมทอกซาโซลระยะยาวถือว่ามีประสิทธิภาพ
ในผู้ป่วยที่มีภูมิคุ้มกันบกพร่อง โรคอาจรุนแรง ดังนั้นการวินิจฉัยแต่เนิ่นๆ และการรักษาที่เหมาะสมจึงสำคัญ
โรคท็อกโซพลาสโมซิสทางตา คือ จอประสาทตา อักเสบร่วมกับคอรอยด์ อักเสบที่เกิดจากการติดเชื้อที่จอประสาทตา ด้วยโปรโตซัวที่ต้องอาศัยภายในเซลล์ Toxoplasma gondii เป็นสาเหตุที่พบบ่อยที่สุดของม่านตาอักเสบ ชนิดติดเชื้อ และในบางประเทศคิดเป็นมากกว่า 50% ของม่านตาอักเสบ ส่วนหลังทั้งหมด7)
T. gondii มีแมวเป็นโฮสต์สุดท้าย และสัตว์เลี้ยงลูกด้วยนมเกือบทั้งหมดรวมถึงมนุษย์เป็นโฮสต์ตัวกลาง ทำให้เป็นโรคติดต่อจากสัตว์สู่คน การติดเชื้อเกิดจากการกินโอโอซิสต์ที่ปนเปื้อนในดินหรือน้ำจากอุจจาระแมว หรือจากการกินซีสต์ในเนื้อสัตว์ที่ปรุงไม่สุก (เนื้อหมู เนื้อแกะ เนื้อกวาง ฯลฯ) ประมาณหนึ่งในสามของประชากรโลกติดเชื้อ7) และอัตราการมีแอนติบอดีในผู้ใหญ่ญี่ปุ่นอยู่ที่ 20-30% โรคท็อกโซพลาสโมซิสทางตาคิดเป็นประมาณ 1% ของสาเหตุม่านตาอักเสบ ชนิดติดเชื้อ8)
โปรโตซัวมีสามรูปแบบดังนี้:
โอโอซิสต์ (oocyst) : รูปที่อยู่ในดินซึ่งถูกขับออกมากับอุจจาระแมวทาคิโซอิต (tachyzoite) : รูปที่เพิ่มจำนวนอย่างรวดเร็วระหว่างการติดเชื้อระยะ activeซีสต์เนื้อเยื่อ (tissue cyst) : รูปที่เจริญช้า (bradyzoite) ซึ่งอยู่ในสถานะพักตัวภายในจอประสาทตา
สัดส่วนของโรคตาที่เกิดจากท็อกโซพลาสโมซิสที่ตาประมาณ 2% ในสหรัฐอเมริกา 18% ในบราซิล และสูงถึง 43% ในแอฟริกา อัตราการติดเชื้อสูงที่สุดในเขตร้อน ซึ่งสะท้อนถึงสภาพแวดล้อมที่อบอุ่นและชื้นที่เหมาะสมต่อการเจริญเติบโตของโปรโตซัว
โครงสร้างประชากรของ T. gondii มีลักษณะเป็นโคลนสูง โดยมีสามสายพันธุ์หลักในอเมริกาเหนือและยุโรป: ชนิด I, II และ III7) ชนิด II เป็นสาเหตุส่วนใหญ่ของโรคตาที่ได้มา ในขณะที่ชนิด I มักเกี่ยวข้องกับท็อกโซพลาสโมซิสแต่กำเนิด ในบราซิล ชนิด I และชนิดผิดปกติมีส่วนเกี่ยวข้องกับการติดเชื้อที่ได้มา และความแตกต่างของจีโนไทป์อาจนำไปสู่ความหลากหลายของภาพทางคลินิก7)
Q
การติดเชื้อแต่กำเนิดและการติดเชื้อที่ได้มาต่างกันอย่างไร?
A
การติดเชื้อแต่กำเนิดติดต่อผ่านรกไปยังทารกในครรภ์ระหว่างการติดเชื้อครั้งแรกของมารดา โดยมีลักษณะเฉพาะคือรอยโรคแผลเป็นที่จุดภาพชัด ของตาทั้งสองข้าง อัตราการติดต่อผ่านรกจะสูงขึ้นในไตรมาสที่สองและสามของการตั้งครรภ์ แต่ความรุนแรงของโรคมักจะสูงกว่าหากการติดเชื้อเกิดขึ้นในช่วงต้นของการตั้งครรภ์ การติดเชื้อที่ได้มาเกิดขึ้นหลังคลอดผ่านอาหารหรือน้ำที่ปนเปื้อน และแสดงออกเป็นจอประสาทตา อักเสบร่วมกับคอรอยด์ อักเสบแบบโฟกัสโดยไม่มีรอยโรคเก่าที่บริเวณรอบนอกของจอตา ดูรายละเอียดเพิ่มเติมในหัวข้อ “พยาธิสรีรวิทยา”
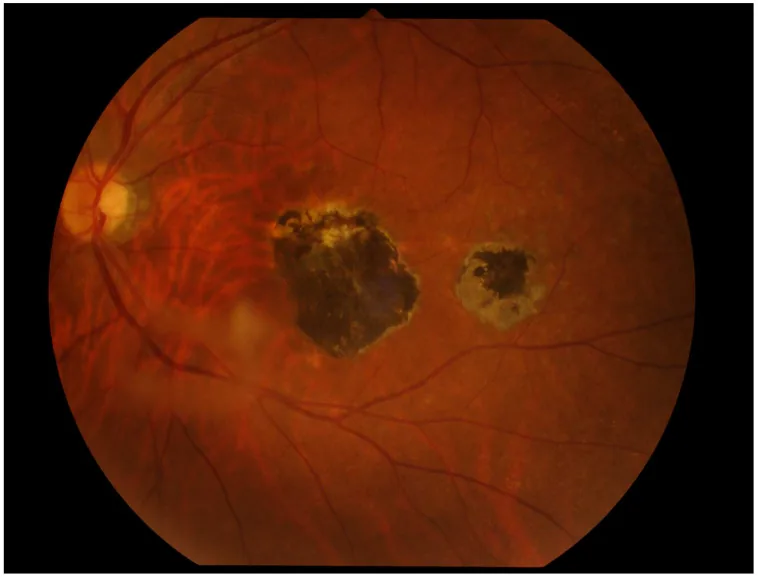
ภาพถ่ายจอตาของท็อกโซพลาสโมซิสที่ตา พบรอยแผลเป็นของคอรอยด์และจอประสาทตาที่มีเม็ดสีใกล้จุดภาพชัดและรอยโรครอบข้าง Miyagaki M, et al. Ocular Toxoplasmosis: Advances in Toxoplasma gondii Biology, Clinical Manifestations, Diagnostics, and Therapy. Pathogens. 2024. Figure 2. PM
CI D: PMC11509995. License: CC BY.
ที่ขั้วหลังของจอตามีรอยโรคแผลเป็นของคอรอยด์ และจอประสาทตา ที่มีเม็ดสี และใกล้ๆ มีรอยโรครอบข้างขนาดเล็ก ภาพนี้แสดงรอยโรคคอรอยด์ และจอประสาทตา ที่เป็นลักษณะเฉพาะของท็อกโซพลาสโมซิสที่ตา ซึ่งเหมาะสมสำหรับอธิบายอาการแสดงทางคลินิก
ในท็อกโซพลาสโมซิสที่ตาระยะ active จะพบอาการต่อไปนี้:
จุดลอยในตา (floaters) : อาการที่พบบ่อยที่สุด เกี่ยวข้องกับภาวะวุ้นตา อักเสบตามัว (การมองเห็น ลดลง) : แตกต่างจากเล็กน้อยถึงรุนแรง ขึ้นอยู่กับตำแหน่งและขนาดของรอยโรคปวดตา และตาแดง ม่านตาอักเสบ ร่วมกับซิลิอารีบอดี อักเสบแบบทุติยภูมิ
อาการแสดงทางคลินิกของท็อกโซพลาสโมซิสที่ตาแบ่งออกเป็นอาการแสดงแบบทั่วไปและแบบไม่ทั่วไป
อาการแสดงแบบทั่วไป
“ไฟหน้ารถในหมอก” : จอประสาทตา อักเสบเฉพาะที่สีขาวร่วมกับวุ้นตา เสื่อม เป็นอาการแสดงที่บ่งชี้โรคนี้ได้อย่างมาก
แผลเป็นคอริโอเรตินัล : แผลเป็นเก่าที่มีเม็ดสี รอยโรคที่กลับเป็นซ้ำมักปรากฏที่ขอบของแผลเป็นนี้
วุ้นตา เสื่อม
หลอดเลือดจอประสาทตาอักเสบ
ยูเวียอักเสบส่วนหน้า : ม่านตา และซิลิอารีบอดี อักเสบแบบไม่เป็นเม็ดโลหิตที่เกิดตามมา อาจพบตะกอนที่กระจกตา ชั้นหลังแบบรูปดาวและเป็นเม็ดโลหิต
อาการแสดงแบบไม่ทั่วไป
ปุ่มประสาทตาอักเสบ / จอประสาทตา ประสาทตาอักเสบ : ปุ่มประสาทตาบวม อาจร่วมกับจอประสาทตา ลายดาว
จอประสาทตา ชั้นนอกอักเสบแบบจุด (PORT )จอประสาทตา ชั้นลึก อาจพบถุงน้ำจอประสาทตา ชั้นนอกขนาดยักษ์ (HORC) ในการตรวจ OCT 2)
หลอดเลือดจอประสาทตา อุดตัน : อาจเกิดหลอดเลือดแดงแขนงอุดตันหรือหลอดเลือดอักเสบแบบกิ่งไม้
ตาขาว อักเสบ / จอประสาทตาลอก
จอประสาทตา อักเสบแบบตายหลายจุดกระจาย7)
ในการติดเชื้อแต่กำเนิด พบรอยโรคแผลเป็นที่จอประสาทตา ทั้งสองข้างเป็นรอยโรคหลัก (เนื้อเยื่อเส้นใยเจริญสีขาวเทาตรงกลางร่วมกับเม็ดสีน้ำตาลดำ และวงแหวนสีจางรอบข้าง) ใกล้ๆ อาจพบแผลเป็นเม็ดสีเล็กๆ เรียกว่ารอยโรคลูกสาว ร่วมกับการอักเสบในช่องหน้าม่านตา และวุ้นตา ขุ่นมาก (“ไฟหน้ารถในหมอก”) และเป็นสองข้างต่างจากการติดเชื้อภายหลัง รอยโรคที่กลับเป็นซ้ำไม่เกิดพร้อมกันทั้งสองข้าง ในการติดเชื้อภายหลัง พบจอประสาทตา และคอรอยด์ อักเสบแบบมีน้ำเหลืองเฉพาะที่สีขาวถึงขาวเทาโดยไม่มีแผลเป็นเก่าที่จอประสาทตา ส่วนปลาย ร่วมกับวุ้นตา ขุ่นมากและหลอดเลือดจอประสาทตาอักเสบ เมื่อหายดีจะกลายเป็นแผลเป็นฝ่อขอบเขตชัดเจนมีเม็ดสี
รอยโรคบริเวณรอบหัวประสาทตาเรียกว่า จอประสาทตา อักเสบชนิดจัสตาแพพิลลารีแบบเอ็ดมันด์-เจนเซน (Edmund-Jensen type juxtapapillary chorioretinitis) ในการตรวจหลอดเลือดด้วยฟลูออเรสซีน ระยะแรกจะพบการย้อมสีเนื้อเยื่อรอบรอยโรคและข้อบกพร่องเงาตรงกลาง เมื่อเวลาผ่านไปจะเกิดการย้อมฟลูออเรสเซนต์ในบริเวณข้อบกพร่อง และในระยะหลังจะพบการรั่วของฟลูออเรสซีน อย่างชัดเจน
ในกรณีที่ไม่ปกติ อาจแยกความแตกต่างจากจอประสาทตาตายเฉียบพลัน (ARN ) และมะเร็งต่อมน้ำเหลืองในลูกตาได้ยาก 5) ในกลุ่มตัวอย่างชาวดัตช์กลุ่มหนึ่ง ผู้ป่วย 4 ใน 18 รายที่มีรอยโรคขนาดใหญ่เส้นผ่านศูนย์กลางมากกว่า 3 หัวประสาทตา ได้รับการวินิจฉัยเบื้องต้นว่าเป็นจอประสาทตาตายเฉียบพลัน 5)
รอยโรคที่ขั้วหลัง (จอประสาทตา หรือหัวประสาทตา) มักมีการพยากรณ์โรคทางสายตาที่ไม่ดี และในกลุ่มตัวอย่างชาวดัตช์จำนวน 154 ราย พบว่า 24% มีภาวะตาบอดตามกฎหมาย (20/200 หรือแย่กว่า) อย่างน้อยในตาข้างเดียว 5) รอยโรคที่จอประสาทตา เป็นสาเหตุ 80% จอประสาทตาลอก 13% และฝ่อของประสาทตา 7%
เส้นทางการติดเชื้อ T. gondii ส่วนใหญ่มี 3 เส้นทางดังนี้
การติดเชื้อทางปาก : การกินซีสต์ในเนื้อเยื่อจากเนื้อสัตว์ที่ปรุงไม่สุก (เนื้อหมู เนื้อแกะ เนื้อกวาง ฯลฯ) อาจเกิดจากการกินโอโอซิสต์จากน้ำหรือผักที่ปนเปื้อนได้เช่นกันการติดเชื้อจากแมว : การสัมผัสกับโอโอซิสต์ที่ขับออกมาในอุจจาระแมวการติดเชื้อผ่านรก : การแพร่เชื้อไปยังทารกในครรภ์ระหว่างการติดเชื้อครั้งแรกของมารดาในระหว่างตั้งครรภ์ อัตราการติดเชื้อต่ำในช่วงต้นของการตั้งครรภ์ แต่ความรุนแรงของโรคสูง และอัตราการแพร่เชื้อผ่านรกจะเพิ่มขึ้นเมื่อการตั้งครรภ์ดำเนินไป
ปัจจัยเสี่ยงหลักมีดังนี้
การกินเนื้อสัตว์ที่ปรุงไม่สุก : เนื้อสัตว์ป่า (เนื้อกวาง) มีความเสี่ยงสูงเป็นพิเศษ ในกลุ่มผู้ป่วยกลุ่มหนึ่ง อาการทางระบบปรากฏภายใน 1-2 สัปดาห์ และอาการทางตาโดยเฉลี่ย 2.6 เดือนหลังจากกินเนื้อกวางที่ปรุงไม่สุก 4) การสัมผัสกับแมว : การเลี้ยงแมว 3 ตัวขึ้นไปหรือลูกแมวภาวะภูมิคุ้มกันบกพร่อง : โรคเอดส์ มะเร็งเม็ดเลือด การใช้ยากดภูมิคุ้มกัน ในผู้ป่วย CLL มีรายงานว่าเป็นการติดเชื้อฉวยโอกาสระหว่างการใช้ยาไอบรูทินิบ 3) ผู้สูงอายุ : มีแนวโน้มที่จะมีอุบัติการณ์ของรอยโรคทางตาจากการติดเชื้อที่ได้รับสูงกว่า 7)
Kohler และคณะ (2023) รายงานผู้ป่วยติดเชื้อครั้งแรก 4 รายที่เกี่ยวข้องกับการบริโภคเนื้อกวาง ทั้งหมดเป็นเพศชาย อายุเฉลี่ย 56 ปี สัมผัสเชื้อในช่วงฤดูล่าสัตว์เดือนตุลาคม-พฤศจิกายน และแสดงลำดับเวลาที่ชัดเจนโดยมีอาการทางระบบภายในไม่กี่สัปดาห์และอาการทางตาหลังจากนั้น 1-3 เดือน 4)
Q
การติดเชื้อระหว่างตั้งครรภ์จำเป็นต้องส่งผลต่อทารกในครรภ์หรือไม่?
A
แม้ว่ามารดาจะติดเชื้อปฐมภูมิ การแพร่เชื้อไปยังทารกในครรภ์ไม่ได้เกิดขึ้นเสมอไป และส่วนใหญ่การติดเชื้อจะไม่แสดงอาการ อย่างไรก็ตาม บางกรณีอาจนำไปสู่โรคทอกโซพลาสโมซิสแต่กำเนิดที่มีอาการทางตาและระบบประสาทรุนแรง (จอประสาทตา อักเสบร่วมกับคอรอยด์ อักเสบ, ภาวะน้ำคั่งในโพรงสมอง, การกลายเป็นปูนในกะโหลกศีรษะ และความผิดปกติทางการเคลื่อนไหว) ดังนั้นการตรวจคัดกรองแอนติบอดีในหญิงตั้งครรภ์และการรักษาตั้งแต่เนิ่นๆ จึงมีความสำคัญ
การวินิจฉัยโรคทอกโซพลาสโมซิสทางตาส่วนใหญ่ขึ้นอยู่กับผลการตรวจทางคลินิก การรวมกันของสัญญาณ “ไฟหน้ารถในหมอก” และรอยแผลเป็นจากจอประสาทตา อักเสบร่วมกับคอรอยด์ อักเสบที่มีเม็ดสีเป็นลักษณะเฉพาะ และในกรณีส่วนใหญ่สามารถวินิจฉัยทางคลินิกได้ การมีทั้งผลการตรวจทางคลินิกและแอนติบอดีต่อทอกโซพลาสมาเป็นบวกสนับสนุนการวินิจฉัยนี้อย่างมาก 8)
การตรวจ ความสำคัญ ข้อควรระวัง แอนติบอดี IgG ยืนยันการติดเชื้อในอดีต หากเป็นลบ สามารถแยกการติดเชื้อออกได้ อัตราการเป็นบวกเพิ่มขึ้นตามอายุ แอนติบอดี IgM บ่งชี้การติดเชื้อล่าสุด อาจสูงอยู่ได้นานกว่า 1 ปี ไม่เพิ่มขึ้นเมื่อมีการกลับเป็นซ้ำของการติดเชื้อแต่กำเนิด ความคงทนของ IgG (IgG avidity) ประเมินว่าการติดเชื้อใหม่หรือเก่า ความคงทนสูงบ่งชี้การติดเชื้อเรื้อรัง5)
ในผู้ที่มีภูมิคุ้มกันปกติ หากแอนติบอดี IgG เป็นลบโดยสมบูรณ์ ก็สามารถแยกโรคท็อกโซพลาสโมซิสออกได้เกือบทั้งหมด อย่างไรก็ตาม ในผู้ป่วยที่มีภูมิคุ้มกันบกพร่อง อาจมีการติดเชื้อที่ยังดำเนินอยู่แม้แอนติบอดีจะเป็นลบ3) ในผู้ป่วย CLL ที่มีภาวะแกมมาโกลบูลินในเลือดต่ำ ต้องระวังผลลบลวง3) .
ในกรณีติดเชื้อภายหลังเกิด การเพิ่มขึ้นของระดับแอนติบอดี IgM ในซีรัมแล้วลดลงในภายหลังมีค่าทางการวินิจฉัย นอกจากนี้ยังพบการเพิ่มขึ้นของระดับแอนติบอดี IgG แต่เนื่องจากการติดเชื้อแบบไม่แสดงอาการมีมาก ระดับที่สูงจึงไม่จำเป็นต้องหมายถึงจอประสาทตา อักเสบจากท็อกโซพลาสมาเสมอไป เมื่อมีการกลับเป็นซ้ำของการติดเชื้อแต่กำเนิด จะไม่พบการเพิ่มขึ้นของระดับ IgM
การตรวจ PCR จากน้ำในช่องหน้าหรือน้ำวุ้นตา มีประโยชน์ในกรณีที่ไม่ปกติหรือวินิจฉัยยาก
ความไว: ประมาณ 64% สำหรับ PCR จากน้ำในช่องหน้า1) , 27-75% สำหรับ PCR จากน้ำวุ้นตา 5)
ความจำเพาะ: 100%5)
ในผู้ป่วยที่มีภูมิคุ้มกันบกพร่อง ความไวเพิ่มขึ้นเป็น 75%3)
วิธีการคำนวณอัตราส่วนของระดับแอนติบอดีต่อท็อกโซพลาสมาต่อ IgG ในน้ำในลูกตา (Goldmann-Witmer coefficient: ค่า Q) ก็มีประโยชน์เช่นกัน โดยมีความไว 29-81% และความจำเพาะ 83-100%5) เมื่อใช้ร่วมกับวิธีอิมมูโนบล็อต ความไวจะสูงถึง 85-97% และความจำเพาะ 93%5) .
Shakha และคณะ (2024) รายงานชายอายุ 33 ปีที่มีจอประสาทตา อักเสบหลายจุดผิดปกติ ซึ่งตรวจพบ T. gondii โดย PCR จากน้ำในช่องหน้า นำไปสู่การวินิจฉัยที่แน่ชัด ผู้ป่วยแย่ลงหลังฉีดสเตียรอยด์ ใต้เยื่อหุ้ม Tenon ซึ่งแสดงให้เห็นอันตรายของการให้สเตียรอยด์ ชนิดออกฤทธิ์นานก่อนการวินิจฉัยที่แน่ชัด1) .
คณะทำงานด้านศัพท์บัญญัติมาตรฐานสำหรับม่านตาอักเสบ (SUN) ได้เผยแพร่เกณฑ์การจำแนกประเภทจอประสาทตา อักเสบจากท็อกโซพลาสมาในปี 2021 9) นอกเหนือจากจอประสาทตา อักเสบชนิดเนื้อตายแบบเฉพาะจุดหรือแบบน้อยจุดแล้ว ยังต้องมีผล PCR บวก หรือ IgM บวก หรือลักษณะทางคลินิกที่จำเพาะ (แผลเป็นมีเม็ดสี จอประสาทตา อักเสบรูปกลมถึงรี ดำเนินโรคแบบเฉียบพลันและเป็นซ้ำ) เกณฑ์เหล่านี้ซึ่งผสานผลทางคลินิกและผลตรวจทางห้องปฏิบัติการ มีประโยชน์ในการระบุผู้ป่วยในการศึกษาหลายศูนย์และการทดลองทางคลินิก
ติดเชื้อ : วัณโรค จอประสาทตา อักเสบจากไวรัส (CMV, HS V, VZV), โรคพยาธิตัวจี๊ด, ซิฟิลิส, บาร์โทเนลลา, เยื่อบุตาอักเสบ ภายในลูกตาไม่ติดเชื้อ : โรคเบห์เซ็ต, ซาร์คอยโดซิส , มะเร็งต่อมน้ำเหลืองในลูกตาการวินิจฉัยแยกโรคที่ควรระวังเป็นพิเศษ : จอประสาทตาอักเสบจาก CMV ในผู้ป่วยภูมิคุ้มกันบกพร่อง, จอประสาทตาตายเฉียบพลัน , มะเร็งต่อมน้ำเหลืองในลูกตา 3) 5)
Q
ผลตรวจเลือดบวกหมายถึงเป็นโรคท็อกโซพลาสมาที่ตาหรือไม่?
A
การมีแอนติบอดี IgG บวกบ่งชี้เพียงการติดเชื้อในอดีต และไม่ได้หมายความว่ามีรอยโรคที่ตาเสมอไป เนื่องจากการติดเชื้อแบบไม่แสดงอาการพบได้บ่อย การวินิจฉัยโรคท็อกโซพลาสมาที่ตาจึงต้องอาศัยการประเมินร่วมกับลักษณะทางคลินิกอย่างครอบคลุม แนวทางการรักษาม่านตาอักเสบ ยังระบุว่าการมีลักษณะทางคลินิกร่วมกับแอนติบอดีบวกสนับสนุนการวินิจฉัยโรคนี้อย่างมาก 8)
ไม่ใช่ทุกรอยโรคที่ต้องรักษา การอักเสบเล็กน้อยที่จำกัดอยู่ที่จอประสาทตา ส่วนปลายมีแนวโน้มหายได้เอง ข้อบ่งชี้ในการรักษามีดังนี้:
รอยโรคที่คุกคามจุดรับภาพ, รอยโรคที่หัวประสาทตาหรือมัดประสาทตาจุดรับภาพ
รอยโรคที่อยู่ติดกับหลอดเลือดจอประสาทตา หลัก
ความขุ่นของวุ้นตา อย่างรุนแรงการมองเห็น บกพร่องอย่างมีนัยสำคัญ, รอยโรคขนาดใหญ่ (≥ ครึ่งหนึ่งของเส้นผ่านศูนย์กลางหัวประสาทตา)ภาวะภูมิคุ้มกันบกพร่อง, การตั้งครรภ์, ภาวะตาข้างเดียว
อะเซทิลสไปรามัยซิน (0.8–1.2 กรัม/วัน แบ่งให้ 3–4 ครั้ง) ให้อย่างน้อย 30 วัน อาจให้ต่อเนื่อง 2–3 เดือนจนกว่าการอักเสบที่ยังดำเนินอยู่จะหายไป หยุดการรักษาเมื่อรอยโรคแบบมีสารคัดหลั่งเกิดแผลเป็นและระดับแอนติบอดีต่อทอกโซพลาสมาลดลง
หากมีการอักเสบของวุ้นตา อย่างรุนแรง ให้ใช้สเตียรอยด์ ชนิดรับประทานร่วมด้วย (เพรดนิโซน 20–30 มก./วัน เป็นขนาดเริ่มต้น) แต่ควรเริ่มหลังจากให้ยาปฏิชีวนะไปแล้วสองสามวัน 8) การใช้สเตียรอยด์ ชนิดรับประทาน 0.5 มก./กก./วัน ช่วยให้อาการทางตาดีขึ้นเร็วขึ้น รอยโรคที่ขั้วหลังหรือรอยโรคที่กลับเป็นซ้ำซึ่งมีเส้นผ่านศูนย์กลางมากกว่าครึ่งหนึ่งของเส้นผ่านศูนย์กลางจานประสาทตา จำเป็นต้องใช้ยาต้านทอกโซพลาสมาร่วมกับสเตียรอยด์
นอกจากนี้ยังมีวิธีใช้คลินดามัยซิน 1.2 กรัม แบ่งให้ 4 ครั้ง รับประทานนาน 4–6 สัปดาห์เป็นหนึ่งคอร์ส
การให้ไพริเมธามีน + ซัลฟาไดอะซีน + สเตียรอยด์ ร่วมกันเป็นการรักษาแบบคลาสสิก และ 32% ของผู้ตอบแบบสำรวจของสมาคมยูเวียอักเสบแห่งสหรัฐอเมริกาเลือกเป็นอันดับแรก เนื่องจากไพริเมธามีนเป็นยาต้านโฟเลต จึงให้โฟลิเนต (ลิวโคโวริน) ร่วมด้วยเพื่อป้องกันการกดไขกระดูก โดยปกติให้เป็นเวลา 4–6 สัปดาห์
TMP-SMX (160/800 มก.) วันละสองครั้งเป็นทางเลือกที่ปลอดภัยและมีประสิทธิภาพแทนไพริเมธามีน + ซัลฟาไดอะซีน 7) มีข้อดีคือผลข้างเคียงน้อยและหาง่าย
Kohler และคณะ (2023) รักษาผู้ป่วยติดเชื้อปฐมภูมิ 4 รายทั้งหมดด้วย TMP-SMZ เพียงอย่างเดียว และได้ผลลัพธ์คือรอยโรคจอประสาทตา ดีขึ้นอย่างรวดเร็ว อย่างไรก็ตาม จำเป็นต้องให้ยาต่อเนื่องอย่างน้อย 3 เดือนเพื่อป้องกันการกลับเป็นซ้ำของอาการทางระบบ 4)
การฉีดคลินดามัยซิน 1 มก. + เด็กซาเมทาโซน 0.4 มก. เข้าแก้วตาแสดงประสิทธิภาพเทียบเท่าการให้ยาทางระบบ โดยมีอัตราการกลับเป็นซ้ำที่ 2 ปี 6–15% เท่ากัน 5) ใช้ในผู้ป่วยที่มีข้อห้ามในการให้ยาทางระบบ 7) แทบไม่มีผลข้างเคียง และระยะเวลาที่รอยโรคหายไปประมาณ 2.5 ± 1 สัปดาห์ 5)
อะซิโธรมัยซิน 500 มก. ครั้งแรก จากนั้น 250 มก./วัน แสดงประสิทธิภาพเทียบเท่า TMP-SMX 5) เมื่อใช้ร่วมกับไพริเมธามีน สามารถใช้แทนซัลฟาไดอะซีนได้ และความถี่ของผลข้างเคียงต่ำ 7)
Syed Mohd Khomsah และคณะ (2023) รักษาหญิงอายุ 35 ปีที่เป็นโรคทอกโซพลาสมาที่ตาทั้งสองข้างด้วยอะซิโธรมัยซิน 500 มก./วัน และเพรดนิโซโลนแบบลดขนาดลงเป็นเวลา 6 สัปดาห์ ภาวะวุ้นตา อักเสบและจานประสาทตา บวมหายไปใน 4 สัปดาห์ แต่การมองเห็น ตาขวาไม่ดีเนื่องจากพังผืดของมัดประสาทตาจุดรับภาพและเยื่อเหนือจอประสาทตา 6)
อะโทวาควอน 750 มก. วันละ 4 ครั้ง ใช้ในกรณีที่ผู้ป่วยไม่สามารถทนต่อยาทางเลือกแรกได้ 5) การตอบสนองจะเกิดขึ้นภายใน 1–3 สัปดาห์หลังจากเริ่มการรักษา และผลข้างเคียงที่รุนแรงพบได้น้อย
การศึกษาแบบสุ่มที่มีกลุ่มควบคุมแสดงให้เห็นว่าการให้ TMP-SMX (160/800 มก.) สัปดาห์ละ 3 ครั้งในระยะยาวช่วยลดอัตราการกลับเป็นซ้ำจาก 23.8% เหลือ 6.6% 7) ในการศึกษาแบบสุ่มอีกชิ้นหนึ่ง การให้ยา 1 เม็ดวันเว้นวันเป็นเวลา 311 วัน ส่งผลให้อัตราการกลับเป็นซ้ำที่ 6 ปีเท่ากับ 1.4% (กลุ่มยาหลอก 27.5%) 5)
การติดเชื้อทอกโซพลาสมาโดยตัวมันเองไม่มีข้อบ่งชี้ในการผ่าตัด แต่การผ่าตัดน้ำวุ้นตา จะทำในกรณีจอประสาทตาลอก เยื่อเหนือจอประสาทตา (ERM ) และเลือดออกในน้ำวุ้นตา ที่เกิดเป็นภาวะแทรกซ้อน 5)
ในรายงานของ Kohler และคณะ (2023) เกิดภาวะแทรกซ้อนใน 2 ใน 4 รายของการติดเชื้อครั้งแรก: ERM ร่วมกับจอประสาทตา บวมน้ำชนิดถุงน้ำ และการดึงรั้งของน้ำวุ้นตา จากเส้นเลือดใหม่ที่ฝ่อ 4) ในราย ERM การมองเห็น ดีขึ้นหลังผ่าตัดน้ำวุ้นตา และลอกเยื่อ
ยาต้านทอกโซพลาสมาทั้งหมดมีประสิทธิภาพเฉพาะต่อรูปแบบที่กำลังเจริญเติบโต (tachyzoite) และไม่มีผลต่อซีสต์ในเนื้อเยื่อ (bradyzoite) ดังนั้นจึงรักษาให้หายขาดได้ยาก และยังคงมีความเสี่ยงต่อการกลับเป็นซ้ำ
การใช้สเตียรอยด์ ชนิดสะสม (การฉีด triamcinolone ใต้เยื่อหุ้ม Tenon หรือการฝัง dexamethasone ในน้ำวุ้นตา ) ก่อนการวินิจฉัยที่แน่ชัดอาจทำให้โรครุนแรงขึ้น 1) 5) ควรหลีกเลี่ยงการใช้สเตียรอยด์ เดี่ยวโดยไม่มียาต้านปรสิต
Pyrimethamine อาจทำให้เกิดการกดไขกระดูก (เม็ดเลือดขาวต่ำ เกล็ดเลือดต่ำ) ดังนั้นจึงจำเป็นต้องตรวจเลือดเป็นประจำและให้กรดโฟลินิกร่วมด้วย
หลังการรักษา ทอกโซพลาสมายังคงอยู่ในรูปซีสต์ที่ดื้อยาภายในรอยโรคที่เป็นแผลเป็น และเกิดการกลับเป็นซ้ำซ้ำในประมาณ 5–30% ของผู้ป่วย
Q
จำเป็นต้องรักษาทุกครั้งที่กลับเป็นซ้ำหรือไม่?
A
รอยโรคขนาดเล็กที่จำกัดอยู่บริเวณจอประสาทตา ส่วนปลายอาจหายได้เอง อย่างไรก็ตาม เนื่องจากจำนวนซีสต์ในจอประสาทตา เพิ่มขึ้นทุกครั้งที่กลับเป็นซ้ำ จึงมีความคิดว่าควรรักษาทุกครั้งที่กลับเป็นซ้ำด้วยยาปฏิชีวนะเพื่อลดความเสี่ยงในการกลับเป็นซ้ำในอนาคต รอยโรคที่ขั้วหลังหรือที่มีการมองเห็น ลดลงจำเป็นต้องได้รับการรักษา
T. gondii ติดเชื้อที่จอประสาทตา เป็นตำแหน่งหลัก และแพร่กระจายไปยังคอรอยด์ น้ำวุ้นตา และช่องหน้าม่านตา 7) รอยโรคที่คอรอยด์ เกิดขึ้นเป็นลำดับรองจากการติดเชื้อที่จอประสาทตา และไม่ปรากฏเพียงลำพัง
โอโอซิสต์หรือซีสต์เนื้อเยื่อที่รับประทานเข้าไปจะเปลี่ยนเป็นรูปแบบโทรโฟซอยต์ (ทาคิซอยต์) ในลำไส้ แล้วแพร่กระจายไปทั่วร่างกายทางกระแสเลือด เส้นทางไปถึงจอประสาทตา รวมถึงเส้นทางที่เม็ดเลือดขาวนำพาปรสิต และเส้นทางที่ทาคิซอยต์ผ่านเซลล์บุผนังหลอดเลือดโดยตรง6)
ทาคิซอยต์ติดเชื้อในเซลล์ต่างๆ ภายในจอประสาทตา แต่เซลล์โฮสต์ที่ไวต่อการติดเชื้อมากที่สุดคือเซลล์เกลียของมุลเลอร์6) เมื่อเซลล์เยื่อบุผิวรงควัตถุจอประสาทตา (RPE ) ติดเชื้อ จะเกิดความผิดปกติในการผลิตปัจจัยการเจริญเติบโต ซึ่งกระตุ้นการเพิ่มจำนวนของเซลล์ RPE ข้างเคียงที่ไม่ติดเชื้อ กลไกนี้เชื่อว่ามีส่วนเกี่ยวข้องกับการเกิดแผลเป็นที่มีเม็ดสีลักษณะเฉพาะ
ในจอประสาทตา อักเสบแบบเนื้อตาย จะเกิดหลอดเลือดอักเสบและการทำลายจอประสาทตา ที่ดำเนินไป ทางจุลกายวิภาคศาสตร์พบการแทรกซึมของเซลล์อักเสบชนิดแกรนูโลมาอย่างกว้างขวางร่วมกับเนื้อตายของเยื่อบรูค 7) การเกิดแผลเป็นดำเนินไปจากขอบเข้าสู่ศูนย์กลาง และระดับของเม็ดสีแตกต่างกันไปในแต่ละกรณี
แม้จะมีการติดเชื้อผ่านรก แต่การแสดงอาการพบได้น้อย และส่วนใหญ่ยังคงเป็นการติดเชื้อที่ไม่แสดงอาการ อาการหลักของทอกโซพลาสโมซิสแต่กำเนิดคือสี่ประการ: จอประสาทตา คอรอยด์ อักเสบ, ภาวะน้ำคั่งในโพรงสมอง (หรือศีรษะเล็ก), การกลายเป็นปูนในกะโหลกศีรษะ, และความผิดปกติด้านจิตใจและการเคลื่อนไหว ประมาณ 70% ของทารกที่ติดเชื้อในครรภ์มีรอยโรคแผลเป็นที่คอรอยด์ (บริเวณศูนย์กลางของจุดรับภาพ) และ 1-2% ในจำนวนนี้มีความบกพร่องทางการมองเห็น อย่างรุนแรง การกลับเป็นซ้ำมักเกิดขึ้นในช่วงวัยรุ่น และเกิดขึ้นประมาณหนึ่งในสามของรอยโรคแผลเป็น
ในการประเมินผู้ป่วยทอกโซพลาสโมซิสแต่กำเนิดที่ได้รับการรักษา 430 ราย พบรอยโรคทางตาใน 30% ในระหว่างการติดตามผลเฉลี่ย 12 ปี7) อย่างไรก็ตาม ความบกพร่องทางการมองเห็น สองตาอย่างรุนแรงเกิดขึ้นเพียง 2 ใน 130 ราย และการพยากรณ์โรคด้านการทำงานโดยรวมดีกว่าที่คาดการณ์ไว้ในเอกสาร7)
สาเหตุของการกลับเป็นซ้ำยังไม่เป็นที่เข้าใจอย่างสมบูรณ์ แต่สันนิษฐานว่าเกิดจากการแตกของซีสต์ที่อยู่เฉยๆ ในจอประสาทตา 7) หรือการมีส่วนร่วมของทอกโซพลาสมาที่ไหลเวียนในเลือดส่วนปลาย หลังการรักษา ซีสต์ที่ดื้อยายังคงมีอยู่ในรอยโรคแผลเป็นฝ่อ และการกลับเป็นซ้ำอาจเกิดขึ้นได้จากภูมิคุ้มกันลดลงหรือการตั้งครรภ์ ความเสี่ยงในการกลับเป็นซ้ำสูงที่สุดภายในปีแรกหลังจากครั้งแรก อัตราการกลับเป็นซ้ำในการติดเชื้อแต่กำเนิดรายงานว่าประมาณ 5-30%
Pidro Miokovic และคณะ (2024) รายงานการเปลี่ยนแปลงคล้ายถุงน้ำขนาดใหญ่ในจอประสาทตา ชั้นนอก (HORC) ในหญิงอายุ 16 ปีที่เป็นโรคทอกโซพลาสโมซิสทางตา2) HORC เป็นลักษณะที่พบได้ยาก โดยพบเพียง 2.5% ของผู้ป่วยทอกโซพลาสโมซิสทางตาทั้งหมด และอยู่ระหว่างเยื่อจำกัดชั้นนอกกับขอบด้านในของ RPE สองสัปดาห์หลังการรักษา HORC หายไป และการมองเห็น ดีขึ้นจาก 0.5 เป็น 1.0
ในผู้ป่วยภูมิคุ้มกันบกพร่อง มักมีอาการทางคลินิกที่ไม่ปกติ ทำให้การวินิจฉัยล่าช้า เนื่องจากการตรวจทางซีรัมวิทยาแบบดั้งเดิมอาจให้ผลลบเท็จ บทบาทของการตรวจ PCR จึงมีความสำคัญยิ่งขึ้น
Yazdanpanah และคณะ (2021) รายงานกรณีผู้หญิงอายุ 74 ปีที่เป็น CLL และมีท็อกโซพลาสโมซิสที่ตาซึ่งแยกได้ยากจากมะเร็งต่อมน้ำเหลืองในลูกตา 3) การตรวจโฟลว์ไซโตเมทรีและเซลล์วิทยาของน้ำวุ้นตา ปฏิเสธมะเร็งต่อมน้ำเหลือง และ PCR ด้วยไพรเมอร์จำเพาะ ITS ตรวจพบ DNA ของ T. gondii มากกว่า 5 ล้านสำเนา นอกจากนี้ยังมีรายงานการตรวจพบ DNA ของท็อกโซพลาสมาจากเซลล์มะเร็งต่อมน้ำเหลืองในลูกตา ซึ่งบ่งชี้ถึงความสัมพันธ์ระหว่างทั้งสอง 3)
Dillon และคณะ (2022) รายงานสองกรณีที่มีรอยโรคจอประสาทตา หลายจุดกว้างขวาง 5) กรณีแรกได้รับการวินิจฉัยทางคลินิกว่าเป็นจอประสาทตาตายเฉียบพลัน และรักษาในโรงพยาบาล แต่ PCR ของน้ำวุ้นตา ให้ผลบวกต่อท็อกโซพลาสมา กรณีที่สองได้รับการตัดชิ้นเนื้อคอรอยด์ และจอประสาทตา เพื่อแยกจากมะเร็งต่อมน้ำเหลืองในลูกตา และการย้อมอิมมูโนยืนยันพบ tachyzoite จำนวนมาก ทั้งสองกรณีมีรอยโรคขนาดใหญ่และหลายจุดที่มีเส้นผ่านศูนย์กลางมากกว่า 3 เท่าของเส้นผ่านศูนย์กลางหัวประสาทตา ซึ่งแตกต่างอย่างมากจากรอยโรคเดี่ยวทั่วไปที่มีขนาด 1-2 เท่าของเส้นผ่านศูนย์กลางหัวประสาทตา
ในรัฐมินนิโซตา สหรัฐอเมริกา อัตราความชุกของซีรัมบวกต่อ T. gondii ในกวางหางขาวสูงถึง 22.5-32.2% และสูงกว่าในรัฐใกล้เคียง 4) มีรายงานรูปแบบการเกิดอาการทางตาในฤดูหนาวหลังจากบริโภคเนื้อกวางที่ปรุงไม่สุกในช่วงฤดูล่าสัตว์ (ฤดูใบไม้ร่วง) 4) แนะนำให้ปรุงเนื้อกวางจนอุณหภูมิภายใน ≥64°C หรือเก็บในที่เย็นก่อนเพื่อความปลอดภัย
Shakha, Chawla R, Sinha A, Meena S. Atypical acquired toxoplasmosis. Indian J Ophthalmol. 2024;72:772-774.
Pidro Miokovic A, Ratkovic M, Pidro Gadzo A. Toxoplasmosis in the outer retina. Rom J Ophthalmol. 2024;68(2):198-201.
Yazdanpanah O, Monday LM, Surapaneni S, Singh V, Chi J. Ocular toxoplasmosis mimicking lymphoma: exploring the correlation and distinction. Cureus. 2021;13(1):e13014.
Kohler JM, Mammo DA, Bennett SR, Davies JB. Primary ocular toxoplasmosis secondary to venison consumption. Am J Ophthalmol Case Rep. 2023;29:101776.
Dillon AB, Budoff G, McCannel CA, Tsui E, Pullarkat ST, Schwartz SD. Ocular toxoplasmosis: no stranger to the masquerade ball. J Vitreoret Dis. 2022;6(5):391-398.
Syed Mohd Khomsah SN, Muhammed J, Wan Hitam WH. Macular pucker: a devastating complication in ocular toxoplasmosis. Cureus. 2023;15(2):e34617.
Commodaro AG, Belfort RN, Rizzo LV, Muccioli C, Silveira C, Burnier MN Jr, Belfort R Jr. Ocular toxoplasmosis: an update and review of the literature. Mem Inst Oswaldo Cruz. 2009;104(2):345-350.
日本眼炎症学会ぶどう膜炎診療ガイドライン作成委員会. ぶどう膜炎診療ガイドライン. 日眼会誌. 2019;123(6):635-696(眼トキソプラズマ症の項).
Jabs DA, Belfort R Jr, Bodaghi B, et al. Classification Criteria for Toxoplasmic Retinitis. Am J Ophthalmol. 2021;228:134-141.