前部PVR
玻璃体基底部的收缩:前部视网膜和睫状体被向前牵引。
漏斗状视网膜脱离:严重病例呈前后狭窄的漏斗状脱离形态。
牵引力强:膜附着于玻璃体基底部,使剥离难以治疗。

增殖性玻璃体视网膜病变(Proliferative Vitreoretinopathy; PVR)是由孔源性视网膜脱离(RRD)手术或RD本身引发的异常伤口愈合反应。视网膜色素上皮(RPE)细胞、胶质细胞和肌成纤维细胞增殖,在视网膜前、视网膜后和玻璃体基底部形成纤维收缩膜。这些膜的收缩牵拉视网膜,产生固定皱襞,导致视网膜再次脱离。
PVR是RD手术失败的主要原因。75%的RD手术失败归因于PVR,3) 总体RD中PVR的发生率为5%~10%。3) 常在RD术后30~60天发病。1)
1983年视网膜学会提出了PVR的统一分类,之后1991年发表了Silverstone分类等修订版。PVR是孔源性视网膜脱离最重要的预后决定因素,早期发现和适当干预直接影响视力预后。
慢性孔源性视网膜脱离、下方孔源性视网膜脱离、眼内炎、葡萄膜炎、急性视网膜坏死(ARN)5) 等是主要风险因素。详情请参阅“原因与风险因素”一节。
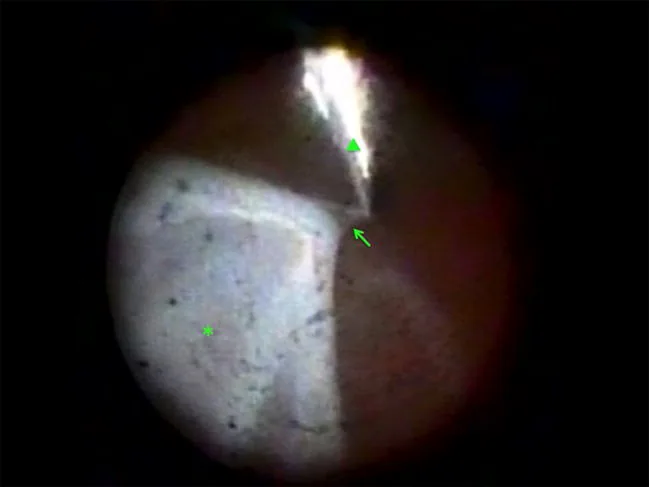
PVR的自觉症状常与基础疾病视网膜脱离的症状重叠。
黄斑部PVR(mPVR)在PPV后10至28天相对早期发生。2) 报告病例中,术后BCVA从20/38降至20/166。2)
PVR最具特征性的所见是固定皱襞(星形皱襞)。增殖膜收缩使视网膜折叠,形成即使在玻璃体手术时也无法展开的所谓“固定”皱襞。
前部PVR
玻璃体基底部的收缩:前部视网膜和睫状体被向前牵引。
漏斗状视网膜脱离:严重病例呈前后狭窄的漏斗状脱离形态。
牵引力强:膜附着于玻璃体基底部,使剥离难以治疗。
后部PVR
黄斑部PVR(mPVR)在OCT检查中显示特征性表现。据报道,中心凹视网膜厚度(CMT)从711μm显著增厚至354μm,2) 与通常的黄斑前膜(ERM)的鉴别很重要。ERM形成表面光滑的膜,而mPVR可见指状突起样结构。2)
超声检查可见V字形(后部PVR)或T字形(重度漏斗状脱离)的特征性表现。
PVR的根本原因是血-视网膜屏障(BRB)的破坏。BRB破坏后,血清中的生长因子(TGF-β、PDGF、IL-6等)进入玻璃体腔和视网膜下腔,诱导RPE细胞和神经胶质细胞的增殖和迁移。RPE细胞经上皮-间充质转化(EMT)分化为肌成纤维细胞,3) 产生收缩性的细胞外基质(ECM)。
已报道以下风险因素。
| 风险因素 | 分类 |
|---|---|
| 慢性/大型孔源性视网膜脱离 | 解剖学因素 |
| 下方裂孔性视网膜脱离 | 解剖学因素 |
| 裂孔大或多发 | 解剖学因素 |
| 眼内炎、葡萄膜炎 | 炎症性因素 |
| 急性视网膜坏死(ARN) | 炎症性因素 |
| 糖尿病视网膜病变 | 全身性因素 |
| 肾功能障碍 | 全身性因素 |
| 吸烟 | 生活习惯因素 |
ARN(急性视网膜坏死)会导致血-视网膜屏障(BRB)的大规模破坏,并引起严重的PVR。ARN后裂孔性视网膜脱离的发生率超过50%。5) 此外,糖尿病患者牵引性视网膜脱离(TRD)术后可能出现持续性视网膜下液(SRF),肾功能障碍是其持续存在的危险因素。4)
PVR的诊断主要通过裂隙灯显微镜(联合前房角镜)和间接检眼镜进行眼底检查。确认固定皱襞是诊断的关键。在玻璃体手术中无法展平的固定视网膜皱襞是PVR的确切表现。
PVR的严重程度分级广泛采用视网膜学会(1983年)的以下分类。
| 分级 | 表现 |
|---|---|
| A | 玻璃体混浊、RPE变性、内界膜皱褶(仅少量) |
| B | 视网膜内面皱褶、视网膜裂孔边缘卷曲、僵硬 |
| C | 固定皱襞(1/4圆周计为1CP) |
| D | 漏斗状视网膜脱离(宽口型、窄口型、闭合型) |
在C级中,皱襞的范围通过其占据的时钟方位(CP)来量化,例如“C3”表示固定皱襞占据3个时钟方位。
通常在RD术后30至60天的定期随访中发现。1) 术前应识别慢性或下方孔源性视网膜脱离等风险因素,术后需密切观察固定皱襞的形成。在mPVR中,OCT上检测到指状突起有助于早期诊断。2)
PVR的标准治疗是玻璃体切除术(PPV:经睫状体扁平部玻璃体切除术),包括增殖膜剥离和视网膜复位。主要手术要素如下:
对于黄斑部PVR(mPVR),有报道称膜剥离后最佳矫正视力从20/166改善至20/57,2) 建议积极手术干预。
关于术后持续性视网膜下液(SRF),糖尿病TRD术后报告显示术后1个月75%、3个月50%、6个月30%、12个月10%残留。平均持续时间为4.4±4.7个月。4)
目前尚未建立标准的药物治疗,但已有几种方法被报道。
| 药物 | 给药方式 | 证据级别 |
|---|---|---|
| MTX(甲氨蝶呤) | 玻璃体内注射200–400 μg | 临床试验中(研究阶段) |
| 硅油 | 玻璃体腔填充 | 标准辅助治疗 |
| 类固醇 | - | 非PVR治疗靶点 3) |
甲氨蝶呤(MTX)是最有希望的候选药物,但详情请参阅“最新研究与未来展望”一节。类固醇不被认为是PVR的治疗靶点。3)
PVR的核心发病机制是RPE细胞的上皮-间充质转化(EMT)。3) 因RD脱离的RPE细胞释放到玻璃体腔,在生长因子的刺激下发生以下变化。
PVR膜的主要组成细胞如下。2, 3)
BRB破坏导致以下因子进入玻璃体腔,诱导增殖。
前部PVR发生在玻璃体基底部(睫状体平坦部至周边视网膜)。该区域的膜将睫状体、前部视网膜和玻璃体基底部整体向前牵引,导致眼球低眼压、漏斗状脱离和完全失明等严重病变。解剖上手术难度高,硅油填充尤为重要。
ARN(急性视网膜坏死)后的PVR尤其严重。5) ARN病毒(VZV/HSV)引起的大规模BRB破坏导致血清蛋白和炎症细胞因子大量进入玻璃体腔。这提供了强烈的增殖刺激,使得孔源性视网膜脱离的发生率超过50%,且发生的PVR往往严重。5)
MTX是一种抑制二氢叶酸还原酶的抗叶酸药物,具有抗增殖和抗炎作用。通过玻璃体内局部给药预防或治疗PVR的研究正在全球范围内进行。
GUARD试验(3期RCT):术中及术后给予MTX可显著降低再脱离率,提供了最可靠的证据。1)
Ambati等人(2024)报告了对先天性无虹膜症背景下的PVR病例,采用MTX 200μg每2周一次共5次,随后每月一次维持治疗。GUARD试验(3期RCT)显示术中及术后MTX可显著降低再脱离率。1)
Babel等人(2022)报告了一例伴有PVR的复发性视网膜脱离,使用硅油1000cSt联合单次MTX 400μg/0.10mL治疗。3) MTX在玻璃体内的半衰期为3-5天,其通过抑制IL-6抑制PVR的机制已被提出。
FIXER试验(NCT06541574):一项评估MTX预防PVR效果的新3期RCT正在进行中。1) 该试验的结果可能决定MTX是否被纳入标准治疗。
局限于黄斑部的PVR(mPVR)近年来作为PPV后10-28天早期发生的独立病因而受到关注。2) OCT上指状突起的识别是诊断的关键,早期膜剥离可改善视力。2)
Khateb等人(2021)报告了一例PPV后最佳矫正视力从20/38降至20/166的病例,行膜剥离后术后视力改善至20/57。2) CMT从711μm恢复正常至354μm,提示mPVR应被视为独立的临床实体。
目前,它仍处于研究或临床试验阶段,并未纳入日本的标准治疗。GUARD试验和FIXER试验等临床试验正在验证其有效性,1) 可能影响未来的指南修订。希望接受治疗的患者应咨询主治医生。