第1期
潜伏期:10〜90日。
下疳:接種部位に無痛性硬結。約4週間で消失。結膜や眼周囲に生じることもある。

梅毒トレポネーマ(Treponema pallidum)が血行性に眼部に侵入し、眼内炎症を引き起こす病態が梅毒性ぶどう膜炎である。梅毒はスピロヘータの一種である Treponema pallidum による性感染症で、症状のある顕性梅毒は第1期から第4期まで区分される。近年、第3・4期の梅毒に遭遇することはまれで、大半が皮膚や粘膜に病変を認めない潜伏梅毒である。後天梅毒でぶどう膜炎が発症するのは第2期のおよそ5%とされる。先天性梅毒による眼病変は周産期医療の充実から国内では新鮮例をほとんど認めない。
世界全体で年間570〜600万件の新規梅毒感染が15〜49歳で報告される1)5)。眼梅毒の頻度は梅毒全症例の約0.6〜2%とされ1)2)、感染性ぶどう膜炎全体の約10%を占める3)。North Carolinaの研究では4,232例中63例(1.5%)に眼梅毒が認められ、そのうち38%が第1期・第2期の時点で診断された1)。
国内でも感染例が再び増加しており、2011年には1,000件未満であった報告数が2017年には6,000件を超えるまでに至っている。近年はMSM(男性と性交渉を持つ男性)やHIV共感染を含む患者を中心に増加傾向にある。臨床像が多彩なため「偉大なる模倣者(the great imitator)」と呼ばれる1)5)。治療上は神経梅毒に準じて扱う。
眼梅毒は第1期から第3期、潜伏期を含むあらゆる病期で発症しうる。後天梅毒第2期での発症が最も多く、ぶどう膜炎が主体となる。眼症状が梅毒診断の最初のきっかけとなるケースもあるため、原因不明のぶどう膜炎では常に梅毒を考慮する必要がある。
梅毒の眼病変は前眼部炎症・ぶどう膜炎・視神経炎・脈絡網膜炎など多岐にわたり、他の多くの眼疾患と酷似する所見を呈する。そのため診断が遅れやすく、この多彩な臨床像が「偉大なる模倣者」と称される理由である5)。
経胎盤感染で発症する。早期先天梅毒(出生〜生後3か月)では網脈絡膜炎を呈する。遅発性先天梅毒では典型的なHutchinson三徴候(永久歯のM型欠損、内耳性難聴、角膜実質炎)が特徴的である。陳旧性先天梅毒の眼底には網膜色素細胞の増殖を伴うsalt-and-pepper眼底(散在性の脈絡網膜萎縮像)がみられ、時に網膜色素変性症様の眼底を呈する。
HIV共感染は眼梅毒の重要なリスク要因であり、梅毒診断時にはHIV検査が全例に推奨される1)。HIV陽性ではぶどう膜炎の重症度が増し、両眼性になりやすいなど臨床像が変化する。また、AIDSでは血清学的検査が偽陰性となる場合がある点にも注意が必要である。
第1期
潜伏期:10〜90日。
下疳:接種部位に無痛性硬結。約4週間で消失。結膜や眼周囲に生じることもある。
第2期
出現時期:下疳出現後4〜10週。
全身播種:血行性に神経・眼・消化器・肝臓を侵す。眼は約10%で関与する。手掌・足底の斑状丘疹状発疹が70%以上に認められる。
眼所見:ぶどう膜炎・網膜炎・視神経炎が主体。
潜伏期
分類:早期(1年以内)と後期(1年以降)。
経過:未治療の約1/3が第3期へ進行する。無症状でも眼梅毒が顕在化することがある。
第3期
心血管系:大動脈炎、大動脈瘤。
神経梅毒:髄膜梅毒、髄膜血管梅毒、脊髄癆、進行性麻痺。
眼所見:アーガイル・ロバートソン瞳孔、視神経萎縮、ゴム腫。
ゴム腫:良性局所肉芽腫反応。脈絡膜・虹彩を含む全身に発生。
梅毒の病期によって眼所見は大きく異なる。
| 分類 | 発症時期 | 主な眼症状 |
|---|---|---|
| 先天梅毒(早期) | 出生時〜生後3か月 | 網脈絡膜炎 |
| 先天梅毒(晩期) | 学童期以降 | 角膜実質炎、虹彩炎、涙囊炎 |
| 後天・第1期 | 3週〜3か月 | 眼瞼・結膜の下疳 |
| 後天・第2期 | 4〜10週 | 眼瞼炎、結膜炎、角膜炎、虹彩毛様体炎、虹彩結節、強膜炎、網脈絡膜炎、硝子体炎、視神経炎、網膜血管炎、滲出性網膜剥離 |
| 後天・晩期 | 数年〜数十年 | 眼瞼ゴム腫、角膜実質炎、強膜炎、ぶどう膜炎、視神経乳頭炎、Argyll Robertson瞳孔、水晶体偏位、二次性網膜色素変性症 |
| 病型 | 頻度 |
|---|---|
| 汎ぶどう膜炎 | 75%3) |
| 脈絡網膜炎 | 93%4) |
| 肉芽腫性虹彩毛様体炎 | 46%1) |
| 前房蓄膿 | 6%2) |
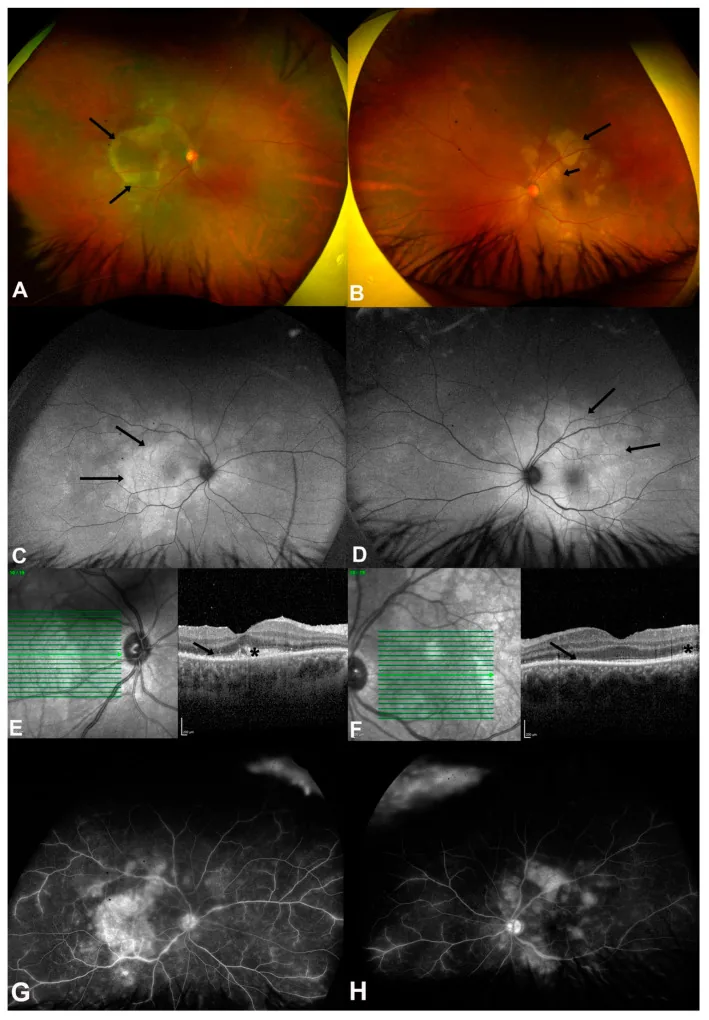
眼梅毒の所見は侵される部位によって多彩な形態をとる。病型は汎ぶどう膜炎が最多(75%)であり3)、後眼部病変として脈絡網膜炎が93%に認められる4)。
前眼部所見
ぶどう膜・後眼部
中間部・後部・汎ぶどう膜炎:前部・後部・汎ぶどう膜炎のいずれもとりうる。肉芽腫性または非肉芽腫性。
ASPPC(急性梅毒性後部類円板状脈絡網膜炎):第2期梅毒患者に特徴的な特殊型。黄斑部〜乳頭近傍のRPEレベルに類円板状・黄色の病変。OCTで外層網膜・RPE部の断裂と過反射性隆起を認める3)。FAFで過蛍光・低蛍光パッチ。抗生物質治療に良好に反応する。
網膜血管炎・網膜炎:動脈炎が特徴的とされるが、静脈炎も多くみられ白線化に至ることがある9)。無灌流領域→増殖性変化を形成しうる。「すりガラス様網膜浸潤」および「クリーム色の小さな網膜表面沈着物」が特徴的所見1)5)。
強い硝子体混濁:ペニシリン系抗菌薬投与後数日で急激に消退することも多い。
視神経・神経眼科
視神経炎:片眼性または両眼性。前部・球後視神経炎、乳頭浮腫、神経網膜炎、視神経萎縮。眼梅毒の12〜78%に視神経関与が認められる3)。治療が遅れると視神経萎縮となり視力予後に影響する。
アーガイル・ロバートソン瞳孔:縮瞳・対光反射消失だが近接視反応は保たれる。第3期に多いが早期にも出現しうる5)。
ASPPC(Acute Syphilitic Posterior Placoid Chorioretinitis)は梅毒に特異性の高い後眼部所見で、後極部に大型の胎盤状(プラコイド)の黄白色病変が形成される5)。蛍光眼底造影では特徴的な早期低蛍光・後期過蛍光を呈する。OCTでは外層網膜・RPE部の断裂と過反射性隆起を認め、抗菌薬治療に良好に反応する。
原因不明のぶどう膜炎では常に梅毒を考慮し、高い疑いの指数(index of suspicion)を持つことが重要である。ぶどう膜炎の原因精査を進めるうえで、梅毒の血清学的検査を必ず行う。
診療では非トレポネーマ検査と特異的トレポネーマ検査を組み合わせる。
| 検査の種類 | 代表的検査 | 特徴・用途 |
|---|---|---|
| 非トレポネーマ検査(STS) | RPR(rapid plasma reagin)、VDRL | 感度高く早期に陽性。生物学的偽陽性あり。感染活動性と並行→スクリーニング・治療効果判定に使用 |
| トレポネーマ検査(TP抗原法) | TPHA、FTA-ABS、TP-PA、EIA | 陽性で梅毒確定。治療後も長期陽性持続→治療判定には不適 |
硝子体液中のEIAによる梅毒抗体検出は感度90.9%・特異度100%と高い精度を示す4)。血清検査が偽陰性となりうるHIV合併例でも診断に有用である。
| 検査 | 感度 | 特異度 |
|---|---|---|
| 血清EIA | 高感度(スクリーニング) | 高特異度 |
| 硝子体EIA | 90.9%4) | 100%4) |
眼梅毒では神経梅毒合併の評価のためCSF検査が推奨される4)。孤立性の眼症状・確認された眼異常・トレポネーマ検査陽性が揃う場合は、治療前のCSF検査は必須ではないとされる3)。視神経炎・眼筋麻痺・脳神経症状が疑われる場合は腰椎穿刺を行う。
血清梅毒検査が偽陰性になりやすいHIV合併例や、血清検査陰性にもかかわらず梅毒性ぶどう膜炎が強く疑われる症例に有用である4)。硝子体EIAは特異度100%であり、陽性であれば梅毒性ぶどう膜炎の診断的根拠となる。
サルコイドーシス、結核性ぶどう膜炎、急性網膜壊死(ARN)/PORN、APMPPE、蛇行状脈絡膜炎、サイトメガロウイルス網膜炎、トキソプラズマ網膜炎、ベーチェット病、眼内リンパ腫などとの鑑別が必要である4)7)。眼梅毒は眼領域での T. pallidum の直接検出が不可能であるため、血清学的検査と臨床所見の統合判断が重要となる10)。HIV陽性患者では特に注意を要し、AIDSでは血清学的検査が偽陰性となる場合がある。
経口駆梅療法(軽症例・外来管理の場合):
神経梅毒・眼梅毒(入院・静注療法):
梅毒性ぶどう膜炎は神経梅毒合併例が多く、高用量ペニシリン静注療法が標準である。第一選択は水性ペニシリンGの静脈内投与である。
| レジメン | 投与量・方法 |
|---|---|
| 水性結晶ペニシリンG(第一選択) | 1,800〜2,400万単位/日(300〜400万単位を4時間ごとIVまたは持続点滴)× 10〜14日間1)2)3)5) |
| プロカインペニシリンG(代替) | 240万単位 筋注1日1回 + プロベネシド 500 mg 1日4回経口 × 10〜14日間1)2) |
| セフトリアキソン(代替) | 1〜2 g 筋注または静注 1日1回 × 14日間1)4)6) |
治療成功率は約90%と報告されている3)。
Nwaobi et al.(2023)が報告した46歳男性では、RPR 1:64、TPHA 1:512の眼梅毒に対してIV PCG 400万単位 q4hによる神経梅毒治療を実施し、6ヶ月後に視力が回復した2)。
RPR(脂質抗原法)の推移を参考にする。抗体価8倍以下、あるいは初期値の1/4以下への低下をもって駆梅効果ありと判断する10)。治療後も再発の可能性があり、RPRの定期的な確認を継続する。
ペニシリン脱感作(desensitization)が第一に推奨される1)7)。
Cubelo et al.(2022)は、HIV陽性・PCGアレルギーの24歳男性にドキシサイクリン100 mg BID 14日間を投与し、RPRが1:1,024から1:32へと低下したことを報告した7)。その後PCG脱感作を実施した。
治療開始24時間以内に死滅した梅毒トレポネーマ由来の炎症性リポタンパク質に対する反応として発症する。眼科的には虹彩炎の再発(炎症の再燃)としてみられることがある。
ペニシリン脱感作が第一に推奨される。これが困難な場合、代替薬としてセフトリアキソン(1〜2 g 1日1回 × 14日間)またはドキシサイクリン(200 mg/日 × 28日間)が用いられる1)7)。ただし、いずれも眼梅毒に対するエビデンスはペニシリンに比べ限られています。
治療は中止せず継続する。発熱や頭痛などの全身症状には解熱剤・鎮痛剤による対症療法を行います。眼症状(視力低下・乳頭腫脹等)を含む反応は通常一時的であり、治療の継続とともに改善する1)。
ステロイドは、適切な抗菌薬投与を十分に行ったうえで炎症が残存する場合に限り、補助的に使用が検討される。免疫抑制なしにステロイドを先行投与することは、梅毒の増悪につながるため禁忌である5)。
T. pallidum は初感染部位から血行性に播種され、眼組織を含む全身臓器に到達する。血液網膜関門を通過し、脈絡膜・網膜・硝子体に炎症を引き起こす。梅毒の眼病変は第1期〜晩期梅毒のいずれの病期にも生じうるが、後眼部病変は第2期以降に多い。
梅毒トレポネーマはTLR2/TLR4/TLR5依存性シグナルを介してIL-1β、IL-6、IL-12、TNF-αの産生を誘導し、遅延型過敏反応類似の組織障害を引き起こす1)。CD4+細胞とマクロファージが第1期病変を支配し、CD8+細胞が第2期を支配する。IFN-γの産生はマクロファージを活性化・遊走させる。
梅毒性角膜実質炎では、T. pallidum 自体による直接感染ではなく、梅毒トレポネーマ抗原に対する免疫反応(角膜実質へのリンパ球浸潤と血管侵入)が主な病態である。このため、ステロイドには反応するがペニシリン単独では症状が消退しないことがある。
梅毒トレポネーマは緩徐な増殖と、眼・CNS・胎盤などの免疫特権組織への侵入能を持つ1)。Fas関連死経路を介したCD4+細胞のアポトーシスにより免疫クリアランスが不完全となり、慢性感染が成立する。
HIV陽性患者では第2期後の眼梅毒進行が加速する。両眼性関与はHIV陽性患者の62%に対しHIV陰性患者の38%と高頻度である(96例の研究)1)。AIDSでは血清学的検査が偽陰性となる場合があり、診断に注意を要する。
HIV陽性患者が梅毒眼病変を有する場合、抗レトロウイルス療法(ART)開始後に炎症が一過性に増悪するIRIS(免疫再構築炎症症候群)が発生することがある11)。
Pipitoら(2023)のレビューでは、IRIS症例においてART前のCD4細胞数は低値(中央値196/μL)であったが、ART後に318/μLへ回復したことが報告されている11)。CD4低値例では梅毒血清検査が偽陰性となるリスクもある11)。
ペニシリン系抗菌薬に対する反応は一般に良好で、投与後数日で硝子体混濁が急激に消退することも多い。治療成功率は約90%と報告される3)。視神経炎合併例では治療が遅れると視神経萎縮となり、視力予後に影響する。HIV重複感染例では治療後の再発リスクが高く、RPR推移の長期モニタリングが必要である。
ART開始後28日前後に炎症が増悪する場合はIRISを疑う。Unmasking型とparadoxical型を鑑別し、梅毒の治療が不十分な場合はペニシリンG治療を先行させる11)。ステロイドの追加は抗梅毒治療を確立したうえで検討します。
炎症性脈絡膜新生血管(iCNV)に対する抗VEGF療法:眼梅毒に合併するiCNVは極めて稀な病態である。Świerczyńska et al.(2021)の報告では、アフリベルセプト硝子体内注射により約1/3が1回の注射で病勢安定、約2/3が2回の注射で視力安定に至った6)。iCNVは抗菌薬治療のみでは消退せず、抗VEGF硝子体内注射の追加が有効であった。
静脈優位型梅毒性網膜血管炎:通常、梅毒性網膜血管炎は動脈炎または混合型が多いとされるが、HIV共感染例で静脈炎優位の症例が報告されている。Mammo et al.(2022)は、53歳のHIV陽性男性に静脈炎優位の汎ぶどう膜炎を認め、IV PCG 400万単位 14日間 × 2コースで治療した症例を報告した9)。治療後に傍静脈色素性網膜症(paravenous pigmentary retinopathy)に進行した。
マルチモーダルイメージングによる診断精度の向上:EDI-OCT・超広角自家蛍光(FAF)・ICGの組み合わせにより、眼梅毒の診断精度向上が期待されている1)3)。ICGでは脈絡膜の暗点ドット、ホットスポット、ぼやけた脈絡膜血管が検出される。これらのマルチモーダルイメージング所見の蓄積が、サルコイドーシスや結核との鑑別に貢献する可能性がある。
眼内液を用いた診断技術の発展:硝子体液中のEIAによる梅毒抗体検出(感度90.9%・特異度100%)は、血清学的偽陰性例や難治性後眼部炎症例に対して診断価値が高い4)。特にHIV合併例や免疫不全状態では血清診断の信頼性が低下するため、眼内液検査は重要な補助診断法として位置づけられつつある。
IRIS管理の最適化:ART開始に伴うIRISの発生機序と最適な管理戦略についての研究が進んでいる11)。IRISの予防・治療における抗梅毒治療とARTのタイミングの最適化が今後の課題である。