前部ぶどう膜炎の特徴
豚脂様(mutton-fat)KP:灰白色・大型、角膜下半部に分布
虹彩結節:Koeppe結節(瞳孔縁)、Busacca結節(虹彩面)
隅角結節:比較的特異性が高い所見。テント状周辺虹彩前癒着の原因となる
虹彩後癒着:頻度が高く、全周性では膨隆虹彩を形成する

サルコイドーシスは全身の臓器に非乾酪性類上皮細胞肉芽腫を形成する原因不明の全身性炎症性疾患である。病理組織学的には類上皮細胞や巨細胞からなる壊死を伴わない肉芽腫病変が特徴であり、好発部位は肺・縦隔リンパ節・眼・皮膚であるが、心臓・脳・骨・腎臓・消化管など全身に発症しうる。
1878年にJonathan Hutchinson卿が皮膚疾患として初報告した。1909年にデンマークの眼科医Heerfordtが「ぶどう膜炎・耳下腺炎・発熱」を主徴とする症例を報告し、これがヘールフォルト症候群(Heerfordt syndrome)と呼ばれる9)。
ぶどう膜炎の原因疾患の第1位である。2002年疫学調査で全ぶどう膜炎の13.3%、2009年調査で10.7%(いずれも第1位)を占める1)。サルコイドーシス患者の20〜50%に眼病変が生じ2)、30〜40%で眼症状が初発症状となる。85%以上が両眼性である2)。
発生年齢は男性では20歳代にピーク、女性では20歳代と50〜60歳代に二峰性分布を示す。女性に多く(男女比1:1.8)1)、50歳以上では女性の比率が高まる。
小児サルコイドーシスは成人と病態が異なる3)。5歳以下で発症する「早期発症型(EOS)」はNOD2遺伝子変異(R334W, R334Q)を伴うBlau症候群に相当し、関節炎・皮膚炎・ぶどう膜炎を三徴とする。8〜15歳で発症する「成人型」は環境抗原への過剰免疫応答によると考えられている3)。
ぶどう膜炎の原因疾患の第1位を占め、欧米や東南アジアでは比率が低い。遺伝的背景(HLA-DRB1アリル)や環境因子の差が関与すると推測されるが、正確な理由は未解明である1)。
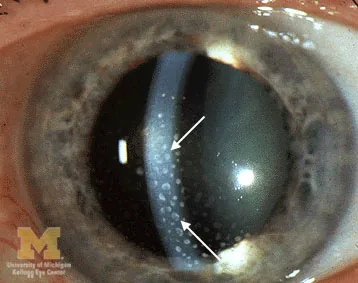
眼症状は炎症の部位と程度により異なる。霧視が最も多く、飛蚊症(硝子体混濁による)・視力低下・羞明・充血・眼痛が続く。慢性型では無症状のまま経過し、診断が遅れることがある2)。眼症状が全身症状に数年先行する場合もある。
:::caution 自覚症状がない場合も要注意 慢性に経過する症例では症状が乏しい。定期的な眼科受診によって初めて活動性炎症が判明することがある。 :::
前部ぶどう膜炎の特徴
豚脂様(mutton-fat)KP:灰白色・大型、角膜下半部に分布
虹彩結節:Koeppe結節(瞳孔縁)、Busacca結節(虹彩面)
隅角結節:比較的特異性が高い所見。テント状周辺虹彩前癒着の原因となる
虹彩後癒着:頻度が高く、全周性では膨隆虹彩を形成する
後部ぶどう膜炎の特徴
硝子体混濁:雪玉状(snowball)・数珠状(string of pearls)1)
網膜静脈周囲炎:分節状血管鞘「蝋涙状変化(candle wax drippings)」1)
脈絡膜肉芽腫:散在性黄橙色病変。大型では漿液性網膜剝離を合併
視神経乳頭肉芽腫:5%未満7)。マクロアニュリズムも報告2)
涙腺の肉芽腫による涙腺腫脹から乾燥性角結膜炎が生じる。結膜結節(無症状が多い)、強膜炎(まれ・非壊死性)、眼瞼皮膚の肉芽腫も認められる。顔面神経麻痺などの脳神経麻痺を生じることもある。
病因は不明である。遺伝的感受性を有する個体が環境抗原(吸入抗原・感染物質)に曝露された際に過剰免疫応答が誘発されると考えられている。
Cutibacterium acnes(旧Propionibacterium acnes)の関与が報告されている。結核菌DNA・各種ウイルスの関与も示唆されている2)。遺伝的素因としてHLA-DRB1との関連が知られ1)、家族内発症例ではリスクが上昇する2)。
| リスク因子 | 内容 |
|---|---|
| 人種 | アフリカ系アメリカ人に多く(白人の約10倍)、北欧系にも多い |
| 性別 | 女性にやや多い(男女比1:1.8) |
| 年齢 | 男性20歳代・女性20歳代+50〜60歳代 |
| HLA | HLA-DRB1アリルとの関連1) |
| 家族歴 | 一等親にサルコイドーシス患者がいるとリスク上昇2) |
小児早期発症型(EOS)ではNOD2変異(R334W, R334Q)によりNF-κBシグナルが過剰亢進し、病的Th17細胞が出現する3)。
:::tip 予防法と日常生活 現時点で確立された予防法はない。早期発見のためには、霧視・飛蚊症が続く場合に眼科を受診することが重要である。 :::
診断の原則は臨床所見・検査所見・組織学的所見の総合判断である。
:::caution 診断前のステロイド全身投与に注意 ステロイド全身投与は病変を縮小させ組織生検結果を偽陰性化する。緊急でない限り、診断確定まで全身ステロイド投与は避ける。 :::
確実(組織診断群): 2臓器以上の病変+病理で乾酪壊死を伴わない肉芽腫
ほぼ確実(臨床診断群): 2臓器以上の病変+検査所見2項目以上陽性
6項目中2項目以上でサルコイドーシス眼病変を疑い、診断基準に準じて診断する。
参考となる眼病変:角膜乾燥症、上強膜炎・強膜炎、涙腺腫脹、顔面神経麻痺
確定(Definitive)
生検で非乾酪性肉芽腫が証明され、適合するぶどう膜炎所見を有する
推定(Presumed)
両側肺門リンパ節腫脹(BHL)+眼内徴候2つ以上
または、BHL以外の全身検査異常2つ以上+眼内徴候2つ以上
疑い(Possible)
眼内徴候3つ以上、BHL陰性だが全身検査所見2つ以上
IWOS 7つの眼内徴候2): (1)豚脂様KP/虹彩結節、(2)隅角結節/テント状PAS、(3)硝子体雪玉状/数珠状混濁、(4)網膜血管周囲炎・血管周囲結節、(5)ろう様・光凝固斑様病変、(6)乳頭・脈絡膜肉芽腫、(7)両眼性
| 検査項目 | 特性・数値 |
|---|---|
| 血清ACE | 感度73%、特異度83%2)。ステロイド治療中・ACE阻害薬服用中は偽陰性に注意 |
| 血清リゾチーム | 8mg/L超で感度60%、特異度76%2) |
| 血清sIL-2R | 疾患活動性バイオマーカー2) |
| 胸部X線・CT | BHL(約90%で異常)。CT感度73%8) |
| ⁶⁷Ga-シンチ/FDG-PET | PET感度85.7%、特異度95.5%2, 8) |
| BAL CD4/CD8比 | >3.5で陽性1, 2) |
| ツベルクリン/IGRA陰性 | 結核除外に必須1) |
| 組織生検 | 確定診断のゴールドスタンダード。経気管支(陽性率63〜80%)5)、結膜・リンパ節・皮膚も対象 |
否定できない。感度73%であり約4分の1は正常値を示す。ステロイド治療中やACE阻害薬服用中は偽陰性となる。臨床所見・画像・他の検査項目との総合評価が必要である2)。
いずれも脈絡膜病変やリンパ節腫脹を呈しうる。前房水・硝子体液中のIL-10/IL-6比(>1でリンパ腫を示唆)や、FDG-PETの集積パターンで鑑別を進める。確定には組織生検が必要である5)。
トリアムシノロンアセトニド(ケナコルト-A®)40mg(保険適用外)1)。
全身投与の適応1):局所投与に抵抗する重篤な前眼部炎症・高度硝子体混濁・広範な網脈絡膜炎・網膜血管炎・黄斑浮腫・視神経乳頭の浮腫・肉芽腫
プレドニゾロン 0.5〜1.0mg/kg/日で2〜4週間から開始し、4〜8週ごとに5〜10mg/日ずつ漸減する1)。全投与期間は半年〜1年以上を要することがある1)。
漸減スケジュール例:
| 投与量 | 期間 |
|---|---|
| 30mg/日 | 2週間 |
| 20mg/日 | 1か月 |
| 15mg/日 | 1か月 |
| 10mg/日 | 1か月 |
| 7.5mg/日 | 1か月 |
| 5mg/日 | 1か月 |
| 5mg/日(隔日) | 1か月 |
:::caution ステロイド長期投与の注意点 骨粗鬆症・糖尿病・高血圧・感染リスクに注意する。長期投与例では胃粘膜保護薬・ビスホスホネートの併用を検討する。 :::
難治例・ステロイド節約のために使用する1, 2)。
通常12〜24か月で中止可能。重度再発例は5年以上継続することもある2)。
アダリムマブ(ヒュミラ®):40mg/2週 皮下注射2, 4)。非感染性ぶどう膜炎に承認された抗TNF-α抗体。VISUAL I・VISUAL II試験で再燃抑制効果が確認されている4)。
インフリキシマブ(レミケード®):5mg/kg 点滴静注、8週間隔1)。保険適用はBehçet病難治性網膜ぶどう膜炎であり、サルコイドーシスは適応外使用。
エタネルセプトの有効性は低い1)。生物学的製剤投与前には結核・B型肝炎の除外スクリーニングが必須4)。
白内障手術:消炎時期に施行。完全消炎困難なら比較的落ち着いた時期にステロイド内服併用で手術。後に濾過手術の可能性がある場合は上方結膜を温存し角膜切開を選択する。
続発緑内障:降圧点眼(PG製剤・β遮断薬・炭酸脱水酵素阻害薬・α₂刺激薬)→ CAI内服 → D-マンニトール点滴の順で対処する。線維柱帯切開術はステロイド緑内障に特に有効。不十分な場合は線維柱帯切除術を行う。
網膜光凝固:閉塞性血管炎による無血管野に対して施行。網膜細動脈瘤には直接凝固。
硝子体手術:黄斑上膜・黄斑円孔・硝子体出血・ステロイド抵抗性嚢胞様黄斑浮腫が対象となる。
軽症の前眼部炎症例では可能である。後眼部病変(嚢胞様黄斑浮腫・広範な網脈絡膜炎・視神経病変)がある場合は後部Tenon囊下注射や全身投与が必要となる。
約2/3は良性の自己限定的経過をたどり、ステロイド全身投与なしで視力予後が良好な症例が多い。慢性化する症例もあり長期治療を要する。前眼部中心の炎症は予後良好、後眼部侵襲が繰り返されると網膜変性・視神経萎縮をきたし重篤な視機能障害に至る。
肉芽腫形成は以下の免疫カスケードによる2):
肉芽腫の組織学的特徴:非乾酪性類上皮細胞・リンパ球の集塊。多核巨細胞内に星状体・シャウマン小体。周囲にリング状線維化が生じる2)。
眼内での主要病態:線維柱帯への肉芽腫沈着 → 房水流出障害 → 続発緑内障6)。網膜血管壁への肉芽腫浸潤 → 静脈周囲炎 → 蝋涙状滲出物形成。炎症環境下のVEGF産生亢進 → 脈絡膜新生血管10)。
ビタミンD過剰産生(マクロファージによる1,25(OH)₂D₃合成亢進)→ 高カルシウム尿症・高カルシウム血症も生じうる2)。
小児早期発症型(NOD2変異)では、NF-κBシグナルの過剰亢進と病的Th17細胞の出現が肉芽腫形成を促進する3)。
:::danger 研究段階の情報について 本セクションに記載された治療法・研究成果の一部は研究段階のものを含む。実際の診療においては専門医と相談のうえ判断すること。 :::
ファリシマブの難治性嚢胞様黄斑浮腫への応用12):VEGF+Ang-2の二重阻害薬。Lin 2025の報告では、82歳女性・ステロイド抵抗性CMEに対し2回注射後にBCVAが両眼で改善(右20/200→20/50、左20/400→20/63)し、中心窩網膜厚も著明に改善(右562→371μm、左717→286μm)した。眼サルコイドーシスへの世界初の応用報告である12)。
免疫チェックポイント阻害薬との関連11):Read 2025では重症眼サルコイドーシス既往患者にペムブロリズマブを2年以上投与して眼再燃がみられなかった。慎重なモニタリング下での安全使用の可能性を示す症例報告である。
サルコイドーシスと悪性腫瘍の関連(サルコイド-リンパ腫症候群)5):免疫調節機構の破綻がリンパ腫発症の素因となる可能性があり、長期経過観察中の腫瘍発症に注意が必要である。
マルチモーダルイメージングの進歩2):EDI-OCTは脈絡膜肉芽腫を均質・低反射な境界明瞭病変として描出する。OCTA(光干渉断層血管造影)により脈絡毛細血管血流欠損の検出が可能となった。ICGA(インドシアニングリーン蛍光造影)は潜在的脈絡膜肉芽腫の検出・治療反応評価に有用である。
小児サルコイドーシスの長期予後3):52例の小児成人型(中央値11.5年追跡)で、50%が成人期も活動性疾患を維持。小児期寛解患者の19%が成人期に再発した。生涯にわたる経過観察が推奨される。
炎症性脈絡膜新生血管の新規報告10):小児14歳例でアダリムマブ併用下でも周乳頭CNVが進行し、抗VEGF硝子体内注射を追加した症例が報告されている。