主要リスク因子
高血圧:患者の51〜75%に合併する最大のリスク因子。持続的な高血圧が血管壁のヒアリン変性と動脈硬化を促進する9)。
動脈硬化:ヒアリン変性・コラーゲン化による血管壁の脆弱化。長期の血管壁障害が拡張の基盤となる1, 9)。
加齢:60歳以上に好発。加齢に伴う血管壁の脆弱化が背景にある。
女性性別:患者の70〜78%を女性が占める。性差の詳細な機序は不明である9)。

後天性網膜細動脈瘤(Retinal Arterial Macroaneurysm; RAM)は、第3分枝以内の網膜動脈に認める嚢状または紡錘状の局所的拡張である。網膜動脈の分枝部や動静脈交叉部の動脈から突出して観察されることが多い。RAMからの滲出や出血により形態変化および機能障害が生じる。1973年にRobertsonが初めて報告した疾患概念である。
一般的なサイズは100〜250μmである1, 3)。上耳側動脈に約50%、下耳側動脈に約45%が発生し、鼻側は稀である3)。耳側に多いが鼻側にも生じる。片眼単発性が多いが、両眼性・多発例も存在する。高血圧症・動脈硬化症の既往のある高齢者に多い。
視神経乳頭上に発生するRAMは全体の3.7〜8%と稀な病態とされる7, 10)。RAMは自然退縮傾向を持つことが知られており、この点が治療方針の決定に影響する。
比較的稀な疾患だが、高齢化に伴い遭遇機会が増えている。視神経乳頭上のRAMはさらに稀であり、全体の3.7〜8%と報告されている7, 10)。出血型では黄斑部に出血や滲出が及ぶと深刻な視力障害を生じるため、早期の診断と対応が重要である。
滲出や出血が黄斑部に及ぶと視力低下や歪視を生じる。出血や滲出を生じていなければ自覚症状もなく発見されにくい。
黄斑部に出血や滲出が及んだ場合、以下の症状を生じる。
RAMは臨床的に以下の3型に分類される3, 9)。
| 型 | 主な症状 | 代表的所見 |
|---|---|---|
| 無症候型 | なし | 偶然発見 |
| 出血型 | 急性視力低下 | 多層性出血 |
| 滲出型 | 緩徐な視力低下 | 硬性白斑・浮腫 |
RAMに特徴的な出血は多層性であり、網膜下・網膜内・内境界膜(ILM)下・網膜前・硝子体の複数の層に及ぶ9)。この多層性出血パターンはRAMの特徴的所見の一つである。
眼底検査では、網膜細動脈に沿って赤色を呈し、フィブリンを伴えば白色に、線維化していれば灰白色として認める。出血や滲出により動脈瘤が特定できない場合もある。滲出型では輪状硬性白斑(circinate retinopathy)、網膜浮腫、漿液性網膜剥離を認め、動脈瘤の周囲に輪状の硬性白斑(輪状網膜症)を伴うこともある。
RAMの合併症として、破裂後の黄斑円孔形成7)や網膜動脈分枝閉塞10)が報告されている。視神経乳頭上のRAMは早期に硝子体出血を来しやすく、特に注意が必要である10)。
多層性出血(網膜下・網膜内・硝子体の複数層にわたる出血)はRAMに特徴的な所見であり、診断の重要な手がかりとなる9)。一方、出血が広範な場合はRAMの瘤本体が視認しにくくなることがあり、IAやOCT・OCTAによる補助的な評価が診断に不可欠である3)。
RAMの発症には、血管壁の脆弱化を促進する複数のリスク因子が関与する。高血圧症・動脈硬化症の既往のある高齢者に多い。血管壁の筋層が失われ、中膜がコラーゲン線維化することで弾性が低下し、内腔圧による拡張が生じると考えられている1, 9)。
主要リスク因子
高血圧:患者の51〜75%に合併する最大のリスク因子。持続的な高血圧が血管壁のヒアリン変性と動脈硬化を促進する9)。
動脈硬化:ヒアリン変性・コラーゲン化による血管壁の脆弱化。長期の血管壁障害が拡張の基盤となる1, 9)。
加齢:60歳以上に好発。加齢に伴う血管壁の脆弱化が背景にある。
女性性別:患者の70〜78%を女性が占める。性差の詳細な機序は不明である9)。
その他のリスク因子
脂質異常症:動脈硬化の進行を促進し、血管壁障害を悪化させる1, 3)。
心血管疾患:冠動脈疾患・大動脈瘤との関連が報告されている。全身血管病変の一環としてRAMが生じる場合がある9)。
Lynch症候群:DNA修復遺伝子変異による血管ネットワーク複雑化の可能性が示唆されている。RAMとの関連では初の報告例である1)。
Valsalva手技:急激な血圧変動がRAM破裂の誘因となりうる。重労働・咳嗽・排便時の怒責などが誘因として報告されている9)。
RAMの正確な診断にはマルチモーダルイメージングが不可欠である3)。特に出血が多い場合、FAだけでは瘤本体の同定が困難なことがあり、複数の検査を組み合わせる必要がある。
鑑別診断として加齢黄斑変性が最も重要であり、次いで網膜静脈分枝閉塞症(BRVO)、糖尿病網膜症、Coats病が挙げられる。眼底所見・FAおよびIAで、網膜動脈に沿って瘤状病巣の存在の有無を確認する。OCTで網膜色素上皮(RPE)の隆起所見がなければ、滲出型加齢黄斑変性の可能性は低い。
| 検査 | 主な所見 | 適応・利点 |
|---|---|---|
| FA | 瘤状過蛍光・漏出 | 診断の標準的手法 |
| IA | 出血下の瘤描出 | 出血例で特に有用 |
| OCT | 球状高反射・浮腫 | 網膜層構造の定量 |
蛍光眼底造影(FA):動脈相でRAMの瘤状過蛍光を認め、後期には漏出・組織染色を呈する。蛍光色素の漏出や組織染による過蛍光が強い場合には、動脈瘤の血管壁の透過性が亢進していて活動性のある所見と判断する。活動性の評価に有用で、診断の標準的手法である。
インドシアニングリーン蛍光造影(IA):出血が多い場合にFAよりRAMの検出に優れる3)。インドシアニングリーンはフルオレセインより動脈瘤からの蛍光漏出が弱いため、IAで過蛍光を示す場合はより活動性が高いと判断できる。
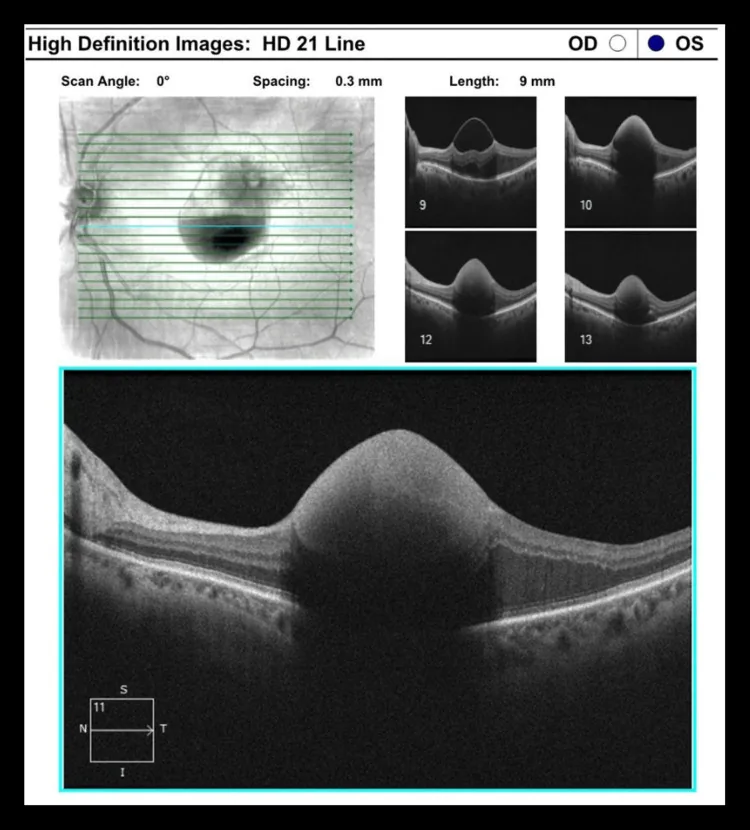
光干渉断層計(OCT):内網膜の高反射球状構造としてRAMを描出する。網膜浮腫・漿液性網膜剥離の確認・定量が可能であり、出血の部位(網膜前・網膜下)の層別化にも有用である。
光干渉断層血管撮影(OCTA):血流シグナルを非侵襲的に可視化する。血管壁の解離様変化による壁内通路の描出が可能である8)。
レーザースペックルフローグラフィー(LSFG):血流を非侵襲的に定量評価する手法である。MBR(Mean Blur Rate)の値がRAMの退縮と相関し、治療経過のモニタリングに活用できる5)。
近赤外線反射イメージング(NIR-R):発症3年前にcuff型の血管壁肥厚を検出した症例報告があり、早期発見ツールとしての可能性が示唆されている6)。
Bモード超音波:硝子体出血により眼底透見が不能な場合に使用する7, 10)。眼球内の病変の大まかな評価が可能である。
RAMの治療方針は、病型・黄斑部への影響・自然退縮傾向を考慮して決定する。自然寛解傾向があるが、黄斑部への持続する滲出や出血の程度によって視機能障害の程度と回復は異なる。
治療の段階的アプローチ:
保存的治療
経過観察:自然寛解傾向があるため、黄斑非関与・無症候型が対象。定期的な眼底検査で経過を追う。
薬物療法:カルバゾクロム(アドナ錠30mg)3錠 分3を用いる。血管透過性亢進の抑制・止血作用を目的とした補助的治療である。
リスク因子管理:血圧・脂質の厳格な管理が再発予防と病勢コントロールに不可欠である。
侵襲的治療
レーザー光凝固:動脈瘤の透過性亢進した壁や破裂した壁の創傷治癒促進が目的。動脈を閉塞させないよう動脈瘤の表面をあぶるように行い、動脈瘤全体を灰白色凝固斑が出るまで重ね打ちする必要はない。スポットサイズ300〜500μm・照射時間0.2〜0.3秒・出力120mW〜が目安。合併症として動脈閉塞のリスクあり。
抗VEGF硝子体内注射:滲出性RAMに対して用いる。日本では保険適用外である2, 3, 4)。
硝子体手術:血液がILMと神経線維層の間に貯留する場合はILM剥離を伴う硝子体手術を行う。持続する硝子体出血も硝子体手術の適応となる。
間接凝固:動脈瘤周囲の網膜を凝固し、漏出を黄斑部から遠ざける手法である。直接凝固と組み合わせることも多い。
レーザー+抗VEGF併用療法:3症例の検討では、平均中心窩網膜厚(CRT)が275.7μm減少し、視力が0.55 logMAR改善したと報告されている4)。
Nd:YAGレーザー:ILM下出血のドレナージ目的に用いる。早期実施が推奨される9)。
硝子体内ガス注入(血腫移動術):網膜下出血が黄斑部に存在してから2週間以内が適応である。出血がすでに器質化している場合は非適応となる。SF6またはC3F8を0.2〜0.8mL注入し、術後1〜2週間の腹臥位保持が必要となる。tPA(組織プラスミノゲンアクチベーター)との併用で黄斑下血腫の移動効果を高める場合がある。
サブスレッショルドレーザー:従来のレーザーと同等の効果を持ちながら合併症が少ないとされる9)。
RAMには自然退縮傾向があり、無症候型では経過観察のみで改善する例も多い。しかし、黄斑部に出血や滲出が及んだ場合は視力予後に影響するため、積極的な治療介入を検討する必要がある。自然経過と治療介入の選択は病型・病勢・患者背景を総合して判断する。
RAMの病態生理の中核は血管壁構造の変性と内腔圧の亢進である。高血圧症・動脈硬化症による血管壁の脆弱化が基盤となり、動脈壁の透過性亢進による漏出と破裂による出血が視機能障害をもたらす。
血管壁の変性過程:高血圧によるヒアリン変性と動脈硬化が血管壁の筋層を障害し、中膜のコラーゲン線維化が進行する9)。その結果、血管壁の弾性が低下し、内腔圧に対する抵抗性が失われて局所拡張が生じる1, 9)。
Gass仮説:アテローム塞栓が血管壁を損傷し、局所虚血が生じることでVEGF発現が亢進する。その結果として透過性亢進と血管拡張が促進される2)。VEGFは内皮NO産生を介して動脈拡張と透過性亢進を引き起こし、滲出型RAMの病態に関与する3)。
解離様変化:適応的光学眼底鏡(AOSLO)・OCT・OCTAを用いた詳細な観察により、血管壁にcrack(亀裂)が生じ、壁内通路が形成される病態が報告されている8)。この壁内通路から隣接部位に新たなRAMが形成される場合がある。
破裂機序:内腔圧が脆弱化した血管壁の閾値を超えた時点で破裂が生じる9)。Valsalva手技(咳嗽・重労働・排便時の怒責など)による急激な血圧上昇が破裂の誘因となりうる9)。
Meng Y らは、Valsalva手技を契機とするRAM破裂例の文献をレビューし、急激な腹腔内圧上昇による静脈圧・動脈圧の急上昇が脆弱な血管壁を破綻させる機序を論じた9)。
血液網膜関門の破綻:滲出型RAMでは血液網膜関門の障害が黄斑浮腫や硬性白斑の背景となる15)。
視神経乳頭上RAMの特性:乳頭近傍の動脈は口径が大きく血流速度が高い。そのため壁ストレスが大きく、早期に硝子体出血を来しやすい10)。
適応的光学眼底鏡(AOSLO)による微細構造解析:ASOLOを用いた詳細な観察により、RAM内の拍動消失・血栓形成過程・血管壁の亀裂構造が可視化された8)。これにより血管壁の解離様変化という新たな病態が明らかとなり、発症機序の理解が深まった。
レーザースペックルフローグラフィー(LSFG)による経時的評価:RAMの退縮に伴い、MBR(Mean Blur Rate)が6.8 AUから1.1 AUへと著明に低下したことが報告されている5)。LSFGによる非侵襲的血流モニタリングは、治療効果の客観的評価ツールとして有望である。
Hanazaki H らは、治療を受けたRAMの眼血流をLSFGで経時的に評価し、MBRの低下がRAM退縮と相関することを示した5)。
近赤外線反射イメージング(NIR-R)による早期検出:RAMが臨床的に顕在化する3年前に、NIR-R画像でcuff型の血管壁肥厚が検出された症例が報告されている6)。高血圧患者における予測因子としての可能性があり、早期スクリーニングツールへの応用が期待される。
レーザー+抗VEGF併用療法の有効性:3例のシリーズ研究において、焦点レーザー照射と硝子体内ベバシズマブを組み合わせた治療で、平均CRTが275.7μm減少し、視力が0.55 logMAR改善した4)。抗VEGFによる血管安定化とレーザーによる壁修復の相乗効果が示唆されており、今後の大規模試験が期待される。
サブスレッショルドレーザー:従来の閾値レーザーに比べ、ヒートショックプロテインを介したサブリーサルな網膜温熱療法により合併症を軽減しながら同等の効果が得られるとされる9)。
Lynch症候群とRAMの関連:DNA修復遺伝子変異を持つLynch症候群患者でのRAM発症が初めて報告された1)。DNA修復遺伝子変異により血管ネットワークが複雑化し、VEGF-A発現亢進がRAMの発症に寄与する可能性が示唆されている。
治療ガイドラインの必要性:治療法の多様化に伴い、エビデンスに基づく診療ガイドラインの策定が求められている9)。
多層性出血と非侵襲的画像評価の症例蓄積:破裂RAMでは網膜下・網膜内・硝子体など多層性出血を示す症例が報告されている11)。硝子体下出血合併例ではNd:YAGレーザーや硝子体手術の適応判断が重要となる12)。近赤外反射ビデオグラフィーはRAMの拍動性評価に、OCTAは病変内血流の非侵襲的評価に用いられる13, 14)。
症例報告や小規模シリーズにおいて、滲出性RAMに対する抗VEGF硝子体内注射の有効性が報告されている2, 3, 4)。特にレーザーとの併用療法では有望な結果が得られている4)。ただし日本では保険適用外であり2)、大規模なランダム化試験はまだ行われていない。使用にあたっては担当医と十分な相談が必要である。