主要危险因素
高血压:51%~75%的患者合并,是最大的危险因素。持续性高血压促进血管壁玻璃样变性和动脉硬化9)。
动脉硬化:玻璃样变性和胶原化导致血管壁脆弱。长期的血管壁损伤是扩张的基础1, 9)。
年龄增长:好发于60岁以上人群。年龄增长相关的血管壁脆弱是背景因素。
女性性别:女性占患者的70%~78%。性别差异的具体机制尚不清楚9)。

获得性视网膜动脉大动脉瘤(RAM)是发生在第三级分支以内视网膜动脉的囊状或梭形局部扩张。常从视网膜动脉的分支处或动静脉交叉处突出观察到。RAM的渗出或出血导致形态变化和功能障碍。该疾病概念由Robertson于1973年首次报道。
典型大小为100-250μm 1, 3)。约50%发生在颞上动脉,约45%发生在颞下动脉,鼻侧罕见 3)。虽然颞侧多见,但也可发生在鼻侧。多为单眼单发,但也有双眼或多发的情况。常见于有高血压和动脉硬化病史的老年人。
发生在视乳头上的RAM占所有病例的3.7-8%,是一种罕见情况 7, 10)。RAM具有自然消退的趋势,这一点影响治疗决策。
虽然是一种相对罕见的疾病,但随着人口老龄化,遇到的机会正在增加。视盘上的RAM更为罕见,据报道占所有病例的3.7-8% 7, 10)。在出血型中,出血或渗出累及黄斑会导致严重的视力障碍,因此早期诊断和处理很重要。
当渗出或出血累及黄斑时,会导致视力下降和视物变形。如果没有出血或渗出,则没有自觉症状,难以发现。
当出血或渗出波及黄斑时,会出现以下症状:
RAM在临床上分为以下三种类型 3, 9)。
| 类型 | 主要症状 | 典型所见 |
|---|---|---|
| 无症状型 | 无 | 偶然发现 |
| 出血型 | 急性视力下降 | 多层出血 |
| 渗出型 | 缓慢视力下降 | 硬性渗出、水肿 |
RAM特征性出血为多层性,累及视网膜下、视网膜内、内界膜(ILM)下、视网膜前及玻璃体等多个层次9)。这种多层出血模式是RAM的特征性表现之一。
眼底检查时,沿视网膜小动脉呈红色,伴有纤维蛋白时呈白色,纤维化时呈灰白色。出血或渗出可能导致动脉瘤无法识别。渗出型可见环形硬性渗出(环形视网膜病变)、视网膜水肿和浆液性视网膜脱离,动脉瘤周围可伴有环形硬性渗出(环形视网膜病变)。
RAM的并发症包括破裂后黄斑裂孔形成7)和视网膜分支动脉阻塞10)。视盘上的RAM易早期发生玻璃体出血,需特别注意10)。
多层出血(累及视网膜下、视网膜内和玻璃体等多个层次的出血)是RAM的特征性表现,是诊断的重要线索9)。然而,当出血广泛时,动脉瘤本身可能难以看清,因此IA、OCT或OCTA的辅助评估对诊断至关重要3)。
RAM的发生涉及多种促进血管壁脆弱的危险因素。多见于有高血压和动脉硬化病史的老年人。据认为,血管壁肌层丧失、中膜胶原纤维化导致弹性降低,从而因腔内压力引起扩张1, 9)。
主要危险因素
高血压:51%~75%的患者合并,是最大的危险因素。持续性高血压促进血管壁玻璃样变性和动脉硬化9)。
动脉硬化:玻璃样变性和胶原化导致血管壁脆弱。长期的血管壁损伤是扩张的基础1, 9)。
年龄增长:好发于60岁以上人群。年龄增长相关的血管壁脆弱是背景因素。
女性性别:女性占患者的70%~78%。性别差异的具体机制尚不清楚9)。
其他危险因素
血脂异常:促进动脉硬化进展,加重血管壁损伤1, 3)。
心血管疾病:据报道与冠状动脉疾病和主动脉瘤相关。RAM可能作为全身血管病变的一部分发生9)。
林奇综合征:提示DNA修复基因突变可能导致血管网络复杂化。这是首例与RAM相关的报道1)。
Valsalva动作:急剧的血压波动可能诱发RAM破裂。重体力劳动、咳嗽、排便时屏气等已被报道为诱因9)。
多模态成像对于RAM的准确诊断至关重要3)。尤其在出血较多时,仅凭FA可能难以确定瘤体本身,需要结合多种检查。
最重要的鉴别诊断是年龄相关性黄斑变性,其次是视网膜分支静脉阻塞(BRVO)、糖尿病视网膜病变和Coats病。通过眼底检查、FA和IA确认沿视网膜动脉是否存在瘤样病灶。如果OCT未显示视网膜色素上皮(RPE)隆起,则渗出性年龄相关性黄斑变性的可能性较低。
| 检查 | 主要表现 | 适应症/优点 |
|---|---|---|
| FA | 瘤样高荧光和渗漏 | 标准诊断方法 |
| IA | 出血下的瘤体显示 | 在出血病例中尤其有用 |
| OCT | 球形高反射和水肿 | 视网膜层结构的定量 |
荧光素眼底血管造影(FA):动脉期可见RAM的瘤样高荧光,晚期出现渗漏和组织染色。当荧光素渗漏或组织染色导致高荧光强烈时,判断为动脉瘤血管壁通透性增高且具有活动性。该检查有助于评估活动性,是标准诊断方法。
吲哚青绿血管造影(IA):在出血较多的情况下,IA比FA更优地检测RAM 3)。由于吲哚青绿从动脉瘤的荧光渗漏弱于荧光素,因此IA上出现高荧光提示活动性更高。
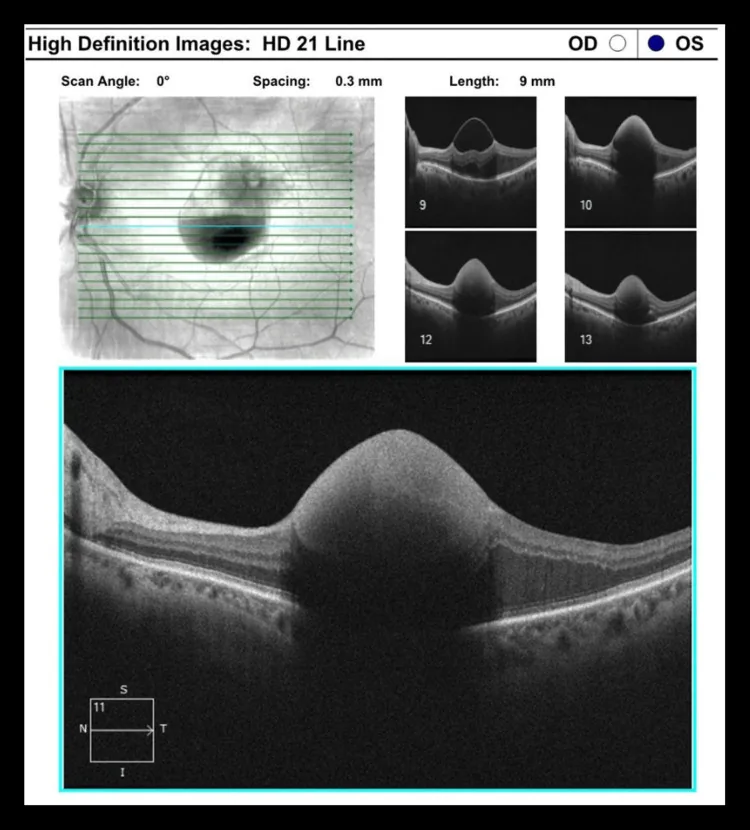
光学相干断层扫描(OCT):将RAM显示为内视网膜的高反射球形结构。可确认和量化视网膜水肿及浆液性视网膜脱离,并有助于出血部位(视网膜前或视网膜下)的分层。
光学相干断层扫描血管成像(OCTA):无创显示血流信号。可显示因血管壁夹层样变化形成的壁内通道8)。
激光散斑血流成像(LSFG):一种无创定量评估血流的方法。平均模糊率(MBR)值与RAM消退相关,可用于监测治疗过程5)。
近红外反射成像(NIR-R):有病例报告在发病前3年检测到袖套样血管壁增厚,提示其作为早期发现工具的潜力6)。
B型超声:用于因玻璃体积血而无法看清眼底的情况7, 10)。可粗略评估眼内病变。
RAM的治疗方案根据病变类型、对黄斑的影响以及自然消退趋势决定。虽然存在自然缓解的可能,但黄斑区持续渗出或出血的程度决定了视功能损伤的程度和恢复情况。
分步治疗方法:
保守治疗
观察:由于存在自然消退趋势,适用于黄斑未受累或无症状的病例。定期进行眼底检查随访。
药物治疗:卡巴克络(阿度那片30mg)3片,分3次服用。这是一种辅助治疗,旨在抑制血管通透性增加和止血。
危险因素管理:严格控制血压和血脂对于预防复发和控制病情至关重要。
侵入性治疗
激光光凝:目的是促进动脉瘤通透性增加或破裂的管壁愈合。应轻轻烧灼动脉瘤表面,避免闭塞动脉,无需重复照射直至整个动脉瘤出现灰白色凝固斑。参考参数:光斑大小300–500μm,曝光时间0.2–0.3秒,功率120mW以上。并发症包括动脉闭塞风险。
玻璃体内抗VEGF注射:用于渗出性RAM。在日本不属于医保范围2, 3, 4)。
玻璃体切除术:当血液积聚在内界膜和神经纤维层之间时,进行伴有内界膜剥离的玻璃体切除术。持续性玻璃体积血也是玻璃体切除术的适应证。
间接凝固:一种凝固动脉瘤周围视网膜,使渗漏远离黄斑的技术。常与直接凝固联合使用。
激光联合抗VEGF治疗:一项3例病例研究报道,平均中央视网膜厚度(CRT)减少275.7μm,视力改善0.55 logMAR4)。
Nd:YAG激光:用于引流内界膜下出血。建议早期实施9)。
玻璃体内注气(血肿移位术):适用于黄斑部视网膜下出血出现2周内。出血已机化则不适合。注入SF6或C3F8 0.2–0.8mL,术后需俯卧位1–2周。联合tPA(组织型纤溶酶原激活剂)可增强黄斑下血肿的移位效果。
阈下激光:据报道与传统激光疗效相当,但并发症较少9)。
RAM有自然消退的趋势,许多无症状病例仅通过观察即可改善。然而,当出血或渗出累及黄斑时,会影响视力预后,因此需要考虑积极的治疗干预。自然病程和治疗干预的选择需综合疾病类型、疾病活动度和患者背景来判断。
RAM的病理生理核心是血管壁结构变性和腔内压增高。高血压和动脉硬化导致血管壁脆弱化,动脉壁通透性增高引起的渗漏和破裂导致的出血引起视功能障碍。
血管壁变性过程:高血压引起的玻璃样变性和动脉硬化损害血管壁肌层,导致中膜胶原纤维化进展 9)。结果,血管壁弹性降低,对腔内压的抵抗力丧失,发生局部扩张 1, 9)。
Gass假说:动脉粥样硬化栓塞损伤血管壁,引起局部缺血,导致VEGF表达上调。结果促进通透性增高和血管扩张 2)。VEGF通过内皮NO产生引起动脉扩张和通透性增高,参与渗出型RAM的病理过程 3)。
夹层样改变:使用自适应光学扫描激光检眼镜(AOSLO)、OCT和OCTA的详细观察报告了血管壁出现裂纹、形成壁内通道的病理 8)。从该壁内通道可能在邻近部位形成新的RAM。
破裂机制:当腔内压超过脆弱血管壁的阈值时发生破裂 9)。Valsalva动作(咳嗽、重体力劳动、排便时屏气等)引起的血压急剧升高可能诱发破裂 9)。
Meng Y等人回顾了以Valsalva动作诱发的RAM破裂病例,讨论了腹腔内压急剧升高导致静脉压和动脉压迅速上升,从而使脆弱血管壁破裂的机制 9)。
血-视网膜屏障破坏:在渗出型RAM中,血-视网膜屏障的损伤是黄斑水肿和硬性渗出的基础 15)。
视盘上RAM的特征:视盘附近的动脉口径大、血流速度快。因此,壁应力大,容易早期发生玻璃体出血 10)。
自适应光学扫描激光检眼镜(AOSLO)的微结构分析:使用AOSLO进行详细观察,可视化了RAM内搏动消失、血栓形成过程和血管壁裂隙结构8)。这揭示了血管壁夹层样变化这一新病理状态,加深了对发病机制的理解。
激光散斑血流成像(LSFG)的纵向评估:据报道,随着RAM消退,平均模糊率(MBR)从6.8 AU显著下降至1.1 AU5)。LSFG的无创血流监测有望成为治疗效果的客观评估工具。
Hanazaki H等人使用LSFG纵向评估了接受治疗的RAM患者的眼部血流,并显示MBR的下降与RAM消退相关5)。
近红外反射成像(NIR-R)的早期检测:有病例报告在RAM临床显现前3年,NIR-R图像上检测到袖套样血管壁增厚6)。这提示其作为高血压患者预测因子的可能性,并有望应用于早期筛查工具。
激光联合抗VEGF治疗的有效性:在一项3例病例系列研究中,联合聚焦激光光凝和玻璃体内贝伐珠单抗治疗后,平均中央视网膜厚度(CRT)减少275.7 μm,视力改善0.55 logMAR4)。提示抗VEGF的血管稳定作用和激光的血管壁修复具有协同效应,期待未来大规模试验。
阈下激光:与传统阈值激光相比,通过热休克蛋白介导的亚致死性视网膜温热疗法可在减少并发症的同时获得同等效果9)。
Lynch综合征与RAM的关联:首次报道了具有DNA修复基因突变的Lynch综合征患者发生RAM1)。提示DNA修复基因突变可能使血管网络复杂化,VEGF-A表达升高可能促进RAM的发生。
治疗指南的必要性:随着治疗方法的多样化,需要制定基于循证医学的临床实践指南9)。
多层出血和非侵入性影像评估的病例积累:破裂的RAM可表现为视网膜下、视网膜内和玻璃体等多层出血11)。合并玻璃体下出血的病例中,Nd:YAG激光或玻璃体手术的适应症判断至关重要12)。近红外反射视频成像用于评估RAM的搏动性,OCTA用于病变内血流的无创评估13, 14)。
病例报告和小规模系列研究报道了玻璃体内注射抗VEGF药物对渗出性RAM的有效性2, 3, 4)。特别是与激光联合治疗时,已获得有希望的结果4)。然而,在日本这不在保险覆盖范围内2),且尚未进行大规模随机试验。使用前需要与主治医生充分协商。