非增殖性RR
微动脉瘤:视网膜毛细血管瘤散在分布。作为早期表现重要。
毛细血管扩张:不规则血管扩张和迂曲。荧光素眼底血管造影(FA)可清晰显示。
视网膜出血:散在的点状和火焰状出血。
硬性渗出:脂质沉积所致的黄白色浸润。
黄斑水肿(ME):对视力预后影响最大的表现。OCT上表现为囊样水肿或弥漫性水肿。
放射线眼损伤是放射线对眼组织造成损伤的总称。主要类型包括放射性白内障、放射性视网膜病变和放射性视神经病变。
| 类型 | 靶组织 | 阈值剂量 | 发病时间 | 视力预后 |
|---|---|---|---|---|
| 放射性白内障 | 晶状体(赤道部上皮细胞) | 0.5 Gy 以下(ICRP 2011年修订) | 照射后数月至数年 | 可通过手术改善 |
| 放射性视网膜病变 | 视网膜血管内皮细胞 | 35 Gy(有报告称20 Gy也可发生) | 照射后半年以上,尤其2~3年后 | 预后多不良 |
| 放射性视神经病变 | 视神经和视交叉 | 单次>2 Gy、总量>50 Gy时有风险 | 照射后3个月至数年 | 约半数无光感 |
放射性白内障由眼部辐射暴露引起。即使是低剂量暴露,长期白内障风险也会增加,核电站事故应急工作人员的暴露、医疗工作者的职业暴露、CT等医疗暴露等,长期来看也会成为白内障的风险。
放射性视网膜病变(Radiation Retinopathy; RR)是眼内肿瘤、眼眶或鼻窦肿瘤、颅内疾病等放射治疗中视网膜进入照射野时发生的慢性进行性闭塞性视网膜微血管疾病。一项荟萃分析显示,脑头颈部肿瘤放疗后RR患病率约为6%,视神经病变约为2% 3)。包括迟发性病例在内的总体发病率约为17% 4)。
不同照射部位的发病率如下:
| 照射部位 | 发病率 |
|---|---|
| 眼眶 | 85.7% |
| 鼻窦 | 45.4% |
| 鼻咽 | 36.4% |
| 脑 | 3.1% |
放射性视神经病变在鼻窦肿瘤或颅底病变放疗后罕见发生。好发部位是视交叉或其前后。
发病率因照射部位、剂量、分割方式和合并症而异。据报道,放射性视网膜病变的总发病率为17% 4),并非所有患者都会发病。放射性白内障即使低剂量也有长期风险,因此有辐射暴露史者定期进行眼科检查非常重要。
辐射引起的晶状体混浊始于后囊下中央的多色性细微点状混浊和空泡。这些变化逐渐扩大,形成斑块状和颗粒状混浊。同时,可能出现Y字缝分离的水隙。随着进展,出现中央相对透明的环形后囊下混浊。进一步进展形成由前后两层膜样混浊组成的盘状混浊,导致明显的视功能下降。
放射性白内障所见的进展模式:
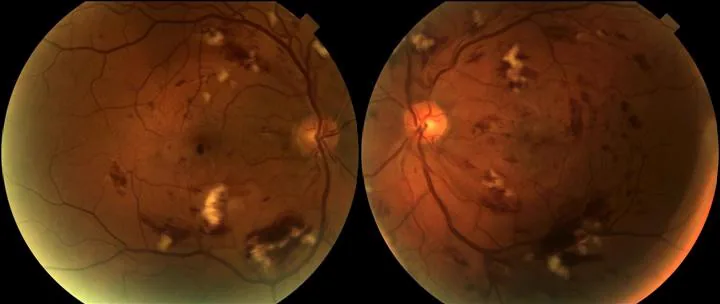
眼底所见类似于糖尿病视网膜病变,始于微动脉瘤、视网膜出血和硬性渗出,随后出现棉絮斑。进展时出现视网膜新生血管,导致玻璃体积血。黄斑水肿和中心凹周围毛细血管闭塞导致视力下降。一旦发病,进展比糖尿病视网膜病变更快。
放射性视网膜病变大致分为非增殖性和增殖性。
非增殖性RR
微动脉瘤:视网膜毛细血管瘤散在分布。作为早期表现重要。
毛细血管扩张:不规则血管扩张和迂曲。荧光素眼底血管造影(FA)可清晰显示。
视网膜出血:散在的点状和火焰状出血。
硬性渗出:脂质沉积所致的黄白色浸润。
黄斑水肿(ME):对视力预后影响最大的表现。OCT上表现为囊样水肿或弥漫性水肿。
增殖性RR
作为迟发性特殊表现,在17年后发病的病例中,OCT确认了囊腔内胆固醇结晶所致的洋葱环征(onion ring sign),作为慢性期治疗抵抗的标志物受到关注 6)。
此外,在30Gy全脑照射后16个月发生局限于上方视网膜的RR病例中,病变分布与照射野的30Gy等剂量线一致,证实即使在低剂量区域也表现出与照射野对应的发病模式 7)。
发病时间为照射后3个月至数年,视力进行性下降。机制为血管内皮损伤导致的缺血性视神经病变,约半数病例最终视力为无光感,视力预后不良。
照射后半年以上,特别是2~3年后发病较多。诊断时的中位时间为照射后39个月3),但也有17年后的迟发案例4)。照射后需要长期定期进行眼底检查。
2011年,ICRP(国际放射防护委员会)修订了阈值,建议对所有照射条件下导致视力下降的白内障,总照射剂量阈值定为0.5 Gy以下。对于职业照射,眼部照射上限从每年150 mSv改为5年内平均20 mSv,且单年不得超过50 mSv。
剂量阈值通常认为是35 Gy4)。超过45 Gy的照射容易发病,超过50 Gy则风险特别高3)。然而,在20~40 Gy的立体定向分割外照射后也观察到迟发性放射性视网膜病变8),因此即使低于阈值剂量也需注意。
| 风险因素 | 内容 |
|---|---|
| 总剂量 | >35 Gy(阈值)4),超过45 Gy高风险 |
| 分割剂量 | 高分割照射 |
| 照射部位 | 眼眶或视交叉附近3) |
| 糖尿病 | 加重微血管脆弱性 |
| 联合化疗 | 敏感性增加 |
增殖性RR约占所有RR的3%至25% 5)。靠近视交叉的照射与RR发病有显著相关性(p=0.009)3)。
单次照射剂量≤2Gy且总照射剂量≤50Gy被认为是相对安全的。近年来,伽玛刀治疗已成为主流,放射性视神经病变的发生率已显著降低。
糖尿病是放射性视网膜病变的重要危险因素。糖尿病引起的微血管脆弱性与放射线引起的内皮损伤协同作用,即使在较低剂量下也可能发病。除了维持血糖控制外,建议放射治疗后更频繁地进行眼底检查。
详细询问暴露史(剂量、类型、时间)很重要。使用裂隙灯显微镜确认后囊下混浊。应认为低剂量放射线暴露会加速晶状体的老化变化。由于年龄相关性白内障也会产生空泡、后囊下混浊、水裂和皮质浅层混浊,因此判断老年晶状体的混浊是否由放射线引起并不容易。确认暴露史是鉴别的关键。
荧光素眼底血管造影(FA)与分期
FA是诊断和分期RR的基本检查。早期可见视网膜毛细血管通透性增加,进展时毛细血管闭塞。小动脉也闭塞,导致视网膜无灌注区广泛扩大,并产生视网膜新生血管。Amoaku FA分级(1-4级)被广泛使用 1)。
| 分级 | 主要表现 |
|---|---|
| 1 | 微动脉瘤、局限性毛细血管扩张 |
| 2 | 毛细血管闭塞、广泛血管异常 |
| 3 | 视盘或视网膜新生血管 |
| 4 | 玻璃体积血、牵拉性视网膜脱离 |
吲哚青绿(ICG)荧光造影还可观察到脉络膜血管闭塞。
OCT·OCTA
OCT用于根据Horgan分级(1~5级)对ME进行定量评估,在 plaques 近距离放射治疗后4个月时即可通过OCT检测到1)。OCTA可无创地显示毛细血管脱落、无灌注区及FAZ的变化,对早期检测有用1)。
进行视力检查、视野检查和OCT视神经评估。随时间追踪视盘萎缩和视野缺损的进展。
由于眼底表现与糖尿病视网膜病变相似,需要进行鉴别。通过确认有无放射线照射史,通常容易鉴别。
眼底表现(微动脉瘤、出血、渗出、新生血管)两者相似。最重要的鉴别点是有无放射线照射史。此外,放射性视网膜病变一旦发病,进展比糖尿病视网膜病变更快,且照射后半年至数年的时间过程具有特征性。两病合并时管理尤为困难。
典型的后囊下白内障,当混浊直径超过2mm时,视功能下降,需要手术。白内障手术有望改善视力。
预防方面,对于医护人员或从事放射线工作的人员,使用含铅玻璃或含铅丙烯酸制成的防护眼镜非常有用。
抗VEGF治疗(一线选择)
抗VEGF药物是目前RR治疗的一线选择。使用的药物包括贝伐珠单抗(IVB)、雷珠单抗和阿柏西普1)。也有使用高剂量雷珠单抗2mg的报道1)。
预防性抗VEGF给药旨在抑制放疗后RR的发生。一项纳入4项研究共2109例患者的荟萃分析显示以下结果2)。
推荐方案为IVB 1.25~1.5 mg,每4个月一次,持续24个月2)。一项为期48个月的预防性抗VEGF给药报告显示,最佳矫正视力显著改善:预防组0.54 logMAR,对照组2.00 logMAR5)。注意,VEGF抑制剂的玻璃体注射治疗放射性视网膜病变不在医保范围内。
Victor等人(2023年)对4项研究共2109例患者进行的荟萃分析证实,预防性IVB给药可显著减少斑块近距离放疗后的ME(50%)和RON(38%)2)。
激光光凝
对视网膜无血管区进行激光光凝,以预防视网膜新生血管和新生血管性青光眼。全视网膜光凝(PRP)用于增殖性RR,报告消退率为66%5)。局灶激光辅助用于ME。
局部类固醇给药
曲安奈德(TA)、地塞米松玻璃体内植入剂(DEX)和氟轻松(FA)用于抗VEGF治疗抵抗时的辅助治疗5)。玻璃体注射曲安奈德被认为可暂时减轻黄斑水肿并改善视力,但不在医保范围内。
增殖性RR的处理
玻璃体积血需行玻璃体切除术。牵拉性视网膜脱离也适用玻璃体切除术。NVG可能需要滤过手术或睫状体光凝术。没有有效方法阻止进展,预后通常较差。
基本上没有根治性治疗。对于尚未发生视神经萎缩的早期病例,全身类固醇、肝素等抗凝治疗以及高压氧治疗可能有一定作用。所有这些方法的证据均有限,需根据具体病例判断。
预防性给药推荐每4个月一次,持续24个月的方案2)。治疗性给药的持续时间根据疾病活动性而变化。在治疗抵抗的慢性病例中,可能需要超过72次注射6)。
晶状体是对放射线非常敏感的组织。具有高分裂能力的赤道部(生发区)晶状体上皮细胞受到放射线照射后,细胞内产生自由基,导致DNA损伤。晶状体蛋白——晶状体蛋白的结构发生变化,上皮细胞和有核晶状体纤维变性并向后移动,迷入至晶状体后囊中央部,从而产生混浊。这是临床上观察到的后囊下白内障特征性混浊模式的原因。
放射线导致视网膜损伤的核心机制是视网膜血管内皮细胞的选择性消失。增殖能力高的视网膜血管内皮细胞最易受损,脉络膜血管内皮也会受损。内皮细胞对放射线特别敏感,DNA损伤和凋亡导致毛细血管壁崩解。
病理进展遵循以下阶段:
晚期糖基化终末产物(AGE)的积累、周细胞消失和基底膜增厚也被认为有助于内皮损伤。这一机制与糖尿病视网膜病变相似,解释了为什么合并糖尿病的患者放射性视网膜病变风险增加。从照射到临床发病存在至少半年,尤其是2-3年的潜伏期。这反映了内皮细胞损伤积累和毛细血管闭塞在临床上显现所需的时间。
主要机制是血管内皮受损引起的缺血性视神经病变。对鼻窦肿瘤或颅底病变进行放射治疗后,视交叉或其前后的视神经发生缺血性改变,导致进行性视力下降。
Victor等人(2023)的荟萃分析是目前显示预防性抗VEGF给药有效性的最大规模证据,但纳入的研究多为观察性研究,需要通过随机对照试验(RCT)进一步验证2)。最佳给药间隔、药物和疗程的标准化也是未来的课题。
OCTA无需造影剂即可定量评估毛细血管脱落、FAZ扩大和毛细血管密度降低。从放疗后早期阶段即可检测无灌注区,其在放射性视网膜病变(RR)筛查和监测中的应用正在推进1)。
Kayabai等人(2025)报告了一例眼内肿瘤放疗后19年的53岁男性病例6)。OCT上观察到的洋葱环征(囊腔内胆固醇结晶的多层沉积)作为慢性、治疗抵抗性放射性视网膜病变的影像标志物受到关注,记录显示需要超过72次玻璃体内注射的长期病程。
brolucizumab、faricimab(血管生成素/VEGF双靶点)等下一代抗VEGF药物在RR中的应用正在研究中5)。它们有望作为现有药物耐药病例的替代选择。
除了传统的X线和伽马射线外,质子线和重离子线(碳离子线)治疗后放射性视网膜病变的风险评估也在进行中。即使剂量集中性高的粒子线治疗,如果视网膜包含在照射野内也可能发病,因此治疗计划中的视网膜剂量评估和术后监测是课题。
RR和放射性视神经病变(RON)可能在同一照射野同时发生。据报道,EBRT后RON的发生率约为2% 3),在RR和RON合并的病例中,视功能损害更为严重,因此,除眼底检查外,定期进行视野检查和OCT视神经评估已成为重要的研究课题。