非增殖性RR
微動脈瘤:視網膜微血管瘤散在分布。作為早期發現重要。
微血管擴張:不規則血管擴張和迂曲。螢光眼底血管攝影(FA)可清晰顯示。
視網膜出血:散在的點狀和火焰狀出血。
硬性滲出:脂質沉積所致的黃白色浸潤。
黃斑水腫(ME):對視力預後影響最大的表現。OCT上表現為囊樣水腫或瀰漫性水腫。
放射線眼損傷是放射線對眼組織造成損傷的總稱。主要類型包括放射性白內障、放射性視網膜病變和放射性視神經病變。
| 類型 | 靶組織 | 閾值劑量 | 發病時間 | 視力預後 |
|---|---|---|---|---|
| 放射性白內障 | 水晶體(赤道部上皮細胞) | 0.5 Gy 以下(ICRP 2011年修訂) | 曝露後數個月至數年 | 可透過手術改善 |
| 放射性視網膜病變 | 視網膜血管內皮細胞 | 35 Gy(有報告指出20 Gy也可能發生) | 照射後半年以上,尤其2~3年後 | 預後多不良 |
| 放射性視神經病變 | 視神經與視交叉 | 單次>2 Gy、總量>50 Gy時有風險 | 照射後3個月至數年 | 約半數無光感 |
放射性白內障由眼部輻射暴露引起。即使是低劑量暴露,長期白內障風險也會增加,核電廠事故緊急工作人員的暴露、醫療工作者的職業暴露、CT等醫療暴露等,長期來看也會成為白內障的風險。
放射性視網膜病變(Radiation Retinopathy; RR)是眼內腫瘤、眼眶或鼻竇腫瘤、顱內疾病等放射治療中視網膜進入照射野時發生的慢性進行性閉塞性視網膜微血管疾病。一項統合分析顯示,腦頭頸部腫瘤放療後RR盛行率約為6%,視神經病變約為2% 3)。包括遲發性病例在內的總體發生率約為17% 4)。
不同照射部位的發生率如下:
| 照射部位 | 發生率 |
|---|---|
| 眼眶 | 85.7% |
| 鼻竇 | 45.4% |
| 鼻咽 | 36.4% |
| 腦 | 3.1% |
放射性視神經病變在鼻竇腫瘤或顱底病變放療後罕見發生。好發部位是視交叉或其前後。
發生率因照射部位、劑量、分割方式和合併症而異。據報導,放射性視網膜病變的總發生率為17% 4),並非所有患者都會發病。放射性白內障即使低劑量也有長期風險,因此有輻射暴露史者定期進行眼科檢查非常重要。
輻射引起的晶狀體混濁始於後囊下中央的多色性細微點狀混濁和空泡。這些變化逐漸擴大,形成斑塊狀和顆粒狀混濁。同時,可能出現Y字縫分離的水隙。隨著進展,出現中央相對透明的環形後囊下混濁。進一步進展形成由前後兩層膜樣混濁組成的盤狀混濁,導致明顯的視功能下降。
放射性白內障所見的進展模式:
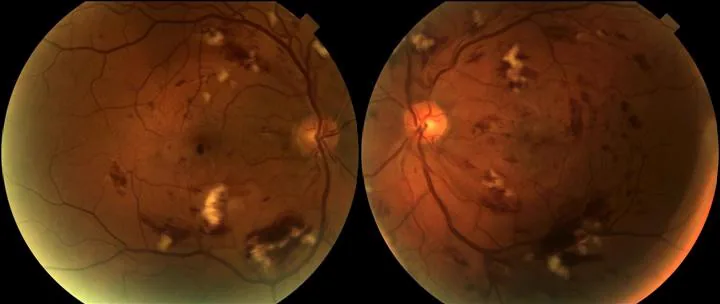
眼底所見類似於糖尿病視網膜病變,始於微動脈瘤、視網膜出血和硬性滲出,隨後出現棉絮斑。進展時出現視網膜新生血管,導致玻璃體積血。黃斑水腫和中心凹周圍毛細血管閉塞導致視力下降。一旦發病,進展比糖尿病視網膜病變更快。
放射性視網膜病變大致分為非增殖性和增殖性。
非增殖性RR
微動脈瘤:視網膜微血管瘤散在分布。作為早期發現重要。
微血管擴張:不規則血管擴張和迂曲。螢光眼底血管攝影(FA)可清晰顯示。
視網膜出血:散在的點狀和火焰狀出血。
硬性滲出:脂質沉積所致的黃白色浸潤。
黃斑水腫(ME):對視力預後影響最大的表現。OCT上表現為囊樣水腫或瀰漫性水腫。
增殖性RR
作為遲發性特殊表現,在17年後發病的病例中,OCT確認了囊腔內膽固醇結晶所致的洋蔥環徵(onion ring sign),作為慢性期治療抵抗的標誌物受到關注 6)。
此外,在30Gy全腦照射後16個月發生局限於上方視網膜的RR病例中,病變分布與照射野的30Gy等劑量線一致,證實即使在低劑量區域也表現出與照射野對應的發病模式 7)。
發病時間為照射後3個月至數年,視力進行性下降。機製為血管內皮損傷導致的缺血性視神經病變,約半數病例最終視力為無光感,視力預後不良。
照射後半年以上,特別是2~3年後發病較多。診斷時的中位時間為照射後39個月3),但也有17年後的遲發案例4)。照射後需要長期定期進行眼底檢查。
2011年,ICRP(國際放射防護委員會)修訂了閾值,建議對所有照射條件下導致視力下降的白內障,總照射劑量閾值定為0.5 Gy以下。對於職業照射,眼部照射上限從每年150 mSv改為5年內平均20 mSv,且單年不得超過50 mSv。
劑量閾值通常認為是35 Gy4)。超過45 Gy的照射容易發病,超過50 Gy則風險特別高3)。然而,在20~40 Gy的立體定向分割外照射後也觀察到遲發性放射性視網膜病變8),因此即使低於閾值劑量也需注意。
| 風險因素 | 內容 |
|---|---|
| 總劑量 | >35 Gy(閾值)4),超過45 Gy高風險 |
| 分割劑量 | 高分割照射 |
| 照射部位 | 眼眶或視交叉附近3) |
| 糖尿病 | 加重微血管脆弱性 |
| 合併化學治療 | 感受性增加 |
增殖性RR約占所有RR的3%至25% 5)。靠近視交叉的照射與RR發生有顯著相關性(p=0.009)3)。
單次照射劑量≤2Gy且總照射劑量≤50Gy被認為相對安全。近年來,伽瑪刀治療已成為主流,放射性視神經病變的發生率已顯著降低。
糖尿病是放射性視網膜病變的重要危險因子。糖尿病引起的微血管脆弱性與放射線引起的內皮損傷協同作用,即使在較低劑量下也可能發病。除了維持血糖控制外,建議放射治療後更頻繁地進行眼底檢查。
詳細詢問暴露史(劑量、類型、時間)很重要。使用裂隙燈顯微鏡確認後囊下混濁。應認為低劑量放射線暴露會加速水晶體的老化變化。由於年齡相關性白內障也會產生空泡、後囊下混濁、水裂和皮質淺層混濁,因此判斷老年水晶體的混濁是否由放射線引起並不容易。確認暴露史是鑑別的關鍵。
螢光素眼底血管造影(FA)與分期
FA是診斷和分期RR的基本檢查。早期可見視網膜毛細血管通透性增加,進展時毛細血管閉塞。小動脈也閉塞,導致視網膜無灌注區廣泛擴大,並產生視網膜新生血管。Amoaku FA分級(1-4級)被廣泛使用 1)。
| 分級 | 主要發現 |
|---|---|
| 1 | 微血管瘤、局部微血管擴張 |
| 2 | 微血管阻塞、廣泛血管異常 |
| 3 | 視神經盤或視網膜新生血管 |
| 4 | 玻璃體出血、牽引性視網膜剝離 |
靛氰綠(ICG)螢光血管攝影也可觀察到脈絡膜血管阻塞。
OCT·OCTA
OCT用於根據Horgan分級(1~5級)對ME進行定量評估,在 plaques 近接治療後4個月時可透過OCT檢測到1)。OCTA可非侵入性顯示微血管脫落、無灌流區域及FAZ的變化,對早期檢測有幫助1)。
進行視力檢查、視野檢查及OCT視神經評估。隨時間追蹤視神經盤萎縮及視野缺損的進展。
由於眼底所見與糖尿病視網膜病變相似,需要進行鑑別。透過確認有無放射線照射史,通常容易鑑別。
眼底所見(微動脈瘤、出血、滲出、新生血管)兩者相似。最重要的鑑別點是有無放射線照射史。此外,放射性視網膜病變一旦發病,進展比糖尿病視網膜病變更快,且照射後半年至數年的時間過程具有特徵性。兩病合併時管理尤為困難。
典型的後囊下白內障,當混濁直徑超過2mm時,視功能下降,需要手術。白內障手術有望改善視力。
預防方面,對於醫護人員或從事放射線工作的人員,使用含鉛玻璃或含鉛丙烯酸製成的防護眼鏡非常有用。
抗VEGF治療(第一線選擇)
抗VEGF藥物是目前RR治療的第一線選擇。使用的藥物包括貝伐珠單抗(IVB)、雷珠單抗和阿柏西普1)。也有使用高劑量雷珠單抗2mg的報導1)。
預防性抗VEGF給藥旨在抑制放療後RR的發生。一項納入4項研究共2109名患者的統合分析顯示以下結果2)。
建議方案為IVB 1.25~1.5 mg,每4個月一次,持續24個月2)。一項為期48個月的預防性抗VEGF給藥報告顯示,最佳矯正視力顯著改善:預防組0.54 logMAR,對照組2.00 logMAR5)。請注意,VEGF抑制劑的玻璃體內注射治療放射性視網膜病變不在健保給付範圍內。
Victor等人(2023年)對4項研究共2109例患者進行的統合分析證實,預防性IVB給藥可顯著減少斑塊近接治療後的ME(50%)和RON(38%)2)。
雷射光凝
對視網膜無血管區進行雷射光凝,以預防視網膜新生血管和新生血管性青光眼。全視網膜光凝(PRP)用於增殖性RR,報告消退率為66%5)。局部雷射輔助用於ME。
局部類固醇給藥
曲安奈德(TA)、地塞米松玻璃體內植入劑(DEX)和氟輕鬆(FA)用於抗VEGF治療抵抗時的輔助治療5)。玻璃體內注射曲安奈德被認為可暫時減輕黃斑水腫並改善視力,但不在健保給付範圍內。
增殖性RR的處理
玻璃體出血需行玻璃體切除術。牽引性視網膜剝離也適用玻璃體切除術。NVG可能需要濾過手術或睫狀體光凝術。沒有有效方法阻止進展,預後通常較差。
基本上沒有根治性治療。對於尚未發生視神經萎縮的早期病例,全身性類固醇、肝素等抗凝血治療以及高壓氧治療可能有一定作用。所有這些方法的證據均有限,需根據具體病例判斷。
預防性給藥建議每4個月一次,持續24個月的方案2)。治療性給藥的持續時間根據疾病活動性而變化。在治療抵抗的慢性病例中,可能需要超過72次注射6)。
水晶體是對放射線非常敏感的組織。具有高分裂能力的赤道部(生發區)水晶體上皮細胞受到放射線照射後,細胞內產生自由基,導致DNA損傷。水晶體蛋白——水晶體蛋白的結構發生變化,上皮細胞和有核水晶體纖維變性並向後移動,迷入至水晶體後囊中央部,從而產生混濁。這是臨床上觀察到的後囊下白內障特徵性混濁模式的原因。
放射線導致視網膜損傷的核心機制是視網膜血管內皮細胞的選擇性消失。增殖能力高的視網膜血管內皮細胞最易受損,脈絡膜血管內皮也會受損。內皮細胞對放射線特別敏感,DNA損傷和凋亡導致毛細血管壁崩解。
病理進展遵循以下階段:
晚期糖基化終產物(AGE)的積累、周細胞消失和基底膜增厚也被認為有助於內皮損傷。這一機制與糖尿病視網膜病變相似,解釋了為什麼合併糖尿病的患者放射性視網膜病變風險增加。從照射到臨床發病存在至少半年,尤其是2-3年的潛伏期。這反映了內皮細胞損傷積累和毛細血管閉塞在臨床上顯現所需的時間。
主要機轉是血管內皮受損引起的缺血性視神經病變。對鼻竇腫瘤或顱底病變進行放射治療後,視交叉或其前後的視神經發生缺血性變化,導致進行性視力下降。
Victor等人(2023)的統合分析是目前顯示預防性抗VEGF給藥有效性的最大規模證據,但納入的研究多為觀察性研究,需要透過隨機對照試驗(RCT)進一步驗證2)。最佳給藥間隔、藥物和療程的標準化也是未來的課題。
OCTA無需顯影劑即可定量評估微血管脫落、FAZ擴大和微血管密度降低。從放療後早期階段即可偵測無灌流區域,其在放射性視網膜病變(RR)篩檢和監測中的應用正在推進1)。
Kayabai等人(2025)報告了一例眼內腫瘤放療後19年的53歲男性病例6)。OCT上觀察到的洋蔥環徵(囊腔內膽固醇結晶的多層沉積)作為慢性、治療抵抗性放射性視網膜病變的影像標誌物受到關注,記錄顯示需要超過72次玻璃體內注射的長期病程。
brolucizumab、faricimab(血管生成素/VEGF雙重標靶)等下一代抗VEGF藥物在RR中的應用正在研究中5)。它們有望作為現有藥物抗藥病例的替代選擇。
除了傳統的X射線和伽瑪射線外,質子線和重粒子線(碳離子線)治療後放射性視網膜病變的風險評估也在進行中。即使劑量集中性高的粒子線治療,如果視網膜包含在照射野內也可能發病,因此治療計畫中的視網膜劑量評估和術後監測是課題。
RR和放射性視神經病變(RON)可能在同一照射野同時發生。據報導,EBRT後RON的發生率約為2% 3),在RR和RON合併的病例中,視功能障礙更為嚴重,因此,除眼底檢查外,定期進行視野檢查和OCT視神經評估已成為重要的研究課題。