主要危險因子
高血壓:51%~75%的患者合併,是最大的危險因子。持續性高血壓促進血管壁玻璃樣變性和動脈硬化9)。
動脈硬化:玻璃樣變性和膠原化導致血管壁脆弱。長期的血管壁損傷是擴張的基礎1, 9)。
年齡增長:好發於60歲以上人群。年齡增長相關的血管壁脆弱是背景因素。
女性性別:女性佔患者的70%~78%。性別差異的具體機制尚不清楚9)。

後天性視網膜動脈大動脈瘤(RAM)是發生在第三級分支以內視網膜動脈的囊狀或梭形局部擴張。常從視網膜動脈的分支處或動靜脈交叉處突出觀察到。RAM的滲出或出血導致形態變化和功能障礙。該疾病概念由Robertson於1973年首次報導。
典型大小為100-250μm 1, 3)。約50%發生在顳上動脈,約45%發生在顳下動脈,鼻側罕見 3)。雖然顳側多見,但也可發生在鼻側。多為單眼單發,但也有雙眼或多發的情況。常見於有高血壓和動脈硬化病史的老年人。
發生在視乳頭上的RAM佔所有病例的3.7-8%,是一種罕見情況 7, 10)。RAM具有自然消退的趨勢,這一點影響治療決策。
雖然是相對罕見的疾病,但隨著人口老化,遇到機會正在增加。視神經盤上的RAM更為罕見,據報告佔所有病例的3.7-8% 7, 10)。在出血型中,出血或滲出累及黃斑部會導致嚴重的視力障礙,因此早期診斷和處理很重要。
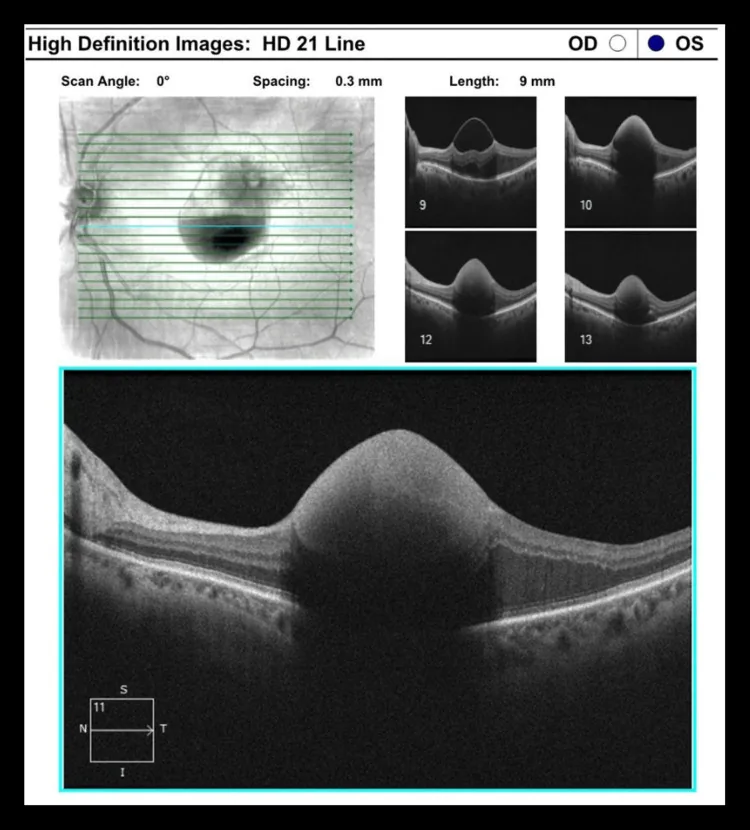
當滲出或出血累及黃斑部時,會導致視力下降和視物變形。如果沒有出血或滲出,則沒有自覺症狀,難以發現。
當出血或滲出波及黃斑部時,會出現以下症狀:
RAM在臨床上分為以下三種類型 3, 9)。
| 類型 | 主要症狀 | 典型所見 |
|---|---|---|
| 無症狀型 | 無 | 偶然發現 |
| 出血型 | 急性視力下降 | 多層出血 |
| 滲出型 | 緩慢視力下降 | 硬性滲出、水腫 |
RAM特徵性出血為多層性,涉及視網膜下、視網膜內、內界膜(ILM)下、視網膜前及玻璃體等多個層次9)。這種多層出血模式是RAM的特徵性表現之一。
眼底檢查時,沿視網膜小動脈呈紅色,伴有纖維蛋白時呈白色,纖維化時呈灰白色。出血或滲出可能導致動脈瘤無法識別。滲出型可見環形硬性滲出(環形視網膜病變)、視網膜水腫和漿液性視網膜剝離,動脈瘤周圍可伴有環形硬性滲出(環形視網膜病變)。
RAM的併發症包括破裂後黃斑裂孔形成7)和視網膜分支動脈阻塞10)。視盤上的RAM易早期發生玻璃體出血,需特別注意10)。
多層出血(涉及視網膜下、視網膜內和玻璃體等多個層次的出血)是RAM的特徵性表現,是診斷的重要線索9)。然而,當出血廣泛時,動脈瘤本身可能難以看清,因此IA、OCT或OCTA的輔助評估對診斷至關重要3)。
RAM的發生涉及多種促進血管壁脆弱的危險因子。多見於有高血壓和動脈硬化病史的老年人。被認為是因血管壁肌層喪失、中膜膠原纖維化導致彈性降低,從而引起腔內壓力擴張1, 9)。
主要危險因子
高血壓:51%~75%的患者合併,是最大的危險因子。持續性高血壓促進血管壁玻璃樣變性和動脈硬化9)。
動脈硬化:玻璃樣變性和膠原化導致血管壁脆弱。長期的血管壁損傷是擴張的基礎1, 9)。
年齡增長:好發於60歲以上人群。年齡增長相關的血管壁脆弱是背景因素。
女性性別:女性佔患者的70%~78%。性別差異的具體機制尚不清楚9)。
其他危險因子
血脂異常:促進動脈硬化進展,加重血管壁損傷1, 3)。
心血管疾病:據報導與冠狀動脈疾病和主動脈瘤相關。RAM可能作為全身血管病變的一部分發生9)。
林奇症候群:提示DNA修復基因突變可能導致血管網絡複雜化。這是首例與RAM相關的報導1)。
Valsalva動作:急劇的血壓波動可能誘發RAM破裂。重體力勞動、咳嗽、排便時屏氣等已被報導為誘因9)。
多模態影像對於RAM的準確診斷至關重要3)。尤其在出血較多時,僅憑FA可能難以確定瘤體本身,需要結合多種檢查。
最重要的鑑別診斷是年齡相關性黃斑部退化,其次是視網膜分支靜脈阻塞(BRVO)、糖尿病視網膜病變和Coats病。透過眼底檢查、FA和IA確認沿視網膜動脈是否存在瘤狀病灶。如果OCT未顯示視網膜色素上皮(RPE)隆起,則滲出性年齡相關性黃斑部退化的可能性較低。
| 檢查 | 主要發現 | 適應症/優點 |
|---|---|---|
| FA | 瘤狀過螢光及滲漏 | 標準診斷方法 |
| IA | 出血下的瘤體描繪 | 在出血病例中特別有用 |
| OCT | 球形高反射及水腫 | 視網膜層結構的定量 |
螢光眼底血管攝影(FA):動脈期可見RAM的瘤狀過螢光,晚期出現滲漏及組織染色。當螢光素滲漏或組織染色導致過螢光強烈時,判斷為動脈瘤血管壁通透性增加且具有活動性。此檢查有助於評估活動性,是標準診斷方法。
靛氰綠血管攝影(IA):在出血較多的情況下,IA比FA更優地檢測RAM 3)。由於靛氰綠從動脈瘤的螢光滲漏弱於螢光素,因此IA上出現過螢光提示活動性更高。
光學同調斷層掃描(OCT):將RAM顯示為內視網膜的高反射球形結構。可確認和量化視網膜水腫及漿液性視網膜剝離,並有助於出血部位(視網膜前或視網膜下)的分層。
光學同調斷層掃描血管攝影(OCTA):非侵入性顯示血流訊號。可顯示因血管壁剝離樣變化形成的壁內通道8)。
雷射斑點血流成像(LSFG):一種非侵入性定量評估血流的方法。平均模糊率(MBR)值與RAM消退相關,可用於監測治療過程5)。
近紅外線反射成像(NIR-R):有病例報告在發病前3年檢測到袖套樣血管壁增厚,提示其作為早期發現工具的潛力6)。
B型超音波:用於因玻璃體出血而無法看清眼底的情況7, 10)。可粗略評估眼內病變。
RAM的治療方針根據病變類型、對黃斑部的影響以及自然消退趨勢決定。雖然存在自然緩解的可能,但黃斑部持續滲出或出血的程度決定了視功能障礙的程度和恢復情況。
分步治療方法:
保守治療
觀察:由於存在自然消退趨勢,適用於黃斑部未受累或無症狀的病例。定期進行眼底檢查追蹤。
藥物治療:卡巴克絡(阿度那錠30mg)3錠,分3次服用。這是一種輔助治療,旨在抑制血管通透性增加和止血。
危險因子管理:嚴格控制血壓和血脂對於預防復發和控制病情至關重要。
侵入性治療
雷射光凝:目的是促進動脈瘤通透性增加或破裂的管壁癒合。應輕輕燒灼動脈瘤表面,避免阻塞動脈,無需重複照射直至整個動脈瘤出現灰白色凝固斑。參考參數:光斑大小300–500μm,曝光時間0.2–0.3秒,功率120mW以上。併發症包括動脈阻塞風險。
玻璃體內抗VEGF注射:用於滲出性RAM。在日本不屬於健保給付範圍2, 3, 4)。
玻璃體切除術:當血液積聚在內界膜和神經纖維層之間時,進行伴有內界膜剝離的玻璃體切除術。持續性玻璃體出血也是玻璃體切除術的適應症。
間接凝固:一種凝固動脈瘤周圍視網膜,使滲漏遠離黃斑的技術。常與直接凝固合併使用。
雷射合併抗VEGF治療:一項3例病例研究報告,平均中央視網膜厚度(CRT)減少275.7μm,視力改善0.55 logMAR4)。
Nd:YAG雷射:用於引流內界膜下出血。建議早期實施9)。
玻璃體內注氣(血腫移位術):適用於黃斑部視網膜下出血出現2週內。出血已機化則不適合。注入SF6或C3F8 0.2–0.8mL,術後需俯臥1–2週。合併tPA(組織型纖溶酶原激活劑)可增強黃斑下血腫的移位效果。
閾下雷射:據報導與傳統雷射療效相當,但併發症較少9)。
RAM有自然消退的傾向,許多無症狀病例僅透過觀察即可改善。然而,當出血或滲出累及黃斑部時,會影響視力預後,因此需要考慮積極的治療介入。自然病程與治療介入的選擇需綜合疾病類型、疾病活動度和患者背景來判斷。
RAM的病理生理核心是血管壁結構變性和腔內壓增高。高血壓和動脈硬化導致血管壁脆弱化,動脈壁通透性增高引起的滲漏和破裂導致的出血引起視功能障礙。
血管壁變性過程:高血壓引起的玻璃樣變性和動脈硬化損害血管壁肌層,導致中膜膠原纖維化進展 9)。結果,血管壁彈性降低,對腔內壓的抵抗力喪失,發生局部擴張 1, 9)。
Gass假說:動脈粥樣硬化栓塞損傷血管壁,引起局部缺血,導致VEGF表現上調。結果促進通透性增高和血管擴張 2)。VEGF透過內皮NO產生引起動脈擴張和通透性增高,參與滲出型RAM的病理過程 3)。
剝離樣變化:使用自適應光學掃描雷射檢眼鏡(AOSLO)、OCT和OCTA的詳細觀察報告了血管壁出現裂紋、形成壁內通道的病理 8)。從該壁內通道可能在鄰近部位形成新的RAM。
破裂機轉:當腔內壓超過脆弱血管壁的閾值時發生破裂 9)。Valsalva動作(咳嗽、重體力勞動、排便時屏氣等)引起的血壓急劇升高可能誘發破裂 9)。
Meng Y等人回顧了以Valsalva動作誘發的RAM破裂病例,討論了腹腔內壓急劇升高導致靜脈壓和動脈壓迅速上升,從而使脆弱血管壁破裂的機制 9)。
血-視網膜屏障破壞:在滲出型RAM中,血-視網膜屏障的損傷是黃斑水腫和硬性滲出的基礎 15)。
視神經盤上RAM的特性:視盤附近的動脈口徑大、血流速度快。因此,壁應力大,容易早期發生玻璃體出血 10)。
自適應光學掃描雷射檢眼鏡(AOSLO)的微結構分析:使用AOSLO進行詳細觀察,可視化了RAM內搏動消失、血栓形成過程和血管壁裂隙結構8)。這揭示了血管壁剝離樣變化這一新病理狀態,加深了對發病機制的理解。
雷射斑點血流成像(LSFG)的縱向評估:據報導,隨著RAM消退,平均模糊率(MBR)從6.8 AU顯著下降至1.1 AU5)。LSFG的無創血流監測有望成為治療效果的客觀評估工具。
Hanazaki H等人使用LSFG縱向評估了接受治療的RAM患者的眼部血流,並顯示MBR的下降與RAM消退相關5)。
近紅外反射成像(NIR-R)的早期檢測:有病例報告在RAM臨床顯現前3年,NIR-R影像上檢測到袖套樣血管壁增厚6)。這提示其作為高血壓患者預測因子的可能性,並有望應用於早期篩檢工具。
雷射聯合抗VEGF治療的有效性:在一項3例病例系列研究中,聯合聚焦雷射光凝和玻璃體內貝伐珠單抗治療後,平均中央視網膜厚度(CRT)減少275.7 μm,視力改善0.55 logMAR4)。提示抗VEGF的血管穩定作用和雷射的血管壁修復具有協同效應,期待未來大規模試驗。
閾下雷射:與傳統閾值雷射相比,通過熱休克蛋白介導的亞致死性視網膜溫熱療法可在減少併發症的同時獲得同等效果9)。
Lynch症候群與RAM的關聯:首次報導了具有DNA修復基因突變的Lynch症候群患者發生RAM1)。提示DNA修復基因突變可能使血管網絡複雜化,VEGF-A表現升高可能促進RAM的發生。
治療指南的必要性:隨著治療方法的多樣化,需要制定基於實證醫學的臨床實踐指南9)。
多層出血和非侵入性影像評估的病例積累:破裂的RAM可表現為視網膜下、視網膜內和玻璃體等多層出血11)。合併玻璃體下出血的病例中,Nd:YAG雷射或玻璃體手術的適應症判斷至關重要12)。近紅外反射視頻成像用於評估RAM的搏動性,OCTA用於病變內血流的無創評估13, 14)。
病例報告和小型系列研究報告了玻璃體內注射抗VEGF藥物對滲出性RAM的有效性2, 3, 4)。特別是與雷射聯合治療時,已獲得有希望的結果4)。然而,在日本這不在保險給付範圍內2),且尚未進行大規模隨機試驗。使用前需要與主治醫師充分討論。