第1~2期
第1期:仅见视网膜毛细血管扩张,不伴渗出。
Stage 2A:除毛细血管扩张外,在中心凹外可见渗出物。
Stage 2B:渗出物累及中心凹。视力下降变得明显。

Coats病是1908年由George Coats报告的特发性视网膜血管疾病。其本质是视网膜毛细血管异常扩张(毛细血管扩张症)以及血管壁向视网膜内和视网膜下渗出物积聚。
该病为散发性、非遗传性,与全身疾病或家族史无关1)。发病率约为每10万人0.09例,十分罕见2)。约75%的患者为男性,95%为单眼发病,好发于20岁以下(平均约5岁)。
成人发病非常罕见,但呈现与儿童型不同的临床特征。成人发病病例比儿童型症状轻、进展缓慢,治疗反应也良好3)。某报告显示,48只成人发病眼中仅21%发生渗出性视网膜脱离,显著低于儿童发病的81%3)。
轻型也称为Leber粟粒状血管瘤病,构成Coats病谱系的一部分。1型特发性黄斑毛细血管扩张症也被认为属于同一疾病谱系。
已有35岁以上发病的病例报告,被认定为成人发病型Coats病3)。与儿童型相比,病变进展缓慢,渗出性视网膜脱离的发生频率低,治疗反应通常良好。但发病本身罕见,在成人中发现类似表现时,与其他疾病的鉴别很重要。
婴幼儿期发病时,患儿自身很少主诉症状。
成人发病病例视力相对保持较好,有时在体检中偶然发现3)。
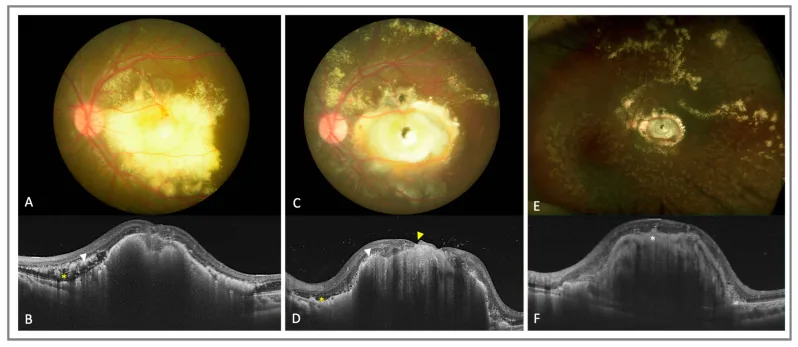
眼底所见特征为集中于周边部的异常扩张视网膜血管,以及黄白色视网膜下和视网膜内渗出物的蓄积。荧光眼底造影显示周边部视网膜血管闭塞、毛细血管扩张、毛细血管瘤、新生血管等特征性表现。病情进展可导致渗出性视网膜脱离,最终发展为全脱离。超声检查、CT、MRI显示视网膜下液均匀分布,这一点与伴有钙化的不均匀影像的视网膜母细胞瘤是重要的影像学鉴别点。
后期可出现虹膜红变和新生血管性青光眼等眼前节并发症。黄斑裂孔是罕见并发症,文献中仅报道约7例4)。纤维性结节是视力预后不良的因素,OCTA显示结节内存在3型新生血管(SVC→DVC→无血管复合体)5)。
Shields分类将Coats病的病程分为以下5期。用于选择治疗方案和预后评估。
第1~2期
第1期:仅见视网膜毛细血管扩张,不伴渗出。
Stage 2A:除毛细血管扩张外,在中心凹外可见渗出物。
Stage 2B:渗出物累及中心凹。视力下降变得明显。
Stage 3
Stage 3A1:伴有中心凹外的次全视网膜脱离。
Stage 3A2:伴有累及中心凹的次全视网膜脱离。视力预后不良。
Stage 3B:发生全视网膜脱离。需要紧急干预。
Stage 4~5
Stage 4:全视网膜脱离合并继发性青光眼,为终末期前阶段。可能伴有疼痛。
Stage 5:终末期。眼球痨(萎缩)。可考虑眼球摘除。
多种疾病可表现为白瞳症,Coats病只是其中之一。最重要的鉴别诊断是视网膜母细胞瘤(Rb),因其直接关系到生命预后,需要紧急评估。其他鉴别诊断包括早产儿视网膜病变、永存原始玻璃体增生症(PHPV)、眼内炎等。详见“诊断与检查方法”一节。
Coats病的发病原因不明,未发现与全身性疾病或家族史有关。有报告提示遗传背景,如第3、13号染色体不稳定,以及与NDP基因(Norrie病相关)、CRB1基因的关联,但尚未确立。
作为病理的起点,内血-视网膜屏障(iBRB)的破坏被认为起着核心作用1)。周细胞(支持血管内皮的细胞)减少导致血管壁脆弱,形成异常扩张的毛细血管和动脉瘤1)。血浆成分渗漏并积聚在血管壁内和视网膜层内,导致血管壁增厚,进一步加重渗出,形成恶性循环2)。
高VEGF环境也被认为促进周边毛细血管扩张2),这一机制构成了抗VEGF治疗的理论基础。
诊断需结合多种检查,其中最关键的是与视网膜母细胞瘤(Rb)的鉴别。
散瞳下眼底检查可见周边部迂曲的异常血管网和黄白色视网膜下渗出物。渗出物累及黄斑时呈硬性白斑样外观。
这是诊断Coats病最重要的检查之一。特征性表现包括毛细血管显著扩张、毛细血管瘤、动静脉吻合以及“灯泡样”荧光渗漏。对于确定异常血管范围和激光光凝部位至关重要。
确认无实体肿块。Rb在B超中常显示实体肿块内高回声(钙化),而Coats病不形成实体肿块。
评估有无钙化。Rb常伴有钙化,而Coats病不发生钙化。这一发现是鉴别诊断的重要依据。
Coats病与视网膜母细胞瘤的主要鉴别点如下所示。
| 项目 | Coats病 | 视网膜母细胞瘤 |
|---|---|---|
| 好发年龄 | 5岁左右 | 1~2岁 |
| 性别差异 | 男性75% | 无 |
| 双眼性 | 约5% | 约40% |
| 钙化 | 无 | 有(高概率) |
| 实性肿块 | 无 | 有 |
| 超声 | 视网膜下液体积聚 | 实性肿块、内部钙化、后方声影 |
| MRI | 视网膜下液均匀 | 不均匀(肿块信号) |
其他鉴别诊断包括视网膜血管瘤、von Hippel-Lindau病、永存原始玻璃体增生症(PHPV)、家族性渗出性玻璃体视网膜病变(FEVR)、弓蛔虫病、血管增生性肿瘤、Eales病等。
治疗目标是闭塞异常血管,停止渗出物的产生。根据疾病分期采取逐步治疗策略。
这是一线治疗。通过FA确认的异常扩张血管和微动脉瘤直接进行光凝,同时对周围的无灌注区域也进行光凝。在儿童中,需在全身麻醉下进行。通常需要多次治疗,治疗后需定期通过FA重新评估并重复追加光凝。
这是用于前部周边病变或光凝困难部位的后续选择。有时会与光凝联合使用。
激光光凝
适应症:1至3A期的异常血管和渗出性病变。
方法:在FA引导下直接光凝毛细血管扩张区域和无灌注区。儿童在全身麻醉下进行。
特点:可重复进行。治疗后定期FA重新评估和追加光凝是标准管理。
冷冻凝固
适应症:光凝困难的前部周边病变,以及3B期以下重症病例的辅助治疗。
方法:经巩膜应用冷冻探头,凝固并闭塞异常血管。
特点:在混浊介质或最周边部也可施行。
玻璃体视网膜手术
适应症:3B期(全视网膜脱离)及以上,冷冻凝固无效的病例。
方法:通过外部引流或玻璃体手术引流视网膜下液,并进行内部视网膜复位8)。重症病例可联合视网膜下液引流和巩膜扣带术。
特点:对于合并黄斑裂孔的病例,有报道内界膜(ILM)翻转术有效4)。
抗VEGF药物用于Coats病尚未达成共识,不是标准治疗,而是作为与光凝联合使用的辅助治疗。
有报告称,一例成人发病的Coats病患者接受了雷珠单抗0.5mg玻璃体内注射联合激光光凝治疗,最终矫正视力从指数提高到20/603)。
在一例儿童病例中,每6周在全身麻醉下进行贝伐珠单抗1.25mg玻璃体内注射、Tenon囊下曲安奈德和激光联合治疗,有报告指出治疗后可能出现反常性渗出性视网膜病变2)。
也有报告称布罗鲁珠单抗对贝伐珠单抗耐药病例有效2)。抗VEGF治疗可能有助于预防纤维结节形成5)。
对于疼痛性失明眼(4~5期)且难以排除视网膜母细胞瘤时,选择眼球摘除。
Coats病中,有些病例在数年内复发或再次脱离,也有双眼发病时间不同的病例。治疗完成后也需要定期进行荧光眼底造影重新评估,如果发现新病变,需要追加光凝或冷冻治疗。
目前,关于抗VEGF药物用于Coats病尚未达成共识,不被视为标准治疗。虽然作为激光光凝的辅助联合疗法的报告正在积累,但其有效性和安全性评估仍需进一步研究。
Coats病的核心发病机制是内血-视网膜屏障(inner blood-retinal barrier; iBRB)的破坏1)。
iBRB由视网膜毛细血管内皮细胞和支持它们的周细胞构成。在Coats病中,周细胞数量显著减少,导致血管内皮支持功能下降1)。免疫染色和电子显微镜观察已证实内皮细胞本身的数量也减少1)。
内皮BRB的破坏导致血浆成分(主要是脂蛋白和胆固醇)渗漏并积聚在血管壁内、视网膜内和视网膜下1)。积聚的脂质引发含脂巨噬细胞(泡沫细胞)的浸润和肉芽肿性免疫反应,加剧组织损伤1)。
高VEGF环境促进周边毛细血管进一步扩张,参与病变进展2)。OCTA观察显示,在晚期病变的黄斑纤维结节内存在3型新生血管(按SVC→DVC→无血管复合体的顺序形成)5),对新生血管形成过程的认识正在深入。
黄斑裂孔形成的机制被认为是周边激光光凝导致视网膜缩短,产生切线方向牵引,从而在黄斑部造成穿孔4)。
OCTA使得无创评估纤维结节内的微血管结构成为可能。
Ong等人(2021)利用OCTA详细分析了黄斑结节内的血管结构,揭示了按SVC→DVC→无血管复合体顺序形成的3型新生血管的存在5)。这一发现对于阐明结节形成机制以及作为抗VEGF治疗的靶点具有重要意义。
有报道称在抗VEGF治疗开始后出现矛盾性渗出加重现象,需要阐明机制并建立管理方法。
Kalavar等人(2022)报告了一例儿童Coats病在治疗开始后出现一过性渗出加重和黄斑星芒状渗出的病例2)。对于bevacizumab抵抗的病例,使用brolucizumab有效,作为新的治疗选择受到关注2)。
Nawrocka等人(2023)报告了一例对Coats病合并黄斑裂孔采用内界膜翻转瓣法进行玻璃体手术的病例4)。术后18个月确认黄斑裂孔闭合,最终矫正视力为20/40。Coats病相关黄斑裂孔在PubMed上仅报告约7例,是一种罕见的并发症4)。
Shields等人(2019)分析了351眼、45年的Coats病病例,显示不同年代的治疗效果有所改善9)。Dalvin等人(2019)按年龄类别分析了同一队列,显示儿童发病病例比成人发病病例病变更易加重,视力预后更差10)。
成人发病Coats病是传统上被低估的疾病概念,报告数量正在增加3)。与儿童型的临床差异(轻症、缓慢进展、治疗反应良好)正在整理中,建立成人适当的治疗方案成为课题。