血管痉挛期
全身性小动脉狭窄:动静脉直径比(AVR)从正常的2:3减小1)3)。
局灶性小动脉狭窄:表现为管径不均1)3)。
血管痉挛:在年轻人和继发性高血压中明显。通过适当降压可以改善的阶段。

高血压视网膜病变(Hypertensive Retinopathy)是全身性动脉高血压导致视网膜微血管和视网膜神经纤维层受损的疾病。高血压定义为SBP≥140 mmHg和/或DBP≥90 mmHg 1)。根据2017年ACC/AHA标准,进一步分为血压升高(120~129/<80 mmHg)、1期(130~139/80~89 mmHg)和2期(≥140/≥90 mmHg)。
全球高血压患者超过14亿,每年有超过1000万人死于高血压相关疾病 1)。预计到2025年将超过15亿 1)。高血压视网膜病变在40岁以上非糖尿病人群中检出率为6%~15% 1)3),在所有高血压患者中为30.6%~51% 3)9)。约50%的美国成年人患有高血压 7),眼底改变患病率很高。慢性高血压引起的动脉硬化性改变在无症状中进展,常在健康体检中发现。
病理生理涉及两个过程。急性血管痉挛性改变在年轻人和继发性高血压中显著,通过适当降压可逆性改善。慢性动脉硬化性改变在长期高血压的中老年患者中占主导,且不可逆。
本病最早由Marcus Gunn于19世纪末描述。20世纪30年代,Keith-Wagener-Barker(KWB)分类法确立,至今仍被广泛使用1)。高血压视网膜病变不仅是眼科表现,也是心血管疾病和脑卒中的重要独立风险指标。
有报道称继发性高血压的病因可触发眼底改变。嗜铬细胞瘤中,恶性高血压和视网膜病变可能是首发症状5)。IgA肾病可合并Purtscher样视网膜病变8)。Goodpasture综合征4)和结核病6)也有通过继发性高血压导致视网膜病变的病例报道。
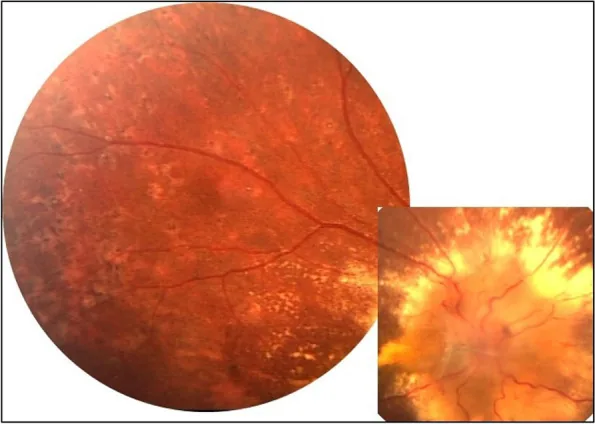
慢性高血压引起的动脉硬化性改变本身通常无症状。在以下情况下会出现症状:
高血压视网膜病变的眼底所见根据病期呈现特征性变化。血管痉挛期、硬化期和渗出期三个阶段依次进展。
血管痉挛期
全身性小动脉狭窄:动静脉直径比(AVR)从正常的2:3减小1)3)。
局灶性小动脉狭窄:表现为管径不均1)3)。
血管痉挛:在年轻人和继发性高血压中明显。通过适当降压可以改善的阶段。
硬化期
血柱反射增强:动脉的光反射带变宽,进展为铜丝动脉和银丝动脉1)3)。
动静脉交叉征(AV nicking):在动静脉交叉处静脉被压迫和狭窄1)3)。这是当前和过去血压持续性的指标1)。在交叉处可见静脉偏转(Salus征)、交叉两侧静脉变细(Gunn征)和静脉直角偏转(Bonnet征)。
硬化性改变:由于内膜增厚、中膜增生和玻璃样变性导致的不可逆变化。
渗出期
出血:火焰状出血、点状出血和斑片状出血1)3)。
白斑:硬性白斑(脂蛋白沉积)和软性白斑(神经纤维层梗死)1)3)。在恶性高血压中,硬性白斑在黄斑部呈放射状排列,形成星芒状白斑(macular star)。
视乳头水肿:恶性高血压中出现的严重表现1)。可能伴有Elschnig斑2)。
Elschnig斑是由于脉络膜小动脉的纤维蛋白样坏死导致视网膜色素上皮(RPE)损伤而形成的黄白色病变2)7)。在OCTA上,它们在脉络膜毛细血管层表现为低信号斑点2)。
在OCTA上,观察到浅层和深层毛细血管丛的逐渐变细模式(血管向末梢变细)的破坏以及中心凹无血管区(FAZ)扩大2)。表层血管丛(SVP)的血管密度降低也是特征性表现1)。
SD-OCT可检测到视网膜增厚、视网膜下液(SRF)和视网膜内高反射沉积物2)5)。
有报道称恶性高血压患者中观察到2+以上的玻璃体细胞7)。有时需要与眼内炎、葡萄膜炎进行鉴别。
代表性分类有KWB分类(I~IV级):I级:轻度小动脉狭窄、硬化;II级:明显狭窄、动静脉交叉征;III级:出血、渗出、视网膜水肿;IV级:视乳头水肿。Scheie分类独立评估高血压性改变(H1~4)和动脉硬化性改变(S1~4)。Wong-Mitchell分类(2004年)分为无、轻度、中度、重度四级,用于现代流行病学研究。基于OCT的新分类提出三种类型:①轻度至中度,②无SRF的恶性,③有SRF的恶性1)。
高血压视网膜病变的发生以高血压本身为必要条件,以下因素通过高血压增加视网膜病变风险。
已鉴定出与视网膜血管直径相关的SNPs:中心视网膜静脉等效直径(CRVE)涉及8个SNPs,中心视网膜动脉等效直径(CRAE)涉及2个SNPs1)。
小动脉狭窄不仅是高血压的结果,也可能是原因。一项针对10,229人的荟萃分析显示,视网膜小动脉狭窄与未来10年内发生高血压的风险相关1)。
一项针对12,603人的荟萃分析报告,降压药的不依从率高达45.1%1)。依从性差直接导致眼底病变的长期进展。
常通过内科的眼底检查申请发现,有时视力下降会揭示肾脏疾病或继发性高血压。初诊时通过血压测量和血液检查确诊。
眼底检查是诊断的基础。由于直接检眼镜观察者间变异较大,推荐使用散瞳下的裂隙灯眼底检查或眼底照相机1)。
KWB分级是高血压视网膜病变的经典严重程度分级。
| KWB组 | 主要表现 | 临床意义 |
|---|---|---|
| I组 | 轻度小动脉狭窄、光反射亢进 | 轻度高血压 |
| II组 | 明显狭窄、动静脉交叉征 | 持续性高血压 |
| III组 | 出血、渗出、视网膜水肿 | 重度高血压 |
| IV组 | III组 + 视乳头水肿 | 恶性高血压 |
Scheie分类通过独立评估高血压性变化(H1~H4)和动脉硬化性变化(S1~S4),可以区分血压的急性影响和慢性硬化变化。
| Scheie分级 | 评估对象 | 主要表现 |
|---|---|---|
| H(高血压性)1~4 | 血管痉挛 | 局灶性狭窄→弥漫性狭窄→出血和渗出→视乳头水肿 |
| S(硬化性)1~4 | 动脉硬化 | 光反射增强→铜丝动脉→银丝动脉→玻璃样变性 |
需要与糖尿病视网膜病变(双侧软性渗出、硬性渗出、新生血管)、放射性视网膜病变、贫血性视网膜病变、眼缺血综合征、视网膜静脉阻塞相鉴别。IgA肾病中已有与Purtscher样视网膜病变重叠的报道8)。
OCTA无需造影剂即可分层显示视网膜和脉络膜血管层。在高血压视网膜病变中,可定量评估浅层和深层毛细血管丛的血管密度及FAZ面积,比传统荧光素眼底血管造影更详细地检测缺血区域和Elschnig斑(脉络膜毛细血管层的低信号斑点)1)2)。无创且适合重复随访评估。
高血压视网膜病变治疗的根本是全身血压管理。对于恶性高血压的紧急降压,建议在最初1小时内将平均动脉压(MAP)降低10-15%,并在24小时内控制在基线的25%以内。急剧降压会导致视网膜、脑和肾脏缺血,因此禁忌。目标是在2-3个月内达到SBP<130 mmHg、DBP<80 mmHg。
厄贝沙坦+阿替洛尔+氨氯地平三联疗法持续10个月后,报告显示KWB IV级改善至I级,改善4个级别1)。
继发性高血压的特异性治疗也很重要。在嗜铬细胞瘤中,使用拉贝洛尔持续静脉输注(0.25 mg/kg/h)紧急降压后,行腹腔镜肾上腺切除术的病例获得了最佳矫正视力20/20的完全恢复5)。
通过血压控制,出血和软性渗出可在约3个月内消失4)。另一方面,动静脉交叉征和动脉狭窄往往不可逆地残留。多数情况下,随着肾功能的改善而减轻,但硬性渗出沉积和视网膜色素上皮萎缩导致的不可逆损伤可能残留。需要与内科定期协作确认全身状况。
Khojasteh等人(2021)报告了对中心凹视网膜内积血行23G微切口玻璃体手术(MIVS)+41G针直接引流积血+内界膜(ILM)瓣技术后,最佳矫正视力从20/400改善至20/509)。
能否改善取决于病期。血管痉挛期的改变(小动脉狭窄、出血、软性渗出)通过适当降压可在数周至3个月内改善4)。而慢性高血压引起的动脉硬化性改变(铜丝/银丝动脉、动静脉交叉征)基本不可逆,降压后仍残留。详见“病理生理学·详细发病机制”一节。
高血压性视网膜病变可理解为视网膜血管对管腔内压升高的阶段性反应。
管腔内压升高激活自身调节机制,导致小动脉痉挛1)3)。平均动脉压每升高10 mmHg,视网膜小动脉直径减少约3 μm1)。此阶段的改变是可逆的。
持续性高血压导致内膜增厚、中膜平滑肌增殖和玻璃样变性1)3)。中膜平滑肌细胞变性坏死及中膜外膜纤维性肥厚引起器质性狭窄,眼底表现为血柱反射增强(铜丝动脉→银丝动脉)和动静脉交叉征。硬化的动脉压迫周围静脉,增加静脉血栓风险。
血-视网膜屏障破坏导致血浆成分渗漏至视网膜,引起出血、硬性渗出和软性渗出1)3)。纤维素样坏死是最严重的变化3);脉络膜小动脉的纤维素样坏死导致脉络膜毛细血管节段性梗死,形成Elschnig斑2)。慢性肾衰竭末期可发生脉络膜循环障碍,外血-视网膜屏障破坏,引起视网膜下渗出和浆液性视网膜脱离。随着毛细血管闭塞进展,出现微动脉瘤、静脉管径不均和血管吻合;罕见情况下出现视网膜无灌注区和新生血管,导致增殖性视网膜病变。
视网膜血管具有血-视网膜屏障、缺乏交感神经支配和血流自身调节功能的特点3)。这些特性决定了其对全身和局部血压变化的反应。
根本预防是将血压控制在正常范围内。定期测量家庭血压、减盐、适度运动、戒烟、限酒等生活方式的改善是有效的。持续服用处方的降压药也很重要,荟萃分析显示不依从率高达45.1%,这是一个挑战1)。定期眼底检查可以在无症状阶段发现病变,早期干预可以防止进展为不可逆变化。
自适应光学(AO)与OCT/OCTA的融合使得在活体中测量视网膜小动脉的壁腔比(WLR)成为可能1)。微血管密度的量化作为高血压视网膜病变的早期诊断标志物正在研究中2)。OCTA在缺血区域和Elschnig斑的详细可视化方面优于FA2),有望成为非侵入性的病情评估工具。
血清尿酸(SUA)、海蟾蜍精(marinobufagenin)和GlycA被评估为高血压视网膜病变的预测生物标志物1)。基因研究中已鉴定出与视网膜血管直径相关的SNPs,可能有助于早期发现遗传高风险人群1)。
使用BPH/2J小鼠(遗传性高血压模型)的研究详细分析了视网膜血管的自身调节机制1)。由于与人类高血压视网膜病变的同源性,这些模型被用于新疗法的临床前评估。