血管痙攣期
全身性小動脈狹窄:動靜脈直徑比(AVR)從正常的2:3減少1)3)。
局部性小動脈狹窄:表現為管徑不均1)3)。
血管痙攣:在年輕人和次發性高血壓中明顯。經適當降壓可改善的階段。

高血壓視網膜病變(Hypertensive Retinopathy)是全身性動脈高血壓導致視網膜微血管和視網膜神經纖維層受損的疾病。高血壓定義為SBP≥140 mmHg和/或DBP≥90 mmHg 1)。根據2017年ACC/AHA標準,進一步分為血壓升高(120~129/<80 mmHg)、第1期(130~139/80~89 mmHg)和第2期(≥140/≥90 mmHg)。
全球高血壓患者超過14億,每年有超過1000萬人死於高血壓相關疾病 1)。預計到2025年將超過15億 1)。高血壓視網膜病變在40歲以上非糖尿病人群中檢出率為6%~15% 1)3),在所有高血壓患者中為30.6%~51% 3)9)。約50%的美國成年人患有高血壓 7),眼底變化患病率很高。慢性高血壓引起的動脈硬化性變化在無症狀中進展,常在健康檢查中發現。
病理生理涉及兩個過程。急性血管痙攣性變化在年輕人和繼發性高血壓中顯著,通過適當降壓可逆性改善。慢性動脈硬化性變化在長期高血壓的中老年患者中佔主導,且不可逆。
本病最早由Marcus Gunn於19世紀末描述。1930年代,Keith-Wagener-Barker(KWB)分類法確立,至今仍被廣泛使用1)。高血壓視網膜病變不僅是眼科表現,也是心血管疾病和腦中風的重要獨立風險指標。
有報告指出繼發性高血壓的病因可觸發眼底變化。嗜鉻細胞瘤中,惡性高血壓和視網膜病變可能是首發症狀5)。IgA腎病可合併Purtscher樣視網膜病變8)。Goodpasture症候群4)和結核病6)也有通過繼發性高血壓導致視網膜病變的病例報告。
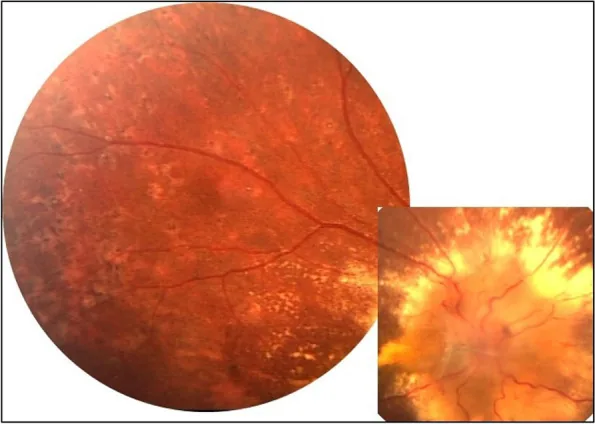
慢性高血壓引起的動脈硬化性改變本身通常無症狀。在以下情況下會出現症狀:
高血壓視網膜病變的眼底所見根據病期呈現特徵性變化。血管痙攣期、硬化期和滲出期三個階段依次進展。
血管痙攣期
全身性小動脈狹窄:動靜脈直徑比(AVR)從正常的2:3減少1)3)。
局部性小動脈狹窄:表現為管徑不均1)3)。
血管痙攣:在年輕人和次發性高血壓中明顯。經適當降壓可改善的階段。
硬化期
血柱反射增強:動脈的光反射帶變寬,進展為銅線動脈和銀線動脈1)3)。
動靜脈交叉現象(AV nicking):在動靜脈交叉處靜脈被壓迫和狹窄1)3)。這是當前和過去血壓持續性的指標1)。在交叉處可見靜脈偏轉(Salus徵)、交叉兩側靜脈變細(Gunn徵)和靜脈直角偏轉(Bonnet徵)。
硬化性變化:由於內膜增厚、中膜增生和玻璃樣變性導致的不可逆變化。
滲出期
出血:火焰狀出血、點狀出血和斑片狀出血1)3)。
白斑:硬性白斑(脂蛋白沉積)和軟性白斑(神經纖維層梗塞)1)3)。在惡性高血壓中,硬性白斑在黃斑部呈放射狀排列,形成星芒狀白斑(macular star)。
視乳頭水腫:惡性高血壓中出現的嚴重表現1)。可能伴有Elschnig斑2)。
Elschnig斑是由於脈絡膜小動脈的纖維蛋白樣壞死導致視網膜色素上皮(RPE)損傷而形成的黃白色病變2)7)。在OCTA上,它們在脈絡膜毛細血管層表現為低訊號斑點2)。
在OCTA上,觀察到淺層和深層毛細血管叢的逐漸變細模式(血管向末梢變細)的破壞以及中心凹無血管區(FAZ)擴大2)。表層血管叢(SVP)的血管密度降低也是特徵性表現1)。
SD-OCT可檢測到視網膜增厚、視網膜下液(SRF)和視網膜內高反射沉積物2)5)。
有報告指出惡性高血壓患者中觀察到2+以上的玻璃體細胞7)。有時需要與眼內炎、葡萄膜炎進行鑑別。
代表性分類有KWB分類(I~IV級):I級:輕度小動脈狹窄、硬化;II級:明顯狹窄、動靜脈交叉徵;III級:出血、滲出、視網膜水腫;IV級:視乳頭水腫。Scheie分類獨立評估高血壓性改變(H1~4)和動脈硬化性改變(S1~4)。Wong-Mitchell分類(2004年)分為無、輕度、中度、重度四級,用於現代流行病學研究。基於OCT的新分類提出三種類型:①輕度至中度,②無SRF的惡性,③有SRF的惡性1)。
高血壓視網膜病變的發生以高血壓本身為必要條件,以下因素通過高血壓增加視網膜病變風險。
已鑑定出與視網膜血管直徑相關的SNPs:中心視網膜靜脈等效直徑(CRVE)涉及8個SNPs,中心視網膜動脈等效直徑(CRAE)涉及2個SNPs1)。
小動脈狹窄不僅是高血壓的結果,也可能是原因。一項針對10,229人的統合分析顯示,視網膜小動脈狹窄與未來10年內發生高血壓的風險相關1)。
一項針對12,603人的統合分析報告,降壓藥的不遵從率高達45.1%1)。遵從性差直接導致眼底病變的長期進展。
常透過內科的眼底檢查申請發現,有時視力下降會揭示腎臟疾病或續發性高血壓。初診時透過血壓測量和血液檢查確診。
眼底檢查是診斷的基礎。由於直接檢眼鏡觀察者間變異較大,建議使用散瞳下的裂隙燈眼底檢查或眼底照相機1)。
KWB分級是高血壓視網膜病變的經典嚴重程度分級。
| KWB組 | 主要表現 | 臨床意義 |
|---|---|---|
| I群 | 輕度小動脈狹窄、光反射增強 | 輕度高血壓 |
| II群 | 明顯狹窄、動靜脈交叉壓迫 | 持續性高血壓 |
| III群 | 出血、白斑、視網膜水腫 | 重度高血壓 |
| IV群 | III群 + 視乳頭水腫 | 惡性高血壓 |
Scheie分類將高血壓性變化(H1~H4)與動脈硬化性變化(S1~S4)獨立評估,可區分血壓的急性影響與慢性硬化變化。
| Scheie分級 | 評估對象 | 主要發現 |
|---|---|---|
| H(高血壓性)1~4 | 血管痙攣 | 局部狹窄→瀰漫性狹窄→出血和白斑→視乳頭水腫 |
| S(硬化性)1~4 | 動脈硬化 | 光反射增強→銅線動脈→銀線動脈→玻璃樣變性 |
需要與糖尿病視網膜病變(雙側軟性滲出、硬性滲出、新生血管)、放射性視網膜病變、貧血性視網膜病變、眼缺血症候群、視網膜靜脈阻塞相鑑別。IgA腎病中已有與Purtscher樣視網膜病變重疊的報告8)。
OCTA無需顯影劑即可分層顯示視網膜和脈絡膜血管層。在高血壓視網膜病變中,可定量評估淺層和深層毛細血管叢的血管密度及FAZ面積,比傳統螢光眼底血管攝影更詳細地檢測缺血區域和Elschnig斑(脈絡膜毛細血管層的低訊號斑點)1)2)。無創且適合重複追蹤評估。
高血壓視網膜病變治療的根本是全身血壓管理。對於惡性高血壓的緊急降壓,建議在最初1小時內將平均動脈壓(MAP)降低10-15%,並在24小時內控制在基線的25%以內。急劇降壓會導致視網膜、腦和腎臟缺血,因此禁忌。目標是在2-3個月內達到SBP<130 mmHg、DBP<80 mmHg。
厄貝沙坦+阿替洛爾+氨氯地平三藥聯合持續10個月後,報告顯示KWB IV級改善至I級,改善4個級別1)。
繼發性高血壓的特異性治療也很重要。在嗜鉻細胞瘤中,使用拉貝洛爾持續靜脈輸注(0.25 mg/kg/h)緊急降壓後,行腹腔鏡腎上腺切除術的病例獲得了最佳矯正視力20/20的完全恢復5)。
通過血壓控制,出血和軟性滲出可在約3個月內消失4)。另一方面,動靜脈交叉徵和動脈狹窄往往不可逆地殘留。多數情況下,隨著腎功能的改善而減輕,但硬性滲出沉積和視網膜色素上皮萎縮導致的不可逆損傷可能殘留。需要與內科定期協作確認全身狀況。
Khojasteh等人(2021)報告了對中心凹視網膜內積血行23G微切口玻璃體手術(MIVS)+41G針直接引流積血+內界膜(ILM)瓣技術後,最佳矯正視力從20/400改善至20/509)。
能否改善取決於病期。血管痙攣期的變化(小動脈狹窄、出血、軟性滲出)透過適當降壓可在數週至3個月內改善4)。而慢性高血壓引起的動脈硬化性變化(銅絲/銀絲動脈、動靜脈交叉現象)基本上不可逆,降壓後仍殘留。詳見「病理生理學·詳細發病機轉」一節。
高血壓性視網膜病變可理解為視網膜血管對管腔內壓升高的階段性反應。
管腔內壓升高激活自身調節機制,導致小動脈痙攣1)3)。平均動脈壓每升高10 mmHg,視網膜小動脈直徑減少約3 μm1)。此階段的變化是可逆的。
持續性高血壓導致內膜增厚、中膜平滑肌增殖和玻璃樣變性1)3)。中膜平滑肌細胞變性壞死及中膜外膜纖維性肥厚引起器質性狹窄,眼底表現為血柱反射增強(銅絲動脈→銀絲動脈)和動靜脈交叉現象。硬化的動脈壓迫周圍靜脈,增加靜脈血栓風險。
血-視網膜屏障破壞導致血漿成分滲漏至視網膜,引起出血、硬性滲出和軟性滲出1)3)。纖維素樣壞死是最嚴重的變化3);脈絡膜小動脈的纖維素樣壞死導致脈絡膜毛細血管節段性梗死,形成Elschnig斑2)。慢性腎衰竭末期可發生脈絡膜循環障礙,外血-視網膜屏障破壞,引起視網膜下滲出和漿液性視網膜剝離。隨著毛細血管閉塞進展,出現微動脈瘤、靜脈管徑不均和血管吻合;罕見情況下出現視網膜無灌注區和新生血管,導致增殖性視網膜病變。
視網膜血管具有血-視網膜屏障、缺乏交感神經支配和血流自身調節功能的特點3)。這些特性決定了其對全身和局部血壓變化的反應。
根本預防是將血壓控制在正常範圍內。定期測量家庭血壓、減鹽、適度運動、戒菸、限酒等生活習慣改善是有效的。持續服用處方的降壓藥也很重要,統合分析顯示不遵從率高達45.1%,這是一個挑戰1)。定期眼底檢查可以在無症狀階段發現病變,早期介入可以防止進展為不可逆變化。
自適應光學(AO)與OCT/OCTA的融合使得在活體中測量視網膜小動脈的壁腔比(WLR)成為可能1)。微血管密度的量化作為高血壓視網膜病變的早期診斷標誌物正在研究中2)。OCTA在缺血區域和Elschnig斑的詳細可視化方面優於FA2),有望成為非侵入性的病情評估工具。
血清尿酸(SUA)、海蟾蜍精(marinobufagenin)和GlycA被評估為高血壓視網膜病變的預測生物標誌物1)。基因研究中已鑑定出與視網膜血管直徑相關的SNPs,可能有助於早期發現遺傳高風險族群1)。
使用BPH/2J小鼠(遺傳性高血壓模型)的研究詳細分析了視網膜血管的自身調節機制1)。由於與人類高血壓視網膜病變的同源性,這些模型被用於新療法的臨床前評估。