Стадии 1–2
Стадия 1 : только телеангиэктазии сетчатки без экссудата.
Стадия 2A: Телеангиэктазии с экссудатом вне фовеа.
Стадия 2B: Экссудат распространяется на фовеа. Явное снижение зрения.

Болезнь Коутса, описанная Джорджем Коутсом в 1908 году, является идиопатическим заболеванием сосудов сетчатки. Характеризуется аномальным расширением капилляров сетчатки (телеангиэктазиями) и накоплением экссудата интра- и субретинально из сосудистых стенок.
Заболевание носит спорадический и ненаследственный характер, без связи с системными заболеваниями или семейным анамнезом1). Заболеваемость составляет 0,09 на 100 000 человек, что редко2). Около 75% пациентов — мужчины, 95% случаев односторонние, и оно возникает преимущественно в возрасте до 20 лет (средний возраст около 5 лет).
Начало во взрослом возрасте очень редко, но имеет другую клиническую картину, чем детская форма. Взрослые случаи протекают легче, с медленным прогрессированием и хорошим ответом на лечение3). В одном отчете только у 21% из 48 глаз с началом во взрослом возрасте развилась экссудативная отслойка сетчатки, по сравнению с 81% при детском начале3).
Легкая форма также называется милиарными аневризмами Лебера и является частью спектра болезни Коутса. Идиопатическая макулярная телеангиэктазия 1-го типа также считается частью того же спектра.
Сообщалось о случаях начала после 35 лет, которые признаются как болезнь Коутса взрослых3). По сравнению с детской формой, прогрессирование более медленное, частота экссудативной отслойки ниже, а ответ на лечение часто хороший. Однако начало редкое, и при обнаружении подобных признаков у взрослых важна дифференциальная диагностика с другими заболеваниями.
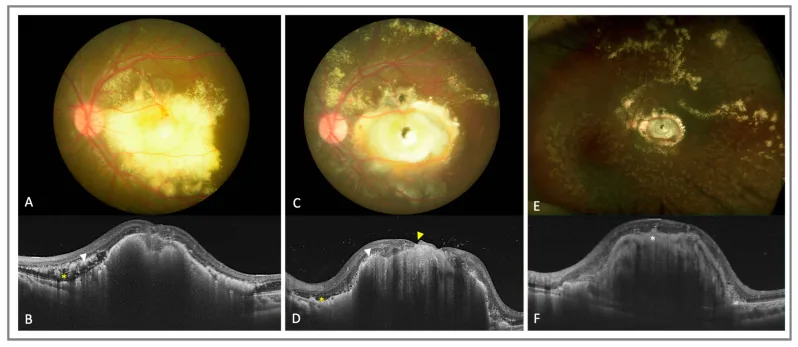
При возникновении в раннем детском возрасте больной ребенок редко предъявляет жалобы.
При взрослом начале заболевания острота зрения относительно сохранена, и иногда заболевание обнаруживается случайно при профилактическом осмотре3).
Характерными признаками глазного дна являются аномально расширенные сосуды сетчатки, сконцентрированные на периферии, и скопление желтовато-белого субретинального и интраретинального экссудата. При флюоресцентной ангиографии визуализируются окклюзия периферических сосудов сетчатки, телеангиэктазии, микроаневризмы и неоваскуляризация. При прогрессировании возникает экссудативная отслойка сетчатки, которая в конечном итоге может стать тотальной. При УЗИ, КТ и МРТ субретинальная жидкость визуализируется гомогенно во всех отделах, что является важным дифференциально-диагностическим признаком от ретинобластомы, которая дает негомогенную картину с кальцификатами.
На поздних стадиях возникают осложнения переднего отрезка, такие как рубеоз радужки и неоваскулярная глаукома. Макулярное отверстие является редким осложнением, описанным в литературе лишь в 7 случаях4). Фиброзный узел является фактором плохого зрительного прогноза, и на ОКТА подтверждено наличие неоваскуляризации 3-го типа (SVC→DVC→аваскулярный комплекс) внутри узла5).
Классификация Шилдса делит болезнь Коутса на следующие 5 стадий. Она используется для выбора тактики лечения и оценки прогноза.
Стадии 1–2
Стадия 1 : только телеангиэктазии сетчатки без экссудата.
Стадия 2A: Телеангиэктазии с экссудатом вне фовеа.
Стадия 2B: Экссудат распространяется на фовеа. Явное снижение зрения.
Стадия 3
Стадия 3A1: Субтотальная отслойка сетчатки вне фовеа.
Стадия 3A2: Субтотальная отслойка сетчатки с вовлечением фовеа. Плохой зрительный прогноз.
Стадия 3B: Тотальная отслойка сетчатки. Требуется неотложное вмешательство.
Стадии 4–5
Стадия 4: Тотальная отслойка сетчатки с вторичной глаукомой. Может быть болезненной.
Стадия 5: Терминальная стадия. Фтизис глазного яблока (атрофия). Рассматривается энуклеация.
Лейкокория встречается при нескольких заболеваниях, болезнь Коутса — лишь одно из них. Наиболее важным дифференциальным диагнозом является ретинобластома (РБ), требующая срочной оценки из-за угрозы жизни. Другие дифференциальные диагнозы включают ретинопатию недоношенных, персистирующее гиперпластическое первичное стекловидное тело (ПГПСТ) и эндофтальмит. Подробнее см. в разделе «Диагностика и методы обследования».
Причина болезни Коутса неизвестна, связи с системными заболеваниями или семейным анамнезом не выявлено. Сообщалось о генетических факторах, таких как нестабильность хромосом 3 и 13, а также ассоциации с генами NDP (болезнь Норри) и CRB1, но они не установлены.
Отправной точкой патогенеза считается нарушение внутреннего гематоретинального барьера (ВГРБ) 1). Уменьшение количества перицитов (клеток, поддерживающих эндотелий сосудов) ослабляет сосудистую стенку, что приводит к образованию аномально расширенных капилляров и аневризм 1). Компоненты плазмы просачиваются и накапливаются в сосудистой стенке и слоях сетчатки, вызывая утолщение стенки и порочный круг дальнейшей экссудации 2).
Предполагается, что среда с высоким содержанием VEGF способствует расширению периферических капилляров 2), что является теоретическим обоснованием анти-VEGF терапии.
Диагноз ставится на основании комбинации нескольких исследований, причем наиболее важной задачей является надежное разграничение с ретинобластомой (РБ).
При осмотре глазного дна с расширенным зрачком выявляются извитые аномальные сосуды на периферии и желтовато-белые субретинальные экссудаты. При распространении экссудатов на макулу они приобретают вид твердых белых бляшек.
Это одно из наиболее важных исследований для диагностики болезни Коутса. Характерными признаками являются выраженное расширение капилляров, микроаневризмы, артериовенозные анастомозы и «лампочки» (грушевидные очаги просачивания флюоресцеина). Это исследование необходимо для определения границ аномальных сосудов и выбора участков для лазеркоагуляции.
Подтверждает отсутствие солидного образования. При РБ в В-режиме часто выявляются гиперэхогенные сигналы (кальцинаты) внутри солидного образования, тогда как при болезни Коутса солидное образование не формируется.
Оценивают наличие кальцинатов. РБ часто сопровождается кальцификацией, в то время как болезнь Коутса не приводит к кальцификации. Этот признак является важным основанием для дифференциальной диагностики.
Основные различия между болезнью Коутса и ретинобластомой приведены ниже.
| Параметр | Болезнь Коутса | Ретинобластома |
|---|---|---|
| Возраст начала | Около 5 лет | 1–2 года |
| Пол | Мужчины 75% | Нет |
| Двусторонность | Около 5% | Около 40% |
| Кальцификация | Отсутствует | Присутствует (часто) |
| Солидная опухоль | Отсутствует | Присутствует |
| УЗИ | Субретинальное скопление жидкости | Солидная опухоль, внутренние кальцинаты, задняя тень |
| МРТ | Субретинальная жидкость однородна | Неоднородна (опухолевый сигнал) |
Другие дифференциальные диагнозы включают ретинальную гемангиому, болезнь фон Гиппеля-Линдау, персистирующее гиперпластическое первичное стекловидное тело (PHPV), семейную экссудативную витреоретинопатию (FEVR), токсокароз, вазопролиферативную опухоль, болезнь Илза и др.
Цель лечения — закрыть аномальные сосуды и остановить продукцию экссудата. Применяется поэтапный подход в зависимости от стадии.
Это терапия первой линии. Непосредственно коагулируются аномально расширенные сосуды и микроаневризмы, выявленные при ФАГ, а также проводится фотокоагуляция периферических зон неперфузии. У детей процедура выполняется под общей анестезией. Часто требуется несколько сеансов, и после лечения регулярно повторяются ФАГ-оценка и дополнительная коагуляция.
Это следующий вариант для поражений передней периферии или участков, труднодоступных для фотокоагуляции. Может использоваться в комбинации с фотокоагуляцией.
Лазерная коагуляция
Показания : Аномальные сосуды и экссудативные поражения стадий 1–3A.
Метод : Непосредственная коагуляция участков телеангиэктазий и неперфузии под контролем ФАГ. У детей под общей анестезией.
Особенности : Возможно повторное проведение. Регулярная послеоперационная ФАГ-оценка и дополнительная коагуляция являются стандартным ведением.
Криокоагуляция
Показания : Труднодоступные для фотокоагуляции передние периферические поражения, вспомогательное лечение при тяжелых случаях стадии 3B и ниже.
Метод : Транссклеральное приложение криозонда для коагуляции и окклюзии аномальных сосудов.
Особенности : Может выполняться даже при мутных средах или в самых периферических областях.
Витрэктомия и хирургия сетчатки
Показания : Стадия 3B (тотальная отслойка сетчатки) и выше, случаи, рефрактерные к криокоагуляции.
Метод : Наружное дренирование или витрэктомия для дренирования субретинальной жидкости и внутреннего прилегания сетчатки 8). В тяжелых случаях может проводиться дренирование субретинальной жидкости в сочетании с циркляжем (склеральное пломбирование).
Особенности : При случаях, осложненных макулярным разрывом, сообщается об эффективности техники переворота внутренней пограничной мембраны (ILM) 4).
Применение анти-VEGF препаратов при болезни Коутса еще не имеет консенсуса и рассматривается как вспомогательная терапия в сочетании с фотокоагуляцией, а не как стандартное лечение.
Сообщается об одном случае болезни Коутса у взрослого, который лечили комбинацией интравитреальной инъекции ранибизумаба 0,5 мг и лазерной коагуляции, с улучшением максимально корригированной остроты зрения от счета пальцев до 20/603).
В отчете о педиатрических случаях, получавших комбинированную терапию интравитреальной инъекцией бевацизумаба 1,25 мг, субтенонового триамцинолона и лазера каждые 6 недель под EUA (исследование под общей анестезией), было отмечено, что после лечения может возникнуть парадоксальная экссудативная ретинопатия2).
Появляются также сообщения об эффективности бролуцизумаба в случаях, резистентных к бевацизумабу2). Высказывается предположение, что анти-VEGF-терапия может способствовать предотвращению образования фиброзных узелков5).
Энуклеация выбирается при болезненном слепом глазе (стадия 4–5) и когда трудно исключить ретинобластому.
При болезни Коутса могут наблюдаться случаи рецидива или повторной отслойки в течение нескольких лет, а также случаи двустороннего поражения с разным временем начала. Даже после завершения лечения необходима регулярная переоценка с помощью флуоресцентной ангиографии, и при выявлении новых поражений следует провести дополнительную фотокоагуляцию или криокоагуляцию.
В настоящее время не существует консенсуса относительно применения анти-VEGF препаратов при болезни Коутса, и они не считаются стандартным лечением. Накоплены сообщения об их использовании в качестве вспомогательной терапии к лазерной фотокоагуляции, но оценка эффективности и безопасности требует дальнейших исследований.
Центральным механизмом болезни Коутса является нарушение внутреннего гематоретинального барьера (ВГРБ) 1).
ВГРБ состоит из эндотелиальных клеток капилляров сетчатки и поддерживающих их перицитов. При болезни Коутса количество перицитов значительно снижено, что приводит к снижению функции поддержки сосудистого эндотелия 1). Снижение количества самих эндотелиальных клеток также подтверждено иммуногистохимией и электронной микроскопией 1).
Нарушение эндотелиального ГРБ приводит к утечке и накоплению компонентов плазмы (в основном липопротеинов, холестерина) в сосудистой стенке, сетчатке и субретинальном пространстве 1). Накопленные липиды вызывают инфильтрацию липидсодержащих макрофагов (пенистых клеток) и гранулематозную иммунную реакцию, усугубляя повреждение тканей 1).
Среда с высоким содержанием VEGF способствует дальнейшему расширению периферических капилляров и участвует в прогрессировании поражения 2). Наблюдение с помощью ОКТА выявило наличие неоваскуляризации 3-го типа (формирующейся в порядке SVC → DVC → аваскулярный комплекс) внутри макулярных фиброзных узлов при прогрессирующих поражениях 5), и понимание процесса неоваскуляризации продолжает углубляться.
Механизм образования макулярного отверстия считается связанным с укорочением сетчатки из-за периферического лазерного воздействия, что вызывает тангенциальную тракцию и приводит к перфорации макулы 4).
ОКТА позволила неинвазивно оценить микрососудистую структуру внутри фиброзных узлов.
Ong и соавт. (2021) детально проанализировали сосудистую структуру внутри макулярных узлов с помощью ОКТА и выявили наличие неоваскуляризации 3-го типа, формирующейся в порядке SVC → DVC → аваскулярный комплекс 5). Это открытие важно для понимания механизма формирования узлов и как мишень для анти-VEGF терапии.
Сообщается о феномене парадоксального усиления экссудации после начала анти-VEGF терапии, что требует выяснения механизма и разработки методов лечения.
Kalavar и соавт. (2022) сообщили о случае болезни Коутса у ребенка, у которого после начала лечения развилось временное усиление экссудации и образование звездчатого макулярного экссудата (macular star formation)2). Бролуцизумаб оказался эффективным у пациента, резистентного к бевацизумабу, и привлекает внимание как новый вариант лечения2).
Nawrocka и соавт. (2023) сообщили об одном случае витрэктомии с использованием техники инвертированного лоскута внутренней пограничной мембраны (inverted ILM flap) при макулярном разрыве, ассоциированном с болезнью Коутса4). Через 18 месяцев после операции было подтверждено закрытие макулярного разрыва, максимально корригированная острота зрения составила 20/40. Макулярный разрыв, связанный с болезнью Коутса, является редким осложнением, о котором в PubMed сообщено лишь около 7 случаев4).
Shields и соавт. (2019) проанализировали 351 глаз с болезнью Коутса за 45 лет, показав улучшение результатов лечения с течением десятилетий9). Dalvin и соавт. (2019) проанализировали ту же когорту по возрастным категориям и показали, что случаи с началом в детском возрасте, как правило, более тяжелые и имеют худший зрительный прогноз по сравнению со случаями с началом во взрослом возрасте10).
Болезнь Коутса с началом во взрослом возрасте является традиционно недооцененной нозологической формой, однако число сообщений растет3). Продолжается уточнение клинических различий с детской формой (легкое течение, медленное прогрессирование, хороший ответ на лечение), и разработка соответствующих протоколов лечения у взрослых остается актуальной задачей.