المرحلة 1-2
المرحلة 1: توسع الشعيرات الدموية الشبكية فقط دون إفرازات.
المرحلة 2A: توسع الشعيرات الدموية مع وجود إفرازات خارج النقرة.
المرحلة 2B: تمتد الإفرازات إلى النقرة. يظهر انخفاض الرؤية.

مرض كوتس (Coats disease) هو مرض وعائي شبكي مجهول السبب وصفه جورج كوتس عام 1908. يتميز بتوسع غير طبيعي في الشعيرات الدموية الشبكية (توسع الشعيرات) وتراكم الإفرازات داخل الشبكية وتحتها من جدران الأوعية.
المرض متقطع وغير وراثي، ولا يرتبط بأمراض جهازية أو تاريخ عائلي 1). معدل الإصابة نادر، حوالي 0.09 لكل 100,000 شخص 2). حوالي 75% من المرضى ذكور، و95% يصابون في عين واحدة، ويحدث غالبًا تحت سن 20 عامًا (متوسط حوالي 5 سنوات).
البداية عند البالغين نادرة جدًا، لكنها تظهر بصورة سريرية مختلفة عن النوع الطفلي. حالات البداية عند البالغين أخف وتتقدم ببطء، وتستجيب جيدًا للعلاج 3). في إحدى الدراسات، حدث انفصال شبكي إفرازي في 21% فقط من 48 عينًا لدى البالغين، مقارنة بـ 81% لدى الأطفال، وهو أقل بشكل ملحوظ 3).
يُطلق على النوع الخفيف اسم داء تمدد الأوعية الدموية الدبقية في ليبر (Leber’s miliary aneurysms)، وهو جزء من طيف مرض كوتس. يُعتقد أيضًا أن توسع الشعيرات الشبكي المجهول السبب من النوع 1 يندرج ضمن نفس الطيف.
تم الإبلاغ عن حالات بداية بعد سن 35 عامًا، ويُعرف باسم مرض كوتس عند البالغين 3). مقارنة بالنوع الطفلي، يكون تقدم المرض أبطأ، وتكون نسبة حدوث انفصال شبكي إفرازي أقل، وغالبًا ما يكون الاستجابة للعلاج جيدة. لكن الإصابة نفسها نادرة، وعند ملاحظة نتائج مماثلة لدى البالغين، من المهم التمييز بينها وبين أمراض أخرى.
عند حدوث المرض في مرحلة الطفولة المبكرة، نادرًا ما يشكو الطفل المصاب من الأعراض.
في حالات البالغين، تكون الرؤية محفوظة نسبيًا، وقد يتم اكتشافها بالصدفة أثناء الفحص الطبي 3).
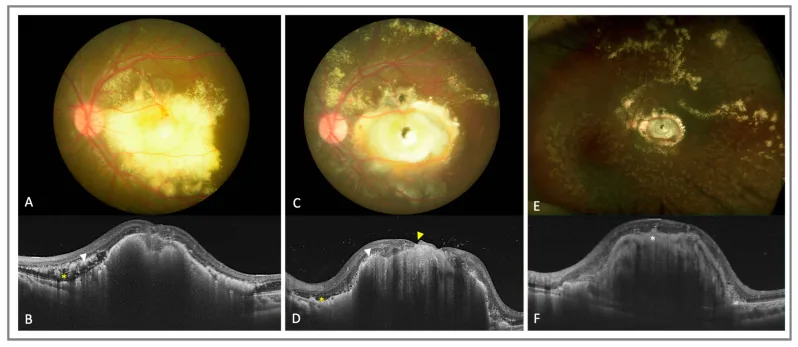
تتميز علامات قاع العين بوجود أوعية دموية شبكية متوسعة بشكل غير طبيعي تتركز في المنطقة المحيطية، وتراكم إفرازات صفراء-بيضاء تحت الشبكية وداخلها. في تصوير الأوعية بالفلوريسين، تُظهر العلامات المميزة انسداد الأوعية الدموية الشبكية المحيطية، وتوسع الشعيرات، وأم الدم الشعيرية، والأوعية الجديدة. مع التقدم، يحدث انفصال شبكي نضحي، وقد يؤدي في النهاية إلى انفصال كامل. في الفحص بالموجات فوق الصوتية والتصوير المقطعي المحوسب والرنين المغناطيسي، يُصوَّر السائل تحت الشبكية بشكل متجانس في جميع الزوايا، وهذه نقطة فارقة مهمة في التصوير عن الورم الأرومي الشبكي الذي يظهر صورة غير متجانسة مع تكلسات.
في المراحل المتأخرة، تحدث مضاعفات في الجزء الأمامي مثل روبيوز القزحية والزرق الوعائي الجديد. الثقب البقعي هو مضاعف نادر، وقد تم الإبلاغ عن حوالي 7 حالات فقط في الأدبيات 4). العقيدة الليفية هي عامل سوء الإنذار البصري، وقد تم تأكيد وجود أوعية دموية جديدة من النوع 3 (SVC→DVC→مركب لا وعائي) داخل العقيدة باستخدام OCTA 5).
يصنف تصنيف شيلدز مراحل مرض كوتس إلى 5 مراحل كما يلي. يُستخدم لاختيار خطة العلاج وتقدير الإنذار.
المرحلة 1-2
المرحلة 1: توسع الشعيرات الدموية الشبكية فقط دون إفرازات.
المرحلة 2A: توسع الشعيرات الدموية مع وجود إفرازات خارج النقرة.
المرحلة 2B: تمتد الإفرازات إلى النقرة. يظهر انخفاض الرؤية.
المرحلة 3
المرحلة 3A1: انفصال الشبكية الجزئي خارج النقرة.
المرحلة 3A2: انفصال الشبكية الجزئي يشمل النقرة. سوء الإنذار البصري.
المرحلة 3B: انفصال الشبكية الكلي. يتطلب تدخلاً عاجلاً.
المرحلة 4-5
المرحلة 4: انفصال الشبكية الكلي مع الجلوكوما الثانوية. قد يكون مؤلماً.
المرحلة 5: المرحلة النهائية. ضمور العين (phthisis bulbi). يُنظر في استئصال العين.
هناك عدة أمراض تسبب حدقة بيضاء، ومرض كوتس هو واحد منها فقط. أهم تشخيص تفريقي هو الورم الأرومي الشبكي (Rb)، والذي يتطلب تقييماً عاجلاً لأنه يهدد الحياة. تشمل التشخيصات الأخرى اعتلال الشبكية الخداجي، متلازمة استمرار الأوعية الجنينية (PHPV)، والتهاب باطن العين. انظر قسم التشخيص وطرق الفحص للتفاصيل.
سبب مرض كوتس غير معروف، ولا توجد علاقة بأمراض جهازية أو تاريخ عائلي. تم اقتراح ارتباطات مع عدم استقرار الكروموسومات 3 و13، وجين NDP (مرض نوري)، وجين CRB1، لكنها غير مؤكدة.
يُعتقد أن انهيار الحاجز الدموي الشبكي الداخلي (iBRB) يلعب دوراً مركزياً في بداية المرض 1). يؤدي نقص الخلايا الحوطية (التي تدعم بطانة الأوعية) إلى ضعف جدار الوعاء وتشكل شعيرات دموية متوسعة بشكل غير طبيعي وأم الدم 1). تتسرب مكونات البلازما إلى جدار الوعاء وطبقات الشبكية، مما يسبب سماكة جدار الوعاء ويزيد من الإفرازات، مكونة حلقة مفرغة 2).
يُقترح أيضاً أن بيئة VEGF العالية تعزز توسع الشعيرات الدموية الطرفية 2)، وهذا هو الأساس المنطقي للعلاج المضاد لـ VEGF.
لتشخيص المرض، يتم الجمع بين عدة فحوصات، ويعتبر التمييز الدقيق عن الورم الأرومي الشبكي (Rb) هو الأهم.
يكشف فحص قاع العين تحت التوسيع عن شبكة أوعية دموية غير طبيعية متعرجة في المنطقة المحيطية وإفرازات صفراء-بيضاء تحت الشبكية. إذا امتدت الإفرازات إلى البقعة، فإنها تظهر بمظهر يشبه اللويحات الصلبة.
يعد أحد أهم الفحوصات في تشخيص مرض كوتس. يتميز بتوسع واضح في الشعيرات الدموية، وأم الدم الشعيرية، ومفاغرة شريانية وريدية، وتسرب فلوريسئين على شكل لمبات ضوئية. لا غنى عنه لتحديد مدى الأوعية غير الطبيعية وتحديد مواقع الليزر.
يتم التأكد من عدم وجود كتلة صلبة. غالبًا ما يُظهر الورم الأرومي الشبكي صدى عالي الكثافة (تكلسات) داخل الكتلة الصلبة في الوضع B، بينما لا يتكون كتلة صلبة في مرض كوتس.
يتم تقييم وجود التكلسات. يصاحب الورم الأرومي الشبكي تكلسات بنسبة عالية، بينما لا يسبب مرض كوتس تكلسات. هذه النتيجة هي أساس مهم للتمييز.
فيما يلي الاختلافات الرئيسية بين مرض كوتس وورم الأرومة الشبكية.
| العنصر | مرض كوتس | ورم الأرومة الشبكية |
|---|---|---|
| العمر الشائع | حوالي 5 سنوات | 1-2 سنوات |
| الجنس | 75% ذكور | لا يوجد |
| إصابة العينين | حوالي 5% | حوالي 40% |
| التكلس | لا يوجد | موجود (بنسبة عالية) |
| ورم صلب | لا يوجد | موجود |
| الموجات فوق الصوتية | تراكم السوائل تحت الشبكية | كتلة صلبة، تكلسات داخلية، ظل خلفي |
| التصوير بالرنين المغناطيسي | السائل تحت الشبكية متجانس | غير متجانس (إشارة الكتلة) |
تشمل الأمراض التفريقية الأخرى: الورم الوعائي الشبكي، مرض فون هيبل لينداو، فرط تنسج الجسم الزجاجي الأولي المستمر (PHPV)، اعتلال الشبكية الزجاجي النضحي العائلي (FEVR)، داء المقوسات، الورم الوعائي التكاثري، مرض إيلز.
الهدف من العلاج هو إغلاق الأوعية الدموية غير الطبيعية ووقف إنتاج الإفرازات. يتم اتباع نهج تدريجي حسب مرحلة المرض.
هو العلاج الأولي. يتم تخثير الأوعية المتوسعة غير الطبيعية والأورام الوعائية الشعرية التي تم تأكيدها بواسطة تصوير الأوعية الفلوريسيني (FA) مباشرة، بالإضافة إلى إجراء التخثير الضوئي في مناطق عدم التروية المحيطة. عند الأطفال، يتم إجراؤه تحت التخدير العام. غالبًا ما تكون هناك حاجة إلى جلسات متعددة، ويتم تكرار إعادة التقييم الدوري باستخدام FA والتخثير الإضافي بعد العلاج.
هو الخيار التالي المستخدم للآفات في المنطقة الأمامية المحيطية أو المواقع التي يصعب فيها التخثير الضوئي. يمكن استخدامه أيضًا مع التخثير الضوئي.
التخثير بالليزر
المؤشرات: الأوعية غير الطبيعية والآفات النضحية في المراحل 1 إلى 3A.
الطريقة: التخثير المباشر لمناطق توسع الشعيرات ومناطق عدم التروية تحت توجيه FA. عند الأطفال، يتم إجراؤه تحت التخدير العام.
الميزات: يمكن إجراؤه بشكل متكرر. إعادة التقييم الدوري باستخدام FA والتخثير الإضافي بعد العلاج هو الإدارة القياسية.
التخثير بالتجميد
المؤشرات: الآفات المحيطية الأمامية التي يصعب تخثيرها ضوئيًا، والمساعدة في الحالات الشديدة حتى المرحلة 3B.
الطريقة: يتم تطبيق مسبار التجميد عبر الصلبة لتخثير وإغلاق الأوعية غير الطبيعية.
الميزات: يمكن إجراؤه في الوسائط المعتمة أو في الأجزاء الأكثر محيطية.
جراحة الزجاجية والشبكية
المؤشرات: المرحلة 3B (انفصال الشبكية الكلي) أو أكثر، والحالات غير المستجيبة للتخثير بالتجميد.
الطريقة: تصريف السائل تحت الشبكية عن طريق التصريف الخارجي أو جراحة الزجاجية، وإعادة تثبيت الشبكية من الداخل 8). في الحالات الشديدة، يمكن الجمع بين تصريف السائل تحت الشبكية ورأب الصلبة (الربط الحلقي).
الميزات: تم الإبلاغ عن أن تقنية قلب الغشاء الداخلي المحدد (ILM) فعالة في الحالات المصحوبة بثقب البقعة 4).
استخدام الأدوية المضادة لـ VEGF لمرض كوتس لم يتم التوصل إلى إجماع عليه بعد، ويُعتبر علاجًا مساعدًا مع التخثير الضوئي وليس علاجًا قياسيًا.
هناك تقرير عن حالة واحدة من مرض كوتس لدى البالغين تم علاجها بمزيج من حقن ranibizumab 0.5 ملغ داخل الزجاجي والتخثير بالليزر، وتحسنت حدة البصر المصححة النهائية من عد الأصابع إلى 20/60 3).
في تقرير عن حالات أطفال تم علاجهم بحقن bevacizumab 1.25 ملغ داخل الزجاجي، و triamcinolone تحت المحفظة، والليزر تحت التخدير العام كل 6 أسابيع، لوحظ أنه قد يحدث تفاقم نضحي متناقض بعد العلاج 2).
ظهرت تقارير تفيد بأن brolucizumab كان فعالاً في حالات مقاومة للـ bevacizumab 2). يُقترح أن العلاج المضاد لـ VEGF قد يساهم في منع تكوين العقيدات الليفية 5).
في حالات العين العمياء المؤلمة (المرحلة 4-5) والتي يصعب فيها استبعاد الورم الأرومي الشبكي، يتم اختيار استئصال العين.
في مرض كوتس، هناك حالات تعاني من انتكاس أو انفصال متكرر على مدى عدة سنوات، كما توجد حالات ثنائية الجانب تختلف في وقت ظهورها. بعد اكتمال العلاج، من الضروري إجراء إعادة تقييم دورية بتصوير الأوعية الفلوريسيني، وإذا تم اكتشاف آفات جديدة، يجب إجراء تخثير ضوئي أو تخثير بالتبريد إضافي.
في الوقت الحالي، لم يتم التوصل إلى إجماع حول استخدام الأدوية المضادة لـ VEGF في مرض كوتس، ولا تعتبر علاجًا قياسيًا. تتراكم التقارير حول استخدامها كعلاج مساعد مع التخثير الضوئي بالليزر، لكن تقييم الفعالية والسلامة يتطلب مزيدًا من البحث.
محور آلية حدوث مرض كوتس هو انهيار الحاجز الدموي الشبكي الداخلي (iBRB) 1).
يتكون iBRB من الخلايا البطانية للشعيرات الدموية الشبكية والخلايا الحوطية الداعمة لها. في مرض كوتس، ينخفض عدد الخلايا الحوطية بشكل ملحوظ، مما يؤدي إلى ضعف وظيفة الدعم البطاني الوعائي 1). كما تم تأكيد انخفاض عدد الخلايا البطانية نفسها عن طريق الصبغ المناعي والمجهر الإلكتروني 1).
يؤدي انهيار حاجز الدم الشبكي البطاني إلى تسرب وتراكم مكونات البلازما (خاصة البروتينات الدهنية والكوليسترول) داخل جدار الوعاء الدموي وداخل الشبكية وتحت الشبكية 1). الدهون المتراكمة تحفز تسلل البلاعم المحتوية على الدهون (الخلايا الرغوية) والاستجابة المناعية الورمية الحبيبية، مما يؤدي إلى تفاقم الضرر النسيجي 1).
البيئة عالية VEGF تعزز توسع الشعيرات الدموية الطرفية بشكل أكبر، وتشارك في تطور الآفة 2). باستخدام OCTA، تم تأكيد وجود أوعية دموية جديدة من النوع 3 (تتشكل بالترتيب SVC → DVC → المركب اللاوعائي) داخل العقيدات الليفية البقعية في الآفات المتقدمة 5)، ويتقدم فهم عملية تكوين الأوعية الجديدة.
كآلية لحدوث الثقب البقعي، يُعتقد أن تقصير الشبكية الناتج عن التخثير الضوئي الطرفي يسبب جرًا مماسيًا، مما يؤدي إلى ثقب في البقعة 4).
أتاح OCTA التقييم غير الجراحي للبنية الوعائية الدقيقة داخل العقيدات الليفية.
قام Ong وآخرون (2021) بتحليل البنية الوعائية داخل العقيدات البقعية بالتفصيل باستخدام OCTA، وكشفوا عن وجود أوعية دموية جديدة من النوع 3 تتشكل بالترتيب SVC → DVC → المركب اللاوعائي 5). هذه النتيجة مهمة لفهم آلية تكوين العقيدات وكهدف للعلاج المضاد لـ VEGF.
تم الإبلاغ عن ظاهرة تفاقم الإفرازات بشكل متناقض بعد بدء العلاج المضاد لـ VEGF، وهناك حاجة لتوضيح الآلية ووضع بروتوكول إدارة.
أبلغ كالافار وآخرون (2022) عن حالة طفل مصاب بمرض كوتس أظهرت تفاقمًا عابرًا للإفرازات وتشكل نجمي في البقعة (macular star formation) بعد بدء العلاج2). وقد وُجد أن استخدام برولوسيزوماب (brolucizumab) كان فعالاً في حالة مقاومة للبيفاسيزوماب (bevacizumab)، مما يجعله خيارًا علاجيًا جديدًا واعدًا2).
أبلغ ناوروكا وآخرون (2023) عن حالة واحدة من ثقب البقعة المصاحب لمرض كوتس تم علاجها باستخدام جراحة الزجاجية بتقنية قلب الغشاء الداخلي المحدد (inverted ILM flap)4). تم تأكيد إغلاق ثقب البقعة بعد 18 شهرًا من الجراحة، وكانت حدة البصر المصححة النهائية 20/40. يعتبر ثقب البقعة المرتبط بمرض كوتس من المضاعفات النادرة، حيث تم الإبلاغ عن 7 حالات فقط في PubMed4).
حلل شيلدز وآخرون (2019) 351 عينًا من حالات مرض كوتس على مدى 45 عامًا، وأظهروا تحسنًا في نتائج العلاج عبر العقود9). حلل دالفين وآخرون (2019) نفس المجموعة حسب الفئات العمرية، وأظهروا أن الحالات التي تبدأ في الطفولة تميل إلى أن تكون أكثر شدة ولها تشخيص بصري أسوأ مقارنة بالحالات التي تبدأ في البلوغ10).
مرض كوتس الذي يبدأ في البلوغ هو مفهوم مرضي كان غير معترف به بشكل كافٍ في السابق، وقد تزايد عدد التقارير عنه3). يتم تنظيم الاختلافات السريرية عن النوع الطفلي (أخف، تقدم بطيء، استجابة علاجية جيدة)، ويظل وضع بروتوكول علاجي مناسب للبالغين تحديًا.