早期症状
白瞳症(leukocoria):最常见的初发症状。眼内肿瘤增大,瞳孔呈现白色反光。
斜视:因黄斑部肿瘤导致视力不良所致。视力不良眼向外偏斜。
自觉视力下降:见于年长儿童。
揉眼动作:见于视力不良的婴幼儿。

视网膜母细胞瘤是婴幼儿视网膜的恶性肿瘤。它是未成熟视网膜细胞恶变增殖形成肿瘤的结果,被认为是位于13号染色体长臂(13q14.2)的RB1基因突变导致的单基因疾病。无性别差异,95%在5岁前确诊。
发病率为1/15,00023,000活产儿,日本每年7080例。单侧与双侧比例为3:2,双侧确诊较早(平均8个月),单侧平均21个月。发达国家眼内期5年生存率超过95%。
视网膜母细胞瘤根据基因突变的类型大致分为两类。
| 分类 | 突变类型 | 病理特征 | 遗传风险 |
|---|---|---|---|
| 遗传性(生殖细胞突变) | 生殖细胞系RB1突变 | 常为双侧性和多发性肿瘤 | 子女有50%的遗传风险 |
| 非遗传性(体细胞突变) | 单个视网膜细胞的体细胞突变 | 单侧性和孤立性肿瘤 | 不会遗传给下一代 |
遗传性(生殖细胞突变):身体所有细胞中都存在第一次打击突变。当发生第二次打击时,就会致癌。容易引起双侧性和多发性肿瘤,有50%的几率遗传给子女。存在继发性癌症(如骨肉瘤,20年风险为15.7%)的风险。
非遗传性(体细胞突变):视网膜单个细胞中RB1基因的两个等位基因均发生突变。表现为单侧性、孤立性肿瘤,不会遗传给下一代。
然而,部分单眼病例也包含生殖细胞系RB1突变。不能因为单眼就否定遗传性,必须在遗传咨询和遗传学评估的前提下,结合家族史、发病年龄和肿瘤数量进行解读。1)
分期直接关系到眼球保留治疗方案的制定。
| 分期 | 病变状态 | 眼球保留率参考 |
|---|---|---|
| T1(眼内早期病变) | 局限于眼内,无进展 | 90%以上 |
| T2(眼内进展期病变) | 眼内进展 | 约50% |
| T3 | 伴有眼外浸润的进展期病变 | 约10% |
约40%为遗传性(生殖细胞系RB1突变),有50%的概率遗传给子女。其余约60%为非遗传性(仅体细胞突变),无遗传给下一代的风险。遗传性病例倾向于双侧和多发性。诊断时建议进行基因检测和遗传咨询。
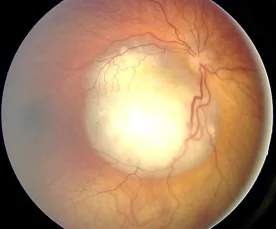
多数情况下,肿瘤在眼内增大,表现为白瞳症而被发现。当肿瘤位于黄斑部时,可因视力不良导致斜视而被发现。年长儿童可自觉视力下降,婴幼儿则可能因视力不良而出现揉眼动作。
早期症状
白瞳症(leukocoria):最常见的初发症状。眼内肿瘤增大,瞳孔呈现白色反光。
斜视:因黄斑部肿瘤导致视力不良所致。视力不良眼向外偏斜。
自觉视力下降:见于年长儿童。
揉眼动作:见于视力不良的婴幼儿。
进展期症状
可见富含血管的白色隆起病变,若伴有钙化则易于确诊。常伴有玻璃体种植(肿瘤细胞破碎后播散至玻璃体)。
红光反射法是婴幼儿眼病筛查的基础。判断标准:双眼瞳孔大小相等,呈明亮对称的黄橙色为正常。若反射暗淡或过亮,或左右不对称,则为异常,需进一步检查。
病因是13号染色体长臂(13q14.2)上的RB1基因突变。RB1基因编码RB1蛋白(视网膜母细胞瘤蛋白),该蛋白在调控细胞分裂中起重要作用。
每个细胞内有两个基因位点,仅一个突变时细胞功能仍可维持,但两个位点均发生突变时,细胞分裂失控而恶性转化(二次打击致癌学说,Knudson假说)。
家族史是最大的风险因素。AAOOP(美国眼科肿瘤与病理学会)推荐的风险定义如下所示1)。
| 风险分类 | 定义 | 风险值 |
|---|---|---|
| 高 | 父母患有双侧Rb,或一级或二级亲属为生殖细胞系RB1突变携带者 | >7.5% |
| 中 | 父母患有单侧Rb | 约7.5% |
| 低 | 其他远亲家族史 | <1% |
遗传性病例需注意二次癌症的风险。骨肉瘤是典型代表,遗传性病例中20年内发生率为15.7%。二次癌症常在10岁以后发病。
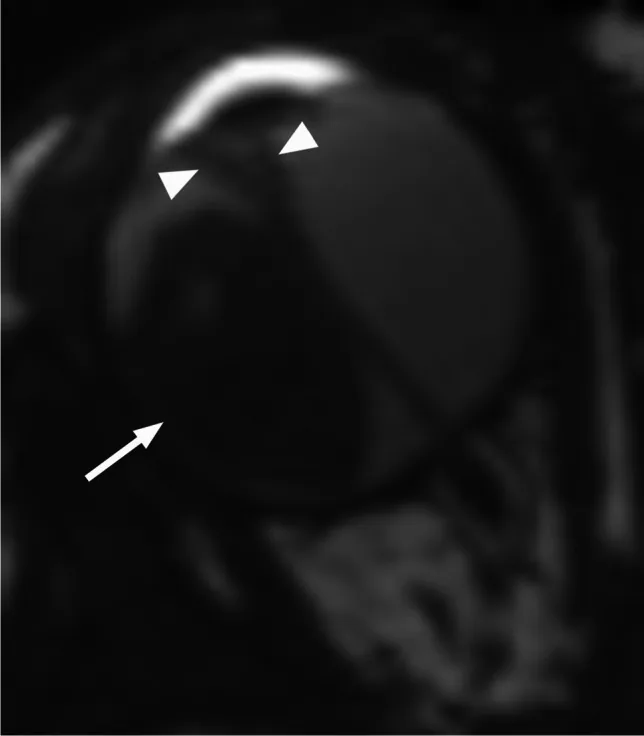
不进行眼内肿瘤活检。眼内病变可通过透明组织直接观察,临床诊断准确性高。此外,眼内肿瘤活检可能导致肿瘤细胞眼外播散,造成不可避免的转移风险。进行保眼治疗时,基于临床诊断开始治疗。
最重要的是鉴别引起白瞳症的疾病。
对于有家族性Rb的儿童筛查,AAOOP 2018推荐在国际上被广泛参考1)。
| 风险 | 筛查时间表 | 结束时间 |
|---|---|---|
| 高(>7.5%) | 出生至8周:每2-4周一次 → 8-12周:每月一次 → 1-2岁:每2个月一次 → 2-3岁:每3个月一次 → 3-4岁:每4个月一次 → 4-7岁:每6个月一次 | 7岁(RB1突变携带者终身) |
| 中(1-7.5%) | 出生至3个月:每月一次 → 逐渐减少 | 7岁 |
| 低(<1%) | 出生至3个月:每月1次 → 逐渐减少 | 7岁 |
一项荷兰全国数据的回顾性队列研究(1991-2019年,332名患者中38名为家族性Rb)显示,接受完全筛查的28名患者均在1岁前确诊(中位18天),而不完全筛查的10名患者确诊时间显著延迟,中位数为420天(59天至4.8岁)2)。此外,有提议将低风险组(<3%)的筛查终止年龄缩短至2岁的方案修订2)。
在家族性病例中,出生后立即开始眼底筛查的持续性直接影响预后。经典登记研究也表明,家族性病例的诊断时机与筛查频率密切相关,目前正朝着结合RB1突变有无来个体化终止时间的方向发展。1, 2)
AAOOP建议定期进行眼底检查直至7岁。进行完全筛查时,绝大多数病例在1岁前确诊。如果基因检测排除RB1突变风险,则可提前终止筛查。对于RB1突变携带者,建议7岁后每1-2年进行不定期随访。
对于眼内早期病变且有望保留视功能的情况,应积极进行保眼治疗。在眼内进展期,视功能往往无法保留,但如果家属希望,可考虑保眼治疗。治疗需要高度专业性,早期转诊至专科中心至关重要。
① 激光治疗(光凝)
适用于直径约3mm以内的肿瘤。通过红外激光直接照射,局部控制率可达90%左右。如果肿瘤位于黄斑部,建议先行全身化疗以避免不可逆的视功能损害。
② 冷冻凝固
适用于赤道部及周边直径约3mm的肿瘤。通常采用三次冻融循环的三重冷冻-解冻法,局部控制率与激光治疗相似,约为90%。
③ 近距离放射治疗
适应症:肿瘤厚度≤5mm,最大直径≤15mm,远离视盘的局限性肿瘤。在日本和欧洲使用¹⁰⁶Ru(钌-106,β射线源),在北美使用¹²⁵I放射源。将放射源暂时缝合在肿瘤对应的巩膜表面。该治疗需要特殊治疗室,仅在有限机构开展。局部控制率可达80-90%。
④ 全身化疗(VEC方案)
用于眼内进展期肿瘤的一线治疗。广泛采用三药联合化疗,但单纯化疗治愈率低于10%。肿瘤缩小后,通过局部治疗(激光、冷冻、近距离放射治疗)进行巩固。
| 药物 | 剂量(体表面积基准) | 剂量(≤36个月体重基准) | 给药方案 |
|---|---|---|---|
| 长春新碱(Oncovin®) | 1.5 mg/m² | 0.05 mg/kg | 第1天 |
| 卡铂(Paraplatin®) | 560 mg/m² | 18.6 mg/kg | 第1天 |
| 依托泊苷(Vepesid®) | 150 mg/m² | 5 mg/kg | 第1、2天 |
每3~4周重复2~6次(均为静脉滴注)。
⑤ 选择性眼动脉灌注化疗(IAC)
通过导管将药物(美法仑;Alkeran®注射液)直接注入眼动脉。通过向眼部局部给予更多药物并减少全身药物量,可以减轻骨髓抑制等副作用。虽然不在医保范围内,但已在全球20多个国家开展,属于研究性治疗。
⑥ 玻璃体注射
对于玻璃体种植,全身化疗和动脉灌注的疗效有限,因此联合使用美法仑(Alkeran®注射液)的玻璃体注射。这是不在医保范围内的研究性治疗。
⑦ 外照射放疗
分次照射40~46 Gy的X射线。直到20世纪90年代,这曾是保眼治疗的主要方法,但后来发现会导致眼眶骨变形和继发性癌症增加,目前仅在其他治疗无法控制时使用。
以下情况建议进行眼球摘除。注意尽量长地切除视神经。
视神经断端阳性或巩膜外浸润是辅助治疗的绝对适应证,需进行全身化疗和放疗。明显的脉络膜浸润或超过筛板的视神经浸润被视为转移的相对危险因素。
可保留眼球的条件
需要摘除眼球的条件
对于眼内早期病变(T1),超过90%的病例可以保留眼球。通过全身化疗(VEC方案)缩小肿瘤,然后使用激光、冷冻凝固或近距离放射治疗进行巩固。对于进展期病例(T3),眼球保留率约为10%,可能需要摘除眼球。治疗方案的选择由专科医生根据分期和视功能预期决定。
位于13号染色体长臂(13q14.2)的RB1基因编码RB1蛋白(pRb),该蛋白在调控细胞分裂中起重要作用。pRb通过与E2F转录因子结合,抑制细胞周期的G1/S期转换,从而作为肿瘤抑制蛋白控制细胞增殖。
Knudson提出的二次打击学说认为,一个细胞内RB1基因的两个等位基因均失活才会导致恶性转化。
在遗传性病例中,全身细胞均存在RB1的第一次打击。当视网膜以外的细胞(如骨、软组织)发生第二次打击时,就会发生第二原发恶性肿瘤。骨肉瘤最常见,通常在10岁以后发病。接受过外照射放疗的遗传性病例,第二原发癌的风险进一步增加,因此目前外照射放疗的使用受到限制。
IAC(眼动脉内化疗)通过将美法仑直接注入眼动脉,在最小化全身毒性的同时实现眼内高浓度药物输送。即使在伴有玻璃体播散的晚期病例中,也能扩大保眼的机会。目前正在进行大规模队列的长期疗效评估。
针对玻璃体播散,采用玻璃体内注射美法仑,但国际上的剂量和给药间隔方案标准化仍是一个挑战。多个病例系列报告了较高的播散控制率,未来通过前瞻性试验确立其地位值得期待。
荷兰队列研究明确显示,完全筛查就诊与早期诊断(中位18天)之间存在相关性,并量化了筛查中断的不利影响2)。此外,针对低风险组缩短筛查终止年龄(至2岁)的提议等,基于风险分层的方案优化正在推进2)。AAOOP建议的全球推广和区域方案的标准化是未来的挑战1)。
虽然罕见,但有病例报告显示视网膜母细胞瘤与先天性脑畸形或染色体异常并存。伴有Dandy-Walker综合征的双侧视网膜母细胞瘤的报告表明,不仅需要关注眼部症状,还需要包括神经发育背景在内的全身评估的重要性。4)
随着下一代测序(NGS)的普及,生殖细胞系RB1突变的检测灵敏度得到提高。利用液体活检(循环肿瘤DNA)进行监测的可能性也在研究中,有望应用于避免侵入性活检的预后分层。
针对遗传性视网膜母细胞瘤长期幸存者的二次癌症监测方案需要标准化。特别是全身MRI多器官筛查的实施频率和终止时间,正在通过持续的队列研究积累证据。
选择性眼动脉灌注(IAC)和玻璃体内化疗(IVitC)作为提高晚期病例和玻璃体播散病例保眼率的治疗方法,正在国际上得到确立。在保守治疗的综述中,它们被定位为在不增加转移风险的情况下扩大保眼机会的策略,各国的实施情况和专业设施的集中化影响疗效。5)
发达国家的5年生存率超过95%,而非洲和亚洲的低收入及中等收入国家报告显示仅为25%至70%。系统综述和按国家收入水平进行的分析一致表明,生存率和眼球保留率存在差距,主要原因包括诊断延迟、医疗可及性不足以及专业设施缺乏。推广包括红反射法在内的社区筛查项目是一项国际挑战。6, 7)