เรติโนบลาสโตมาเป็นเนื้องอกร้ายที่เกิดในจอประสาทตา ของทารกและเด็กเล็ก โดย 95% ได้รับการวินิจฉัยก่อนอายุ 5 ปี
อุบัติการณ์ 1 ใน 15,000-23,000 คนเกิด และมีผู้ป่วย 70-80 รายต่อปีในญี่ปุ่น
การกลายพันธุ์สองขั้นตอน (สมมติฐาน two-hit) ในยีน RB1 (13q14.2) เป็นกลไกหลักของการเกิดโรค
รูม่านตาขาว (leukocoria) เป็นอาการเริ่มแรกที่พบบ่อยที่สุด และการตรวจคัดกรองรีเฟล็กซ์แดงในทารกมีความสำคัญไม่มีการตัดชิ้นเนื้อเนื้องอกภายในลูกตาเนื่องจากเสี่ยงต่อการแพร่กระจาย การรักษาเริ่มต้นจากการวินิจฉัยทางคลินิก
ในรอยโรคระยะเริ่มต้นภายในลูกตา (T1) สามารถรักษาลูกตาไว้ได้มากกว่า 90% ของกรณี การให้เคมีบำบัดทั่วร่างกาย (VEC) เพื่อทำให้เนื้องอกเล็กลง ตามด้วยการรักษาเฉพาะที่เพื่อเสริมสร้าง
อัตราการรอดชีวิต 5 ปีในประเทศพัฒนาแล้วสูงกว่า 95% ในกรณีที่ถ่ายทอดทางพันธุกรรม มะเร็งทุติยภูมิเกิดขึ้น 15.7% ใน 20 ปี
เรติโนบลาสโตมาเป็นเนื้องอกร้ายที่เกิดในจอประสาทตา ของทารกและเด็กเล็ก เป็นภาวะที่เซลล์จอประสาทตา ที่ยังไม่เจริญเต็มที่กลายเป็นมะเร็งและเพิ่มจำนวนจนเกิดเป็นก้อนเนื้องอก และถือเป็นโรคที่เกิดจากยีนเดี่ยวเนื่องจากการกลายพันธุ์ของยีน RB1 ที่อยู่บนแขนยาวของโครโมโซมคู่ที่ 13 (13q14.2) ไม่มีความแตกต่างทางเพศ และ 95% ได้รับการวินิจฉัยก่อนอายุ 5 ปี
อุบัติการณ์คือ 1 ใน 15,000-23,000 คนเกิด และมีผู้ป่วย 70-80 รายต่อปีในญี่ปุ่น อัตราส่วนของโรคข้างเดียวและสองข้างคือ 3:2 โดยอายุเฉลี่ยที่วินิจฉัยโรคข้างเดียวคือ 21 เดือน และโรคสองข้างคือ 8 เดือน ซึ่งบ่งชี้ถึงการวินิจฉัยที่เร็วกว่า อัตราการรอดชีวิต 5 ปีในประเทศพัฒนาแล้วสูงกว่า 95% สำหรับโรคที่จำกัดอยู่ในลูกตา
เรติโนบลาสโตมาแบ่งออกเป็นสองประเภทหลักตามชนิดของการกลายพันธุ์ของยีน
การจำแนกประเภท ชนิดของการกลายพันธุ์ ลักษณะของโรค ความเสี่ยงทางพันธุกรรม กรรมพันธุ์ (การกลายพันธุ์ในเซลล์สืบพันธุ์) การกลายพันธุ์ RB1 ในเซลล์สืบพันธุ์ มักเป็นสองข้างและมีหลายก้อน ถ่ายทอดสู่ลูก 50% ไม่ใช่กรรมพันธุ์ (การกลายพันธุ์ในเซลล์ร่างกาย) การกลายพันธุ์ในเซลล์ร่างกายในเซลล์จอประสาทตา เซลล์เดียว ก้อนเดียวและข้างเดียว ไม่ถ่ายทอดสู่รุ่นต่อไป
กรรมพันธุ์ (การกลายพันธุ์ในเซลล์สืบพันธุ์) : ภาวะที่มีการกลายพันธุ์ครั้งแรกในทุกเซลล์ของร่างกาย เมื่อเกิดการกลายพันธุ์ครั้งที่สองจะเกิดมะเร็ง มักทำให้เกิดเนื้องอกสองข้างและหลายก้อน ถ่ายทอดสู่เด็ก 1 ใน 2 คน (50%) มีความเสี่ยงต่อมะเร็งทุติยภูมิ เช่น มะเร็งกระดูก (15.7% ใน 20 ปี)
ไม่ใช่กรรมพันธุ์ (การกลายพันธุ์ในเซลล์ร่างกาย) : เมื่อเกิดการกลายพันธุ์ที่ตำแหน่งยีน RB1 ทั้งสองตำแหน่งในเซลล์จอประสาทตา เซลล์เดียว มีลักษณะเป็นเนื้องอกข้างเดียวและก้อนเดียว ไม่มีความเสี่ยงในการถ่ายทอดสู่รุ่นต่อไป
อย่างไรก็ตาม แม้ในกรณีที่เป็นตาเดียว บางรายก็มีการกลายพันธุ์ของ RB1 ในเซลล์สืบพันธุ์ ไม่ควรปฏิเสธลักษณะทางพันธุกรรมเพียงเพราะเป็นตาเดียว ควรตีความประวัติครอบครัว อายุที่เริ่มป่วย และจำนวนเนื้องอกโดยอาศัยการให้คำปรึกษาทางพันธุกรรม และการประเมินทางพันธุกรรม 1)
การจำแนกระยะโรคมีความสัมพันธ์โดยตรงกับแนวทางการรักษาเพื่อรักษาลูกตาไว้
ระยะ สภาพของรอยโรค อัตราการรักษาลูกตาไว้โดยประมาณ T1 (ระยะเริ่มต้นในลูกตา) จำกัดอยู่ภายในลูกตา ไม่มีการลุกลาม มากกว่า 90% T2 (ระยะลุกลามในลูกตา) ลุกลามภายในลูกตา ประมาณ 50% T3 รอยโรคลุกลามที่มีการแพร่กระจายนอกลูกตา ประมาณ 10%
Q
เรติโนบลาสโตมาเป็นโรคทางพันธุกรรมหรือไม่?
A
ประมาณ 40% เป็นโรคทางพันธุกรรม (การกลายพันธุ์ RB1 ในเซลล์สืบพันธุ์) และมีโอกาสถ่ายทอดสู่บุตร 50% ส่วนที่เหลืออีกประมาณ 60% เป็นโรคไม่ถ่ายทอดทางพันธุกรรม (การกลายพันธุ์เฉพาะเซลล์ร่างกาย) และไม่มีความเสี่ยงทางพันธุกรรมต่อรุ่นต่อไป ในกรณีที่เป็นพันธุกรรม มักเป็นทั้งสองข้างและหลายตำแหน่ง แนะนำให้ตรวจทางพันธุกรรมเมื่อวินิจฉัยและรับคำปรึกษาทางพันธุกรรม
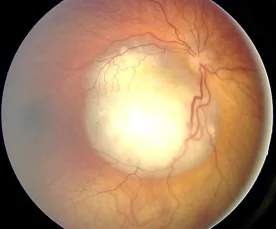
ภาพจอประสาทตาของเรติโนบลาสโตมา: ก้อนสีขาวนูนขึ้นมาอุดมด้วยหลอดเลือด Aerts I, et al. Retinoblastoma. Orphanet J Rare Dis. 2006 Aug 25; 1:31. Figure 2. PM
CI D: PMC1586012. License: CC BY.
ภาพจอประสาทตา ของเรติโนบลาสโตมาที่สังเกตเห็นเป็นรอยโรคสีขาวนูนขึ้นมาอุดมด้วยหลอดเลือด ซึ่งเป็นลักษณะเฉพาะที่ทำให้เกิดม่านตา ขาว (leukocoria) สอดคล้องกับหัวข้อ “2. อาการหลักและอาการแสดงทางคลินิก” ที่กล่าวถึงอาการแสดงทางจอประสาทตา และม่านตา ขาว
ในหลายกรณี เนื้องอกเติบโตใหญ่ภายในตาและถูกพบเมื่อมีม่านตา ขาว (leukocoria) หากเกิดที่จุดรับภาพ อาจทำให้การมองเห็น ไม่ดีและตาเหล่ นำไปสู่การตรวจพบ ในเด็กโต การรับรู้ว่าการมองเห็น ลดลงอาจเป็นอาการเริ่มแรก ส่วนในเด็กเล็ก การขยี้ตาที่มองเห็นไม่ดีอาจเป็นอาการเริ่มแรก
อาการระยะแรก
ม่านตา ขาว (leukocoria)รูม่านตา ดูเป็นสีขาว
ตาเหล่ การมองเห็น ไม่ดีเนื่องจากเนื้องอกที่จุดรับภาพ ตาที่มองเห็นไม่ดีมีแนวโน้มเบนออกด้านนอก
การรับรู้ว่าการมองเห็น ลดลง : พบในเด็กโต
การขยี้ตา : พบในเด็กเล็กในตาที่มองเห็นไม่ดี
อาการระยะลุกลาม
กระจกตา ขุ่นและความดันลูกตา สูงเลนส์แก้วตา โดยเนื้องอก หรือความดันลูกตา สูงจากต้อหิน ชนิดเส้นเลือดใหม่ (NVG )
เยื่อบุตา คั่งและเปลือกตาบวม
อาการปวด : เกิดขึ้นเนื่องจากความดันลูกตา สูงขึ้นหรือเนื้อตายของเนื้องอก
ตาโปน : พบเมื่อมีการลุกลามนอกลูกตา
พบรอยโรคสีขาวนูนขึ้นมา มีหลอดเลือดมาก หากมีหินปูนร่วมด้วยจะช่วยให้วินิจฉัยได้ง่าย มักพบร่วมกับการกระจายในวุ้นตา (เซลล์เนื้องอกแตกตัวและกระจายไปในวุ้นตา )
วิธีรีเฟล็กซ์แดงเป็นพื้นฐานในการคัดกรองโรคตาของทารก ปกติถ้ารูม่านตา ทั้งสองข้างมีขนาดเท่ากัน รีเฟล็กซ์เป็นสีเหลืองส้มสว่างและสมมาตร หากรีเฟล็กซ์มืดหรือสว่างเกินไป หรือมีความแตกต่างระหว่างสองข้าง ถือว่าผิดปกติและต้องตรวจเพิ่มเติม
Q
รูม่านตาขาวหมายถึงเรติโนบลาสโตมาเสมอหรือไม่?
A
นอกจากเรติโนบลาสโตมาแล้ว สาเหตุของรูม่านตาขาว ยังรวมถึงภาวะหลอดเลือดเหลือค้างของตัวอ่อน (persistent hyperplastic primary vitreous), จอประสาทตาผิดปกติในทารกคลอดก่อนกำหนด , โรคคาทส์ และอื่นๆ อย่างไรก็ตาม เมื่อพบรูม่านตาขาว ควรไปพบจักษุแพทย์ทันทีเพื่อแยกโรคเรติโนบลาสโตมาเป็นอันดับแรก ความล่าช้าในการวินิจฉัยส่งผลโดยตรงต่อพยากรณ์โรค ดังนั้นหากสงสัย ควรส่งต่อภายในวันเดียวกัน
สาเหตุเกิดจากการกลายพันธุ์ของยีน RB1 ซึ่งอยู่บนแขนยาวของโครโมโซมคู่ที่ 13 (13q14.2) ยีน RB1 สร้างโปรตีน RB1 (โปรตีนเรติโนบลาสโตมา) ซึ่งมีบทบาทสำคัญในการควบคุมการแบ่งตัวของเซลล์
ในเซลล์หนึ่งมีตำแหน่งยีนสองตำแหน่ง การกลายพันธุ์เพียงตำแหน่งเดียวยังคงรักษาการทำงานของเซลล์ไว้ได้ แต่เมื่อเกิดการกลายพันธุ์ทั้งสองตำแหน่ง เซลล์จะสูญเสียการควบคุมการแบ่งตัวและกลายเป็นมะเร็ง (ทฤษฎีการเกิดมะเร็งสองขั้นตอน สมมติฐานของนัดสัน)
ชนิดถ่ายทอดทางพันธุกรรม (germline mutation) : การกลายพันธุ์ครั้งแรกเป็นการกลายพันธุ์ในเซลล์สืบพันธุ์ (มีอยู่ในทุกเซลล์) เมื่อเกิดการกลายพันธุ์ครั้งที่สองในเซลล์ร่างกายหนึ่งเซลล์ จะเกิดมะเร็ง มักเป็นสองข้างและมีเนื้องอกหลายแห่งชนิดไม่ถ่ายทอดทางพันธุกรรม (somatic mutation) : การกลายพันธุ์ทั้งครั้งแรกและครั้งที่สองเกิดขึ้นในเซลล์ร่างกายเดียวกัน มีลักษณะเป็นเนื้องอกข้างเดียวและก้อนเดียว
ประวัติครอบครัวเป็นปัจจัยเสี่ยงที่สำคัญที่สุด ต่อไปนี้คือคำจำกัดความของความเสี่ยงตามคำแนะนำของ AAO OP (สมาคมจักษุวิทยาและพยาธิวิทยามะเร็งตาแห่งสหรัฐอเมริกา)1)
การจำแนกความเสี่ยง คำจำกัดความ ค่าความเสี่ยง สูง พ่อแม่เป็น Rb ทั้งสองข้าง หรือเป็นพาหะของการกลายพันธุ์ RB1 ในเซลล์สืบพันธุ์ในญาติลำดับที่ 1 หรือ 2 >7.5% ปานกลาง พ่อแม่เป็น Rb ข้างเดียว ประมาณ 7.5% ต่ำ ประวัติครอบครัวที่ห่างไกลอื่นๆ <1%
ในกรณีที่ถ่ายทอดทางพันธุกรรม ต้องระวังความเสี่ยงของมะเร็งทุติยภูมิ โรคกระดูกพรุน (osteosarcoma) เป็นตัวอย่างที่พบได้บ่อย โดยเกิดขึ้นใน 15.7% ของกรณีที่ถ่ายทอดทางพันธุกรรมภายใน 20 ปี มะเร็งทุติยภูมิมักเกิดขึ้นหลังจากอายุ 10 ปีขึ้นไป
การให้คำปรึกษาทางพันธุกรรม
เมื่อได้รับการวินิจฉัยว่าเป็นเรติโนบลาสโตมา แนะนำให้ทำการตรวจทางพันธุกรรมและการให้คำปรึกษาทางพันธุกรรม ในกรณีที่เป็นกรรมพันธุ์ สิ่งนี้ส่งผลต่อการวางแผนครอบครัว การตรวจคัดกรองพี่น้อง และการเฝ้าระวังมะเร็งทุติยภูมิ โปรดพิจารณาส่งต่อไปยังผู้ให้คำปรึกษาทางพันธุกรรมผู้เชี่ยวชาญ
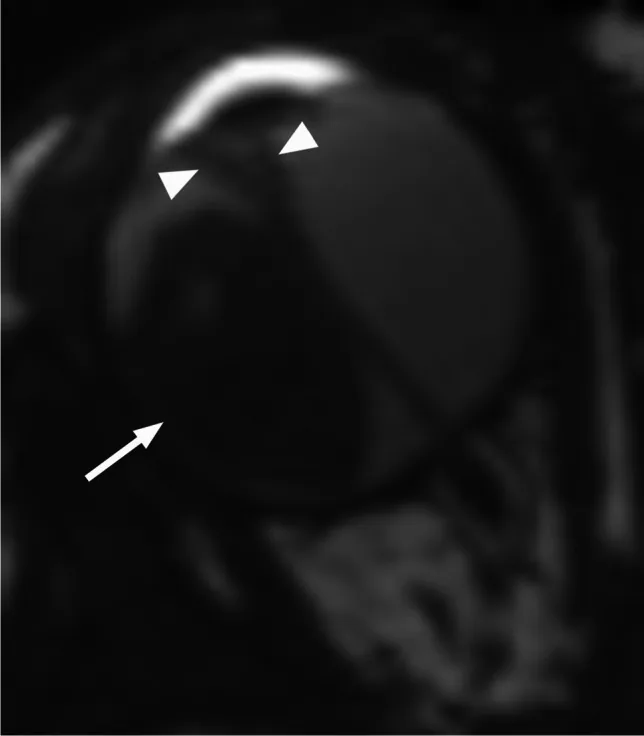
ภาพ MRI ของเรติโนบลาสโตมา: ชนิดการเจริญเติบโตแบบออกนอกลูกตาและจอประสาทตาลอกทุติยภูมิ Kato T, et al. Imaging of intraocular tumors. Neuroradiology. 2025 Dec 27; 67(2):469-492. Figure 2. PM
CI D: PMC11893699. License: CC BY.
ภาพ MRI แกนตา มขวางถ่วงน้ำหนัก T2 แสดงเรติโนบลาสโตมาชนิดเจริญเติบโตแบบออกนอกลูกตา (ลูกศร) ร่วมกับจอประสาทตาลอก รูปตัว V ทุติยภูมิ (หัวลูกศร) ซึ่งสอดคล้องกับรูปแบบการเจริญเติบโตแบบออกนอกและเข้าในลูกตา และผล MRI ที่กล่าวถึงในหัวข้อ “4. การวินิจฉัยและวิธีการตรวจ”
ไม่มีการตัดชิ้นเนื้อเนื้องอกภายในลูกตา รอยโรคภายในลูกตาสามารถสังเกตได้โดยตรงผ่านเนื้อเยื่อโปร่งใส และความแม่นยำของการวินิจฉัยทางคลินิกสูง นอกจากนี้ การตัดชิ้นเนื้อเนื้องอกภายในลูกตาอาจทำให้เซลล์เนื้องอกกระจายออกนอกลูกตา ทำให้เกิดความเสี่ยงต่อการแพร่กระจายที่ไม่สามารถหลีกเลี่ยงได้ เมื่อทำการรักษาเพื่อรักษาลูกตา การรักษาจะเริ่มต้นตามการวินิจฉัยทางคลินิก
การตรวจอวัยวะภายในลูกตา (หลัก): รอยโรคสีขาวนูนขึ้นมีหลอดเลือดมาก + การกลายเป็นปูน เพื่อการวินิจฉัยทางคลินิกที่แน่ชัดการตรวจอัลตราซาวนด์ : ยืนยันเนื้องอกเนื้อแน่นและการกลายเป็นปูน ข้อควรระวัง: การกลายเป็นปูนพบได้น้อยในเด็กอายุมากกว่า 5 ปีMRI : สัญญาณปานกลางใน T1 สัญญาณต่ำเล็กน้อยใน T2 มีการเพิ่มความเข้มของสารทึบรังสี จำเป็นสำหรับการประเมินการลุกลามของเส้นประสาทตา และการลุกลามนอกลูกตาMRI ศีรษะ : ประมาณ 3% ของผู้ป่วยสองตาเกิดเรติโนบลาสโตมาสามตำแหน่ง (เนื้องอกต่อมไพเนียล) ดังนั้นการตรวจคัดกรองจึงจำเป็นCT : ดีเยี่ยมในการแสดงการกลายเป็นปูน แต่มีการได้รับรังสี หากสามารถทำ MRI ได้ CT จะเป็นเพียงการตรวจเสริม
สิ่งที่สำคัญที่สุดคือการแยกโรคที่ทำให้เกิดม่านตา ขาว (leukocoria)
การคงอยู่ของหลอดเลือดของทารกในครรภ์ (Primary hyperplastic persistent vitreous) : การตรวจอัลตราซาวนด์เพื่อยืนยันว่ามีหรือไม่มีเนื้องอกในเนื้อเยื่อจอประสาทตา เสื่อมในทารกคลอดก่อนกำหนดโรค Coats : การสะสมของสารคัดหลั่งสีขาวเหลืองใต้จอประสาทตา รูปแบบหลอดเลือดของเนื้องอกแตกต่างกันHamartoma ของเซลล์ดาวเคราะห์ : การแยกโรคโดยพิจารณาจากการมีหรือไม่มีหลอดเลือดของเนื้องอก ตำแหน่งใน OCT และการมีหรือไม่มีการเจริญเติบโตโรคพยาธิตัวตืดในตา (cysticercosis)รูม่านตา สีขาวได้รับการผ่าตัดเอาลูกตาออกเนื่องจากสงสัยว่าเป็น Rb แต่การวินิจฉัยทางพยาธิวิทยาคือ cysticercosis3)
สำหรับการตรวจคัดกรองเด็กที่มีประวัติครอบครัวเป็น Rb ชนิด familial คำแนะนำของ AAO OP ปี 2018 ถูกอ้างอิงอย่างกว้างขวางในระดับนานาชาติ1) .
ความเสี่ยง ตารางการตรวจคัดกรอง เวลาสิ้นสุด สูง (>7.5%) แรกเกิด–8 สัปดาห์: ทุก 2–4 สัปดาห์ → 8–12 สัปดาห์: เดือนละครั้ง → 1–2 ปี: ทุก 2 เดือน → 2–3 ปี: ทุก 3 เดือน → 3–4 ปี: ทุก 4 เดือน → 4–7 ปี: ทุก 6 เดือน 7 ปี (ผู้ที่มีการกลายพันธุ์ RB1 ตลอดชีวิต) ปานกลาง (1–7.5%) แรกเกิด–3 เดือน: เดือนละครั้ง → ลดลงทีละน้อย 7 ปี ต่ำ (<1%) แรกเกิดถึง 3 เดือน: เดือนละ 1 ครั้ง → ลดลงทีละน้อย 7 ปี
ในการศึกษาย้อนหลังแบบ cohort จากเนเธอร์แลนด์ (1991–2019, 38 ใน 332 รายที่เป็น Rb ชนิด familial) ผู้ที่ได้รับการตรวจคัดกรองอย่างสมบูรณ์ทั้ง 28 รายได้รับการวินิจฉัยก่อนอายุ 1 ปี (มัธยฐาน 18 วัน) ในขณะที่ผู้ที่ได้รับการตรวจคัดกรองไม่สมบูรณ์ 10 รายได้รับการวินิจฉัยที่มัธยฐาน 420 วัน (59 วันถึง 4.8 ปี)2) นอกจากนี้ยังมีการเสนอให้ปรับเปลี่ยนโปรโตคอลเพื่อลดอายุสิ้นสุดการตรวจคัดกรองในกลุ่มความเสี่ยงต่ำ (<3%) เหลือ 2 ปี2)
ในกรณี familial การตรวจคัดกรองจอประสาทตา อย่างต่อเนื่องตั้งแต่แรกเกิดมีความสัมพันธ์โดยตรงกับพยากรณ์โรค แม้ในการศึกษาทะเบียนแบบคลาสสิก ช่วงเวลาการวินิจฉัยในครอบครัวมีความสัมพันธ์อย่างใกล้ชิดกับความถี่ในการตรวจคัดกรอง และปัจจุบันมีแนวโน้มไปสู่การปรับระยะเวลาสิ้นสุดการตรวจคัดกรองเป็นรายบุคคลตามการมีหรือไม่มีการกลายพันธุ์ของ RB11, 2)
Q
หากครอบครัวมีประวัติเป็นเรติโนบลาสโตมา เด็กต้องได้รับการตรวจคัดกรองจนถึงเมื่อใด?
A
AAO OP แนะนำให้ตรวจจอประสาทตา เป็นประจำจนถึงอายุ 7 ปี หากทำการตรวจคัดกรองอย่างสมบูรณ์ ส่วนใหญ่จะได้รับการวินิจฉัยก่อนอายุ 1 ปี หากความเสี่ยงของการกลายพันธุ์ RB1 ถูกตัดออกโดยการตรวจทางพันธุกรรม สามารถยุติการตรวจคัดกรองได้เร็วขึ้น ผู้ที่มีการกลายพันธุ์ RB1 แนะนำให้ติดตามผลอย่างไม่สม่ำเสมอทุก 1–2 ปีแม้หลังจากอายุ 7 ปี
ในระยะเริ่มต้นภายในลูกตาที่คาดว่าการมองเห็น จะดี จะทำการรักษาเพื่อสงวนลูกตาอย่างจริงจัง ในระยะลุกลามภายในลูกตา มักไม่คาดหวังการมองเห็น ที่ดี แต่สามารถพิจารณาการรักษาเพื่อสงวนลูกตาได้หากครอบครัวต้องการ การรักษาต้องอาศัยความเชี่ยวชาญสูง และการส่งต่อผู้ป่วยไปยังศูนย์เฉพาะทางตั้งแต่เนิ่นๆ เป็นสิ่งสำคัญ
① การรักษาด้วยเลเซอร์ (การจี้ด้วยแสง )
เป้าหมายคือเนื้องอกที่มีเส้นผ่านศูนย์กลางประมาณ 3 มม. สามารถควบคุมเฉพาะที่ได้ประมาณ 90% โดยการฉายแสงเลเซอร์อินฟราเรดโดยตรง หากเนื้องอกอยู่ที่จอประสาทตา ส่วนกลาง (macula) แนะนำให้ทำเคมีบำบัดทั่วร่างกายก่อนเพื่อหลีกเลี่ยงความเสียหายทางการมองเห็น ที่ถาวร
② การจี้ด้วยความเย็น
เป้าหมายคือเนื้องอกขนาดประมาณ 3 มม. ในบริเวณรอบนอกของเส้นศูนย์สูตร วิธีที่นิยมคือการแช่แข็งและละลายซ้ำ 3 ครั้ง (triple freeze-thaw) และสามารถควบคุมเฉพาะที่ได้ประมาณ 90% เช่นเดียวกับเลเซอร์
③ การรักษาด้วยแร่ธาตุกัมมันตรังสีเฉพาะที่
ใช้สำหรับเนื้องอกที่จำกัด มีความหนา ≤5 มม. และเส้นผ่านศูนย์กลาง ≤15 มม. ห่างจากจานประสาทตา ในญี่ปุ่นและยุโรปใช้แหล่งกำเนิด ¹⁰⁶Ru (รูทีเนียม-106, ปล่อยรังสีβ) ส่วนในอเมริกาเหนือใช้แหล่งกำเนิด ¹²⁵I แหล่งกำเนิดถูกเย็บติดชั่วคราวบนผิวตาขาว ที่ตรงกับเนื้องอก ต้องใช้ห้องรักษาพิเศษ ทำให้มีสถานที่จำกัด การควบคุมเฉพาะที่ทำได้ 80-90%
④ การให้เคมีบำบัดทั่วร่างกาย (VEC)
ใช้เป็นทางเลือกแรกสำหรับเนื้องอกในลูกตาระยะลุกลาม การให้เคมีบำบัดแบบสามตัวยาร่วมกันเป็นที่นิยม แต่การรักษาเดี่ยวให้หายขาดน้อยกว่า 10% หลังจากเนื้องอกเล็กลง จะทำการรักษาเฉพาะที่ (เลเซอร์, จี้เย็น, การใส่แร่ธาตุกัมมันตรังสี) เพื่อเสริมความแข็งแรง
ยา ขนาดยา (ตามพื้นที่ผิวร่างกาย) ขนาดยา (ตามน้ำหนักสำหรับเด็ก ≤36 เดือน) ตารางการให้ยา วินคริสทีน (Oncovin®) 1.5 มก./ตร.ม. 0.05 มก./กก. วันที่ 1 คาร์โบพลาติน (Paraplatin®) 560 มก./ตร.ม. 18.6 มก./กก. วันที่ 1 อีโทโพไซด์ (Vepesid®) 150 มก./ตร.ม. 5 มก./กก. วันที่ 1, 2
ทำซ้ำ 2–6 รอบ ทุก 3–4 สัปดาห์ (ทั้งหมดให้ทางหลอดเลือดดำ)
⑤ การฉีดยาเข้าหลอดเลือดแดงจักษุแบบเลือก (IAC )
ให้ยา (เมลฟาแลน; สารละลาย Alkeran®) โดยตรงไปยังหลอดเลือดแดงจักษุโดยใช้สายสวน การให้ยาในขนาดสูงเฉพาะที่ดวงตาและขนาดต่ำทั่วร่างกายสามารถลดผลข้างเคียง เช่น การกดไขกระดูกได้ นี่คือการรักษาเชิงวิจัยที่ไม่ครอบคลุมโดยประกัน แต่ดำเนินการในมากกว่า 20 ประเทศทั่วโลก
⑥ การฉีดยาเข้าน้ำวุ้นตา
สำหรับการกระจายในน้ำวุ้นตา ผลของการให้เคมีบำบัดทั่วร่างกายและการฉีดเข้าหลอดเลือดแดงมีจำกัด ดังนั้นจึงใช้การฉีดเมลฟาแลน (สารละลาย Alkeran®) เข้าน้ำวุ้นตา เสริม นี่คือการรักษาเชิงวิจัยที่ไม่ครอบคลุมโดยประกัน
⑦ การฉายรังสีภายนอก
ให้รังสีเอกซ์ขนาด 40–46 เกรย์แบบแบ่งครั้ง เป็นการรักษาหลักในการสงวนลูกตาจนถึงทศวรรษ 1990 แต่หลังจากพบความผิดปกติของเบ้าตา และการเพิ่มขึ้นของมะเร็งทุติยภูมิ ปัจจุบันใช้เฉพาะเมื่อไม่สามารถควบคุมด้วยการรักษาอื่นได้
แนะนำให้ตัดลูกตาในกรณีต่อไปนี้ ควรพยายามตัดเส้นประสาทตา ให้ยาวที่สุด
เมื่อไม่คาดหวังการทำงานของการมองเห็น
เมื่อมีต้อหิน หรือการอักเสบคล้ายเซลลูไลติสร่วมด้วย
เมื่อมีการลุกลามเข้าช่องหน้าม่านตา หรือม่านตา
เมื่อสงสัยว่ามีการลุกลามนอกลูกตา
ขอบเส้นประสาทตา เป็นบวกหรือการลุกลามนอกตาขาว เป็นข้อบ่งชี้สัมบูรณ์สำหรับการรักษาหลังผ่าตัด โดยให้เคมีบำบัดทั่วร่างกายและการฉายรังสี การลุกลามของคอรอยด์ อย่างชัดเจนหรือการลุกลามของเส้นประสาทตา เกิน lamina cribrosa จะถูกประเมินเป็นปัจจัยเสี่ยงสัมพัทธ์ต่อการแพร่กระจาย
เงื่อนไขที่สามารถรักษาลูกตาไว้ได้
T1 (รอยโรคระยะเริ่มต้นในลูกตา) : อัตราการรักษาลูกตาไว้ได้ >90%
เส้นผ่านศูนย์กลางเนื้องอก ≤3 มม. : การรักษาด้วยเลเซอร์ หรือการจี้เย็น เป็นทางเลือกแรก
ความหนาของเนื้องอก ≤5 มม. : การฝังแร่รักษาเป็นข้อบ่งชี้
เคมีบำบัดทั่วร่างกาย → การรักษาเฉพาะที่ : ในกรณีที่ลุกลาม พยายามรักษาลูกตาไว้หลังการทำให้เนื้องอกเล็กลง
เงื่อนไขที่ต้องตัดลูกตา
T3 (การลุกลามนอกลูกตา) : อัตราการรักษาลูกตาไว้ได้ประมาณ 10%
ต้อหิน ชนิดเส้นเลือดใหม่ (NVG )ความดันลูกตา ได้
การลุกลามของช่องหน้าม่านตา หรือม่านตา : ความเสี่ยงต่อการแพร่กระจายนอกลูกตา
เมื่อไม่คาดหวังการฟื้นฟูการมองเห็น : ให้ความสำคัญกับการพยากรณ์ชีวิต
การรักษาเรติโนบลาสโตมาต้องอาศัยความเชี่ยวชาญเฉพาะทางสูง การฉีดยาเข้าหลอดเลือดแดงจักษุแบบเลือกสรร (IAC ) และการปลูกแร่รังสีรักษา (brachytherapy) สามารถทำได้ในสถานพยาบาลที่มีข้อจำกัดเท่านั้น ดังนั้นการส่งต่อผู้ป่วยไปยังสถานพยาบาลเฉพาะทางตั้งแต่เนิ่นๆ จึงเป็นสิ่งสำคัญ หากสงสัย ควรส่งต่อผู้ป่วยไปยังศูนย์เฉพาะทางด้านมะเร็งจักษุวิทยาทันที
Q
มีความเป็นไปได้ที่จะรักษาลูกตาไว้หรือไม่?
A
ในรอยโรคระยะเริ่มต้นภายในลูกตา (T1) สามารถรักษาลูกตาไว้ได้มากกว่า 90% ของกรณี เนื้องอกจะถูกทำให้เล็กลงด้วยเคมีบำบัดทั่วร่างกาย (VEC) จากนั้นจึงทำให้แข็งแรงขึ้นด้วยเลเซอร์ การจี้เย็น หรือการปลูกแร่รังสีรักษา ในกรณีที่ลุกลาม (T3) อัตราการรักษาลูกตาอยู่ที่ประมาณ 10% และอาจจำเป็นต้องตัดลูกตาออก การเลือกวิธีการรักษาขึ้นอยู่กับระยะของโรคและการพยากรณ์การมองเห็น โดยแพทย์ผู้เชี่ยวชาญจะเป็นผู้ตัดสินใจ
ยีน RB1 ซึ่งอยู่บนแขนยาวของโครโมโซมคู่ที่ 13 (13q14.2) เข้ารหัสโปรตีน RB1 (pRb) ซึ่งมีบทบาทสำคัญในการควบคุมการแบ่งตัวของเซลล์ pRb จับกับปัจจัยการถอดรหัส E2F และยับยั้งการเปลี่ยนผ่าน G1/S ของวัฏจักรเซลล์ จึงควบคุมการเพิ่มจำนวนของเซลล์ในฐานะโปรตีนยับยั้งเนื้องอก
ตามทฤษฎีการกลายพันธุ์สองครั้งที่เสนอโดย Knudson การเกิดมะเร็งเกิดขึ้นเมื่ออัลลีลทั้งสองของยีน RB1 ในเซลล์เดียวถูกทำให้ไม่ทำงาน
ชนิดที่ถ่ายทอดทางพันธุกรรม : การกลายพันธุ์ครั้งแรก (การกลายพันธุ์ในเซลล์สืบพันธุ์) มีอยู่ในทุกเซลล์ เมื่อการกลายพันธุ์ครั้งที่สอง (การกลายพันธุ์ในเซลล์ร่างกาย, การสูญเสียเฮเทอโรไซโกซิตี ฯลฯ) เกิดขึ้นในเซลล์จอประสาทตา เซลล์ใดเซลล์หนึ่ง จะเกิดเนื้องอก ดังนั้นเนื้องอกมักเกิดขึ้นทั้งสองข้างและหลายตำแหน่ง และได้รับการวินิจฉัยค่อนข้างเร็วชนิดที่ไม่ถ่ายทอดทางพันธุกรรม : การกลายพันธุ์ทั้งครั้งแรกและครั้งที่สองเกิดขึ้นเป็นการกลายพันธุ์ในเซลล์ร่างกายภายในเซลล์จอประสาทตา เดียวกัน เนื่องจากความน่าจะเป็นที่การกลายพันธุ์ทั้งสองครั้งจะเกิดขึ้นโดยบังเอิญในเซลล์เดียวนั้นต่ำ เนื้องอกจึงมักเกิดขึ้นข้างเดียวและเป็นก้อนเดียว และระยะเวลาในการวินิจฉัยมักจะช้ากว่าชนิดที่ถ่ายทอดทางพันธุกรรม
ในกรณีที่ถ่ายทอดทางพันธุกรรม การกลายพันธุ์ครั้งแรกของ RB1 มีอยู่ในทุกเซลล์ของร่างกาย เมื่อการกลายพันธุ์ครั้งที่สองเกิดขึ้นในเซลล์ที่ไม่ใช่จอประสาทตา (เช่น กระดูก เนื้อเยื่ออ่อน) จะเกิดเนื้องอกมะเร็งปฐมภูมิทุติยภูมิขึ้น Osteosarcoma พบบ่อยที่สุด และมักเกิดขึ้นหลังจากอายุ 10 ปีขึ้นไป ความเสี่ยงของมะเร็งทุติยภูมิจะสูงขึ้นอีกในกรณีที่ถ่ายทอดทางพันธุกรรมซึ่งได้รับการฉายรังสีภายนอก ดังนั้นปัจจุบันจึงมีการใช้การฉายรังสีภายนอกอย่างจำกัด
IAC (เคมีบำบัดทางหลอดเลือดแดง) ฉีดเมลฟาแลนเข้าสู่หลอดเลือดแดงจักษุโดยตรง ทำให้ส่งยาเข้มข้นสูงเข้าสู่ลูกตาโดยมีพิษต่อระบบร่างกายน้อยที่สุด สามารถเพิ่มโอกาสในการสงวนลูกตาได้แม้ในกรณีลุกลามที่มีการกระจายในวุ้นตา ปัจจุบันกำลังมีการประเมินผลระยะยาวในกลุ่มตัวอย่างขนาดใหญ่
การฉีดเมลฟาแลนเข้าวุ้นตา ดำเนินการเพื่อจัดการกับการกระจายในวุ้นตา แต่การทำให้โปรโตคอลขนาดยาและช่วงการให้ยาเป็นมาตรฐานในระดับนานาชาติยังคงเป็นความท้าทาย มีรายงานอัตราการควบคุมการกระจายที่สูงในหลายชุดผู้ป่วย และคาดว่าการศึกษาไปข้างหน้าในอนาคตจะกำหนดบทบาทของมัน
การศึกษากลุ่มตัวอย่างในเนเธอร์แลนด์แสดงความสัมพันธ์ที่ชัดเจนระหว่างการตรวจคัดกรองอย่างสมบูรณ์และการวินิจฉัยเร็ว (มัธยฐาน 18 วัน) และวัดผลเสียของการหยุดตรวจคัดกรอง 2) การปรับโปรโตคอลตามการแบ่งระดับความเสี่ยงก็กำลังดำเนินการ เช่น ข้อเสนอให้ลดอายุสิ้นสุดการตรวจคัดกรอง (2 ปี) สำหรับกลุ่มเสี่ยงต่ำ 2) การเผยแพร่คำแนะนำของ AAO OP ทั่วโลกและการทำให้โปรโตคอลระดับภูมิภาคเป็นมาตรฐานเป็นความท้าทายในอนาคต 1)
แม้จะพบได้ยาก แต่มีรายงานผู้ป่วยเรติโนบลาสโตมาร่วมกับความพิการแต่กำเนิดของสมองหรือความผิดปกติของโครโมโซม รายงานผู้ป่วยเรติโนบลาสโตมาทั้งสองข้างร่วมกับกลุ่มอาการแดนดี-วอล์กเกอร์ชี้ให้เห็นความสำคัญของการประเมินทั้งร่างกายรวมถึงพื้นฐานพัฒนาการทางระบบประสาทนอกเหนือจากอาการทางตา 4)
ด้วยการแพร่หลายของการหาลำดับรุ่นใหม่ (NGS) ความไวในการตรวจหาการกลายพันธุ์ RB1 ในเซลล์สืบพันธุ์เพิ่มขึ้น ความเป็นไปได้ในการติดตามโดยใช้การตรวจชิ้นเนื้อของเหลว (DNA เนื้องอกหมุนเวียนในเลือด) ก็กำลังถูกศึกษา ซึ่งคาดว่าจะนำไปใช้ในการแบ่งระดับพยากรณ์โรคโดยไม่ต้องตรวจชิ้นเนื้อที่รุกล้ำ
จำเป็นต้องมีมาตรฐานโปรโตคอลการเฝ้าระวังมะเร็งทุติยภูมิสำหรับผู้รอดชีวิตระยะยาวของเรติโนบลาสโตมาทางพันธุกรรม โดยเฉพาะอย่างยิ่งเกี่ยวกับความถี่และเวลาสิ้นสุดของการตรวจคัดกรองหลายอวัยวะโดยใช้ MRI ทั้งตัว หลักฐานกำลังถูกสะสมผ่านการศึกษากลุ่มตัวอย่างอย่างต่อเนื่อง
การฉีดเข้าหลอดเลือดแดงจักษุแบบเลือก (IAC ) และเคมีบำบัดเข้าวุ้นตา (IVitC) ได้รับการยอมรับในระดับนานาชาติมากขึ้นว่าเป็นการรักษาที่ยกระดับอัตราการสงวนลูกตาในกรณีลุกลามหรือมีการกระจายในวุ้นตา ในการทบทวนอย่างครอบคลุมของการรักษาแบบอนุรักษ์ พวกมันถูกวางตำแหน่งเป็นกลยุทธ์เพื่อขยายการสงวนลูกตาโดยไม่เพิ่มความเสี่ยงของการแพร่กระจาย และผลลัพธ์ได้รับอิทธิพลจากการนำไปใช้ในแต่ละประเทศและการรวมศูนย์สิ่งอำนวยความสะดวกเฉพาะทาง 5)
แม้ว่าอัตราการรอดชีวิต 5 ปีในประเทศพัฒนาแล้วจะสูงกว่า 95% แต่รายงานระบุว่าในประเทศที่มีรายได้ต่ำและปานกลางในแอฟริกาและเอเชียอยู่ที่เพียง 25-70% การทบทวนอย่างเป็นระบบและการวิเคราะห์ตามระดับรายได้ของประเทศแสดงให้เห็นถึงความเหลื่อมล้ำในอัตราการรอดชีวิตและการรักษาลูกตาอย่างสม่ำเสมอ โดยปัจจัยหลักคือการวินิจฉัยที่ล่าช้า การเข้าถึงบริการสุขภาพที่ไม่เพียงพอ และการขาดแคลนสถานพยาบาลเฉพาะทาง การเผยแพร่โปรแกรมคัดกรองในชุมชน รวมถึงวิธีการสะท้อนแสงแดง เป็นความท้าทายระดับนานาชาติ 6, 7)
Skalet AH, Gombos DS, Gallie BL, et al. Screening children at risk for retinoblastoma: consensus report from the American Association of Ophthalmic Oncologists and Pathologists. Ophthalmology. 2018;125(3):453-458.
Badalova NA, van Hoefen Wijsard M, Dommering CJ, et al. At what age could screening for familial retinoblastoma be stopped? Revised Dutch retrospective population-based cohort study 1991-2019. Ophthalmology. 2024;131(10):1189-1196.
Jakati S, Vempuluru VS, Kaliki S. Intraocular cysticercosis masquerading as cavitary retinoblastoma. Ophthalmology. 2023;130(12):e90.
Lomi N, Das D, Chawla B, et al. Retinoblastoma in Dandy-Walker Syndrome. Cureus. 2025;17(8):e89663.
Munier FL, Beck-Popovic M, Chantada GL, et al. Conservative management of retinoblastoma: challenging orthodoxy without compromising the state of metastatic grace. Prog Retin Eye Res. 2019;73:100764.
Wong ES, Choy RW, Zhang Y, et al. Global retinoblastoma survival and globe preservation: a systematic review and meta-analysis. Lancet Glob Health. 2022;10(3):e380-e389.
Fabian ID, Abdallah E, Abdullahi SU, et al. Global retinoblastoma presentation and analysis by national income level. JAMA Oncol. 2020;6(5):685-695.