เนื้องอกหลอดเลือดฝอยจอตา (เนื้องอกหลอดเลือดจอตา) เป็นเนื้องอกหลอดเลือดชนิดไม่ร้ายที่เกิดขึ้นในจอตาหรือหัวประสาทตา แบ่งออกเป็นชนิดประปราย (โรค Von Hippel) และชนิดทั่วร่างกาย (โรค VHL)โรค VHL เป็นกลุ่มอาการเนื้องอกทางพันธุกรรมแบบถ่ายทอดยีนเด่นบนออโตโซม ความถี่ 1 ใน 36,000 คน ผู้ป่วย VHL 40-70% มี hemangioma จอประสาทตา
ลักษณะ fundus: ก้อนกลมสีส้มแดง ร่วมกับหลอดเลือดแดงนำเข้าและหลอดเลือดดำนำออกที่ขยายและคดเคี้ยว ผลิต VEGF จำนวนมาก ทำให้เกิดจอประสาทตาลอก แบบ exudative
ในชนิดรอบนอก การจี้ด้วยเลเซอร์เป็นทางเลือกแรก หากก้อนมีขนาดเล็กกว่า 1 เส้นผ่านศูนย์กลาง papilla สามารถคาดหวังการหายขาดได้
ชนิด papilla ประสาทตายังไม่มีวิธีการรักษาที่ชัดเจน มากกว่า 50% มีสายตา 0.1 หรือน้อยกว่า เป็นชนิดพยากรณ์โรคไม่ดี
เด็กจากครอบครัว VHL ควรเริ่มตรวจ fundus ตั้งแต่แรกเกิด โดยเฝ้าระวังอย่างน้อยปีละครั้ง
Belzutifan (ยับยั้ง HIF-2α) แสดงผลทำให้ hemangioma จอประสาทตา หดตัว 100% ถือเป็นตัวเลือกการรักษามาตรฐานในอนาคต (ยังอยู่ในขั้นตอนการวิจัย)
hemangioma หลอดเลือดฝอยจอประสาทตา (retinal capillary hemangioma ) เป็นเนื้องอกไม่ร้ายสีส้มที่เกิดขึ้นในจอประสาทตา หรือ papilla ประสาทตาในคนหนุ่มสาว เนื่องจากมีความคล้ายคลึงทางพยาธิวิทยากับ hemangioblastoma สมอง ปัจจุบันจึงเรียกอีกชื่อว่า retinal hemangioblastoma สามารถเกิดแบบเดี่ยว/หลายก้อน ข้างเดียว/สองข้าง กระจาย/เป็นกลุ่มอาการ
เมื่อเกิด retinal hemangioblastoma แบบกระจายเพียงอย่างเดียว เรียกว่าโรค von Hippel หากร่วมกับกลุ่มอาการเนื้องอกทั่วร่างกาย จะวินิจฉัยเป็นโรค VHL (von Hippel-Lindau) ในอภิธานศัพท์ของสมาคมจักษุวิทยาญี่ปุ่น ใช้คำว่า “hemangioma จอประสาทตา ” ตามแนวทางปฏิบัติ VHL (ฉบับปี 2024) แต่บทความนี้ใช้คำทั่วไป “hemangioma หลอดเลือดฝอยจอประสาทตา ”
โรค VHL เป็นกลุ่มอาการเนื้องอกทางพันธุกรรมแบบถ่ายทอดยีนเด่นบนออโตโซม เกิดจากการกลายพันธุ์ของยีน VHL (3p25-26) ซึ่งเป็นยีนกดเนื้องอก ความถี่ 1 ใน 36,000 คน นอกจาก hemangioma จอประสาทตา แล้ว โรค VHL ยังรวมถึง hemangioblastoma ในสมองน้อย เมดัลลาออบลองกาตา พอนส์ และไขสันหลัง มะเร็งเซลล์ไต ฟีโอโครโมไซโตมา และซีสต์ในอวัยวะช่องท้อง (ตับอ่อน ไต ต่อมหมวกไต) การรอดชีวิตขึ้นอยู่กับการจัดการรอยโรคทั่วร่างกาย จึงจำเป็นต้องมีความร่วมมือแบบสหสาขาวิชาชีพ
Q
เมื่อใดที่ควรสงสัยโรค VHL?
A
ตามเกณฑ์การวินิจฉัยของแนวทางปฏิบัติ VHL (ฉบับปี 2024) หากมีประวัติครอบครัว รอยโรคหนึ่งรายการขึ้นไป (hemangioblastoma หรือ hemangioma จอประสาทตา ) ก็เพียงพอสำหรับการวินิจฉัย 1) หากไม่มีประวัติครอบครัว ต้องมีรอยโรคสองรายการขึ้นไป (รวมถึง hemangioblastoma หรือ hemangioma จอประสาทตา ) หรือยืนยันการกลายพันธุ์ของยีน VHL ร่วมกับรอยโรคหนึ่งรายการ ใน hemangioma จอประสาทตา แบบกระจายในคนหนุ่มสาว โดยเฉพาะอายุต่ำกว่า 10 ปี มักได้รับการวินิจฉัยภายหลังเป็นโรค VHL ดังนั้นควรพิจารณาการตรวจร่างกายทั่วร่างกายและการตรวจทางพันธุกรรมอย่างจริงจัง
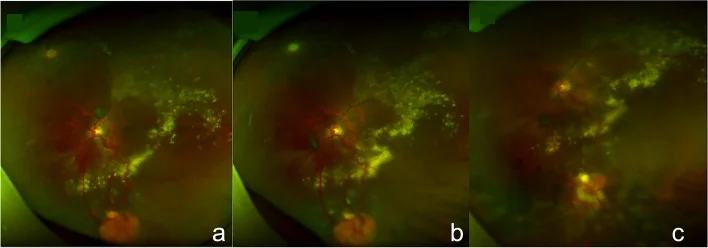
Guo J, et al. Multimodal imaging for eleven retinal capillary hemangioblastomas in a Von Hippel-Lindau syndrome patient: a case report. BMC Ophthalmol. 2022;22:205. Figure 4. PM
CI D: PMC9074324. License: CC BY.
ภาพถ่าย fundus แสดง
hemangioma หลอดเลือดฝอย
จอประสาทตา สีส้มแดงทั่วไปใน
จอประสาทตา ส่วนรอบ โดยมีหลอดเลือดเลี้ยงที่ขยายและคดเคี้ยวอย่างเด่นชัด (หลอดเลือดแดงนำเข้าและหลอดเลือดดำนำออก) และแนวทางการหดตัวของเนื้องอกหลัง
การจี้เย็น สอดคล้องกับลักษณะ fundus ที่กล่าวถึงในหัวข้อ “2. อาการหลักและอาการแสดงทางคลินิก”
เรติโนบลาสโตมา (hemangioblastoma) ของจอประสาทตา แบ่งตามลักษณะการเกิดและตำแหน่งดังนี้:
ชนิดรอบนอก
ความถี่ : ชนิดทั่วไปที่พบได้บ่อยที่สุด
ลักษณะจอตา : ก้อนกลมสีส้มแดงบริเวณรอบนอกจอตา ร่วมกับหลอดเลือดแดงและดำที่ขยายและคดเคี้ยวอย่างเห็นได้ชัด
การดำเนินโรค : ค่อยๆ ดำเนินไปจาก hemangioblastoma ฝอย → ก้อนชัดเจน → การเปลี่ยนแปลงแบบมีสารคัดหลั่ง → จอตาลอกแบบมีสารคัดหลั่ง → การเจริญของเนื้อเยื่อเส้นใย
ชนิดหัวประสาทตา
ความถี่ : ประมาณ 15% ของทั้งหมด
ลักษณะจอตา : เกิดขึ้นใกล้หัวประสาทตา มักระบุหลอดเลือดนำเข้าและออกได้ยาก
พยากรณ์โรค : ชนิดที่มีพยากรณ์โรคไม่ดี โดยการมองเห็น ≤0.1 ในมากกว่า 50% ของกรณี ยังไม่มีการรักษาที่เป็นมาตรฐาน
มักไม่มีอาการในระยะแรก เมื่อรอยโรคดำเนินไป จะมีอาการดังนี้:
การมองเห็น ลดลงจุดลอยและแสงวาบ : อาจพบได้ค่อนข้างเร็วข้อบกพร่องของลานสายตา : ในรอยโรคชนิดรอบนอก ลานสายตาส่วนรอบจะเสียก่อน
เลือดออกพบได้น้อย แต่ในกรณีที่ลุกลามอาจเกิดเลือดออกในน้ำวุ้นตา ได้
ลักษณะเฉพาะของการตรวจอวัยวะภายในตา (fundus) คือ เนื้องอกจอประสาทตา รูปกลมเดี่ยวหรือหลายก้อน เนื้องอกบริเวณรอบนอกมักมีหลอดเลือดแดงและดำที่ขยายและคดเคี้ยวร่วมด้วย และรอยโรคมักปรากฏก่อนอายุ 30 ปี ประมาณครึ่งหนึ่งของกรณีเป็นทั้งสองข้าง และอาจเกิดในตำแหน่งต่างๆ ของอวัยวะภายในตาได้หลายตำแหน่ง
ตัวเนื้องอกเองคือ hemangioblastoma ซึ่งประกอบด้วยเส้นเลือดฝอยและเซลล์สโตรมาที่มีลักษณะเป็นฟอง และผลิต VEGF (vascular endothelial growth factor) ในปริมาณมาก VEGF ทำให้เกิดจอประสาทตาลอก แบบมีน้ำใต้จอประสาทตา (exudative retinal detachment) ซึ่งทำให้การมองเห็น ลดลง
การตรวจหลอดเลือดด้วยสีเรืองแสงแสดงการเปลี่ยนแปลงสามระยะที่มีลักษณะเฉพาะ
ระยะต้น : มองเห็นหลอดเลือดแดงที่ชัดเจนระยะกลาง : ภายในเนื้องอกมีการเรืองแสงมากเกินไป และมองเห็นหลอดเลือดดำระยะปลาย : มีการรั่วของสีเรืองแสงอย่างรุนแรง โดยมีการสะสมของสีเรืองแสงที่สอดคล้องกับจอประสาทตาลอก
เมื่อลุกลาม จะเปลี่ยนไปสู่ภาวะทางพยาธิสภาพที่รุนแรงดังต่อไปนี้:
จอประสาทตาลอก แบบดึงรั้ง (tractional retinal detachment)เยื่อเหนือจอประสาทตา และการดึงรั้งเนื่องจากการเจริญของเนื้อเยื่อเส้นใยต้อหิน ชนิดเส้นเลือดใหม่ (neovascular glaucoma)ความดันลูกตา สูงและปวดตา การขยายตัวของหลอดเลือดเยื่อบุตา และเหนือตาขาว อย่างเด่นชัด : ในกรณีที่ลุกลามมาก มีรายงานตาขวา NLP และความดันลูกตา 45 mmHg 2)
การถ่ายภาพจอประสาทตา มุมกว้างและการตรวจหลอดเลือดด้วย OCT (OCTA ) มีประโยชน์ในการประเมินและติดตามรอยโรค 1) OCT สามารถประเมินรูปร่างของก้อนเนื้อ การมีของเหลวใต้จอประสาทตา และอาการบวมน้ำที่จุดรับภาพ
ความถี่ของโรค VHL คือ 1 ใน 36,000 คน จำนวนผู้ป่วย VHL ในญี่ปุ่นประมาณ 600–1,000 ราย อุบัติการณ์ของ hemangioma จอประสาทตา ในผู้ป่วย VHL อยู่ที่ 40–70% โดยอายุเฉลี่ยที่เริ่มมีอาการคือ 25 ปี 1)
การกระจายอายุที่เริ่มมีอาการ : พบมากในช่วงอายุ 10–40 ปี ประมาณ 5% เริ่มมีอาการก่อนอายุ 10 ปีเป็นทั้งสองข้าง : ประมาณครึ่งหนึ่งของกรณีเป็นทั้งสองข้างหลายก้อน : อาจเกิดก้อนเนื้อหลายก้อนในตาเดียวกันความเสี่ยงของการ发展为 VHL ในกรณีประปราย : ในกรณีที่ได้รับการวินิจฉัยว่าเป็นประปราย 45% ของเด็กอายุต่ำกว่า 10 ปีได้รับการวินิจฉัยในภายหลังว่าเป็นโรค VHL
ยีน VHL ถ่ายทอดทางพันธุกรรมแบบ autosomal dominant (เดิมเรียกว่า dominant autosomal) การกลายพันธุ์ใน germline ที่อัลลีลหนึ่ง (hit แรก) และ hit ที่สองในเซลล์ร่างกายทำให้สูญเสียการทำงานของ tumor suppressor (สมมติฐาน two-hit)
ในฐานะปัจจัยเสี่ยงทางพันธุกรรม สมาชิกทุกคนในครอบครัวที่มีการกลายพันธุ์ที่ก่อโรคของยีน VHL จำเป็นต้องได้รับการเฝ้าระวัง และควรพิจารณาการตรวจยีน VHL ในกรณี hemangioma จอประสาทตา ที่อายุต่ำกว่า 40 ปี 1)
เกณฑ์การวินิจฉัยตามแนวทางปฏิบัติ VHL (ฉบับปี 2024) มีดังนี้ 1) :
สถานการณ์ เกณฑ์การวินิจฉัย ประวัติครอบครัวเป็นบวก รอยโรคอย่างน้อยหนึ่งรอย เช่น hemangioblastoma หรือ hemangioma จอประสาทตา ไม่มีประวัติครอบครัว รอยโรค ≥2 รอยโรค (รวมถึง hemangioblastoma/retinal angioma) หรือการกลายพันธุ์ของยีน VHL + 1 รอยโรค
ในการตรวจอวัยวะรับภาพ (fundus) การพบก้อนสีส้มแดงบริเวณรอบนอกและหลอดเลือดแดงและดำที่ขยายและคดเคี้ยวเป็นลักษณะเฉพาะ การประเมินทำโดยการตรวจร่วมกันดังต่อไปนี้:
การถ่ายภาพอวัยวะรับภาพมุมกว้าง : มีประโยชน์ในการเห็นภาพรวมของรอยโรคบริเวณรอบนอกการถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน (FA ) : การระบุเนื้องอกและการประเมินกิจกรรม การรั่วของฟลูออเรสซีน ในระยะแรกและมากเป็นพื้นฐานของการวินิจฉัยOCT /OCTA จอประสาทตา บวมน้ำและของเหลวใต้จอประสาทตา การตรวจอัลตราซาวนด์ (B-mode) : การยืนยันก้อนเนื้อแข็งและการประเมินจอประสาทตาลอก
ในครอบครัวที่มี VHL การตรวจอวัยวะรับภาพเริ่มตั้งแต่แรกเกิด (อายุ 0 ปี) และตรวจอย่างสม่ำเสมออย่างน้อยปีละครั้ง1) การใช้กล้องถ่ายภาพอวัยวะรับภาพแบบไม่ขยายม่านตา ร่วมกับการถ่ายภาพมุมกว้างช่วยป้องกันการมองข้ามรอยโรคบริเวณรอบนอก
ในโรค VHL รอยโรคหลายแห่งอาจเกิดขึ้นในอวัยวะอื่นนอกเหนือจากจอประสาทตา ดังนั้นการค้นหาทั่วร่างกายอย่างสม่ำเสมอโดยทีมสหสาขาวิชาชีพจึงเป็นสิ่งจำเป็น1)
MRI ศีรษะ : การตรวจคัดกรอง hemangioblastoma ในสมองน้อย ก้านสมอง และไขสันหลังอัลตราซาวนด์ช่องท้อง/CT/MRI : การค้นหามะเร็งเซลล์ไต ถุงน้ำในตับอ่อน ไต และต่อมหมวกไตการตรวจคัดกรอง pheochromocytoma : การวัดสารเมแทบอไลต์ของ catecholamine ในปัสสาวะควรตรวจคัดกรองทั่วร่างกายดังกล่าวข้างต้นอย่างต่อเนื่องปีละครั้งเป็นแนวทาง
การตรวจยีน VHL มีข้อบ่งชี้ในผู้ป่วยอายุต่ำกว่า 40 ปีที่มี hemangioma จอประสาทตา แบบเดี่ยว หรือในผู้ป่วยและครอบครัวที่สงสัยว่าเป็นโรค VHL 1) ควรทำควบคู่กับการให้คำปรึกษาทางพันธุกรรม
จำเป็นต้องแยกโรคจากโรคต่อไปนี้:
โรค Coats : พบมากในเด็กผู้ชาย ไม่มีการขยายและคดเคี้ยวของหลอดเลือดนำเข้าและนำออก แต่มีสารหลั่งแข็งและจอประสาทตาลอก แบบมีสารหลั่งกลุ่มอาการ Wyburn-Mason (angioma racemosum) : ความผิดปกติของหลอดเลือดแดงและดำในจอประสาทตา และสมองHemangioma คอรอยด์ : รอยโรคสีส้มแดง แต่ไม่มีภาวะแทรกซ้อนทางระบบของโรค VHLเนื้องอกหลอดเลือด增生จอประสาทตา (vasoproliferative tumor) : มักเกิดบริเวณส่วนปลายด้านล่าง ต้องแยกจากการเปลี่ยนแปลงทุติยภูมิ
Q
พบรอยโรคที่จอประสาทตาของ hemangioma จอประสาทตาได้ที่ไหน?
A
ชนิดส่วนปลายมักเกิดบริเวณรอบนอกของจอประสาทตา ดังนั้นจึงจำเป็นต้องตรวจจอประสาทตา อย่างละเอียดภายใต้การขยายม่านตา เนื้องอกขนาดเล็กในระยะแรกอาจมีลักษณะคล้าย capillary aneurysm และการใช้การถ่ายภาพจอประสาทตา มุมกว้างสามารถช่วยป้องกันการมองข้ามได้ ชนิด papillary จะปรากฏเป็นก้อนรอบขั้วประสาทตา และมักระบุหลอดเลือดนำเข้าและนำออกได้ยาก
เลือกวิธีการรักษาตามตำแหน่ง ขนาด และระดับการเปลี่ยนแปลงแบบมีสารหลั่งของ hemangioma เนื่องจาก hemangioma จะรักษายากเมื่อมีขนาดใหญ่ขึ้น การตรวจพบและการรักษาตั้งแต่เนิ่นๆ จึงมีความสำคัญ การเริ่มการรักษาเมื่อรอยโรคยังเล็กสามารถช่วยพยากรณ์การมองเห็น ได้ดีขึ้น
การจี้ด้วยเลเซอร์ (Laser Photocoagulation)
ข้อบ่งชี้ : ทางเลือกแรกสำหรับชนิดรอบนอก (peripheral type) สำหรับรอยโรคที่มีขนาด ≤1 เส้นผ่านศูนย์กลางของหัวประสาทตา สามารถคาดหวังการหายขาดได้
วิธีการ : ทำการจี้โดยตรงที่ hemangioma ซ้ำจนกว่าจะได้ผลเพียงพอ แนะนำให้ทำ photocoagulation ตั้งแต่เนิ่นๆ แม้ในรอยโรคขนาดเล็ก <1 เส้นผ่านศูนย์กลางของหัวประสาทตา1)
ข้อจำกัด : รอยโรคขนาดใหญ่ >1 เส้นผ่านศูนย์กลางของหัวประสาทตา จำเป็นต้องรักษาหลายครั้ง
การจี้ด้วยความเย็น (Cryocoagulation)
ข้อบ่งชี้ : รอยโรคขนาดใหญ่ หรือกรณีที่เข้าถึงได้ยากด้วยการจี้ด้วยเลเซอร์
วิธีการ : เลือกการจี้ด้วยความเย็นตามขนาดและระดับการยื่นออกมาของ hemangioma
เมื่อมีการเปลี่ยนแปลงแบบ exudative ร่วมด้วย : ทำการระบายของเหลวใต้จอประสาทตา การจี้ด้วยไฟฟ้า (diathermy) ฯลฯ แต่รักษายาก
จอประสาทตาลอก แบบ tractionalจอประสาทตาลอก แบบ tractional ให้ทำการผ่าตัดน้ำวุ้นตา (vitrectomy)
PDT และการรักษาด้วย Anti-VEGFการรักษาด้วยแสงไดนามิก (PDT ) และยาต้าน VEGF (bevacizumab, ranibizumab ฯลฯ) ทั้งแบบเดี่ยวและแบบผสมผสานสะสมมากขึ้น3) ใช้เพื่อช่วยยับยั้งการเปลี่ยนแปลงแบบ exudative แต่ไม่ครอบคลุมโดยประกัน และต้องพิจารณาเป็นรายกรณี
ยังไม่มีการกำหนดวิธีการรักษามาตรฐานสำหรับชนิดหัวประสาทตา1) การจี้ด้วยเลเซอร์มีความเสี่ยงสูงต่อการทำลายเส้นประสาทตา และจอประสาทตา ส่วนกลาง (macula) ดังนั้นจึงต้องพิจารณาข้อบ่งชี้อย่างระมัดระวังเป็นพิเศษ มีรายงานการรักษาต่อไปนี้ในระดับรายงานผู้ป่วย แต่ยังไม่มีการกำหนดให้เป็นการรักษามาตรฐาน
การฉีดยา Anti-VEGF เข้าในน้ำวุ้นตา : คาดว่ามีผลในการยับยั้งการเปลี่ยนแปลงแบบ exudative แต่ผลในการทำให้เนื้องอกเล็กลงมีจำกัดPDT (การรักษาด้วยแสงไดนามิก )3) 4) การรักษาด้วยโปรตอน (Proton Beam Therapy) : การฉายรังสีแบบเข้มข้นไปที่เนื้องอก5)
จำเป็นต้องประเมินจังหวะเวลาในการแทรกแซงอย่างรอบคอบ และแนะนำให้มีการประชุมสหสาขาวิชาชีพในสถานพยาบาลเฉพาะทาง
หลังการรักษา มักเกิดการกลับเป็นซ้ำและรอยโรคใหม่ ดังนั้นจึงจำเป็นต้องติดตามผลตลอดชีวิต หลังการรักษาแต่ละครั้ง ควรตรวจอวัยวะภายในลูกตาภายใน 3-6 เดือนเพื่อยืนยันประสิทธิภาพและตรวจหารอยโรคใหม่ ในโรค VHL เนื่องจากรอยโรคหลายแห่งปรากฏในเวลาที่ต่างกัน อย่าละเลยการตรวจอวัยวะภายในลูกตาทั้งหมด
ในโรค VHL การจัดการมะเร็งเซลล์ไตและฮีแมงจิโอบลาสโตมาของระบบประสาทส่วนกลางมีความสำคัญต่อการพยากรณ์โรคเพื่อการอยู่รอด ควรดำเนินการเฝ้าระวังและแทรกแซงที่เหมาะสมสำหรับรอยโรคของแต่ละอวัยวะโดยร่วมมือกับสหสาขาวิชาชีพ เช่น ศัลยกรรมประสาท ระบบทางเดินปัสสาวะ ต่อมไร้ท่อ เป็นต้น
ยีน VHL เป็นยีนต้านเนื้องอกที่อยู่บนโครโมโซม 3p25-26 และเข้ารหัสโปรตีน pVHL ซึ่งเป็นส่วนประกอบของคอมเพล็กซ์ E3 ubiquitin ligase หน้าที่หลักของโปรตีน pVHL คือการเติมยูบิควิตินและย่อยสลายสายอัลฟาของปัจจัยเหนี่ยวนำภาวะขาดออกซิเจน (HIF) ผ่านโปรตีอาโซม
ภายใต้สภาวะปกติ HIFα จะถูกจดจำโดย pVHL ถูกเติมยูบิควิติน และถูกย่อยสลายอย่างรวดเร็ว เมื่อยีน VHL ถูกยับยั้งการทำงาน หน้าที่ของ pVHL จะสูญเสียไป และ HIFα จะสะสม
ในโรค VHL นอกจากการกลายพันธุ์ในเซลล์สืบพันธุ์ (การตีครั้งแรก) การตีครั้งที่สองในเซลล์ร่างกาย (เช่น การสูญเสียเฮเทอโรไซโกซิตี) ทำให้การทำงานของยีน VHL สูญเสียไปโดยสิ้นเชิง นำไปสู่การเกิดเนื้องอก
เมื่อ HIFα สะสมในนิวเคลียส การถอดรหัสของยีนที่เกี่ยวข้องกับการสร้างหลอดเลือดและการเพิ่มจำนวนเซลล์หลายชนิด เช่น VEGF, PDGF และ EPO จะถูกกระตุ้นอย่างต่อเนื่อง ในโรค VHL HIF-2α (EPAS 1) ทำหน้าที่เป็นตัวขับเคลื่อนหลัก1)
เรติโนบลาสโตมา (Retinal hemangioblastoma) ประกอบด้วยเซลล์สองชนิด
เซลล์สโตรมาชนิดฟอง (Foamy stromal cells) : อุดมไปด้วยไขมันและผลิตไซโตไคน์จำนวนมากรวมถึง VEGFเส้นเลือดฝอย : ถูกเหนี่ยวนำแบบทุติยภูมิโดย VEGF ที่ผลิตโดยเซลล์สโตรมา
เซลล์สโตรมาเหล่านี้เป็นเนื้อแท้ของเนื้องอก และการผลิต VEGF อย่างต่อเนื่องเป็นสาเหตุโดยตรงของการเพิ่มจำนวนหลอดเลือดในเนื้องอกและการลอกของจอประสาทตา แบบมีน้ำใต้จอประสาทตา (exudative retinal detachment)
ความสัมพันธ์ระหว่างการกลายพันธุ์ของยีน VHL และฟีโนไทป์ทางคลินิก (ชนิดที่ 1: ไม่มีฟีโอโครโมไซโตมา, ชนิดที่ 2: มีฟีโอโครโมไซโตมา เป็นต้น) เป็นที่ทราบกันบางส่วน แต่การจำแนกประเภทโดยละเอียดและความแตกต่างของความถี่ของการเกี่ยวข้องกับตายังคงรอการวิเคราะห์เพิ่มเติมในอนาคต
เนื้อหาต่อไปนี้ยังอยู่ในขั้นตอนการวิจัยหรือการทดลองทางคลินิก และไม่ใช่การรักษามาตรฐานที่สามารถรับได้ในโรงพยาบาลทั่วไป เป็นข้อมูลอ้างอิงสำหรับผู้เชี่ยวชาญเกี่ยวกับความก้าวหน้าทางการแพทย์ในอนาคต
Belzutifan เป็นสารประกอบโมเลกุลเล็กที่ยับยั้ง HIF-2α อย่างจำเพาะ และได้รับการอนุมัติจาก FDA (สำนักงานคณะกรรมการอาหารและยาของสหรัฐอเมริกา) ในปี 2021 สำหรับผู้ป่วย VHL ที่มีมะเร็งเซลล์ไตชนิดแพร่กระจาย, hemangioblastoma ของระบบประสาทส่วนกลาง และ hemangioblastoma ของจอประสาทตา 7)
ผลการทดลองระยะที่ 2 (LITESPARK-004) สำหรับ hemangioma ของจอประสาทตา มีดังนี้1) :
อัตราการตอบสนอง : 100% (12/12 ราย) พบว่าเนื้องอกหดตัวมะเร็งเซลล์ไต : ตอบสนองใน 49%Hemangioblastoma ของระบบประสาทส่วนกลาง : ตอบสนองใน 30%
รายงานอาการไม่พึงประสงค์หลัก ได้แก่ ภาวะโลหิตจาง (ประมาณ 90%) และอ่อนเพลีย (ประมาณ 66%) มีการวางแผนการทดลองทางคลินิกในญี่ปุ่นเช่นกัน และยานี้ได้รับความสนใจในฐานะตัวเลือกการรักษามาตรฐานในอนาคต 1)
ในการศึกษาเฟส 2 ที่รายงานโดย Jonasch และคณะ (2021) ในผู้ป่วย VHL ที่ได้รับ belzutifan 120 มก. รับประทานวันละครั้ง พบว่ามีผลทำให้ hemangioblastoma จอประสาทตา หดตัว 100% 7)
มีการรายงานว่าการรักษาด้วยแสงไดนามิก (PDT ) เหมาะสมทั้งชนิดรอบนอกและชนิดจานประสาทตา
di Nicola และคณะ (2022) รายงานประสิทธิภาพของ PDT สำหรับ hemangioblastoma จอประสาทตา และแสดงให้เห็นถึงความเป็นไปได้ในการประยุกต์ใช้โดยเฉพาะชนิด juxtapapillary 4)
Schmidt-Erfurth และคณะประเมินความเป็นไปได้ในการใช้ PDT กับชนิดจานประสาทตา และความเสี่ยงของภาวะแทรกซ้อน 6)
Hussain และคณะรายงานผลของการรักษาด้วยโปรตอนต่อ hemangioblastoma จอประสาทตา ชนิด juxtapapillary 5) มีการรวบรวมกรณีศึกษาเป็นทางเลือกสำหรับชนิดจานประสาทตา ที่ยากต่อการรักษา
แม้ว่าผลการทำให้เนื้องอกหดตัวโดยตรงจะมีจำกัด แต่รายงานกรณีที่ใช้เป็นการควบคุมเสริมสำหรับการเปลี่ยนแปลงแบบ exudative กำลังเพิ่มขึ้น 1) ยังไม่มีโปรโตคอลที่กำหนดไว้ จำเป็นต้องตัดสินใจเป็นรายกรณี
Q
belzutifan มีใช้ในญี่ปุ่นหรือไม่?
A
ณ เดือนเมษายน 2026 belzutifan ยังไม่ได้รับการอนุมัติให้ใช้ทั่วไปในญี่ปุ่น FDA อนุมัติในปี 2021 แต่ในญี่ปุ่นอยู่ในขั้นตอนเตรียมการทดลองทางคลินิก 1) หากการรักษามาตรฐานทำได้ยากสำหรับผู้ป่วย VHL ควรพิจารณาความเป็นไปได้ในการเข้าร่วมการทดลองทางคลินิกโดยปรึกษาแพทย์ผู้รักษาหรือสถานพยาบาลเฉพาะทาง
Q
จะเกิดอะไรขึ้นหากไม่รักษา hemangioblastoma จอประสาทตา?
A
หาก hemangioblastoma มีขนาดใหญ่ขึ้น จะกลายเป็นดื้อต่อการรักษาและการพยากรณ์การมองเห็น แย่ลงอย่างมีนัยสำคัญ หากจอประสาทตาลอก แบบ exudative ลามไปถึงจุดรับภาพ การสูญเสียการมองเห็น มีแนวโน้มที่จะไม่สามารถฟื้นคืนได้ และหากดำเนินไปจนถึงจอประสาทตาลอก แบบ tractional หรือต้อหิน ชนิด neovascular ในที่สุดอาจทำให้ตาบอดได้ ในโรค VHL รอยโรคใหม่จะปรากฏขึ้นตลอดชีวิต ดังนั้นการตรวจอวัยวะภายในตาอย่างต่อเนื่องควบคู่ไปกับการรักษาจึงเป็นสิ่งจำเป็น
VHL病診療の手引き(2024年版). 厚生労働科学研究費補助金難治性疾患等政策研究事業 VHL病研究班. 2024.
Lin H, Lin X. Pronounced conjunctival vascular engorgement in von Hippel-Lindau syndrome: a case report. BMC Ophthalmol. 2020 (症例報告).
Krivosic V, Massin P, Delyfer MN, et al. Laser photocoagulation for peripheral retinal capillary hemangioblastoma in von Hippel-Lindau disease. Ophthalmol Retina. 2017;1(1):59-67.
di Nicola M, Scupola A, Savastano MC, et al. Photodynamic therapy for retinal hemangioblastoma. Ophthalmol Retina. 2022;6(1):80-88.
Hussain RN, Jmor F, Damato B, et al. Proton beam radiotherapy for retinal capillary haemangioblastoma. Br J Ophthalmol. 2016;100(3):317-321.
Schmidt-Erfurth UM, Kusserow C, Barbazetto IA, et al. Benefits and complications of photodynamic therapy of papillary capillary hemangioma s. Ophthalmology. 2002;109(7):1256-1266.
Jonasch E, Donskov F, Iliopoulos O, et al. Belzutifan for renal cell carcinoma in von Hippel-Lindau disease. N Engl J Med. 2021;385(22):2036-2046.