เมื่อมะเร็งต่อมน้ำเหลืองชนิดร้ายเกิดขึ้นในตาโดยไม่มีมะเร็งต่อมน้ำเหลืองทั่วร่างกาย เรียกว่ามะเร็งต่อมน้ำเหลืองภายในลูกตาปฐมภูมิ (primary intraocular lymphoma; PIOL ) เนื่องจากมักก่อตัวเป็นรอยโรคที่จอตาและวุ้นตา ปัจจุบันจึงเรียกอีกอย่างว่ามะเร็งต่อมน้ำเหลืองวุ้นตา -จอตา (vitreo-retinal lymphoma; VRL) เซลล์ลิมโฟไซต์ที่กลายเป็นมะเร็งแทรกซึมเข้าไปในตา ทำให้เกิดลักษณะคล้ายม่านตาอักเสบ จึงเป็นที่รู้จักในฐานะหนึ่งในกลุ่มอาการพรางตา (masquerade syndrome) ผู้ป่วยจำนวนมากต่อมามีมะเร็งต่อมน้ำเหลืองในระบบประสาทส่วนกลาง (PCNSL) และมักมีแนวโน้มรุนแรงถึงเสียชีวิต
มะเร็งต่อมน้ำเหลืองปฐมภูมิในตาส่วนใหญ่ทางเนื้อเยื่อวิทยาคือมะเร็งต่อมน้ำเหลืองชนิดบีเซลล์ใหญ่กระจาย (diffuse large B-cell lymphoma; DLBCL) มีความร้ายแรงสูงมาก และแตกต่างอย่างมากจากมะเร็งต่อมน้ำเหลือง MALT ระดับต่ำที่พบบ่อยในอวัยวะรอบตา ทั้งในด้านพยาธิวิทยาและการพยากรณ์โรค ควรสังเกตว่ามะเร็งต่อมน้ำเหลืองชนิดร้ายส่วนใหญ่ในจักษุวิทยาคือมะเร็งต่อมน้ำเหลืองชนิดนอนฮอดจ์กิน และ PIOL อยู่ในกลุ่มนี้
Q
ในกรณีม่านตาอักเสบที่ไม่ตอบสนองต่อสเตียรอยด์ ควรสงสัยอะไร?
A
เมื่อการตอบสนองต่อการรักษาด้วยสเตียรอยด์ (ยาหยอดหรือรับประทาน) ไม่ดี ต้องพิจารณามะเร็งต่อมน้ำเหลืองภายในลูกตาชนิดร้าย (PIOL ) เป็นการวินิจฉัยแยกโรคหลักเสมอ PIOL ถูกเรียกว่า “กลุ่มอาการพรางตา” เนื่องจากแสดงลักษณะคล้ายม่านตาอักเสบ จากการอักเสบมาก นอกจากนี้ สเตียรอยด์ อาจทำให้เซลล์มะเร็งต่อมน้ำเหลืองสลายตัวชั่วคราวและอาการดีขึ้น ซึ่งนำไปสู่ผลลบปลอมในการตัดชิ้นเนื้อภายหลัง สงสัยเป็นพิเศษเมื่อมีวุ้นตา ขุ่นอย่างรุนแรงแต่การมองเห็น ยังดี การวัดอัตราส่วน IL-10/IL-6 และการตัดชิ้นเนื้อวุ้นตา เพื่อการวินิจฉัยที่แน่นอนเป็นสิ่งจำเป็น
มะเร็งต่อมน้ำเหลืองในลูกตาแบ่งออกเป็น 4 ชนิดตามตำแหน่งที่เกิด
ชนิด ลักษณะ ตา + ระบบประสาทส่วนกลาง พบบ่อยที่สุด (ประมาณ 60% ของทั้งหมด) สัมพันธ์ใกล้ชิดกับ PCNSL เฉพาะตา (มะเร็งต่อมน้ำเหลืองในลูกตาแบบแคบ) ชนิดจำกัดเฉพาะที่ PVR L เดี่ยว ตา + อวัยวะอื่น แพร่กระจายไปยังอวัยวะนอกระบบประสาทส่วนกลาง ตา + อวัยวะอื่น + ระบบประสาทส่วนกลาง รอยโรคที่กว้างขวางที่สุด
ชนิดที่เกิดในตาและระบบประสาทส่วนกลางพบได้บ่อยที่สุด คิดเป็นประมาณ 60% ของทั้งหมด
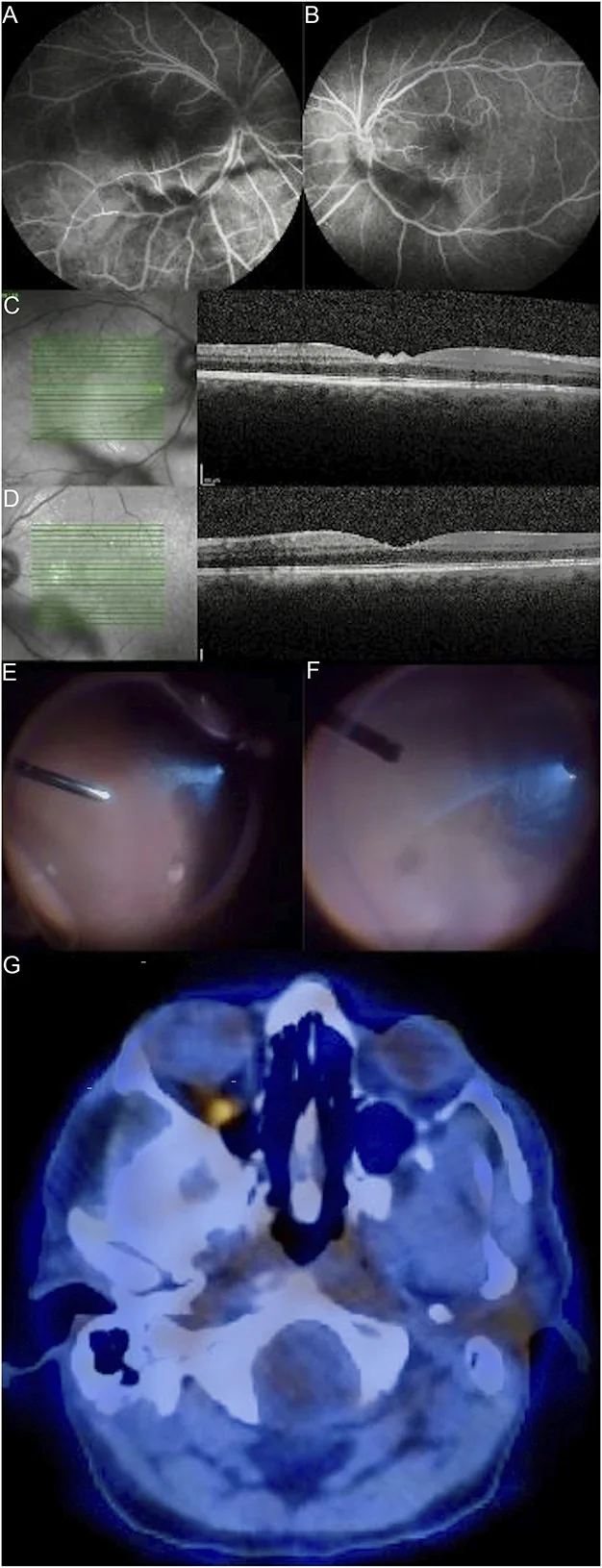
ภาพ fluorescein angiography, OCT และผลการตรวจวุ้นตาของมะเร็งต่อมน้ำเหลืองในลูกตา (รูปแบบ aurora borealis) Naia L, et al. Primary vitreoretinal lymphoma masquerading as refractory uveitis. Porto Biomed J. 2024;9(5):268. Figure 1. PM
CI D: PMC11469907. License: CC BY 4.0.
การตรวจหลอดเลือดด้วยฟลูออเรสซีน ของตาขวาและซ้าย (A และ B) และการตรวจด้วยเครื่องเอกซเรย์การเชื่อมประสานแสง (C และ D) แสดงให้เห็นภาวะวุ้นตา อักเสบระดับปานกลาง และในชิ้นเนื้อระหว่างการตัดวุ้นตา (คอลัมน์ที่ 4) พบการรวมกลุ่มเป็นแผ่นของเซลล์ขนาดใหญ่ที่เหมือนกันในรูปแบบ “ออโรรา บอเรลิส” ซึ่งสอดคล้องกับความขุ่นของวุ้นตา แบบแถบและเส้นที่กล่าวถึงในหัวข้อ “2. อาการหลักและอาการแสดงทางคลินิก”
อาการที่ผู้ป่วยรับรู้ได้โดยทั่วไปแสดงไว้ด้านล่าง
ตามัว (มองเห็นภาพมัวทั้งลานตาเนื่องจากความขุ่นของวุ้นตา )
จุดลอยในตา (เนื่องจากการแทรกซึมของเซลล์มะเร็งต่อมน้ำเหลืองในวุ้นตา )
การมองเห็น ลดลงแบบค่อยเป็นค่อยไปโดยไม่เจ็บปวดการมองเห็น ยังค่อนข้างดีแม้มีความขุ่นของวุ้นตา รุนแรง
ตามัวเป็นอาการที่ผู้ป่วยรับรู้ได้บ่อยที่สุด การมองเห็น ที่ดีไม่สมส่วนกับความรุนแรงของความขุ่นของวุ้นตา เป็นเบาะแสสำคัญที่ทำให้สงสัยโรคนี้
ลักษณะของความขุ่นของวุ้นตา
รูปแบบแถบและเส้น : รูปแบบเฉพาะที่แผ่กระจายเป็นรัศมีจากขั้วหลังไปยังส่วนรอบนอก
ความขุ่นแบบออโรรา : ความหนาแน่นของเซลล์สูง และเมื่อสังเกตแบบพลวัตจะสามารถยืนยันความขุ่นของวุ้นตา ที่อธิบายว่า “แบบออโรรา” ได้
เซลล์ขนาดไม่สม่ำเสมอ : เซลล์มะเร็งต่อมน้ำเหลืองความหนาแน่นสูงมีขนาดไม่สม่ำเสมอ
ความแตกต่างกับการคงไว้ซึ่งการมองเห็น : การมองเห็น ที่ดีเมื่อเทียบกับความรุนแรงของความขุ่นเป็นกุญแจสำคัญในการสงสัยโรคนี้
ผลการตรวจจอตาและอาร์พีอี
รอยโรคจุดเหลือง-ขาว : เซลล์มะเร็งต่อมน้ำเหลืองแทรกซึมใต้ชั้นเยื่อบุผิวเม็ดสีจอตาและใต้เยื่อบรูค ก่อตัวเป็นรอยโรคแบบจุดถึงจุดด่างเหลือง-ขาว
การรวมตัวและขยายของรอยโรค : รอยโรคจุดเล็กๆ รวมตัวกันและขยายเป็นรอยโรคขนาดใหญ่
ลักษณะคล้าย papillitis : การแทรกซึมของเซลล์เนื้องอกใต้จอประสาทตา รอบหัวประสาทตาอาจทำให้เกิดลักษณะคล้าย papillitis (พบได้น้อย)
การเกิดปลอกสีขาว : บางครั้งพบการเกิดปลอกสีขาวรอบหลอดเลือดคล้าย retinal vasculitis
สเตียรอยด์
หากการตอบสนองต่อยาหยอดหรือยาเม็ดสเตียรอยด์ ไม่ดี ต้องพิจารณา lymphoma ในลูกตาชนิดร้ายเป็นโรคที่ต้องแยก สเตียรอยด์ อาจทำให้เซลล์ lymphoma สลายตัวชั่วคราวและอาการดีขึ้น แต่ไม่ใช่การดีขึ้นอย่างแท้จริง และอาจทำให้ผลชิ้นเนื้อเป็นลบปลอม จึงต้องระมัดระวัง
มีรายงานว่าความถี่ของ corneal endothelial deposits (KP) มีแนวโน้มเพิ่มขึ้นเมื่อกลับเป็นซ้ำในลูกตาเมื่อเทียบกับการเป็นครั้งแรก 2)
Q
PIOL วินิจฉัยได้อย่างไร?
A
การวินิจฉัยที่แน่นอนของ PIOL จำเป็นต้องตัดชิ้นเนื้อวุ้นตา คล้ายกับการผ่าตัดวุ้นตา น้ำวุ้นตา ที่เก็บได้จะนำไปตรวจเซลล์วิทยา วัดอัตราส่วน IL-10/IL-6 ค้นหาการจัดเรียงตัวใหม่ของยีน IgH ด้วย PCR และโฟลว์ไซโตเมทรีร่วมกัน การตรวจเซลล์วิทยาเพียงอย่างเดียวมีความไวต่ำ (~50%) ในขณะที่อัตราส่วน IL-10/IL-6 >1 (ความไว 89.4%) โฟลว์ไซโตเมทรี (ความไว 88.0%) และ PCR (ความไว 85.1%) มีประโยชน์เมื่อใช้ร่วมกัน 1) หากใช้สเตียรอยด์ ก่อนการวินิจฉัย มีความเสี่ยงต่อผลลบปลอม ดังนั้นจึงทำการตัดชิ้นเนื้อหลังจากหยุดสเตียรอยด์ หากเป็นไปได้
อายุเฉลี่ยเมื่อวินิจฉัยคือ 63 ปี พบในผู้หญิงมากกว่าเล็กน้อย ความถี่ประมาณ 1-2% ของผู้ป่วยม่านตาอักเสบ ในโรงพยาบาลมหาวิทยาลัย อาการทางตาพบใน 15-20% ของ lymphoma ระบบประสาทส่วนกลาง
ในชุดผู้ป่วย 10 ราย (17 ตา) ที่ฮ่องกง อายุมัธยฐาน 59 ปี ผู้หญิง 70% เป็นสองข้าง 70% 1) ในการศึกษาย้อนหลัง 51 รายที่เซี่ยงไฮ้ รายงานสองข้าง 78.4% 2) โรคนี้มักเป็นสองข้าง ดังนั้นการตรวจและติดตามตาอีกข้างจึงสำคัญแม้เริ่มเป็นข้างเดียว
การวินิจฉัยมักล่าช้าจากเริ่มมีอาการ (เฉลี่ย 12-18 เดือนเนื่องจาก mask syndrome 3) ) ภาวะภูมิคุ้มกันบกพร่อง (เช่น การติดเชื้อ HIV) และภาวะกดภูมิคุ้มกัน (หลังปลูกถ่ายอวัยวะ การใช้ยากดภูมิคุ้มกัน) ถือเป็นปัจจัยเสี่ยง
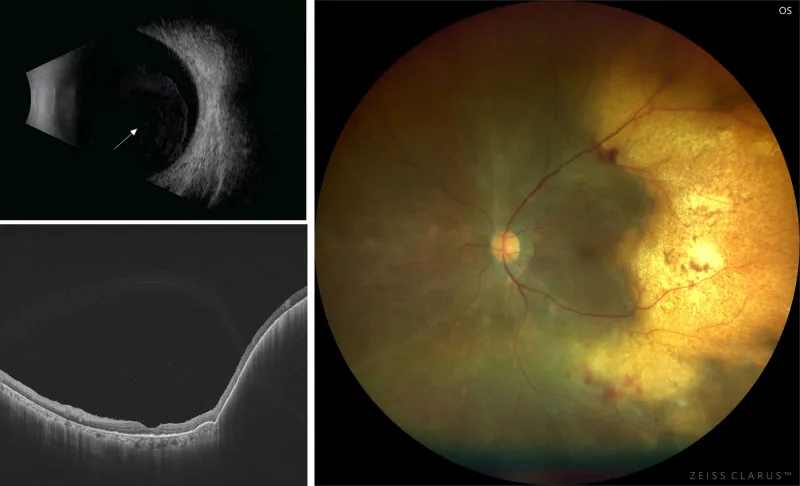
ภาพ OCT ของ intraocular lymphoma (ก้อนสะท้อนสูงใต้ RPE) และภาพถ่ายจอประสาทตา (รอยโรครูปวงแหวนสีเหลืองขาว) Wang SY, et al. Primary vitreoretinal lymphoma: diagnosis, treatment, and prognosis. Blood Sci. 2025;7(2):e00233. Figure 1. PM
CI D: PMC12047895. License: CC BY 4.0.
ภาพหลายรูปแบบของหญิงอายุ 75 ปี: อัลตราซาวนด์ B-scan (ซ้ายบน) แสดงความขุ่นของวุ้นตา ส่วนหลังอย่างกว้างขวาง OCT (ซ้ายล่าง) แสดงการลอกตัวของ RPE ที่รวมกันกับก้อนสะท้อนสูงสม่ำเสมอใต้ RPE ด้านขมับของจุดรับภาพ และภาพถ่ายจอประสาทตา (ขวา) แสดงรอยโรคยกตัวรูปวงแหวนสีเหลืองขาวมีจุดสีเล็กๆ ด้านขมับของจุดรับภาพ ซึ่งสอดคล้องกับการแทรกซึมใต้ RPE ที่สะท้อนสูงใน OCT และรอยโรคใต้จอประสาทตา สีเหลืองขาวที่กล่าวถึงในหัวข้อ 4
เพื่อการวินิจฉัยที่แน่นอน จะทำการตัดชิ้นเนื้อวุ้นตา (vitreous biopsy) คล้ายกับการผ่าตัดวุ้นตา การตรวจเซลล์วิทยาเพียงอย่างเดียวอาจไม่เพียงพอต่อการยืนยันการวินิจฉัย จำเป็นต้องรวมกับการตรวจหาการจัดเรียงตัวใหม่ของยีนอิมมูโนโกลบูลินด้วย PCR และการวัดไซโตไคน์
ไม่ตอบสนองต่อการรักษาด้วยสเตียรอยด์ (ยาหยอดหรือรับประทาน) (สำคัญที่สุด)
การมองเห็น ดีแม้มีความขุ่นของวุ้นตา อย่างรุนแรงอาการคล้ายยูเวียอักเสบที่เกิดขึ้นหลังวัยกลางคน
ความขุ่นของวุ้นตา เป็นเส้นหรือสายลักษณะเฉพาะในตาข้างเดียวหรือทั้งสองข้าง
วิธีการตรวจ ลักษณะและความไว ความสำคัญทางคลินิก เซลล์วิทยา อัตราการให้ผลบวก 50% (ชุดข้อมูลฮ่องกง)1) การตรวจพื้นฐาน ระวังผลลบลวง อัตราส่วน IL-10/IL-6 ความไว 89.4% ถ้า >11) ตัวบ่งชี้ทางชีวภาพ ที่สำคัญที่สุดค่า IL-10 สัมบูรณ์ ≥50 pg/mL มีประโยชน์ เมื่อกลับเป็นซ้ำ อัตราส่วน >1 เชื่อถือได้มากกว่า2) โฟลว์ไซโตเมทรี เซลล์ B ที่มี CD20+ ความไว 88.0%5) การประเมินการเพิ่มจำนวนแบบโมโนโคลนัล PCR (การจัดเรียงยีน IgH ใหม่) ความไว 85.1%5) หลักฐานการเพิ่มจำนวนแบบโคลนของเซลล์ B การวิเคราะห์การกลายพันธุ์ MYD88 ความไว 70%6) ยังมีประโยชน์สำหรับการวินิจฉัยพยาธิสรีรวิทยาระดับโมเลกุล การตรวจหา MYD88 โดยใช้ DNA ที่ปราศจากเซลล์ อัตราการตรวจพบสูงกว่า DNA จากเซลล์ประมาณ 30%1) การวินิจฉัยที่มีการรุกรานน้อยที่สุด สามารถทำได้ในอารมณ์ขันน้ำ9, 10) กรอบการวินิจฉัย 6 รายการ ความไว 97.5% และความจำเพาะ 100%8) การวินิจฉัยความแม่นยำสูงด้วยตัวชี้วัดแบบผสม
ในขณะที่ IL-10 ในของเหลวภายในลูกตาสูงขึ้น IL-6 ซึ่งสูงขึ้นในโรคอักเสบจะต่ำกว่า IL-10 และอัตราส่วน IL-10/IL-6 > 1 มีค่าทางการวินิจฉัย อย่างไรก็ตาม เมื่อเกิดการกลับเป็นซ้ำ อัตราส่วนนี้อาจลดลง (มีเพียง 43.8% ที่ > 1) และค่า IL-10 สัมบูรณ์ ≥ 50 pg/mL เป็นตัวบ่งชี้ที่เชื่อถือได้มากกว่า2)
อัตราส่วน IL-10/IL-6 > 1 ในน้ำวุ้นตา เป็นตัวบ่งชี้ที่ชัดเจนของมะเร็งต่อมน้ำเหลืองภายในลูกตา มีความไว 89.4% และความจำเพาะสูง1) มีประโยชน์ในการแยกจากม่านตาอักเสบ ชนิดอักเสบ อย่างไรก็ตาม ความไวแตกต่างกันระหว่างครั้งแรกและการกลับเป็นซ้ำ ดังนั้นเมื่อกลับเป็นซ้ำ ควรอ้างอิงค่า IL-10 สัมบูรณ์ (≥ 50 pg/mL) ด้วย2)
หลังจากยืนยันการวินิจฉัยมะเร็งต่อมน้ำเหลืองภายในลูกตาแล้ว ให้ทำสิ่งต่อไปนี้เป็นประจำเพื่อตรวจหามะเร็งต่อมน้ำเหลืองในระบบประสาทส่วนกลางตั้งแต่ระยะแรก
MRI ศีรษะด้วยการฉีดแกโดลิเนียม : จำเป็นสำหรับการตรวจหารอยโรค CNS ที่ไม่มีอาการการตรวจ PET ทั่วร่างกาย : มีประโยชน์ในการประเมินการกระจายของรอยโรคเนื้องอกทั่วร่างกาย
การรักษา PIOL ขึ้นอยู่กับการผสมผสานระหว่างการรักษาเฉพาะที่ตาและการให้เคมีบำบัดทั่วร่างกาย เนื่องจากสิ่งกีดขวางเลือด-จอตา (BRB) จำกัดการผ่านของเคมีบำบัดทั่วร่างกายเข้าสู่ตา การรักษาเฉพาะที่จึงจำเป็นในการควบคุมรอยโรคภายในลูกตา
ฉีด methotrexate (สารละลาย Methotrexate สำหรับฉีด 200 มก.) เข้าแก้วตาในขนาด 400 ไมโครกรัม/0.1 มล. โปรโตคอลมาตรฐานมีดังนี้:
ระยะชักนำ : สัปดาห์ละ 2 ครั้ง นาน 4 สัปดาห์ระยะเสริม : สัปดาห์ละ 1 ครั้ง นาน 8 สัปดาห์ระยะบำรุงรักษา : เดือนละ 1 ครั้ง นาน 9 เดือน
ในชุดข้อมูลฮ่องกง รายงานอัตราการหายโรคสมบูรณ์ 77.8% โดยมีค่ามัธยฐานของการฉีด 5 ครั้ง1) นอกจากนี้ยังใช้ในขนาดต่ำ 400 ไมโครกรัม/0.05 มล. ในรายงานขนาดใหญ่ที่รวบรวมประสบการณ์ 20 ปี แสดงอัตราการหายโรคสมบูรณ์ 97%6)
ผลข้างเคียงหลัก : โรคกระจกตา (33-100%) จัดการด้วยยาหยอดตาปราศจากสารกันเสีย, คอนแทคเลนส์ปิดแผล และกรดโฟลิกรับประทาน1)
การฉายรังสีเฉพาะที่ลูกตาด้วยขนาดรวมประมาณ 30 Gy ได้ผลดี ใช้ในกรณีเป็นสองข้าง, ผู้สูงอายุ, ไม่ทนต่อ MTX และเดินทางลำบาก อย่างไรก็ตาม มีความเสี่ยงของผลข้างเคียง เช่น จอประสาทตา ฉายรังสี, เส้นประสาทตา ฉายรังสี และต้อกระจก และมักให้ความสำคัญกับการฉีด MTX หากเป็นไปได้4)
บางกรณีหายโรคสมบูรณ์หลังการตัดวุ้นตา เพื่อวินิจฉัย (ชุดข้อมูลฮ่องกง: 75%1) , รายงานอื่น: 19.7%7) ) กลไกคิดว่าเกิดจากการกำจัดโครงสร้างที่เซลล์มะเร็งต่อมน้ำเหลืองใช้ยึดเกาะและลดปริมาณก้อนเนื้องอก จึงเป็นทางเลือกในกรณีที่ไม่ทนหรือปฏิเสธ MTX
การให้ MTX ขนาดสูงทั่วร่างกายเป็นพื้นฐาน
การรักษาด้วย MTX ขนาดสูง : Methotrexate 100-200 มก./กก. (5-10 กรัมต่อครั้งในผู้ใหญ่) ฉีดเข้าหลอดเลือดดำการช่วยชีวิตด้วย leucovorin : เริ่มวันถัดไปนาน 3 วัน, leucovorin 5 หลอดในน้ำเกลือ 100 มล. ทุก 4 ชั่วโมง จำนวน 4 ครั้ง ฉีดเข้าหลอดเลือดดำต้องดำเนินการตามแนวทางโดยมีการจัดการสารน้ำ, ปริมาณปัสสาวะ และค่า pH ปัสสาวะอย่างเคร่งครัด
หากจำเป็น อาจเพิ่มการฉายรังสีทั่วสมอง (WBRT) แต่เนื่องจากความเสี่ยงของผลข้างเคียง เช่น โรคเนื้อขาวในสมอง ควรพิจารณาข้อบ่งชี้อย่างรอบคอบ โดยเฉพาะในผู้สูงอายุ
การฉายรังสีทั่วสมองเป็นทางเลือกในการรักษาเมื่อมี PCNSL แต่มีความเสี่ยงต่อผลข้างเคียง เช่น โรคเม็ดเลือดขาวในสมอง ในผู้สูงอายุ อาจเกิดผลกระทบทางระบบประสาทที่รุนแรง เช่น การเสื่อมของความรู้ความเข้าใจ ดังนั้นควรพิจารณาข้อบ่งชี้อย่างระมัดระวัง
ภาวะ การรักษาที่แนะนำ เฉพาะรอยโรคในลูกตา ฉีด MTX เข้าแก้วตา ± ฉายรังสีเฉพาะที่ตา (30 Gy) มีการเกี่ยวข้องกับระบบประสาทส่วนกลาง MTX ขนาดสูงทั่วร่างกาย ± ฉายรังสีทั่วสมอง + การรักษาเฉพาะที่ตา เมื่อกลับเป็นซ้ำในลูกตา ฉีด MTX เข้าแก้วตา (หายขาด 55.6%, หายบางส่วน 33.3%) 2)
การรวมเคมีบำบัดทั่วร่างกายและเคมีบำบัดเข้าแก้วตาอาจลดความเสี่ยงของการกลับเป็นซ้ำในลูกตา การไม่มีประวัติเคมีบำบัดเข้าแก้วตาถูกรายงานว่าเป็นปัจจัยเสี่ยงอิสระสำหรับการกลับเป็นซ้ำในลูกตา 2) ซึ่งบ่งชี้ถึงความสำคัญของการรักษาเฉพาะที่ตาอย่างจริงจัง
มะเร็งต่อมน้ำเหลืองปฐมภูมิในลูกตาส่วนใหญ่ (มากกว่า 95%) เป็นชนิด diffuse large B-cell lymphoma (DLBCL) เป็นเนื้องอกร้ายจากการเพิ่มจำนวนแบบโมโนโคลนอลของเซลล์ลิมฟอยด์ และตรงกันข้ามกับมะเร็งต่อมน้ำเหลือง MALT ระดับต่ำที่พบบ่อยในอวัยวะรอบตา มีความร้ายแรงสูงมาก
การกลายพันธุ์ MYD88 L265P ถูกตรวจพบได้บ่อยใน PVR L/PCNSL การกลายพันธุ์นี้ทำให้เกิดการกระตุ้นสัญญาณของ Toll-like receptor อย่างต่อเนื่อง กระตุ้นวิถี NF -κB อย่างถาวร และคงไว้ซึ่งการเจริญเติบโตและการอยู่รอดของเซลล์เนื้องอก 6) BTK (ไทโรซีนไคเนสชนิด Bruton) อยู่ downstream ของวิถีนี้และเป็นเป้าหมายการรักษาที่น่าสนใจ
การแสดงออกสูงของ VEGF และ IL-10 มีส่วนช่วยในการหลบหลีกภูมิคุ้มกันของเซลล์เนื้องอก IL-10 เป็นไซโตไคน์ที่ผลิตโดยเซลล์เนื้องอกเอง และเกี่ยวข้องกับการสร้างสภาพแวดล้อมที่กดภูมิคุ้มกัน
เชื่อกันว่าการเปลี่ยนแปลงของเซลล์เนื้องอกเกิดขึ้นภายนอกระบบประสาทส่วนกลาง จากนั้นจึงย้ายเข้าสู่ลูกตาซึ่งมีเอกสิทธิ์ทางภูมิคุ้มกัน 3) เนื่องจากกำแพงเลือด-ตา (BRB) จำกัดการผ่านของเคมีบำบัดทั่วร่างกายเข้าสู่ลูกตา การรักษาเฉพาะที่ เช่น การฉีดเข้าแก้วตา หรือการฉายรังสีเฉพาะที่จึงจำเป็นในการควบคุมรอยโรคภายในลูกตา
ตำแหน่งการแทรกซึมหลัก:
ช่องว่างแก้วตา (ตำแหน่งหลักของการเพิ่มจำนวนของเซลล์มะเร็งต่อมน้ำเหลือง)
เยื่อบุผิวรงควัตถุจอตา (RPE ) (จุดเริ่มต้นของการแทรกซึมใต้จอตา)
ใต้เยื่อบรูค (การเกิดรอยโรคระหว่าง RPE และเยื่อบรูค )
ความขุ่นของแก้วตามีลักษณะเป็นแถบหรือเส้น กระจายเป็นรัศมีจากขั้วหลังไปยังรอบนอกในรูปแบบที่จำเพาะ เซลล์มะเร็งต่อมน้ำเหลืองที่แทรกซึมจอตาจะค่อยๆ ก่อตัวเป็นรอยโรคจุดสีขาวเหลือง ซึ่งอาจรวมตัวและขยายใหญ่ขึ้น
PIOL และ PCNSL มีรูปแบบการแสดงออกของยีนที่คล้ายคลึงกันหลายประการ และเป็นที่เข้าใจว่าทั้งสองอยู่ในสเปกตรัมโรคเดียวกัน 3) นี่เป็นพื้นฐานของความถี่สูงของรอยโรคในระบบประสาทส่วนกลางในผู้ป่วย PIOL
เนื้อหาต่อไปนี้อยู่ในขั้นตอนการวิจัยหรือการทดลองทางคลินิก และไม่ใช่การรักษามาตรฐานที่สามารถรับได้ในโรงพยาบาลทั่วไป เป็นข้อมูลอ้างอิงสำหรับผู้เชี่ยวชาญเกี่ยวกับการพัฒนาทางการแพทย์ในอนาคต
การตรวจหาการกลายพันธุ์ของ MYD88 โดยใช้ cell-free DNA ในวุ้นตา และอารมณ์ขันในช่องหน้าม่านตา ได้รับความสนใจ อัตราการตรวจพบสูงกว่า DNA ของเซลล์ประมาณ 30% 1) และมีประสิทธิภาพแม้ในตัวอย่างที่เจือจางสูง มีรายงานการตรวจพบในอารมณ์ขันในช่องหน้าม่านตา (การตรวจหาการกลายพันธุ์ MYD88 L265P โดยใช้ ddPCR ที่มีความไวสูงพิเศษ) 9, 10) และคาดว่าจะนำไปใช้ในกรณีที่การตรวจชิ้นเนื้อวุ้นตา ทำได้ยาก
การฉีดริตูซิแมบ (แอนติบอดีต่อ CD20) เข้าในวุ้นตา : กำลังศึกษาการประยุกต์ใช้สำหรับ PIOL แต่ปัจจุบันอยู่ในขั้นตอนการวิจัยสารยับยั้ง BTK (ไอบรูทินิบ) : แสดงประสิทธิภาพใน PCNSL ที่กลับมาเป็นซ้ำ/ดื้อต่อการรักษา และกำลังศึกษาการขยายผลไปยัง PIOL ที่มีการกลายพันธุ์ MYD88 เป็นบวกการบำบัดด้วยเซลล์ CAR-T : การวิจัยเชิงสำรวจในมะเร็งทางโลหิตวิทยากำลังดำเนินอยู่
ในการศึกษาย้อนหลังใน 51 ราย การรวมเคมีบำบัดทั้งระบบและเคมีบำบัดในวุ้นตา แสดงให้เห็นถึงศักยภาพในการลดความเสี่ยงของการกลับเป็นซ้ำในตา 2) ตารางการให้ยาที่เหมาะสมจำเป็นต้องมีการศึกษาไปข้างหน้าเพิ่มเติม
Q
ความเสี่ยงในการลุกลามไปเป็นมะเร็งต่อมน้ำเหลืองในระบบประสาทส่วนกลางมีเท่าใด?
A
ใน PIOL ผู้ป่วยจำนวนมากในที่สุดจะเกิดรอยโรคในระบบประสาทส่วนกลาง (CNS) 55.6% ของ PVR L ที่แยกเฉพาะ (เฉพาะตา) เกิด CNSL ใหม่ (มะเร็งต่อมน้ำเหลืองในระบบประสาทส่วนกลาง) โดยมีค่ามัธยฐาน 35.1 เดือน 2) ในชุดข้อมูลจากฮ่องกง พบรอยโรค CNS ใน 7 จาก 10 ราย (70%) และใน 57.1% ของรายเหล่านั้น รอยโรคที่ตาเกิดขึ้นก่อนรอยโรค CNS 1) ดังนั้นแม้หลังจากยืนยันรอยโรคในตาแล้ว การตรวจ CNS เป็นระยะด้วย MRI ศีรษะแบบฉีดสารทึบรังสีแกโดลิเนียมเป็นสิ่งจำเป็น แม้ว่าการกลับเป็นซ้ำในตาจะไม่ส่งผลโดยตรงต่ออัตราการกลับเป็นซ้ำของ CNS หรือการรอดชีวิตโดยรวม 2) แต่การพยากรณ์โรคหลังจากเกิดรอยโรค CNS ยังคงแย่ในหลายกรณี
Chee ASH, Mak ACY, Kam KW, et al. Diagnostic challenges and treatment outcomes of primary vitreoretinal lymphoma in Hong Kong. Hong Kong Med J. 2024.
Liu S, Zhang H, Su H, et al. Prognosis, risk factors, and clinical features of intraocular recurrence in primary vitreoretinal lymphoma. Ophthalmol Retina. 2024.
Raval V, Binkley EM, Aronow ME, et al. Primary central nervous system lymphoma-ocular variant: an interdisciplinary review on management. Surv Ophthalmol. 2021;66(6):1009-1020.
Riemens A, Bromberg J, Touitou V, et al. Treatment strategies in primary vitreoretinal lymphoma: a 17-center European collaborative study. JAMA Ophthalmol. 2015;133(2):191-197.
Huang RS, Trang M, Cheung V, et al. Diagnostic methods for primary vitreoretinal lymphoma: a systematic review. Surv Ophthalmol. 2024;69(4):456-464.
Habot-Wilner Z, Frenkel S, Goldenberg D, et al. Efficacy and safety of intravitreal methotrexate for vitreoretinal lymphoma: 20 years of experience. Br J Haematol. 2021;194(1):92-100.
Zhou N, Mao J, Gong Y, et al. A proposed protocol of intravitreal injection of methotrexate for treatment of primary vitreoretinal lymphoma. Eye (Lond). 2022;36(7):1448-1455.
Zhang X, Tang LJ, Liu HF, et al. Development of diagnostic recommendations for vitreoretinal lymphoma. Ocul Immunol Inflamm. 2024;32(8):1142-1149.
Hiemcke-Jiwa LS, Leguit RJ, Radersma-van Loon JH, et al. Molecular analysis in liquid biopsies for diagnostics of primary vitreoretinal lymphoma: review of current evidence. Surv Ophthalmol. 2019;64(1):10-16.
Demirci H, Rao RC, Bhatt MD, et al. Aqueous humor-derived MYD88 L265P mutation analysis in vitreoretinal lymphoma. Ophthalmol Retina. 2023;7(2):189-195.