硝子体混濁の特徴
帯状・索状パターン:後極から周辺に放射状に広がる独特なパターンを示す。
オーロラ状混濁:細胞密度が高く、動的に観察すると「オーロラ状」と形容される硝子体混濁が確認できる。
大小不揃いの細胞:高密度のリンパ腫細胞が大小不揃いに存在する。
視力温存との乖離:混濁の強さに比べて視力が良好なことが本疾患を疑う鍵となる。

全身にリンパ腫がなく眼内に悪性リンパ腫が初発した場合を、原発眼内リンパ腫(primary intraocular lymphoma; PIOL)とよぶ。多くは網膜・硝子体に病巣を形成することから、最近は硝子体網膜リンパ腫(vitreo-retinal lymphoma; VRL)と称することもある。腫瘍化したリンパ球が眼内に浸潤してぶどう膜炎様の眼所見を呈するため、代表的な仮面症候群(masquerade syndrome)の一つとして知られる。多くの症例が中枢神経系リンパ腫(PCNSL)を合併し、致命的な経過をたどることが多い。
眼内に原発するリンパ腫のほとんどは、組織学的にびまん性大細胞型B細胞リンパ腫(diffuse large B-cell lymphoma; DLBCL)に相当する。きわめて悪性度が高く、眼付属器に多い低悪性度のMALTリンパ腫とは病態・予後ともに大きく異なる。なお、眼科領域の悪性リンパ腫の多くは非ホジキンリンパ腫であり、PIOLもこの範疇に含まれる。
ステロイド治療(点眼・内服)に対して反応が不良な場合、眼内悪性リンパ腫(PIOL)を代表的な鑑別疾患として必ず考慮する必要があります。PIOLは「仮面症候群」とも称され、炎症性ぶどう膜炎に酷似した所見を呈します。さらに、ステロイドによってリンパ腫細胞が一時的に溶解して症状が改善することがあり、その後の生検での偽陰性につながります。硝子体混濁が強いのに視力が良好である場合は特に疑います。IL-10/IL-6比の測定と硝子体生検による確定診断が必須です。
眼内リンパ腫は発生部位に応じて4型に分類される。
| 病型 | 特徴 |
|---|---|
| 眼+中枢神経系型 | 最多(全体の約60%)。PCNSLとの密接な関連 |
| 眼内のみ(狭義眼内リンパ腫) | 限局型。孤立性PVRL |
| 眼+他臓器型 | CNS以外の臓器に播種 |
| 眼+他臓器+CNS型 | 最も広汎な病変 |
眼と中枢神経系に生じる型が最も多く、全体の約60%を占める。
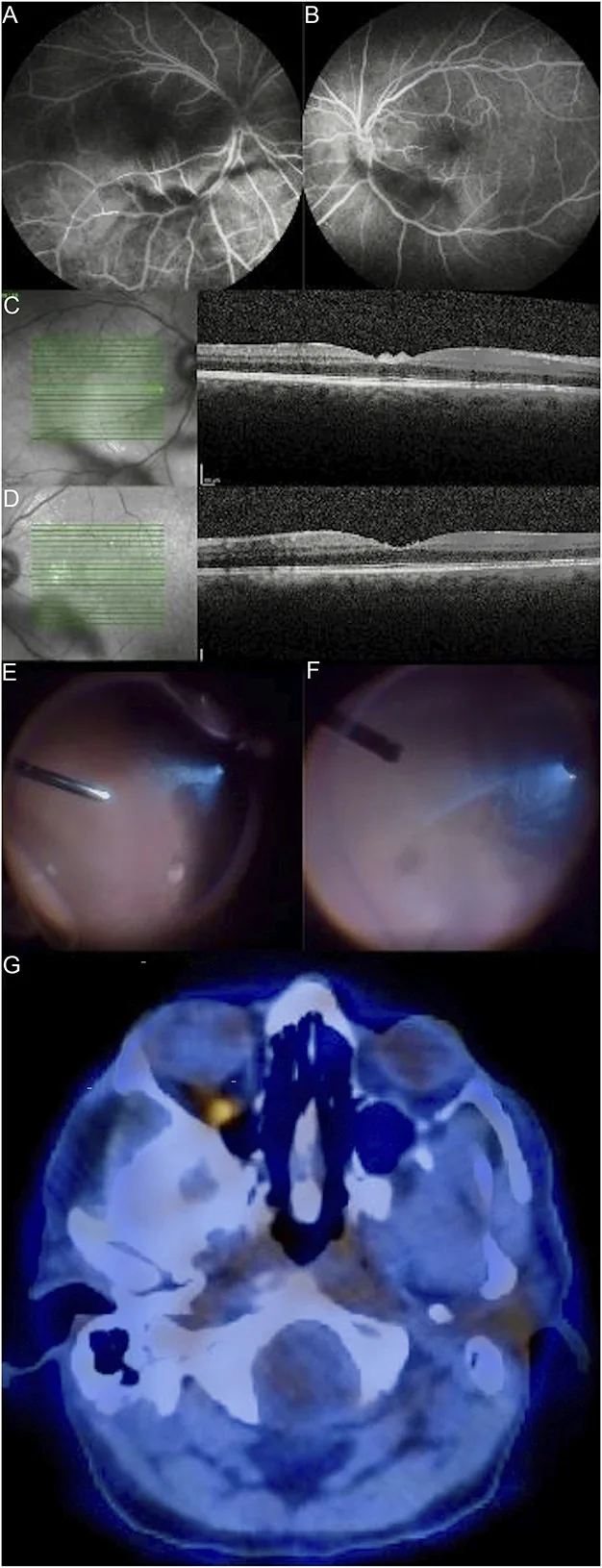
代表的な自覚症状を以下に示す。
霧視は最も頻度の高い自覚症状である。硝子体混濁の強さに不釣り合いな良好な視力は、本疾患を疑う重要な手がかりとなる。
硝子体混濁の特徴
帯状・索状パターン:後極から周辺に放射状に広がる独特なパターンを示す。
オーロラ状混濁:細胞密度が高く、動的に観察すると「オーロラ状」と形容される硝子体混濁が確認できる。
大小不揃いの細胞:高密度のリンパ腫細胞が大小不揃いに存在する。
視力温存との乖離:混濁の強さに比べて視力が良好なことが本疾患を疑う鍵となる。
網膜・RPE所見
黄白色斑状病巣:網膜色素上皮(RPE)下・Bruch膜下にリンパ腫細胞が浸潤し、黄白色の点状〜斑状病巣を形成する。
病巣の癒合拡大:小さな点状病巣が癒合して大型病巣へと拡大する。
乳頭炎様所見:乳頭周囲の網膜下への腫瘍細胞浸潤によって乳頭炎様所見を呈することがある(まれ)。
白鞘形成:網膜血管炎を思わせる血管白鞘形成がみられることもある。
眼内再発時には角膜後面沈着物(KP)の頻度が初発時より増加する傾向が報告されている2)。
PIOLの確定診断には硝子体手術に準じた硝子体生検が必要です。採取した硝子体液を用いて、細胞診・IL-10/IL-6比の測定・PCRによるIgH遺伝子再構成検索・フローサイトメトリーを組み合わせて診断します。細胞診単独では陽性率が50%程度と低く、IL-10/IL-6比>1(感度89.4%)やフローサイトメトリー(感度88.0%)、PCR(感度85.1%)の組み合わせが有用です1)。診断前にステロイドを使用している場合は偽陰性リスクがあるため、可能な限りステロイドを中止したうえで生検を施行します。
診断確定時の年齢は平均63歳で、やや女性に多い。発生頻度は大学病院におけるぶどう膜炎の1〜2%程度とされる。中枢神経系リンパ腫の15〜20%に眼症状がみられる。
香港における10例17眼の症例シリーズでは、中央値59歳、女性70%、両側性70%であった1)。上海における51例の後方視的研究では、両側性78.4%が報告されている2)。両側性が多い疾患であることが示されており、片眼性で発症した場合にも対側眼の精査と経過観察が重要である。
発症から診断確定までに遅延を生じやすい(仮面症候群のため平均12〜18か月ともされる3))。免疫不全(HIV感染症など)や免疫抑制状態(臓器移植後・免疫抑制薬使用中)がリスク因子とされる。
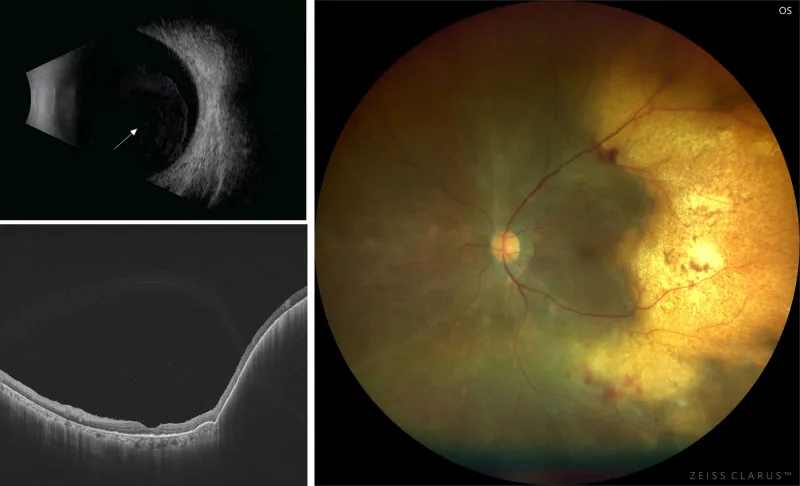
確定診断には硝子体手術に準じた硝子体生検を行う。細胞診のみでは診断を確定できるとは限らず、PCRによる免疫グロブリン遺伝子再構成の検索やサイトカイン測定を組み合わせることが必須である。
| 検査法 | 特徴・感度 | 臨床的意義 |
|---|---|---|
| 細胞診 | 陽性率50%(香港シリーズ)1) | 基本検査。偽陰性に注意 |
| IL-10/IL-6比 | >1で感度89.4%1) | 最重要バイオマーカー |
| IL-10絶対値 | ≥50 pg/mLが有用 | 再発時は比>1より信頼性高い2) |
| フローサイトメトリー | CD20+ B細胞。感度88.0%5) | 単クローン性増殖の評価 |
| PCR(IgH遺伝子再構成) | 感度85.1%5) | B細胞クローン増殖の証明 |
| MYD88変異解析 | 感度70%6) | 分子病態の診断にも有用 |
| cell-free DNAによるMYD88検出 | 細胞DNAより検出率約30%向上1) | 低侵襲診断。房水でも可能9, 10) |
| 6項目診断フレームワーク | 感度97.5%・特異度100%8) | 複合指標による高精度診断 |
眼内液中のIL-10が高値となる一方、炎症性疾患で高値となるIL-6はIL-10より低値となり、IL-10/IL-6比>1が診断的価値を持つ。ただし再発時にはこの比が低下する場合(43.8%のみ>1)があり、IL-10絶対値≥50 pg/mLがより信頼性の高い指標となる2)。
眼内リンパ腫の診断が確定した後は、以下を定期的に施行して中枢神経系リンパ腫の早期発見に努める。
PIOLの治療は眼局所治療と全身化学療法の組み合わせが基本となる。血液眼関門(blood-retinal barrier; BRB)が全身化学療法の眼内移行を制限するため、眼内病変の制御には局所治療が必須である。
メトトレキサート(メソトレキセート注射液200 mg)を400 μg/0.1 mLで硝子体内注入する。標準プロトコルは以下のとおりである。
香港シリーズでは中央値5回の注射で完全寛解率77.8%が報告された1)。また400 μg/0.05 mLの低容量でも使用される。20年間の経験を集積した大規模報告では、完全寛解率97%が示されている6)。
主な副作用:角膜症(33〜100%)。保存剤フリー点眼・バンドコンタクトレンズ(BCL)・葉酸内服で管理する1)。
総量30 Gy程度の眼局所照射が有効である。両側性・高齢・MTX不耐・通院困難例に適用される。ただし放射線網膜症・視神経症・白内障などの副作用リスクがあり、MTX注射が可能であれば優先される傾向がある4)。
診断的硝子体切除後に完全寛解が得られる症例がある(香港シリーズ: 75%1)、別報告: 19.7%7))。リンパ腫細胞増殖の足場除去と腫瘍量減少が機序と考えられており、MTX不耐・拒否例の選択肢となる。
大量MTX全身投与が基本となる。
必要に応じて全脳照射(WBRT)を加える場合もあるが、白質脳症をはじめとする副作用リスクがあるため、特に高齢者では適応を慎重に決定する。
| 病態 | 推奨治療 |
|---|---|
| 眼内病変のみ | MTX硝子体内注射 ± 眼局所放射線(30 Gy) |
| CNS合併 | 大量MTX全身投与 ± 全脳照射 + 眼局所治療 |
| 眼内再発時 | MTX硝子体注射(完全寛解55.6%・部分寛解33.3%)2) |
全身化学療法と硝子体内化学療法の併用が眼内再発リスクを低減させる可能性がある。硝子体内化学療法の既往がないことが眼内再発の独立したリスク因子として報告されており2)、積極的な眼局所治療の重要性が示されている。
眼内に原発するリンパ腫のほとんど(95%以上)はびまん性大細胞型B細胞リンパ腫(DLBCL)に相当する。リンパ球系細胞の単クローン性増殖による悪性腫瘍であり、眼付属器に多い低悪性度のMALTリンパ腫とは対照的にきわめて悪性度が高い。
MYD88 L265P変異がPVRL/PCNSLに高頻度に検出される。この変異はToll様受容体シグナルの恒常的活性化をもたらし、NF-κB経路を持続的に活性化させて腫瘍細胞の増殖・生存を維持する6)。BTK(ブルトン型チロシンキナーゼ)もこの経路の下流に位置し、治療標的として注目されている。
VEGFおよびIL-10の高発現が腫瘍細胞の免疫逃避に寄与する。IL-10は腫瘍細胞自身が産生するサイトカインであり、免疫抑制環境の形成に関与する。
腫瘍細胞の形質転換はCNS外で生じ、その後、免疫特権を有する眼内に移行すると考えられている3)。血液眼関門(BRB)が全身化学療法の眼内移行を制限するため、眼内病変の制御には硝子体内注射や眼局所放射線などの局所治療が必須となる。
主な浸潤部位:
硝子体混濁は帯状・索状を呈し、後極から周辺に放射状に広がる独特なパターンを示す。網膜へ浸潤したリンパ腫細胞は次第に黄白色の斑状病巣を形成し、癒合拡大することもある。
PIOLとPCNSLは遺伝子発現プロファイルに共通点が多く、両者は同一疾患スペクトラムに属すると理解されている3)。これがPIOL患者において高頻度にCNS病変が発症する背景となっている。
硝子体液・房水中のcell-free DNAを用いたMYD88変異検出が注目されている。細胞DNAより検出率が約30%高く1)、高度に希釈された検体でも有効である。房水での検出(超高感度ddPCRを用いたMYD88 L265P変異検出)が報告されており9, 10)、硝子体生検が困難な症例への応用が期待される。
51例を対象とした後方視的研究では、全身化学療法と硝子体内化学療法の併用が眼内再発リスクを低減させる可能性が示されている2)。最適な投与スケジュールについてはさらなる前向き研究が必要である。
PIOLでは最終的に相当数の症例がCNS病変を発症します。孤立性PVRL(眼のみ)の55.6%が新規CNSL(中枢神経系リンパ腫)を発症し、その中央値は35.1か月でした2)。香港シリーズでは10例中7例(70%)にCNS病変が認められ、57.1%では眼病変がCNS病変に先行していました1)。このため眼内病変が確認された後も、ガドリニウム造影頭部MRIによる定期的なCNS精査が不可欠です。眼内再発はCNS再発率や全生存には直接影響しないことが報告されていますが2)、CNS病変発症後の予後は依然として厳しい場合が多いです。