玻璃体混浊的特征
带状和索状模式:从后极向周边呈放射状扩散的独特模式。
极光样混浊:细胞密度高,动态观察可见被形容为“极光样”的玻璃体混浊。
大小不一的细胞:高密度淋巴瘤细胞大小不一地存在。
与视力保留的分离:混浊程度与良好视力不匹配是怀疑本病的关键。

全身无淋巴瘤而眼内首发恶性淋巴瘤的情况称为原发性眼内淋巴瘤(primary intraocular lymphoma; PIOL)。由于多数在视网膜和玻璃体形成病灶,最近也常称为玻璃体视网膜淋巴瘤(vitreo-retinal lymphoma; VRL)。肿瘤性淋巴细胞浸润眼内,呈现葡萄膜炎样眼部表现,因此被认为是典型的伪装综合征之一。许多病例合并中枢神经系统淋巴瘤(PCNSL),常导致致命性病程。
眼内原发淋巴瘤的组织学类型几乎均为弥漫性大B细胞淋巴瘤(diffuse large B-cell lymphoma; DLBCL)。其恶性程度极高,与眼附属器常见的低度恶性MALT淋巴瘤在病理和预后上均有显著差异。此外,眼科领域的恶性淋巴瘤多为非霍奇金淋巴瘤,PIOL也属于这一范畴。
当葡萄膜炎对类固醇治疗(滴眼或口服)反应不佳时,必须将眼内恶性淋巴瘤(PIOL)作为重要的鉴别诊断加以考虑。PIOL也被称为“伪装综合征”,其表现与炎性葡萄膜炎极为相似。此外,类固醇可能暂时溶解淋巴瘤细胞并改善症状,导致后续活检出现假阴性结果。当玻璃体混浊严重但视力良好时,尤其要怀疑。必须检测IL-10/IL-6比值并进行玻璃体活检以确诊。
眼内淋巴瘤根据发生部位分为4型。
| 类型 | 特征 |
|---|---|
| 眼+中枢神经系统型 | 最常见(约占全部病例的60%)。与PCNSL密切相关。 |
| 仅限眼内(狭义眼内淋巴瘤) | 局限型。孤立性PVRL。 |
| 眼+其他器官型 | 播散至CNS以外的器官。 |
| 眼+其他器官+CNS型 | 最广泛的病变。 |
眼和中枢神经系统同时受累的类型最常见,约占全部病例的60%。
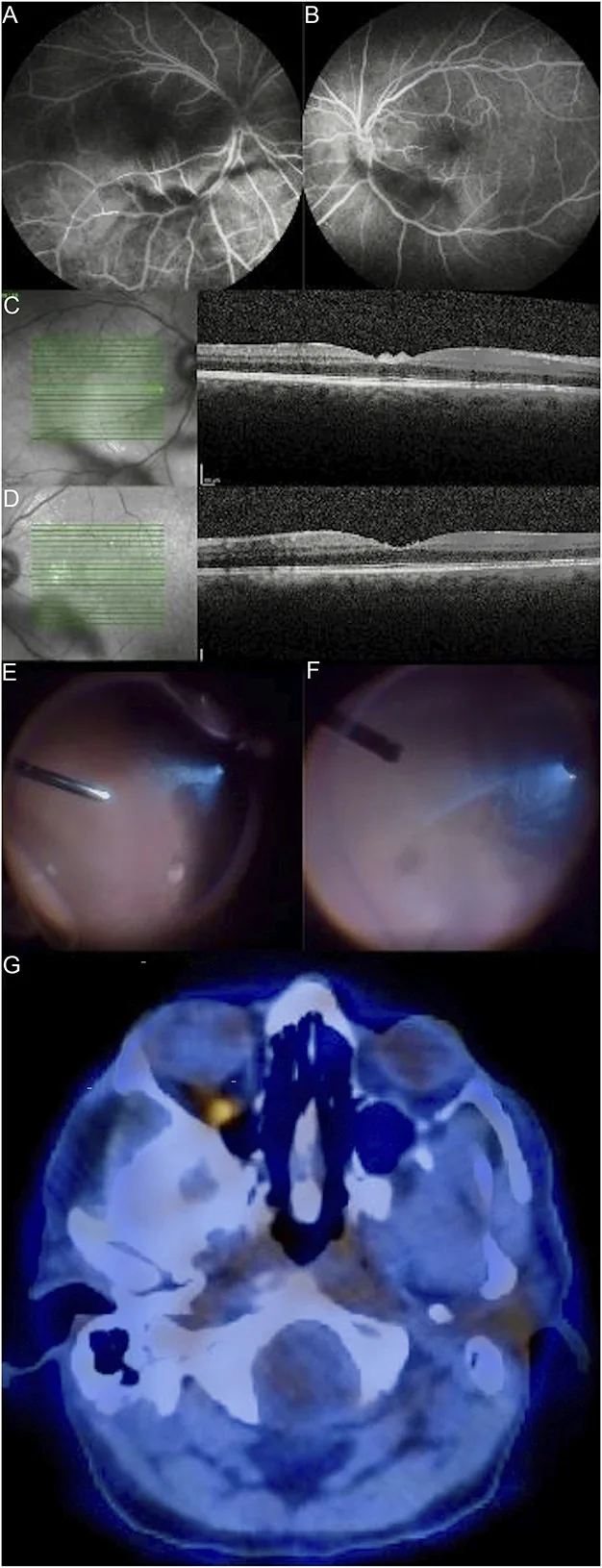
典型的自觉症状如下所示。
视物模糊是最常见的自觉症状。与玻璃体混浊程度不相称的良好视力是怀疑本病的重要线索。
玻璃体混浊的特征
带状和索状模式:从后极向周边呈放射状扩散的独特模式。
极光样混浊:细胞密度高,动态观察可见被形容为“极光样”的玻璃体混浊。
大小不一的细胞:高密度淋巴瘤细胞大小不一地存在。
与视力保留的分离:混浊程度与良好视力不匹配是怀疑本病的关键。
视网膜和RPE表现
黄白色斑状病变:淋巴瘤细胞浸润视网膜色素上皮(RPE)下和Bruch膜下,形成黄白色点状至斑状病变。
病灶融合扩大:小的点状病灶融合并扩大为大病灶。
视乳头炎样表现:肿瘤细胞浸润视乳头周围的视网膜下间隙,可能引起视乳头炎样表现(罕见)。
白鞘形成:也可能出现类似视网膜血管炎的血管白鞘形成。
眼内复发时,角膜后沉着物(KP)的频率有比初发时增加的趋势,已有报道2)。
PIOL的确诊需要进行类似玻璃体切除术的玻璃体活检。利用采集的玻璃体液,结合细胞学检查、IL-10/IL-6比值测定、PCR检测IgH基因重排和流式细胞术进行诊断。单独细胞学检查阳性率仅约50%,但IL-10/IL-6比值>1(敏感性89.4%)、流式细胞术(敏感性88.0%)和PCR(敏感性85.1%)的组合是有用的1)。如果诊断前使用过类固醇,存在假阴性风险,因此应尽可能停用类固醇后再进行活检。
确诊时的平均年龄为63岁,女性略多。在大学医院的葡萄膜炎病例中,发生率约为1-2%。中枢神经系统淋巴瘤患者中15-20%出现眼部症状。
在香港的10例患者(17只眼)的病例系列中,中位年龄59岁,女性占70%,双侧受累占70%1)。上海一项51例的回顾性研究报告双侧受累占78.4%2)。这表明该病多为双侧性,即使单眼发病,对侧眼的检查和随访也很重要。
从发病到确诊常有延迟(由于伪装综合征,平均12-18个月3))。免疫缺陷(如HIV感染)和免疫抑制状态(如器官移植后、使用免疫抑制剂)被认为是危险因素。
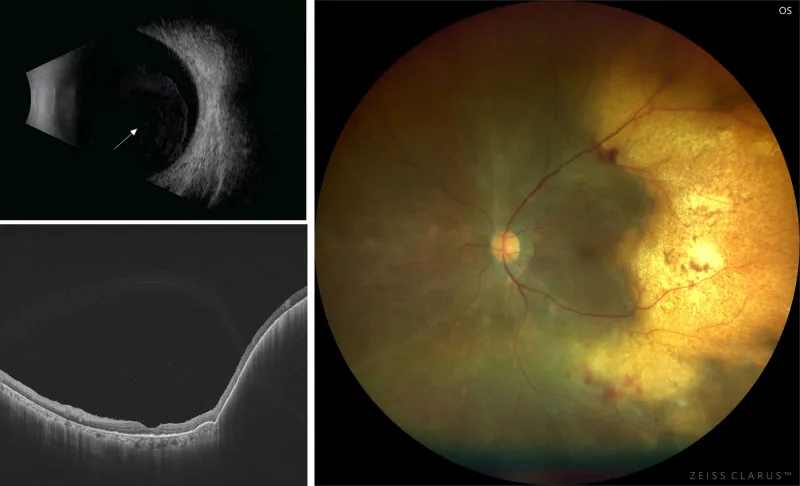
确诊需要进行类似玻璃体切割术的玻璃体活检。仅靠细胞学检查不一定能确诊,必须结合PCR检测免疫球蛋白基因重排和细胞因子测定。
| 检查方法 | 特点/灵敏度 | 临床意义 |
|---|---|---|
| 细胞学检查 | 阳性率50%(香港系列)1) | 基本检查。注意假阴性。 |
| IL-10/IL-6比值 | >1时灵敏度89.4%1) | 最重要的生物标志物 |
| IL-10绝对值 | ≥50 pg/mL有用 | 复发时比比值>1更可靠2) |
| 流式细胞术 | CD20+ B细胞。灵敏度88.0%5) | 单克隆增殖评估 |
| PCR(IgH基因重排) | 灵敏度85.1%5) | B细胞克隆增殖证据 |
| MYD88突变分析 | 灵敏度70%6) | 也有助于分子病理诊断 |
| 通过游离DNA检测MYD88 | 检出率比细胞DNA提高约30%1) | 微创诊断。房水也可行9, 10) |
| 6项诊断框架 | 灵敏度97.5%,特异度100%8) | 复合指标的高精度诊断 |
眼内液中IL-10升高,而炎症性疾病中升高的IL-6低于IL-10,IL-10/IL-6比值>1具有诊断价值。但复发时该比值可能下降(仅43.8%>1),IL-10绝对值≥50 pg/mL是更可靠的指标2)。
确诊眼内淋巴瘤后,应定期进行以下检查以早期发现中枢神经系统淋巴瘤。
PIOL的治疗以眼局部治疗和全身化疗相结合为基础。由于血-视网膜屏障(BRB)限制全身化疗药物进入眼内,局部治疗对于控制眼内病变至关重要。
甲氨蝶呤(甲氨蝶呤注射液200 mg)以400 μg/0.1 mL的剂量进行玻璃体内注射。标准方案如下。
香港系列报告显示,中位注射5次后完全缓解率为77.8%1)。也可使用400 μg/0.05 mL的低剂量。一项积累20年经验的大规模研究报告完全缓解率为97%6)。
主要副作用:角膜病变(33~100%)。通过无防腐剂滴眼液、绷带式隐形眼镜(BCL)和口服叶酸进行管理1)。
总剂量约30 Gy的眼局部照射有效。适用于双侧病变、老年、MTX不耐受或就医困难的患者。但存在放射性视网膜病变、视神经病变和白内障等副作用风险,如果可能,优先考虑MTX注射4)。
部分患者在诊断性玻璃体切除术后获得完全缓解(香港系列:75%1),另一报告:19.7%7))。其机制被认为是去除了淋巴瘤细胞增殖的支架并减少了肿瘤负荷。对于MTX不耐受或拒绝的患者,这是一个选择。
大剂量MTX全身给药是基础治疗。
必要时可加用全脑放疗(WBRT),但由于存在白质脑病等副作用风险,尤其对于老年患者,应谨慎决定适应证。
| 病况 | 推荐治疗 |
|---|---|
| 仅眼内病变 | MTX玻璃体内注射 ± 眼部局部放疗(30 Gy) |
| 合并CNS | 大剂量MTX全身给药 ± 全脑照射 + 眼部局部治疗 |
| 眼内复发时 | MTX玻璃体内注射(完全缓解55.6%,部分缓解33.3%)2) |
全身化疗与玻璃体内化疗联合使用可能降低眼内复发风险。无玻璃体内化疗史被报道为眼内复发的独立危险因素2),表明积极进行眼部局部治疗的重要性。
眼内原发性淋巴瘤中绝大多数(95%以上)为弥漫性大B细胞淋巴瘤(DLBCL)。它是由淋巴细胞单克隆增殖引起的恶性肿瘤,与眼附属器常见的低度恶性MALT淋巴瘤相比,恶性度极高。
MYD88 L265P突变在PVRL/PCNSL中高频检出。该突变导致Toll样受体信号持续激活,持续活化NF-κB通路,维持肿瘤细胞的增殖和存活6)。BTK(布鲁顿酪氨酸激酶)也位于该通路下游,作为治疗靶点备受关注。
VEGF和IL-10的高表达有助于肿瘤细胞的免疫逃逸。IL-10是肿瘤细胞自身产生的细胞因子,参与免疫抑制环境的形成。
肿瘤细胞的转化发生在中枢神经系统之外,随后迁移到具有免疫特权的眼内3)。由于血-视网膜屏障(BRB)限制了全身化疗药物进入眼内,控制眼内病变必须采用玻璃体内注射或眼部局部放疗等局部治疗。
主要浸润部位:
玻璃体混浊呈带状或索状,呈现从后极向周边放射状扩散的独特模式。浸润视网膜的淋巴瘤细胞逐渐形成黄白色斑块状病灶,有时会融合扩大。
PIOL和PCNSL在基因表达谱上有许多共同点,两者被认为属于同一疾病谱系3)。这是PIOL患者频繁发生中枢神经系统病变的背景。
利用玻璃体液和房水中的游离DNA检测MYD88突变正受到关注。其检出率比细胞DNA高约30%1),即使在高度稀释的样本中也有效。已有报道在房水中检测(使用超灵敏ddPCR检测MYD88 L265P突变)9, 10),有望应用于玻璃体活检困难的病例。
一项针对51例病例的回顾性研究表明,全身化疗联合玻璃体内化疗可能降低眼内复发风险2)。最佳给药方案需要进一步的前瞻性研究。
在PIOL中,相当数量的病例最终会发展为CNS病变。孤立性PVRL(仅眼部)的55.6%发生了新的CNSL(中枢神经系统淋巴瘤),中位时间为35.1个月2)。在香港系列中,10例中有7例(70%)出现CNS病变,其中57.1%的眼部病变先于CNS病变1)。因此,即使在确认眼内病变后,也必须定期进行钆增强头部MRI的CNS检查。尽管有报道称眼内复发不会直接影响CNS复发率或总生存期2),但CNS病变发生后的预后通常仍然严峻。